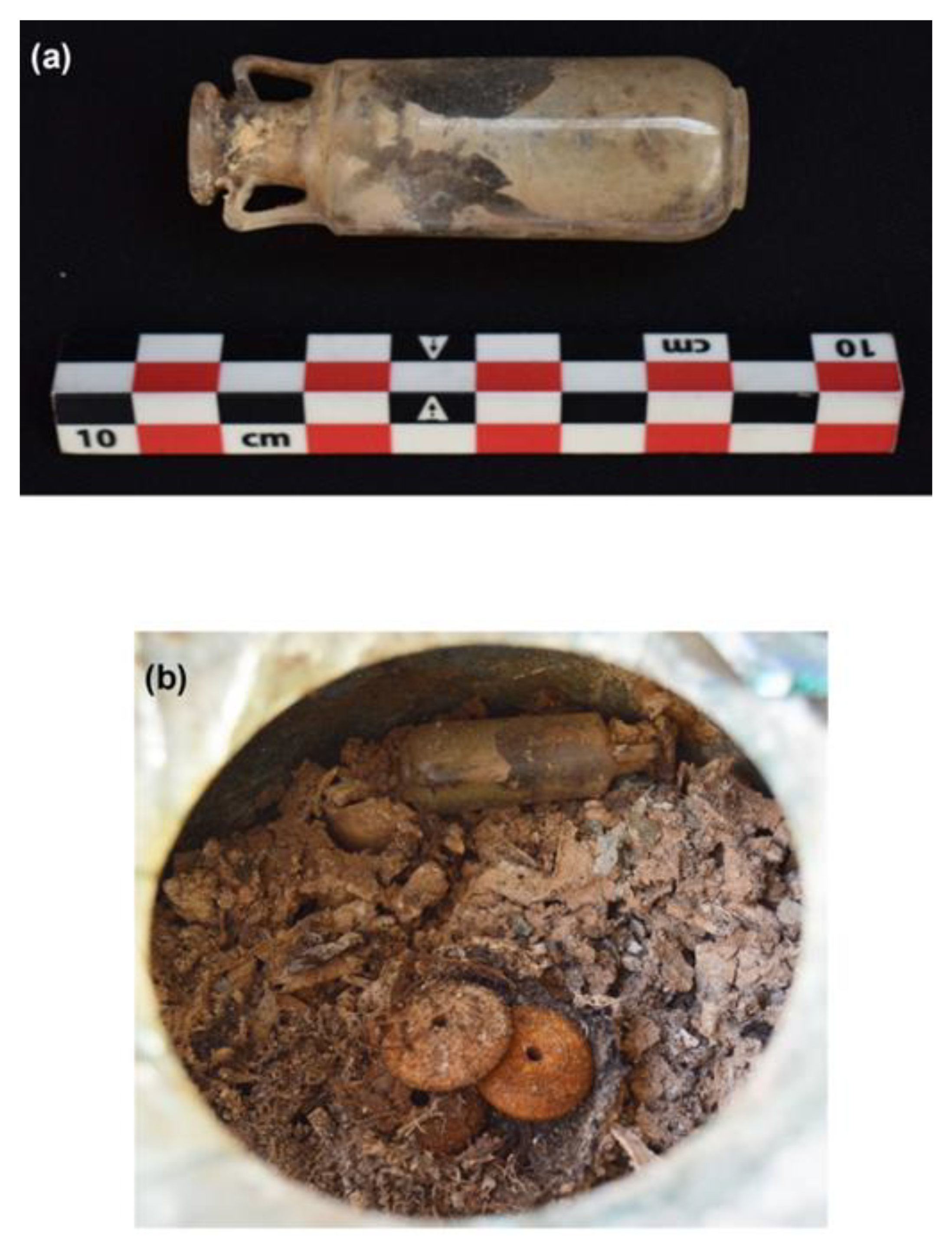
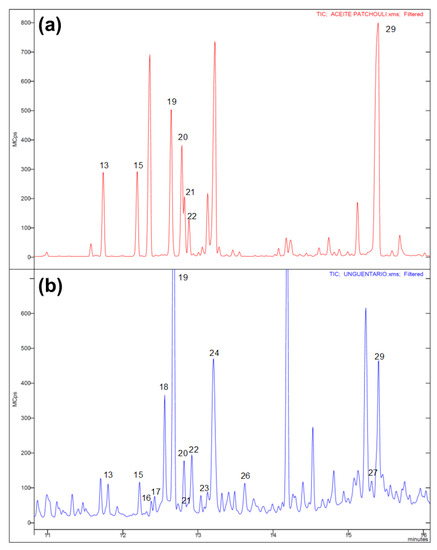
Po tym jak kilka lat temu miałem wątpliwą przyjemność pracować z tiofosgenem liczyłem na to, że już nie będę potrzebował go używać. Ale los jest złośliwy i właśnie pomagam przy jego produkcji.
sobota, 16 grudnia 2023
Ostatnio w laboratorium (90.)
czwartek, 19 października 2023
Kiedyś w laboratorium (89.)
Roztwór chromianu srebra przypomina wyglądam sok pomidorowy z paroma kroplami mleka.
Jest to przykład wyglądu roztworu po przekroczeniu punktu końcowego w metodzie argentometrycznego miareczkowania jonów chlorkowych lub bromkowych. Metoda wykorzystuje tu fakt silniejszego wiązania się jonów srebra z anionami chlorkowymi niż z chromianowymi. Badany roztwór miareczkuje się azotanem srebra po dodaniu niewielkiej ilości chromianu potasu. Początkowo wygrywa silniejsza reakcja wytrącania chlorku lub bromku srebra. Gdy w roztworze skończą się oznaczane aniony, od kolejnej kropli powstaje czerwony chromian srebra, co oznacza koniec miareczkowania. Miareczkowanie prowadzi się w warunkach obojętnych lub tylko lekko zasadowych, ze względu na przeszkadzające przy innym odczynie reakcje uboczne.
środa, 20 września 2023
Kiedyś w laboratorum (88.)
Gdy chemik chce wykonać szybkie sprawdzenie przebiegu reakcji na płytce TLC, to najlepiej jest to zrobić, gdy substrat i/lub produkt są barwne, bo wtedy łatwiej się zorientować, czy pojawiła się lub zniknęła oczekiwana plamka. Jeśli nie ma tak dobrze, może skorzystać z tego, że wiele sprzedawanych płytek świeci w ultrafiolecie, a z kolei wiele związków chemicznych ten ultrafiolet pochłania dając ciemniejszą plamę.
Ale czasem składnik mieszaniny którego się spodziewany, nie jest widoczny ani tak ani tak. I wtedy trzeba zamoczyć całą płytkę w odczynniku, który uwidoczni czy coś jest na niej obecne. Do niektórych typów substancji mogą być użyte odczynniki specyficzne, jak ninhydryna do ujawniania aminokwasów. Często jednak używa się odczynników pokazujących, że w ogóle coś jest w danym miejscu, bez rozróżniania. Takim odczynnikiem może być stężony kas siarkowy, który zwęgla wszelką organikę dając ciemne plamy. A na powyższej płytce użyłem nadmanganianu potasu.
Nadmanganian to silny utleniacz, który reaguje z wieloma substancjami tracąc kolor. Może ujawniać cukry redukujące, różnego typu wrażliwe alkohole i aldehydy oraz związki nienasycone. Co takiego było akurat na tej płytce - nie pamiętam.
czwartek, 3 sierpnia 2023
Nieoczekiwana cyklizacja
Ten przypadek pokazuje, że wiele jest jeszcze mechanizmów chemicznych, które nie przyszły nam wcześniej do głowy. Oraz, że nawet Noblista się myli, ale w tym przypadku wynikło z tego coś dobrego.
 |
| Credit: Angewandte Chemie Int Ed. |
 |
| Prototypowy fulwen |
https://onlinelibrary.wiley.com/doi/10.1002/anie.202303119
środa, 28 czerwca 2023
Chemiczne wieści (28.)
wtorek, 21 marca 2023
Nieładny gips
Ciekawostka geologiczna i chemiczna.
Siarczan wapnia występuje jako minerał w dwóch formach - uwodniony gips mający 2 cząsteczki związanej wody i bezwodny anhydryt. Oba odkładają się na dwie wysychających jezior i zatok morskich, ale w różnych warunkach. Gips w niższej temperaturze i zasoleniu, anhydryt powyżej 40 stopni i w dużym zasoleniu. Często więc warstwy obu minerałów przeplatają się. Pod wpływem, podwyższonego ciśnienia i temperatury po zagrzebaniu w osadach, gips staje się mniej stabilny i zaczyna odwadniać się do bardziej gęstej odmiany anhydrytu. Ta forma potem dość wolno reaguje z wodą w porach skalnych, więc podczas erozji może zachować swój skład a do odsłonięcia.
Ponieważ oba minerały towarzyszą soli kamiennej, wraz z nią często są wypychane pod powierzchnię przez ciśnienie, które zmiękcza sól. Tworzą wówczas "czapę" gipsowo-anhydrytową, która w pewnym stopniu chroni złoże soli przed wypłukiwaniem. Wiele kopalń soli zaczynało w dawniejszych wiekach jako kopalnie gipsu, aż w końcu głęboki szyb dotarł do cenniejszej soli.
Gips używany w budownictwie jest robiony z tego uwodnionego przez podgrzanie i usunięcie połowy związanej wody. Powstała masa dość szybko reaguje z dodaną wodą, która zostaje związana, tworzą się nowe kryształy formy uwodnionej i masa twardnieje. Anhydryt kopalny też może być tak używany ale nie we wszystkich zastosowaniach zachowuje się podczas wiązania masy tak samo.
Główna różnica jest taka, że anhydryt podczas wchłaniania wody bardzo pęcznieje. Przechodzi z gęstszej, odwodnionej na głębokości formy, w dużo luźniejszą nawodnioną. Zwiększa objętość nawet o 60%. Nie za bardzo więc nadaje się do odlewania twardych form. Ma to pewne dodatkowe skutki geologiczne, które brzmią bardzo interesująco. Gdy złoże anhydrytu zostanie odsłonięte przez erozję lub wydobycie albo sól wypycha go płytko pod powierzchnię, reaguje ze słodką wodą deszczową. Zamienia się w gips i zwiększa objętość. Może tworzyć pagórki i grzbiety, pęka, generuje lokalne wstrząsy. Pęcznienie wierzchniej warstwy powoduje jej odspojenie i wypiętrzenie z powstaniem kopuł z pustką pod nimi, lub struktury typu wigwam (płaskie płyty oparte o siebie i tworzące schronisko).
Polscy geolodzy badali jego takie miejsce w Kanadzie na dnie dawnej odkrywki. Nawodnienie wierzchniej warstwy anhydrytu wytworzyło kompleks 40 jaskiń pod widocznymi na wierzchu wypukłościami. Największa to kopuła w kształcie szkiełka zegarkowego tworząca pustkę wysoką na metr i o średnicy 8 metrów, do której można bezpiecznie wejść.[1]
Z drugiej strony zaburzenie przepływu wód podziemnych w miejscu gdzie głębiej są warstwy anhydrytu, tworzy zagrożenie budowlane. Przekonały się o tym władze niemieckiego miasteczka Staufen, które w 2007 roku wykonały odwierty aby założyć instalację pompy ciepła podziemnego do ogrzewania ratusza. Teren okazał się nie do końca dobrze rozpoznany. Warstwa wodonośna okazała się pod sporym ciśnieniem, które popłynęło odwiertem i uszkodziło jego ściany. Głęboka woda zaczęła być wstrzykiwana do soczewki anhydrytu. Ten zaczął się nawadniać i pęcznieć. Teren w pobliżu historycznego centrum zaczął się deformować a wiele kamienic popękało. Najbardziej uszkodzony jest właśnie ratusz.[2] Szybkość wypiętrzania dochodzi do 12 cm rocznie. Po zorientowaniu się w sytuacji założono studnie odwadniające, aby zmniejszyć ciśnienie, ale rozwiązanie to może jedynie przyhamować pęcznienie kolejnych porcji, już powstałych deformacji nie da się odwrócić.
Inne znane zagrożenie wiąże się z niszczeniem ceramiki i cegieł, jeśli glina z której je wykonano nie została właściwie oczyszczona. Jeśli w masie były kawałeczki gipsu, podczas wypalania przechodzą w anhydryt. Potem powoli docierająca do wnętrza woda zamienia go w gips, a wzrost objętości powoduje pękanie. Często więc oglądając starą cegłę z której odpadł kawałek, znajdujemy pośrodku pęknięcia białą bryłkę wewnątrz masy.
----
[1] http://hydrationcaves.com/
[2] https://www.atlasobscura.com/places/staufen-germany
środa, 15 marca 2023
Czy wodór jest litowcem?
Jeśli napatrzyliście się w szkole na tablicę Mendelejewa to zapewne zauważyliście, że układ pierwiastków jest nieco rogaty. Po lewej nad wszystkimi pierwiastkami w górę wystaje zwykle wodór a po prawej nad gazami szlachetnymi hel. Nie jest to jednak jedyny sposób rysowania - czasem wodór umieszczany jest koło helu, zupełnie jakby był najlżejszym fluorowcem.
Jak więc powinno być? Tu już sami chemicy nie są do końca pewni.
Układ okresowy to bardzo przydatne zestawienie naszej wiedzy o pierwiastkach. Każdy jego element jest nieprzypadkowy. Podział na bloki obrazuje na jakiej podpowłoce znajdują się na elektrony walencyjne; okresy wskazują na liczbę powłok elektronowych. Pierwiastki na końcach bloków mają pewne specyficzne właściwości. Niektóre wykazują podobieństwo diagonalne.
Jest multum takich prostych zależności, które można wyjaśnić wielkością atomu, energią jonizacji i właściwościami powłok, a które obrazuje tablica jako podobieństwa sąsiadujących pierwiastków.
Jaką zależność ma obrazować pozycja wodoru? Jest wyrzucany nad wszystkie pierwiastki, bo wraz z helem tworzy pierwszy okres. Rozpoczyna zbiór pierwiastków mających tylko jedną powłokę.
Fluorowce
Za pomysłem aby umieszczać wodór nad fluorem stoją dwie właściwości - wodór potrzebuje tylko jednego elektronu aby uzyskać zamkniętą zewnętrzną powłokę. W jego przypadku to dublet elektronów, u fluorowców oktet. Tworzy wtedy anion wodorkowy. Ponadto ma elektroujemność wyższą niż większość metali. Może więc tworzyć związki z metalami o niższej elektroujemności. Atom metalu alkalicznego jonizuje się tworząc kation, a wodór tworzy anion wodorkowy. Związek nabiera charakteru jonowej soli, ma wysoką temperaturę topnienia. Wodorek sodu przyjmuje strukturę krystaliczną podobną do chlorku sodu. W stanie wolnym formuje dwuatomowe cząsteczki a po schłodzeniu do temperatury krzepnięcia tworzy kryształy molekularne.
Oddając elektron, atom wodoru w zasadzie nie tworzy wolnych kationów. Kation wodorowy niezwiązany to swobodny proton, który w reakcjach chemicznych występuje tylko w formach związanych, zwykle solwatowany rozpuszczalnikiem. Energia jonizacja wodoru do wolnego elektronu i nagiego protonu jest wyższa niż u metali, podobna do fluorowców. No i ostatecznie w stanie ciekłym i stałym nie wykazuje charakteru metalicznego.
Litowce
Z drugiej strony wodór ma elektroujemność niższą od wielu niemetali i tworzy z fluorowcami połączenia, w których ładunek jest przeniesiony na niemetal. Z większością pierwiastków o bardziej pośrednich elektroujemnościach tworzy wiązania kowalencyjne, jak to jest w związkach organicznych. Anion wodorkowy jest nietrwały, natomiast formy kationowe, w których proton jest związany z inną cząsteczką, są stabilne. Pierwiastkowy wodór reaguje z innymi pierwiastkami jako reduktor a nie utleniacz. Wyjątkiem są tylko wspomniane związki z metalami alkalicznymi.
Najważniejszą właściwością, która decyduje o umieszczaniu go zwykle na początku układu, jest budowa zewnętrznej powłoki elektronowej. Posiada jeden elektron na powłoce s, zatem pasuje do pierwiastków bloku s. Budowę [X] 1s mają wszystkie litowce. Pod ekstremalnie wysokimi ciśnieniami nabiera charakteru metalicznego - z drugiej strony teoretycznie każdy pierwiastek pod bardzo wysokim ciśnieniem powinien nabrać takiego charakteru.
Fluorowce posiadają elektrony walencyjne na powłoce p i to na nią ściągają elektron aby uzyskać oktet, a wodór takiej powłoki w ogóle nie posiada.
Za nietypowe właściwości wodoru odpowiada mały rozmiar całego atomu. Tylko jeden elektron na najbliższej orbicie czuje ładunek jądra bardzo efektywnie. Stąd elektroujemność 2,2 w skali Paulinga, podobna do metali przejściowych i półmetali. Za tym idą właściwości i reaktywność pośrednie między metalami alkalicznymi a niemetalami. Stąd nawet propozycja, z którą także się spotkałem, aby na tablicach umieszczać go samotnie gdzieś nad środkiem Układu Okresowego. Dla cząsteczek i atomów o właściwościach trochę podobnych do litowców zaproponowano kategorię pseudometali alkalicznych, analogicznie do pseudohalogenów. Należałby do nich pierwiastek tal, rodnik amonowy (*NH4) [1], niektóre cząsteczki organiczne a w niektórych sytuacjach podobne jest nawet srebro.
------
https://www.reed.edu/reed_magazine/summer2009/columns/NoAA/downloads/CronynHydrogen.pdf
[1] https://chemistry-europe.onlinelibrary.wiley.com/doi/abs/10.1002/chem.201101949
wtorek, 31 stycznia 2023
Wyspy ognia i samotności - Recenzja
Dawno już tu nie wrzucałem recenzji książek popularnonaukowych.
Choć może to nie być takie oczywiste, wulkany i ich wybuchy to temat, który interesuje mnie od bardzo dawna. Będąc małym brzdącem wychowywałem się w otoczeniu książek, rodzice zbierali różne i w każdym pokoju była jakaś półka czy stosik na stoliku. Były też czytane przez rodziców, więc szybko załapałem, że branie którejś i otwieranie jest czymś w porządku. Sam tego nie pamiętam, ale według opowieści mamy pytałem czasem co jest napisane tu, bądź gdzie indziej, w książeczce dla dzieci, lub w podpisie zdjęcia w gazecie, lub na karcie tytułowej książki, a oni mi mówili i czytali mi to słowo, które mnie zainteresowało. Nie mieli za bardzo czasu na jakieś domowe lekcje i zakładali, że nauczę się czytać w przedszkolu, a tak przynajmniej poznam wcześniej literki. I tak widzieli jak otwieram jakieś książki i się w nie wpatruję, albo rozkładam gazety i specjalnie się nie dopytywali.
To, że ja sobie je płynnie czytam, wyszło na jaw przypadkiem podczas Wigilii, gdy miałem 4 lata i krewny usłyszał, jak próbuję odczytać łaciński zwrot na opłatku. Wcześniej nikt na moje zachowanie nie zwrócił uwagi, bo znane słowa czytałem w myślach bez sylabizowania na głos, więc sądzili, że tylko oglądam obrazki. Pociągnęło to za sobą przestawienie niektórych zbyt dorosłych książek poza zasięg małych rączek.
Wśród pierwszych przeczytanych książek jakie pamiętam z tego okresu, poza encyklopedią, słownikiem, "Pchłą szachrajką" i tomikami poezji różnej, była książeczka z popularnej serii w czarnej okładce "Wulkany i trzęsienia ziemi". Tak w sam raz dla początkującego, z wyjaśnieniem jak zbudowana jest ziemia, jak wygląda wulkan, jak gorąca jest lawa, co robi z budynkami trzęsienie ziemi, a do tego masa technicznych szczegółów składu mineralnego, gazów wylotowych, klasyfikacji rodzajów lawy i tak dalej, których wtedy nie rozumiałem ale jakoś utkwiły mi w chłonnej pamięci. A ponieważ większość innych książek w domu niezbyt mnie interesowała, to zczytałem tę książkę wiele razy aż zaczęła się rozpadać i trzeba było ją sklejać taśmą.
Toteż gdy dorośli wtedy pytali mnie, kim chcę zostać w przyszłości, to odpowiadałem, że wulkanologiem. Później pojawiły się inne książeczki z innych dziedzin a poglądy na bycie kimś w przyszłości ewoluowały, a wulkanologia mieszała się z botaniką, archeologią i technologią i nie mogłem zdecydować co by mnie pociągało bardziej, więc czytałem to o tym, to o owym bez ładu i celu.
A potem poszedłem do szkoły podstawowej, w pierwszej klasie odkryłem w bibliotece półkę z książkami Sękowskiego i zmieniłem plany na bycie chemikiem. Co jakoś udało mi się doprowadzić do praktycznej realizacji.
Temat wulkanów jakoś jednak nadal zajmuje swój kącik w moim intelektualnym serduszku i dlatego szukałem w kolejnych latach nowych źródeł wiedzy. I tak kilka lat temu natknąłem się na bloga Wulkany Świata z krótkimi notkami na temat znanych wulkanów i doniesieniami o aktualnej aktywności. Teraz autor tego bloga wydał książkę na ten temat, którą chętnie kupiłem.
Książka
"Wulkany. Sekrety wysp wulkanicznych" to trochę leksykonowy przegląd wybranych wysp o pochodzeniu wulkanicznym. Wybór był pewnie trudny, bo wysp z jakimiś wulkanami jest bardzo dużo. W niektórych przypadkach miałem wrażenie, że z grupy wulkanów z danego obszaru wybrano najpierw najbardziej znane, a później te najmniej, nieinteresujące, nie zasługujące zwykle na wzmiankę, o których być może właśnie po raz pierwszy podano w języku polskim jakiś opis.
Są tutaj zarówno wyspy z wulkanami aktywnymi i stale wypluwającymi iskry, jak choćby Stromboli, jak i wysepki wygasłe, w których magma nie krążyła od tysięcy lat. Zastosowano ogólny podział wulkanów według części oceanu na którym leżą wyspy. W przypadku północnego Atlantyku nie było dużo do opisywania, Islandia, wyspy w jej pobliżu i Jan Mayen. Sporo rozdziałów poświęcono wulkanom na wyspach Sandwich na półkuli południowej, które są mało znane, często widziane są tylko z daleka i obserwowane satelitarnie, zaś ich szczytów nikt nigdy nie zdobył.
.JPG/1280px-Bouvet_Island_ISS017-E-16161_no_text_(cropped).JPG) |
| Wyspa Bouvet, omawiana w książce |
Styl jest prosty i rzeczowy. Nie ma tutaj lania wody, nie zobaczymy tu okrągłych zdań, natomiast dowiemy się ile kilometrów średnicy i metrów wysokości mają omawiane wysepki, oraz na ile tysięcy metrów sięgnęły kolumny popiołów po erupcji. Z drugiej strony widać, że autor nie ma jeszcze wyrobionego story tellingu i o ile jakaś ciekawa historia miejsca nie wpadła mu w ręce, to nie stara się specjalnie układać opowieści o kolejnym wulkanie, tylko spokojnie wymienia po kolei fakty: położenie, kiedy pierwszy raz odkryto, ostatnia erupcja miała miejsce w... Dla jednych będzie to duża zaleta, bo książek popularnonaukowych, których autorzy próbują najwyraźniej pod pretekstem napisać powieść jest sporo, i z czasem ta maniera staje się irytująca; a inni mogą powiedzieć, że książka ich nie porwała bo jest sucha.
Najkrótsze rozdziały zajmują pół strony, a właściwie to nawet mniej, biorąc pod uwagę wielkość zdjęć, jednak nawet w takich przypadkach nie zastosowano podziału jednej strony na dwa opisy wysp. Każda ma więc na siebie przynajmniej jedną stronę, co jest bardzo czytelne. Często dodatkowe informacje i wtrącenia na pośredni temat są umieszczane drobniejszym drukiem na marginesie. Z tego co zauważyłem, w krótszych rozdziałach tekst główny zawiera informacje geograficzne i geologiczne, a dopiski z marginesów fakty historyczne. W sytuacji gdy akurat z daną wyspą wiąże się jakaś historia, może być odwrotnie - w tekście głównym mamy opis tego ciekawego zdarzenia z historii, a na marginesie rozmiary wyspy i wysokość chmury popiołu podczas ostatniego wybuchu. Nie ma stałej zasady, polecam więc przyglądać się uważnie wszystkim napisom aby niczego nie przeoczyć.
W innych przypadkach opisy wulkanów są jednak dłuższe, bo jest to miejsce dobrze znane, dla którego dało się znaleźć więcej informacji, a zwłaszcza wtedy, gdy jest to wulkan, który niedawno przeszedł spektakularną erupcję. Najobszerniejszy jest chyba opis wulkanu Krakatau, więcej jest też opisu na temat Hunga Tonga, Santorynu czy Martyniki. Nic dziwnego. Z ich aktywnością wiążą się ciekawe zdarzenia, są to niejednokrotnie "klasyki" wulkanologii, możliwe są do znalezienia relacje świadków, które są wówczas zacytowane w tekście. Szersze są też generalnie opisy wulkanów, które wybuchły w ostatnich latach.
Ostatnie aktualizacje tekstu musiały pochodzić z połowy roku 2022 dlatego niektóre informacje są całkiem świeże i mamy tu obszerniejszy opis słynnej erupcji na wyspach Tonga z początku roku.
Wyspy historiiAutor szukając informacji o tych wszystkich wyspach, wynajdywał niejednokrotnie ciekawostki, które podczas czytania sprawdzałem sobie w innych źródłach. Jak historia marynarza pozostawionego celowo na Wyspie Wniebowstąpienia, w ramach kary za "sodomię" - czyli jak to dziś byśmy powiedzieli, za homoseksualizm - który musiał przetrwać na suchej wysepce kilka miesięcy, zanim miejsce odwiedzi kolejny statek. W zachowanym dzienniku opisywał jak w zasadzie przymierał z pragnienia, żywiąc się fokami i ptakami i z desperacji pijąc ich krew. Dziennik znaleziono w obozowisku; jego zapiski urywają się po sześciu miesiącach od wyrzucenia na wyspę. Ciała nigdy nie znaleziono.
A takich przypadków jest więcej. Wiele wysp wulkanicznych ma bardzo odizolowany charakter. Wizyta na którejś z nich, samemu, ze sprzętem i zapasami, na kilka dni, byłaby ciekawym doświadczeniem. Ale natura potrafi być nieprzewidywalna i zaskakuje wszystkich, nieraz za bardzo przedłużając lub zbyt nagle skracając pobyt. Więcej miejsca poświęcono erupcji na White Island, u wybrzeży Nowej Zelandii, gdzie zginęli turyści, ale moja ulubiona historia tego typu to opowieść o strażniku z wyspy Raoul. Był jedną z zaledwie kilku osób pilnujących bazy i miał stałą trasę obchodu wyspy. Pewnego dnia, właśnie w chwili gdy zszedł nad jezioro wulkaniczne, aby wykonać pomiar, miała miejsce pierwsza obserwowana erupcja. Trwała 15 minut i wyrzuciła tony gorącego błota i ogromnych kamieni. Gdyby przyszedł tam 10 minut wcześniej, lub tyleż samo się spóźnił, opowiadałby teraz znajomym, że uch, niesamowita sprawa, o tyle tyci mu brakowało. Ale on trafił akurat na ten moment i zginął, a ciała nie odzyskano z krateru.
Nie zdziwiłbym się gdyby takie przypadki kolekcjonowali ufolodzy, szukający tajemniczych historii aby móc wskazać "o tutaj zdarzyło się niezwykle zjawisko i zaginęło ciało - to musiało być porwanie!".
Na plus
Wydanie jest estetyczne. Już okładka przyciąga wzrok interesującym rysunkiem. Wewnątrz dość dużo ilustracji, choć niektóre wysepki nie dostały swojego zdjęcia. Niektóre wykonał sam autor podczas wycieczek na wulkany, inne przysłali mu inni podróżnicy lub czytelnicy, resztę wydawnictwo wzięło z dostępnych im źródeł i często są to ładne widoki. Papier nie jest zbyt cienki i szorstki, nie miałem problemów z rozdzieleniem stron. Font czytelny, łagodny. Literówek wyłapałem niewiele.
Rozdziałów o wulkanicznych wyspach jest prawie sto ale wspomina się przy okazji o innych wysepkach w pobliżu, czasem też o tych efemerycznych, widocznych nad poziomem morza krótki czas zanim nie rozmyją je fale, więc jakąś wzmiankę posiada jeszcze do tego jakieś 20-30 wysp.
Jeśli jest to szerzej wiadome, opisywana jest też przyroda danej wyspy, jej ptaki i rośliny, często endemity charakterystyczne tylko dla niej.
Jak wspominałem, w niektórych przypadkach podawane są bardzo interesujące przypadki historyczne, o których chce się poszukać czegoś więcej, bo to coś o czym się nigdy wcześniej nie słyszało. Na końcu polecane są dodatkowe źródła, którymi można poszerzyć wiedzę, jak na przykład strona internetowa wyspy Tristan da Cunha czy praca naukowa o gatunkach zasiedlających Surtsey. Nie ma natomiast w rozdziałach przypisów identyfikujących dokładne źródło informacji, bo książka jest luźniejsza w formie.
Na minus
Mimo wszystko czytając trochę kręciłem nosem, nie będąc całkowicie ukontentowanym. Autor swobodnie posługuje się tu słownictwem, pisze co chwila o "kalderach zagnieżdżonych", "kopułach lawowych", "piroklastach", gdzieś wspomni o tefrze, ówdzie o ryolicie. Niektóre z tych pojęć są objaśnione w słowniczku na końcu, ale hasła w nim są, cóż, dość skrótowe, jak to w słowniczku. Więc nie wiem czy czytelnik wcześniej nie zapoznany z tematem będzie w stanie sobie wyobrazić dlaczego właściwie kopuła lawowa jest tak niebezpieczna oraz co właściwie odróżnia bardzo szeroki krater od kaldery. W niektórych opisach konkretnych wulkanów zostaje to trochę wyjaśnione, ale inne słowa objaśnia tylko ten słowniczek, lub przewijają się przez tekst tak po prostu.
Może przydałby się jednak trochę obszerniejszy początkowy opis co takiego jest wulkanem i jak nazywamy jego elementy, albo jednak takie bardziej elementarne objaśnienia w opisach jakiegoś wulkanu, typu "Lepka lawa w tym typie erupcji jest mozolnie wyciskana na powierzchnię, jak bardzo gęsta pasta, formując wypukłość nazywaną kopułą lawową, wyglądającą jak dymiąca kupa gruzu..." itd. Zgaduję, że maksymalna objętość tekstu była ograniczona, stąd konieczność trudnego wyboru o których wulkanach rozpisać się bardziej a które ostatecznie pominąć, a później kwestia co objaśnić dokładniej a co bardziej skrótowo i ostatecznie chyba zostało to nie do końca dobrze wyważone.
Ale może jednak czytelnicy nie zwrócą na to aż takiej uwagi, przyjmą że w erupcji pojawia się takie coś o takiej to nazwie a co to jest, to mniej ważne? Nie każdy będzie dociekliwy.
Ogółem
Dobra książka dla miłośników tematyki, ale też osób lubiących czytać o katastrofach, niezwykłych zdarzeniach lub dalekich egzotycznych zakątkach z całego świata. Popularnonaukowych książek na temat tylko wulkanów jest u nas mało, raczej są to tłumaczenia, opisy jakiegoś szczególnego przypadku oraz opowieści mówiące o wulkanach przy okazji czegoś innego. Więc dobrze, że pojawiło się coś polskiego, skoncentrowanego na temacie bez zbędnych dygresji.
5/6



.svg/1280px-Dewar_benzene_(edge_on).svg.png)