Wiele osób lubi zapach skoszonej trawy, niektórzy nawet chcieliby mieć takie perfumy. Ale jakie właściwie związki chemiczne za niego odpowiadają?
Pomysł tego wpisu krążył mi po głowie już od pewnego czasu, ale bezpośrednią inspiracją był zauważony w internecie osobliwy mit. Otóż przy okazji dyskusji o chemicznych środkach bojowych, sprowokowanych najnowszymi wydarzeniami na świecie, po raz drugi spotkałem się z twierdzeniem, że świeżo skoszona trawa wydziela fosgen, gaz o działaniu duszącym. Z krótkiego przeglądu internetu wynika, że pogląd taki czasem pojawia się jako zasłyszany, niekiedy rozszerzany na inne rośliny na przykład geranium.[1],[2].
Skąd taki osobliwy pomysł? Fosgen przypadkiem pachnie podobnie do skoszonej trawy (wedle innych źródeł jak zepsute owoce), a ponieważ pachnący migdałowo cyjanowodór faktycznie jest w pewnych ilościach zawarty w migdałach, komuś musiało się skojarzyć jedno z drugim. Tyle że nie. To, że jakiś związek pachnie jak coś konkretnego, nie oznacza, że jest w tym zawarty.
Jeśli nie fosgen to co?
Większość gatunków traw nie wytwarza specjalnych substancji zapachowych, jedynie te z rodzaju palczatka posiadają własne zapachy, wyczuwalne bez naruszenia rośliny. Jednak sytuacja koszenia, jest dla rośliny sytuacją szczególną. Źdźbła zostają poszatkowane i uszkodzone, co jest dla rośliny czynnikiem stresowym. A na takie akcje biologia przewidziała rozmaite reakcje.
W dawnych czasach, przed pojawieniem się ludzkiego gatunku, liściom roślin zagrażały właściwie tylko dwa czynniki - roślinożerne ssaki i takież owady. Przed zwierzętami krzak czy kępka życicy nie za bardzo mają się jak bronić, jeśli oczywiście nie liczyć kolców, ostrego brzegu liścia czy zachowań podobnych do mimozy. Natomiast na wypadek ataków owadów wykształciły specyficzny mechanizm obronny - po uszkodzeniu liścia wydzielają lotne substancje, które ostrzegają inne rośliny dookoła oraz ściągają na odsiecz owady drapieżne.
Są to najczęściej związki oparte o sześciowęglowy łańcuch, wytwarzane w szybkiej reakcji enzymatycznej rozszczepiania nienasyconych kwasów tłuszczowych omega-6. Zazwyczaj substratem jest kwas linolowy lub kwas alfa-linolenowy. Po uszkodzeniu tkanek z komórki wylewa się jej zawartość. Lipooksygenaza powoduje utlenienie kwasu tłuszczowego dodając grupę nadtlenkową przy wiązaniu podwójnym. Kolejny enzym, liaza, powoduje rozszczepienie wiązania podwójnego. Całość jest biologicznym odpowiednikiem ozonolizy. Zależnie od tego który z kwasów ulegnie rozszczepieniu, powstająca krótka cząsteczka albo jest związkiem nasyconym albo zawiera wiązanie podwójne.
Najczęściej więc produktami rozpadu są heksanol i cis-3-heksenol, który izomeryzuje do formy trans. Alkohole te następnie są utleniane do odpowiednich aldehydów i kwasów karboksylowych, a ponadto estyfikowane grupą acetylową. Wszystkie te związki mają przyjemne zapachy, od słodkawych, przez owocowe do kwiatowych. Najsilniejszy i najlepiej wyczuwalny jest zwykle cis-3-heksenal, stąd niekiedy zbiorczo mówi się o tych związkach "aldehydy liściowe".
Równocześnie z tej samej utlenionej formy kwasu tłuszczowego poprzez szereg innych reakcji powstaje kwas jasmonowy, który akurat specjalnie nie przyczynia się do zapachu, stanowi roślinny hormon regulujący wzrost.
W jakim celu wytwarzane są wszystkie te związki? Aby ściągnąć naturalnych wrogów owadów.
Zapachy wytwarzane podczas uszkadzania liści przez gąsienice czy chrząszcze są bardzo atrakcyjne dla drapieżnych i pasożytniczych owadów, na przykład gatunków os składających jajeczka wewnątrz sparaliżowanego jadem owada.
Kwas jasmonowy wytwarzany w pobocznej reakcji stymuluje w roślinie wytwarzanie inhibitorów proteaz, mających za zadanie blokować u owadów trawienie białek a tym samym sprawić, że w mniejszym stopniu posilą się na roślinie.
Roznoszące się wokół aromaty mogą ponadto ostrzegać inne rośliny przed
atakiem roślinożerców, w związku z czym na wszelki wypadek przygotowują
one nieco więcej substratów reakcji lub wydzielają więcej kwasu jasmonowego. Jak więc widać, zwykłe skoszenie trawnika wprowadza w te naturalne zależności niemało zamieszania.
Pewne znaczenie dla zapachu mogą mieć też inne związki występujące w trawach i drobnych roślinach przerastających trawnik. Jednym z najpospolitszych związków, który występuje w każdej roślinie zielonej, jest fitol, długołańcuchowy alkohol stanowiący podstawnik w cząsteczce chlorofilu i będący prekursorem witaminy K. Ma lekko słodkawy zapach, bywa dodawany do perfum jako utrwalacz.
Niektóre gatunki traw zawierają też kumarynę o słodkim, lekko waniliowym zapachu. Najzasobniejsze są tomka wonna oraz żubrówka, używane do aromatyzowania alkoholi, a z roślin zielnych nostrzyk żółty i koniczyna. Podczas suszenia roślin zawartość kumaryny wzrasta, w związku z rozpadem glikozydów, zaś alkohole liściowe ulatniają się, dlatego kumaryna jest głównym związkiem decydującym o zapachu suszonego siana.
-----
[1] http://pl.sci.chemia.narkive.com/xEHjupyL/fosgen-w-trawie-cyjanowodor-w-pestkach
[2] http://skibicki.pl/forum/viewtopic.php?p=17504
* Plant Volatiles as a Defense against Insect Herbivores, Plant Physiology October 1999, Vol. 121, pp. 325–331
* https://en.wikipedia.org/wiki/Jasmonic_acid
* Alessandra Scala, Silke Allmann, Rossana Mirabella, Michel A. Haring, and Robert C. Schuurink, Green Leaf Volatiles: A Plant’s Multifunctional Weapon against Herbivores and Pathogens,
Int J Mol Sci. 2013 Sep; 14(9): 17781–17811.
informacje
poniedziałek, 14 maja 2018
poniedziałek, 7 maja 2018
Trans/Cis
Kiedyś już omawiałem na blogu jeden z rodzajów izomerii - izomery orto, meta i para. Czas więc opowiedzieć coś o innym, równie często spotykanym - izomerii Trans-Cis, opartej o różne ustawienie podstawników wokół wiązania podwójnego.
Podwójne wiązanie między atomami powstaje wskutek dodania jednego wiązania typu sigma i jednego typu pi. Następuje to po hydrydyzacji orbitali elektronowych, to jest swoistego wymieszania tworzącego orbitale o wyrównanej energii. Wiązanie sigma tworzą orbitale nakładające się na wprost, zaś wiązanie pi jest tworzone przez boczne nałożenie orbitali w kształcie klepsydry po obu stromach wiązania sigma:
W efekcie wiązanie to jest sztywne i płaskie, a grupy na końcach nie zmieniają ustawienia w zwyczajnych warunkach (wysoka temperatura lub naświetlenie mogą wywołać izomeryzację). W związku z tym faktem, gdy na czterech końcach wokół wiązania obecne są różne podstawniki, możliwe stają się różne izomery.
W najprostszym przypadku na dwóch końcach pojawiają się dalsze organiczne części cząsteczki, zaś dwa pozostałe zajmują wodory. Przyjęto więc zasadę nazewnictwa, wedle której izomerami cis są cząsteczki, w których grupy organiczne znajdują się po tej samej stronie, a izomerami trans cząsteczki, w których grupy ustawione są po przeciwnych stronach:
Czasem też korzysta się z tego układu gdy przy wiązaniu pojawiają się inne podstawniki, ale takie same, na przykład dwa podstawniki chlorowe.
Z przedrostkami określającymi izomerię wiązań podwójnych możemy spotkać się w nazwach pospolitych. Słynne w ostatnich latach tłuszcze trans, to tłuszcze zawierające wyłącznie-trans nienasycone kwasy tłuszczowe. Układ taki nadaje im generalnie liniowy kształt co ma wpływ na właściwości fizyczne - tłuszcze trans mają wyższą temperaturę topnienia z powodu ściślejszego przylegania prostych cząsteczek co zwiększa oddziaływania między nimi.
Tłuszcze zawierające przynajmniej jedno wiązanie cis są bardziej wygięte, co utrudnia ścisłe upakowanie. Przykładowo kwas oleinowy, będący głównym kwasem tłuszczowym oliwki z oliwek, posiada tylko jedno wiązanie podwójne na 9 węglu (omega-9) i ma ono układ cis, przez co cząsteczka nabiera wygiętego kształtu a sam związek ma temperaturę topnienia 13°C. Jego izomer trans to kwas elaidynowy o temperaturze topnienia 45°C. Oznacza to, że ten pierwszy pozostaje płynny w temperaturze pokojowej, zaś ten drugi pozostaje stały nawet w temperaturze ludzkiego ciała.
Związkiem o dużej ilości wiązań podwójnych w układzie trans jest karoten, pomarańczowy barwnik marchwi. Z kolei przykładem związku z dużą ilością samych tylko wiązań cis jest bardzo rzadki kwas dokozoheksaenowy (DHA), w którym sześć kolejnych takich wiązań skręca jego cząsteczkę w kółeczko:
W ostatnich dekadach zwraca się uwagę na dostarczanie wraz z dietą odpowiedniej ilości tłuszczy z kwasami cis, które pełnią w organizmie różne funkcje biologiczne.
Ten typ izomerii występuje też w związkach pierścieniowych z wiązaniami pojedynczymi. W takim przypadku cały pierścień pełni rolę drugiego wiązania, powstrzymując rotację sąsiadujących grup. Izomerem cis jest związek, gdy podstawniki na sąsiednich węglach są położone po tej samej stronie pierścienia, a trans gdy po przeciwnych:
Związki różniące się geometrią wokół wiązania podwójnego mogą posiadać różne właściwości nie tylko fizyczne ale i chemiczne. W układzie Cis grupy po obu stronach mogą silniej ze sobą oddziaływać. Przykładem mogą być najprostsze nienasycone kwasy dikarboksylowe - fumarowy i maleinowy. Ten pierwszy zawiera dwie grupy karboksylowe w układzie trans, a więc po przeciwnych stronach. Dzięki temu w kryształach dość chętnie tworzą wiązania wodorowe między cząsteczkami, sam związek ma więc stosunkowo dużą temperaturę topnienia (287 °C ) i jest słabo rozpuszczalny w wodzie.
Natomiast kwas maleinowy posiada dwie grupy karboksylowe w układzie cis, po tej samej stronie, które w tym bliskim położeniu tworzą wewnątrzcząsteczkowe wiązanie wodorowe, kosztem tych pomiędzy cząsteczkami. Słabsze oddziaływania między cząsteczkami w krysztale zwiększają rozpuszczalność w wodzie oraz obniżają temperaturę topnienia niemal dwa razy. (135 °C ) W dodatku utworzenie wewnętrznego wiązania wodorowego do jednej z grup karboksylowym powoduje, że niezwiązany wodór z tej drugiej łatwiej ulega odszczepieniu, przez co kwas maleinowy jest w roztworach silniejszym kwasem niż fumarowy (pKa = 1,9 wobec 3,0). W niektórych przypadkach izomery geometryczne mogą różnić się kolorem.
Izomeria geometryczna może też mieć znaczenie dla stabilności związku. Stosunkowo duże grupy organiczne przeszkadzają sobie w przestrzeni a nawet odpychają się, dlatego ułożenie ich po tej samej stronie, w zbliżeniu, jest bardziej niekorzystne energetycznie. Objawia się to wyższą wartością ciepła spalania dla izomerów cis o dużych grupach niż dla izomerów trans. W warunkach osłabiających lub przejściowo likwidujących wiązanie podwójne obserwuje się izomeryzację i częściej wówczas ustala się równowaga z przewagą układu trans, jako mniej naprężonego.
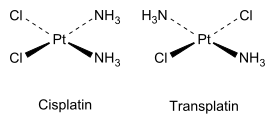
Podobny typ izomerii występuje też w związkach nieorganicznych - jeśli w kompleksie metalu z różnymi ligandami tworzona jest płaska, kwadratowa struktura, zaś kompleks tworzą dwa rodzaje ligandów, możliwe stają się dwa izomery - kompleksy cis, gdy dwa takie same ligandy znajdują się obok siebie, i kompleksy trans, gdy są położone w przeciwnych narożach kwadratu:
W powyższym przypadku kompleks nazywany cisplatyną jest znanym lekiem przeciwnowotworowym.
E/Z
Ale przypadek gdy przy wiązaniu podwójnym dwa podstawniki to wodory a kolejne dwa to grupy organiczne, jest za prosty. Jeśli w takim miejscu pojawią się cztery różne podstawniki, wówczas stosuje się nazewnictwo w systemie E/Z. Oznaczenia pochodzą od niemieckich słów "zusammen" czyli "razem" oraz "entgegen" czyli "naprzeciwko".
Zasada nazewnictwa opiera się o ważność podstawników, główną braną pod uwagę regułą jest ciężar atomowy, kolejną stopień rozbudowania czy obecność wiązań wielokrotnych. Jeśli dwie kolejno najważniejsze grupy są położone po tej samej stronie, to układ oznacza się jako Z, zaś gdy są po przeciwnych stronach, to jako E.
Warto zauważyć, że w zasadzie jest to system bardziej ogólny, w ramach którego izomeria trans/cis stanowi szczególny przypadek.
Izomeryzacja
Proces w wyniku którego następuje obrót grup i zamiana jednego izomeru w drugi, to izomeryzacja. Ze względu na sztywność wiązania podwójnego, proces musi przebiegać poprzez stan pośredni, w którym jest ono osłabione lub nie istnieje. Jedną odmian jest fotoizomeryzacja, gdzie obrót staje się możliwy dzięki energii z pochłoniętego światła. Wiązanie podwójne pochłania kwant światła i przechodzi w stan wzbudzony, w którym nie jest już tak sztywne i staje się podatne na ruchy skręcające. Może więc nastąpić obrót i zamiana w inny izomer.
W przypadku wielu związków organicznych, zakres energii pochłanianego światła lokuje je w obrębie ultrafioletu, czasem też bliżej fioletu z zakresu widzialnego, co nadaje wielu związkom nieco żółtawy kolor. Wiele związków używanych jako filtry UV w kremach do opalania to cząsteczki z wiązaniem podwójnym, które bardzo łatwo izomeryzują w obie strony. Dość chętnie używane są na przykład pochodne kwasu cynamonowego, w formie naturalnej w układzie trans :
Inny przykład to enzokamen, oznaczany jako 4-MBC, będący specyficzną pochodną kamfory:
Fotoizomeryzacja ma znaczenie dla procesu widzenia. W fotoreceptorach oka zawarty jest kompleks białka opsyny z retinalem, czyli aktywną formą witaminy A, która jest cząsteczką z trzema wiązaniami podwójnymi. W formie aktywnej w foceptorze retinal występuje w geometrii 11-cis, a więc wygiętej. Pod wpływem kwantu światła następuje izomeryzacja, przez co cząsteczka się prostuje. Do obu końców cząsteczki przyczepione są fragmenty białkowej opsyny, która po zmianie kształtu retinalu, pociągnięta mechanicznie dwoma końcami musi zmienić kształt. Generuje to kaskadę dalszych reakcji prowadzących w końcu do wytworzenia impulsu nerwowego.
Izomeryzacja może też zajść pod wpływem wysokiej temperatury i reakcji chemicznych. Przykładowo podczas uwodornienia tłuszczów nienasyconych przy produkcji margaryny, reakcja przyłączenia jednego atomu wodoru do jednego z wiązań podwójnych kwasu tłuszczowego, zamienia go w formę karboanionu. Jest to struktura niepłaska z wiązaniem pojedynczym, w której może nastąpić obrót cząsteczki. Jeśli drugi atom wodoru się nie przyłączy, aż ten dodany z powrotem ulegnie odszczepieniu, cząsteczka powróci do stanu nienasyconego ale z częściową izomeryzacją. Tak właśnie podczas tylko częściowego uwodornienia tłuszczu, z kwasów tłuszczowych cis powstają kwasy trans. (podczas całkowitego uwodornienia także wiązania trans ulegają uwodornieniu i znikają).
Izomeryzacja trwalszego kwasu fumarowego w mniej trwały maleinowy następuje w reakcji rodnikowej z bromem lub w stężonych kwasach.
Podwójne wiązanie między atomami powstaje wskutek dodania jednego wiązania typu sigma i jednego typu pi. Następuje to po hydrydyzacji orbitali elektronowych, to jest swoistego wymieszania tworzącego orbitale o wyrównanej energii. Wiązanie sigma tworzą orbitale nakładające się na wprost, zaś wiązanie pi jest tworzone przez boczne nałożenie orbitali w kształcie klepsydry po obu stromach wiązania sigma:
W efekcie wiązanie to jest sztywne i płaskie, a grupy na końcach nie zmieniają ustawienia w zwyczajnych warunkach (wysoka temperatura lub naświetlenie mogą wywołać izomeryzację). W związku z tym faktem, gdy na czterech końcach wokół wiązania obecne są różne podstawniki, możliwe stają się różne izomery.
W najprostszym przypadku na dwóch końcach pojawiają się dalsze organiczne części cząsteczki, zaś dwa pozostałe zajmują wodory. Przyjęto więc zasadę nazewnictwa, wedle której izomerami cis są cząsteczki, w których grupy organiczne znajdują się po tej samej stronie, a izomerami trans cząsteczki, w których grupy ustawione są po przeciwnych stronach:
Czasem też korzysta się z tego układu gdy przy wiązaniu pojawiają się inne podstawniki, ale takie same, na przykład dwa podstawniki chlorowe.
Z przedrostkami określającymi izomerię wiązań podwójnych możemy spotkać się w nazwach pospolitych. Słynne w ostatnich latach tłuszcze trans, to tłuszcze zawierające wyłącznie-trans nienasycone kwasy tłuszczowe. Układ taki nadaje im generalnie liniowy kształt co ma wpływ na właściwości fizyczne - tłuszcze trans mają wyższą temperaturę topnienia z powodu ściślejszego przylegania prostych cząsteczek co zwiększa oddziaływania między nimi.
Tłuszcze zawierające przynajmniej jedno wiązanie cis są bardziej wygięte, co utrudnia ścisłe upakowanie. Przykładowo kwas oleinowy, będący głównym kwasem tłuszczowym oliwki z oliwek, posiada tylko jedno wiązanie podwójne na 9 węglu (omega-9) i ma ono układ cis, przez co cząsteczka nabiera wygiętego kształtu a sam związek ma temperaturę topnienia 13°C. Jego izomer trans to kwas elaidynowy o temperaturze topnienia 45°C. Oznacza to, że ten pierwszy pozostaje płynny w temperaturze pokojowej, zaś ten drugi pozostaje stały nawet w temperaturze ludzkiego ciała.
Związkiem o dużej ilości wiązań podwójnych w układzie trans jest karoten, pomarańczowy barwnik marchwi. Z kolei przykładem związku z dużą ilością samych tylko wiązań cis jest bardzo rzadki kwas dokozoheksaenowy (DHA), w którym sześć kolejnych takich wiązań skręca jego cząsteczkę w kółeczko:
W ostatnich dekadach zwraca się uwagę na dostarczanie wraz z dietą odpowiedniej ilości tłuszczy z kwasami cis, które pełnią w organizmie różne funkcje biologiczne.
Ten typ izomerii występuje też w związkach pierścieniowych z wiązaniami pojedynczymi. W takim przypadku cały pierścień pełni rolę drugiego wiązania, powstrzymując rotację sąsiadujących grup. Izomerem cis jest związek, gdy podstawniki na sąsiednich węglach są położone po tej samej stronie pierścienia, a trans gdy po przeciwnych:
Związki różniące się geometrią wokół wiązania podwójnego mogą posiadać różne właściwości nie tylko fizyczne ale i chemiczne. W układzie Cis grupy po obu stronach mogą silniej ze sobą oddziaływać. Przykładem mogą być najprostsze nienasycone kwasy dikarboksylowe - fumarowy i maleinowy. Ten pierwszy zawiera dwie grupy karboksylowe w układzie trans, a więc po przeciwnych stronach. Dzięki temu w kryształach dość chętnie tworzą wiązania wodorowe między cząsteczkami, sam związek ma więc stosunkowo dużą temperaturę topnienia (287 °C ) i jest słabo rozpuszczalny w wodzie.
Natomiast kwas maleinowy posiada dwie grupy karboksylowe w układzie cis, po tej samej stronie, które w tym bliskim położeniu tworzą wewnątrzcząsteczkowe wiązanie wodorowe, kosztem tych pomiędzy cząsteczkami. Słabsze oddziaływania między cząsteczkami w krysztale zwiększają rozpuszczalność w wodzie oraz obniżają temperaturę topnienia niemal dwa razy. (135 °C ) W dodatku utworzenie wewnętrznego wiązania wodorowego do jednej z grup karboksylowym powoduje, że niezwiązany wodór z tej drugiej łatwiej ulega odszczepieniu, przez co kwas maleinowy jest w roztworach silniejszym kwasem niż fumarowy (pKa = 1,9 wobec 3,0). W niektórych przypadkach izomery geometryczne mogą różnić się kolorem.
Izomeria geometryczna może też mieć znaczenie dla stabilności związku. Stosunkowo duże grupy organiczne przeszkadzają sobie w przestrzeni a nawet odpychają się, dlatego ułożenie ich po tej samej stronie, w zbliżeniu, jest bardziej niekorzystne energetycznie. Objawia się to wyższą wartością ciepła spalania dla izomerów cis o dużych grupach niż dla izomerów trans. W warunkach osłabiających lub przejściowo likwidujących wiązanie podwójne obserwuje się izomeryzację i częściej wówczas ustala się równowaga z przewagą układu trans, jako mniej naprężonego.
Podobny typ izomerii występuje też w związkach nieorganicznych - jeśli w kompleksie metalu z różnymi ligandami tworzona jest płaska, kwadratowa struktura, zaś kompleks tworzą dwa rodzaje ligandów, możliwe stają się dwa izomery - kompleksy cis, gdy dwa takie same ligandy znajdują się obok siebie, i kompleksy trans, gdy są położone w przeciwnych narożach kwadratu:
W powyższym przypadku kompleks nazywany cisplatyną jest znanym lekiem przeciwnowotworowym.
E/Z
Ale przypadek gdy przy wiązaniu podwójnym dwa podstawniki to wodory a kolejne dwa to grupy organiczne, jest za prosty. Jeśli w takim miejscu pojawią się cztery różne podstawniki, wówczas stosuje się nazewnictwo w systemie E/Z. Oznaczenia pochodzą od niemieckich słów "zusammen" czyli "razem" oraz "entgegen" czyli "naprzeciwko".
Zasada nazewnictwa opiera się o ważność podstawników, główną braną pod uwagę regułą jest ciężar atomowy, kolejną stopień rozbudowania czy obecność wiązań wielokrotnych. Jeśli dwie kolejno najważniejsze grupy są położone po tej samej stronie, to układ oznacza się jako Z, zaś gdy są po przeciwnych stronach, to jako E.
Warto zauważyć, że w zasadzie jest to system bardziej ogólny, w ramach którego izomeria trans/cis stanowi szczególny przypadek.
Izomeryzacja
Proces w wyniku którego następuje obrót grup i zamiana jednego izomeru w drugi, to izomeryzacja. Ze względu na sztywność wiązania podwójnego, proces musi przebiegać poprzez stan pośredni, w którym jest ono osłabione lub nie istnieje. Jedną odmian jest fotoizomeryzacja, gdzie obrót staje się możliwy dzięki energii z pochłoniętego światła. Wiązanie podwójne pochłania kwant światła i przechodzi w stan wzbudzony, w którym nie jest już tak sztywne i staje się podatne na ruchy skręcające. Może więc nastąpić obrót i zamiana w inny izomer.
W przypadku wielu związków organicznych, zakres energii pochłanianego światła lokuje je w obrębie ultrafioletu, czasem też bliżej fioletu z zakresu widzialnego, co nadaje wielu związkom nieco żółtawy kolor. Wiele związków używanych jako filtry UV w kremach do opalania to cząsteczki z wiązaniem podwójnym, które bardzo łatwo izomeryzują w obie strony. Dość chętnie używane są na przykład pochodne kwasu cynamonowego, w formie naturalnej w układzie trans :
Inny przykład to enzokamen, oznaczany jako 4-MBC, będący specyficzną pochodną kamfory:
Fotoizomeryzacja ma znaczenie dla procesu widzenia. W fotoreceptorach oka zawarty jest kompleks białka opsyny z retinalem, czyli aktywną formą witaminy A, która jest cząsteczką z trzema wiązaniami podwójnymi. W formie aktywnej w foceptorze retinal występuje w geometrii 11-cis, a więc wygiętej. Pod wpływem kwantu światła następuje izomeryzacja, przez co cząsteczka się prostuje. Do obu końców cząsteczki przyczepione są fragmenty białkowej opsyny, która po zmianie kształtu retinalu, pociągnięta mechanicznie dwoma końcami musi zmienić kształt. Generuje to kaskadę dalszych reakcji prowadzących w końcu do wytworzenia impulsu nerwowego.
Izomeryzacja może też zajść pod wpływem wysokiej temperatury i reakcji chemicznych. Przykładowo podczas uwodornienia tłuszczów nienasyconych przy produkcji margaryny, reakcja przyłączenia jednego atomu wodoru do jednego z wiązań podwójnych kwasu tłuszczowego, zamienia go w formę karboanionu. Jest to struktura niepłaska z wiązaniem pojedynczym, w której może nastąpić obrót cząsteczki. Jeśli drugi atom wodoru się nie przyłączy, aż ten dodany z powrotem ulegnie odszczepieniu, cząsteczka powróci do stanu nienasyconego ale z częściową izomeryzacją. Tak właśnie podczas tylko częściowego uwodornienia tłuszczu, z kwasów tłuszczowych cis powstają kwasy trans. (podczas całkowitego uwodornienia także wiązania trans ulegają uwodornieniu i znikają).
Izomeryzacja trwalszego kwasu fumarowego w mniej trwały maleinowy następuje w reakcji rodnikowej z bromem lub w stężonych kwasach.
czwartek, 26 kwietnia 2018
7 lat blogowania
Tak więc mija kolejna rocznica, a ja nadal piszę bloga.
Na początek podsumowanie statystyk. Wewnętrzny licznik bloga zanotował 1 200 tys. wejść, szacuję że około 20% to boty i różne spamy. Średnia dzienna przeglądalność to około 500-600. Liczba dodanych artykułów doszła do 274.
W ciągu tego roku od poprzedniego podsumowania najchętniej czytanymi nowymi artykułami były:
* Poison Story (8.) - Podstępny grzybek (18 600 wyświetleń)
* Detoksy-Mistyfikacje (16 300 wyświetleń)
* Jaki może być największy atom? (11 950)
* Poison Story (9.) - Błękitny kwiat (9030)
* Spóźnione Pierwiastki (8825)
* Jak zrobić zdjęcie atomu? - (8450)
Bardzo mnie te wyniki cieszą, pokazują bowiem, że forma bloga nie opada.
Co tam u mnie? Cóż, wydarzeniem roku z pewnością była rezygnacja z kontynuowania studiów doktoranckich na UW. Niezbyt dobrze się tam czułem, warunki płacowe były kiepskie, w dodatku zamieszanie związane w promotorem i zmiana tematyki na bardziej teoretyczną w trakcie trwania, budziły obawy czy na pewno się ze wszystkim wyrobię.
Ale nie martwcie się, znalazłem sobie jakąś alternatywę.
Na początek podsumowanie statystyk. Wewnętrzny licznik bloga zanotował 1 200 tys. wejść, szacuję że około 20% to boty i różne spamy. Średnia dzienna przeglądalność to około 500-600. Liczba dodanych artykułów doszła do 274.
W ciągu tego roku od poprzedniego podsumowania najchętniej czytanymi nowymi artykułami były:
* Poison Story (8.) - Podstępny grzybek (18 600 wyświetleń)
* Detoksy-Mistyfikacje (16 300 wyświetleń)
* Jaki może być największy atom? (11 950)
* Poison Story (9.) - Błękitny kwiat (9030)
* Spóźnione Pierwiastki (8825)
* Jak zrobić zdjęcie atomu? - (8450)
Bardzo mnie te wyniki cieszą, pokazują bowiem, że forma bloga nie opada.
 |
| Moje małe hanami |
Ale nie martwcie się, znalazłem sobie jakąś alternatywę.
czwartek, 12 kwietnia 2018
Spóźnione pierwiastki
Wiemy z pewnością, że w dawnych czasach nowe pierwiastki znajdowano po prostu w naturze, wyodrębniając je z minerałów. Oraz, że po pewnym czasie się nam skończyły i zaczęliśmy sztucznie otrzymywać nowe, nietrwałe. Kiedy jednak nastąpiło to przejście? Jaki występujący w naturze pierwiastek był tak rzadki i nieuchwytny, że odkryto go na samym końcu?
Złotym okresem odkryć pierwiastków był zdecydowanie XIX wiek, czas gdy rozwój chemii poszedł ostro do przodu, zaś kolejne pokolenia ciekawskich badaczy wsadzały do próbówek co tylko wpadło im w oko. O ile do końca XVIII wieku znano około 34 pierwiastki (chlor, odkryty w 1784 przez Scheelego początkowo uznawano za bardzo trwały tlenek) to do końca XIX wieku odkryto już 49. Natomiast lista naturalnych pierwiastków w wieku XX jest bardzo krótka.
89
Wiek otwiera pierwiastek Aktyn, którego historia była nieco skomplikowana. Nieco wcześniej, w 1899 roku chemik Andree Louis Debierne korzystając z materiałów otrzymanych z blendy smolistej, które zostały małżonkom Curie po wyizolowaniu Radu i Polonu, uzyskał z nich wysoce radioaktywną sól nieznanego pierwiastka. Ogłosił odkrycie, nadając mu nazwę aktyn, był bowiem radio-aktywny.
Następnie w roku 1902 Friedrich Oscar Giesel zajmując się przeróbką tejże rudy uranu, uzyskał sól bardzo radioaktywnego pierwiastka, który nazwał Emanium, bowiem próbki świeciły w ciemnościach. Gdy minęło parę lat, chemicy uznali, że najprawdopodobniej oba pierwiastki są jednym, w związku z czym pierwszeństwo odkrycia i nazwa przypadły Debierne.
Dopiero w latach 70. chemicy przyjrzeli się uważniej pierwszym doniesieniom. Aktyn Dobiernera opisany w pierwszych artykułach, miał jednak mimo wszystko inne właściwości, niż ten wyizolowany później i poddany dalszym badaniom. Po przeanalizowaniu metody otrzymania uznano, że jednak to Giesel miał rację i to on był odkrywcą pierwiastka. Nazwy jednak nie zmieniono z powrotem na Emanium, bo minęło już kilka dekad i za dużo było zmieniania.[1]
71
Lutet był jednym z ostatnich lantanowców. Jest to grupa pierwiastków, zwykle na tablicach wyrzucana pod resztę pierwiastków, ze względu na właściwości chemiczne niezwykle podobne w jej obrębie. To podobieństwo było zresztą przyczyną problemów w izolacji. Co chwila okazywało się, że zgłoszony nowy lantanowiec w rzeczywistości jest mieszanką dwóch różnych, zaś któryś z tych po wyizolowaniu i zgłoszeniu, ponownie okazywał się mieszaniną. Na końcu takiego ciągu znalazł się lutet.
Zaczęło się od badania minerałów tzw. "ziem rzadkich" nazwanych od nieczęstego występowania. Fiński mineralog John Gadolin w kopalni koło szwedzkiej wioski Ytterby odnalazł minerał, z którego wydzielił tlenek nieznanego pierwiastka. Od nazwy miejsca z którego pochodził, nazwano go Yttrium, czyli po polsku itr. Następnie po kilku dekadach jego kolega po fachu Carl Mossander odkrył, że itr zawiera domieszkę dwóch innych, podobnych pierwiastków, którym nadał niewymyślne nazwy urobione z podziału na sylaby tej pierwotnej - terb i erb. Po kolejnych dekadach Szwajcar de Marignac odkrył, że z kolei erb też nie jest czysty i wydzielił z niego kolejny pierwiastek. Będąc wierny tradycji nadał mu łudząco podobną nazwę Ytterbium, czyli itreb. Jak łatwo się domyśleć, działalność tych panów przyprawia o ból głowy studentów chemii nieorganicznej, którym wszystkie te nazwy się mylą. Natomiast mała szwedzka wioska może się pochwalić tym, że od niej nazwano aż cztery pierwiastki.
W międzyczasie okazało się, że erb zawiera jeszcze domieszkę holmu i tulu, potem, że holm zawiera w sobie dysproz, a znany od dawna didym to mieszanka neodymu i prazeodymu. Gdy na swoje miejsce wskoczyły jeszcze gadolin, samar i europ, w tak uformowanej grupie pozostały tylko dwie irytujące dziury - pierwiastek 61 i pierwiastek 71.
Dla badaczy dość oczywistym pomysłem było szukanie wśród już znanych i wydzielonych pierwiastków. A nuż któryś okaże się mieszanką. Wreszcie w 1907 roku na trop tej samej substancji wpadli równocześnie trzej badacze - Francuz Gregore Urbain i Austriak Carl Auer von Welsbach i Amerykanin Charles James. Ten ostatni opublikował doniesienie dość późno, i nie sposób było mu stawać w szranki w boju o pierwszeństwo, natomiast pozostali panowie wszczęli kłótnię.
Urbain zaproponował dla pierwiastka nowo wydzielonego i dla oczyszczonego itrebu nazwy lutet - od zlatynizowanej nazwy regionu we Francji - i neoitreb; von Welsbach zaproponował cassiuopeium i abldebaranium, od nazw obiektów astronomicznych. Ponieważ pierwiastek nie może posiadać różnych nazw, trzeba było w końcu coś ustalić. W 1909 roku komisja zajmująca się ustalaniem dokładnej masy atomowej pierwiastków rozstrzygnęła spór, uznając że Urbain doniósł o wydzieleniu nowego pierwiastka o miesiąc wcześniej, był zatem pierwszy i może nadać pierwiastkowi nazwę.
Mimo to jeszcze do lat 50. w krajach niemieckojęzycznych używano nazwy Cassiopeium i symbolu Cp. [2]
75
Gdy losy nazwy pierwiastka 71 jeszcze się ważyły, rozpoczynało się podobne zamieszanie z pierwiastkiem 75.
Po odkryciu metody wyznaczania prawdziwej liczby atomowej i uporządkowaniu pierwiastków (zamieniono kolejnością potas i argon, które ułożone wedle masy atomowej nie bardzo pasowały do grup) okazało się, że w grupie platynowców lekkich jest jeszcze jeden pierwiastek nieodkryty. Różne grupy chemików zaczęły więc badać spektroskopowo rudy platyny.
W 1925 roku małżeństwo niemieckich chemików Ida i Otto Noddack ogłosiło wykrycie metodą spektroskopii rentgenowskiej śladów nowego pierwiastka w rudach platyny i minerale kolumbicie. Wraz z współpracownikiem Otto Bergiem wyizolowali 1 g soli tego pierwiastka, po przerobieniu 600 kg kolumbitu. Nazwali go renem, od nazwy rzeki na granicy francusko-niemieckiej.
W późniejszych badaniach ten sam zespół ogłosił wykrycie śladów pierwiastka 43, którego też brakowało w układzie okresowym, proponując dla niego nazwę Masurium, dość zresztą kontrowersyjną (pochodzi od latynizacji nazwy Mazur i w uzasadnieniu miała upamiętniać rdzennie niemiecki region). Tego wyniku nie udało się jednak powtórzyć innym badaczom.
Następnie minęło kilka dekad gdy pojawiło się doniesienie, że nawet w przypadku renu zostali uprzedzeni. W 1909 roku japoński badacz Masataka Ogawa ogłosił wykrycie pierwiastka 43 w thorianicie. Wyizolował niewielką próbkę i nazwał odkryty pierwiastek Nipponium, od jednej z nazw Japonii. Późniejsi badacze z innych krajów nie mogli powtórzyć tego odkrycia, więc nie zostało ono uznane. Dopiero w naszych czasach powrócono do oceny jego dzieł. Po przeanalizowaniu oryginalnych zdjęć z zapisem widma rentgenowskiego Nipponium stwierdzono, że wprawdzie nie zawierały pierwiastka 43, ale mogły zawierać ren, co oznaczałoby, że to Ogawa jest odkrywcą tego pierwiastka mimo błędnego przypisania. Stąd różne źródła uznają za odkrywcę renu albo Ogawę, albo Noddacków albo całą trójkę bez wdawania się w spory.[3]
72
W międzyczasie doszło natomiast do odkrycia pierwiastka 72. Pierwsze zgłoszenie w tej sprawie opublikował znany już nam Urbain przy okazji prac nad oczyszczaniem lantanowców, wydawało się bowiem, że szukany element należy do tej grupy. Ogłoszony w 1911 pierwiastek nazwał Celtium, lecz ponownie nie udało się tego odkrycia potwierdzić innymi metodami. W dużo późniejszym czasie, w związku ze sporami o pierwszeństwo, przebadano spektroskopowo próbki Urbaina, nie znajdując w nich pierwiastka 72.
W 1923 roku pracujący w Kopenhadze fizyk Niels Bohr zasugerował, że z praw okresowości można wywnioskować podobieństwo chemiczne pierwiastka 72 do znanego już cyrkonu, w związku z czym lepiej szukać w jego rudach. Sugestię podłapali chemicy Georg von Hevesy i Dirck Costler. Zbadali oni cyrkon pochodzący z norweskich rud i metodą spektroskopii rentgenowskiej wykazali ślady szukanego pierwiastka. Przy pomocy mozolnej krystalizacji frakcyjnej udało się oddzielić małą próbkę soli nowego pierwiastka. Od zlatynizowanej nazwy Kopenhagi, nazwano go hafnem.
Uznając pierwszeństwo Ogawy w odkryciu renu, hafn okazuje się ostatnim trwałym pierwiastkiem wyizolowanym z próbek naturalnych. Ale nie ostatnim w tym artykule.[4]
91
Istnienie jeszcze jednego pierwiastka między thorem i uranem było przewidywane jeszcze przez Mendelejewa. Ponieważ grupa Aktynowców nie była wtedy uznawana za odrębną, bo znano z niej tylko 2 pierwiastki, brakujący pod numerem 91 był uznawany za podobny do tantalu i w jego rudach go poszukiwano. Dlatego też wszyscy przeoczyli doniesienie Williama Crookesa, który w 1900 roku opisał wyizolowanie z soli uranu substancji, nazwanej przez niego uranem X. On sam nie opisał jej jako pierwiastka, sądził, że to raczej jakaś forma uranu nieco bardziej od niego promieniotwórcza. Na podstawie późniejszych analiz uznano, że uzyskał wtedy mieszankę thoru z pierwiastkiem 91, której dalej nie rozdzielał.
W 1913 roku Kazimierz Fajans i Oswald Göhring wyizolowali szukany pierwiastek badając produkty rozkładu promieniotwórczego uranu. Nazwali go brevium, czyli "krótkotrwały" ocenili bowiem jego czas półtrwania na zaledwie 6 godzin. Następnie w 1917 roku grupa Otto Hanna i Lisie Meitner wyizolowała z rud uranu długożyjący izotop nazwany przez nich protaktynem, bowiem rozpadał się do aktynu. W podobnym czasie na ślad pierwiastka wpadł jeszcze John Cranston, ale nie mógł opublikować odkrycia, bo powołano go na wojnę.
Zawikłany węzeł odkryć przecięła dopiero po drugiej wojnie światowej IUPAC, uznając prawo do nazwania pierwiastka dla Hanna i Meitner, ponieważ wyizolowali oni izotop o najdłuższym okresie półtrwania. Historycy nauki w związku z tym jako odkrywców uznają albo Hanna i Meitner, albo całą czwórkę z Fajansem i Goeringiem.[5]
87
Dziura w układzie okresowym na miejscu 43 została załatana sztucznie, gdy w 1934 roku bombardując neutronami molibden otrzymano technet. Dziura w miejscu 61 została załatana sztucznie wraz z otrzymaniem prometu, tymczasem tuż przed wybuchem II wojny światowej francuskiej chemiczce udało się wyizolować ostatni wyodrębniony ze źródeł naturalnych pierwiastek.
Uczennica Marii Curie Skłodowskiej, chemiczka Marguerite Perey, zajmowała się głównie pracą nad izolowaniem i oczyszczaniem aktynu z próbek lantanowców.
Pod koniec lat 30, przy pomocy precyzyjnych badań aktywności wykazała, że część próbek aktynu jest silniej promieniotwórcza od innych a zakres energii emitowanych cząstek nie pasował do izotopów aktynu. Wniosek, że zawiera dodatek czegoś silniej radioaktywnego nasuwał się sam, zwłaszcza w takiej pracowni. Wprawdzie badana substancja rozpadała się bardzo szybko, ale badając aktywność różnych roztworów, którymi przemywano próbki aktynu stwierdziła, że jest to pierwiastek o właściwościach litowców, czyli poszukiwany od dawna eka-cez.
Perey ogłosiła wyniki w 1939 roku, proponując nazwę catium i symbol Cm, w nawiązaniu do przewidywanej własności najwyższej elektrododatności. Kilka lat później jej przełożona Irena Juliot-Curie zgłosiła zastrzeżenia do takiej nazwy. Zaproponowany skrót zbiegł się ze skrótem proponowanym dla sztucznego pierwiastka kiuru, nazwanego zresztą na cześć jej matki. Ponadto anglojęzycznym chemikom catium kojarzyło się z kotami. Dość, że Perrey zaproponowała ostatecznie zmianę nazwy na francium, czyli frans, od nazwy swojego kraju i ta propozycja została w końcu zaakceptowana.[6]
Był to ostatni pierwiastek, którego odkrywcy izolowali ze źródeł naturalnych. Było co prawda kilka, które otrzymano sztucznie a potem odkryto w śladowych ilościach w naturze, ale to już nie to samo.
---------
* C Fry, M Thoennessen, Discovery of the Actimium, Thoriom, Protactinium and Uranium Izotopes
[1] https://en.wikipedia.org/wiki/Actinium
[2] https://en.wikipedia.org/wiki/Lutetium
[3] https://en.wikipedia.org/wiki/Rhenium
[4] https://en.wikipedia.org/wiki/Hafnium
[5] https://en.wikipedia.org/wiki/Protactinium
[6] https://en.wikipedia.org/wiki/Francium
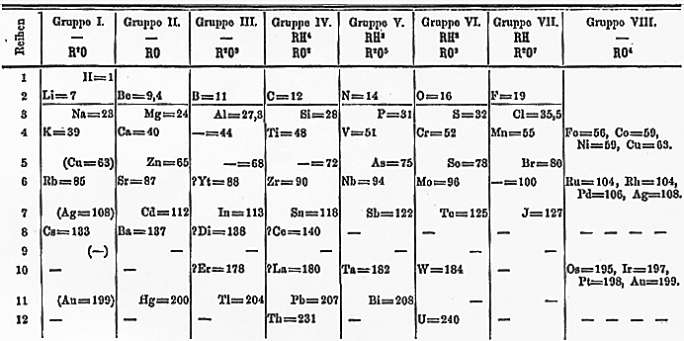 |
| Jedna ze starych wersji tablicy Mendelejewa |
Złotym okresem odkryć pierwiastków był zdecydowanie XIX wiek, czas gdy rozwój chemii poszedł ostro do przodu, zaś kolejne pokolenia ciekawskich badaczy wsadzały do próbówek co tylko wpadło im w oko. O ile do końca XVIII wieku znano około 34 pierwiastki (chlor, odkryty w 1784 przez Scheelego początkowo uznawano za bardzo trwały tlenek) to do końca XIX wieku odkryto już 49. Natomiast lista naturalnych pierwiastków w wieku XX jest bardzo krótka.
89
Wiek otwiera pierwiastek Aktyn, którego historia była nieco skomplikowana. Nieco wcześniej, w 1899 roku chemik Andree Louis Debierne korzystając z materiałów otrzymanych z blendy smolistej, które zostały małżonkom Curie po wyizolowaniu Radu i Polonu, uzyskał z nich wysoce radioaktywną sól nieznanego pierwiastka. Ogłosił odkrycie, nadając mu nazwę aktyn, był bowiem radio-aktywny.
 |
| Świecące pod wpływem własnej promieniotwórczości sole aktynu |
Dopiero w latach 70. chemicy przyjrzeli się uważniej pierwszym doniesieniom. Aktyn Dobiernera opisany w pierwszych artykułach, miał jednak mimo wszystko inne właściwości, niż ten wyizolowany później i poddany dalszym badaniom. Po przeanalizowaniu metody otrzymania uznano, że jednak to Giesel miał rację i to on był odkrywcą pierwiastka. Nazwy jednak nie zmieniono z powrotem na Emanium, bo minęło już kilka dekad i za dużo było zmieniania.[1]
71
Lutet był jednym z ostatnich lantanowców. Jest to grupa pierwiastków, zwykle na tablicach wyrzucana pod resztę pierwiastków, ze względu na właściwości chemiczne niezwykle podobne w jej obrębie. To podobieństwo było zresztą przyczyną problemów w izolacji. Co chwila okazywało się, że zgłoszony nowy lantanowiec w rzeczywistości jest mieszanką dwóch różnych, zaś któryś z tych po wyizolowaniu i zgłoszeniu, ponownie okazywał się mieszaniną. Na końcu takiego ciągu znalazł się lutet.
Zaczęło się od badania minerałów tzw. "ziem rzadkich" nazwanych od nieczęstego występowania. Fiński mineralog John Gadolin w kopalni koło szwedzkiej wioski Ytterby odnalazł minerał, z którego wydzielił tlenek nieznanego pierwiastka. Od nazwy miejsca z którego pochodził, nazwano go Yttrium, czyli po polsku itr. Następnie po kilku dekadach jego kolega po fachu Carl Mossander odkrył, że itr zawiera domieszkę dwóch innych, podobnych pierwiastków, którym nadał niewymyślne nazwy urobione z podziału na sylaby tej pierwotnej - terb i erb. Po kolejnych dekadach Szwajcar de Marignac odkrył, że z kolei erb też nie jest czysty i wydzielił z niego kolejny pierwiastek. Będąc wierny tradycji nadał mu łudząco podobną nazwę Ytterbium, czyli itreb. Jak łatwo się domyśleć, działalność tych panów przyprawia o ból głowy studentów chemii nieorganicznej, którym wszystkie te nazwy się mylą. Natomiast mała szwedzka wioska może się pochwalić tym, że od niej nazwano aż cztery pierwiastki.
 |
| Tlenki kilku lantanowców, tzw "zemie rzadkie" |
W międzyczasie okazało się, że erb zawiera jeszcze domieszkę holmu i tulu, potem, że holm zawiera w sobie dysproz, a znany od dawna didym to mieszanka neodymu i prazeodymu. Gdy na swoje miejsce wskoczyły jeszcze gadolin, samar i europ, w tak uformowanej grupie pozostały tylko dwie irytujące dziury - pierwiastek 61 i pierwiastek 71.
Dla badaczy dość oczywistym pomysłem było szukanie wśród już znanych i wydzielonych pierwiastków. A nuż któryś okaże się mieszanką. Wreszcie w 1907 roku na trop tej samej substancji wpadli równocześnie trzej badacze - Francuz Gregore Urbain i Austriak Carl Auer von Welsbach i Amerykanin Charles James. Ten ostatni opublikował doniesienie dość późno, i nie sposób było mu stawać w szranki w boju o pierwszeństwo, natomiast pozostali panowie wszczęli kłótnię.
Urbain zaproponował dla pierwiastka nowo wydzielonego i dla oczyszczonego itrebu nazwy lutet - od zlatynizowanej nazwy regionu we Francji - i neoitreb; von Welsbach zaproponował cassiuopeium i abldebaranium, od nazw obiektów astronomicznych. Ponieważ pierwiastek nie może posiadać różnych nazw, trzeba było w końcu coś ustalić. W 1909 roku komisja zajmująca się ustalaniem dokładnej masy atomowej pierwiastków rozstrzygnęła spór, uznając że Urbain doniósł o wydzieleniu nowego pierwiastka o miesiąc wcześniej, był zatem pierwszy i może nadać pierwiastkowi nazwę.
Mimo to jeszcze do lat 50. w krajach niemieckojęzycznych używano nazwy Cassiopeium i symbolu Cp. [2]
75
Gdy losy nazwy pierwiastka 71 jeszcze się ważyły, rozpoczynało się podobne zamieszanie z pierwiastkiem 75.
Po odkryciu metody wyznaczania prawdziwej liczby atomowej i uporządkowaniu pierwiastków (zamieniono kolejnością potas i argon, które ułożone wedle masy atomowej nie bardzo pasowały do grup) okazało się, że w grupie platynowców lekkich jest jeszcze jeden pierwiastek nieodkryty. Różne grupy chemików zaczęły więc badać spektroskopowo rudy platyny.
W 1925 roku małżeństwo niemieckich chemików Ida i Otto Noddack ogłosiło wykrycie metodą spektroskopii rentgenowskiej śladów nowego pierwiastka w rudach platyny i minerale kolumbicie. Wraz z współpracownikiem Otto Bergiem wyizolowali 1 g soli tego pierwiastka, po przerobieniu 600 kg kolumbitu. Nazwali go renem, od nazwy rzeki na granicy francusko-niemieckiej.
W późniejszych badaniach ten sam zespół ogłosił wykrycie śladów pierwiastka 43, którego też brakowało w układzie okresowym, proponując dla niego nazwę Masurium, dość zresztą kontrowersyjną (pochodzi od latynizacji nazwy Mazur i w uzasadnieniu miała upamiętniać rdzennie niemiecki region). Tego wyniku nie udało się jednak powtórzyć innym badaczom.
Następnie minęło kilka dekad gdy pojawiło się doniesienie, że nawet w przypadku renu zostali uprzedzeni. W 1909 roku japoński badacz Masataka Ogawa ogłosił wykrycie pierwiastka 43 w thorianicie. Wyizolował niewielką próbkę i nazwał odkryty pierwiastek Nipponium, od jednej z nazw Japonii. Późniejsi badacze z innych krajów nie mogli powtórzyć tego odkrycia, więc nie zostało ono uznane. Dopiero w naszych czasach powrócono do oceny jego dzieł. Po przeanalizowaniu oryginalnych zdjęć z zapisem widma rentgenowskiego Nipponium stwierdzono, że wprawdzie nie zawierały pierwiastka 43, ale mogły zawierać ren, co oznaczałoby, że to Ogawa jest odkrywcą tego pierwiastka mimo błędnego przypisania. Stąd różne źródła uznają za odkrywcę renu albo Ogawę, albo Noddacków albo całą trójkę bez wdawania się w spory.[3]
72
W międzyczasie doszło natomiast do odkrycia pierwiastka 72. Pierwsze zgłoszenie w tej sprawie opublikował znany już nam Urbain przy okazji prac nad oczyszczaniem lantanowców, wydawało się bowiem, że szukany element należy do tej grupy. Ogłoszony w 1911 pierwiastek nazwał Celtium, lecz ponownie nie udało się tego odkrycia potwierdzić innymi metodami. W dużo późniejszym czasie, w związku ze sporami o pierwszeństwo, przebadano spektroskopowo próbki Urbaina, nie znajdując w nich pierwiastka 72.
 |
| Próbki metalicznego hafnu pokrytego warstewką tlenków |
W 1923 roku pracujący w Kopenhadze fizyk Niels Bohr zasugerował, że z praw okresowości można wywnioskować podobieństwo chemiczne pierwiastka 72 do znanego już cyrkonu, w związku z czym lepiej szukać w jego rudach. Sugestię podłapali chemicy Georg von Hevesy i Dirck Costler. Zbadali oni cyrkon pochodzący z norweskich rud i metodą spektroskopii rentgenowskiej wykazali ślady szukanego pierwiastka. Przy pomocy mozolnej krystalizacji frakcyjnej udało się oddzielić małą próbkę soli nowego pierwiastka. Od zlatynizowanej nazwy Kopenhagi, nazwano go hafnem.
Uznając pierwszeństwo Ogawy w odkryciu renu, hafn okazuje się ostatnim trwałym pierwiastkiem wyizolowanym z próbek naturalnych. Ale nie ostatnim w tym artykule.[4]
91
Istnienie jeszcze jednego pierwiastka między thorem i uranem było przewidywane jeszcze przez Mendelejewa. Ponieważ grupa Aktynowców nie była wtedy uznawana za odrębną, bo znano z niej tylko 2 pierwiastki, brakujący pod numerem 91 był uznawany za podobny do tantalu i w jego rudach go poszukiwano. Dlatego też wszyscy przeoczyli doniesienie Williama Crookesa, który w 1900 roku opisał wyizolowanie z soli uranu substancji, nazwanej przez niego uranem X. On sam nie opisał jej jako pierwiastka, sądził, że to raczej jakaś forma uranu nieco bardziej od niego promieniotwórcza. Na podstawie późniejszych analiz uznano, że uzyskał wtedy mieszankę thoru z pierwiastkiem 91, której dalej nie rozdzielał.
W 1913 roku Kazimierz Fajans i Oswald Göhring wyizolowali szukany pierwiastek badając produkty rozkładu promieniotwórczego uranu. Nazwali go brevium, czyli "krótkotrwały" ocenili bowiem jego czas półtrwania na zaledwie 6 godzin. Następnie w 1917 roku grupa Otto Hanna i Lisie Meitner wyizolowała z rud uranu długożyjący izotop nazwany przez nich protaktynem, bowiem rozpadał się do aktynu. W podobnym czasie na ślad pierwiastka wpadł jeszcze John Cranston, ale nie mógł opublikować odkrycia, bo powołano go na wojnę.
 |
| Protaktyn jest błyszczącym, złotawym metalem |
Zawikłany węzeł odkryć przecięła dopiero po drugiej wojnie światowej IUPAC, uznając prawo do nazwania pierwiastka dla Hanna i Meitner, ponieważ wyizolowali oni izotop o najdłuższym okresie półtrwania. Historycy nauki w związku z tym jako odkrywców uznają albo Hanna i Meitner, albo całą czwórkę z Fajansem i Goeringiem.[5]
87
Dziura w układzie okresowym na miejscu 43 została załatana sztucznie, gdy w 1934 roku bombardując neutronami molibden otrzymano technet. Dziura w miejscu 61 została załatana sztucznie wraz z otrzymaniem prometu, tymczasem tuż przed wybuchem II wojny światowej francuskiej chemiczce udało się wyizolować ostatni wyodrębniony ze źródeł naturalnych pierwiastek.
Uczennica Marii Curie Skłodowskiej, chemiczka Marguerite Perey, zajmowała się głównie pracą nad izolowaniem i oczyszczaniem aktynu z próbek lantanowców.
Pod koniec lat 30, przy pomocy precyzyjnych badań aktywności wykazała, że część próbek aktynu jest silniej promieniotwórcza od innych a zakres energii emitowanych cząstek nie pasował do izotopów aktynu. Wniosek, że zawiera dodatek czegoś silniej radioaktywnego nasuwał się sam, zwłaszcza w takiej pracowni. Wprawdzie badana substancja rozpadała się bardzo szybko, ale badając aktywność różnych roztworów, którymi przemywano próbki aktynu stwierdziła, że jest to pierwiastek o właściwościach litowców, czyli poszukiwany od dawna eka-cez.
Perey ogłosiła wyniki w 1939 roku, proponując nazwę catium i symbol Cm, w nawiązaniu do przewidywanej własności najwyższej elektrododatności. Kilka lat później jej przełożona Irena Juliot-Curie zgłosiła zastrzeżenia do takiej nazwy. Zaproponowany skrót zbiegł się ze skrótem proponowanym dla sztucznego pierwiastka kiuru, nazwanego zresztą na cześć jej matki. Ponadto anglojęzycznym chemikom catium kojarzyło się z kotami. Dość, że Perrey zaproponowała ostatecznie zmianę nazwy na francium, czyli frans, od nazwy swojego kraju i ta propozycja została w końcu zaakceptowana.[6]
 |
| 300 tysięcy atomów fransu w pułapce magnetycznej |
Był to ostatni pierwiastek, którego odkrywcy izolowali ze źródeł naturalnych. Było co prawda kilka, które otrzymano sztucznie a potem odkryto w śladowych ilościach w naturze, ale to już nie to samo.
---------
* C Fry, M Thoennessen, Discovery of the Actimium, Thoriom, Protactinium and Uranium Izotopes
[1] https://en.wikipedia.org/wiki/Actinium
[2] https://en.wikipedia.org/wiki/Lutetium
[3] https://en.wikipedia.org/wiki/Rhenium
[4] https://en.wikipedia.org/wiki/Hafnium
[5] https://en.wikipedia.org/wiki/Protactinium
[6] https://en.wikipedia.org/wiki/Francium
Subskrybuj:
Posty (Atom)