Z sitami molekularnymi student chemii zwykle spotyka się na pierwszych pracowniach laboratoryjnych, gdzie zawsze przy ogrzewaniu cieczy do wrzenia upomina się go "ale najpierw wrzuć do kolby sita molekularne" mające postać małych, twardych kuleczek. I bardzo możliwe, że aż do końca studiów będzie znał tylko takie ich zastosowanie. Niemniej co niektórych może jednak zastanowić, czym też są i czemu nazywa się je sitami, skoro wyglądają raczej jak małe granulki jakiejś masy ceramicznej?
Sita molekularne to granulki o tak dobranym składzie i metodzie produkcji, że są bardzo porowate, zaś te pory mają określoną wielkość pozwalającą wnikać wgłąb materiału cząsteczkom odpowiednio małym, zatrzymując cząsteczki za duże. Po prostu tylko cząsteczki mniejsze niż średnica poru będą w niego wchodzić i tym samym będą "odsiewane" od większych. Z tego też powodu najczęściej używa się sit do oddzielania niepożądanych, małocząsteczkowych zanieczyszczeń od cieczy i gazów.
Materiałem budującym sito molekularne są najczęściej syntetyczne minerały podobne do zeolitów posiadające w strukturze pory i kanały o dobrze zdefiniowanej wielkości. Najściślejsze mają pory o średnicy 3,4 i 5 Angstremów, czyli odpowiednio 0,3; 0,4 i 0,5 nanometra. Większe pory mają sita z porowatego szkła od 10 Å w górę. Sita o porach od 20 do 500 Angstremów mogą być stworzone z krzemionki koloidalnej, a te o jeszcze większych z krzemionki mezoporowatej. Ponadto w podobnym celu użyty może być węgiel aktywowany i niektóre porowate tworzywa sztuczne.
Generalnie więc w większości są to materiały niereaktywne, o dobrej wytrzymałości chemicznej i termicznej.
Jakie jest główne zastosowanie? Osuszanie.
Cząsteczka wody jest bardzo mała, szerokość na jaką odsunięte są atomy tlenu to 1,6 A, dlatego dość łatwo wchodzi w kanały porowatego materiału. Dodatkowo glinokrzemiany dość chętnie wiążą wodę czy to wiązaniami wodorowymi w grupach Si-H czy to przez przyciąganie do jonów. Dzięki temu po dodaniu sit do materiału normalnie słabo adsorbowanego, jak olej mineralny czy gaz ziemny, woda jest skutecznie odciągana.
Najdrobniejsze sita 3A mogą odciągać wodę od alkoholu i rozpuszczalników, których cząsteczki są zbyt duże aby wnikać w ich strukturę. Jest to jeden ze stosunkowo prostych sposobów uzyskania bezwodnego alkoholu - zwykle sprzedawany 95% alkohol zasypuje się odpowiednią ilością sit (pochłaniają wodę do 15-20% masy własnej) i zostawia w szczelnym pojemniku na kilkanaście godzin, potem odsącza lub destyluje aby oddzielić od pojawiającej się mineralnej zawiesiny.
Większe sita 4A i 5A mogą też wchłaniać alkohol etylowy, etan, eten i bywają używane do oddzielenia ich śladów z wielkocząsteczkowych rozpuszczalników. Chętnie korzysta z nich przemysł rafineryjny. Służą do usuwania z gazu ziemnego wody, kwasu mrówkowego, tlenków siarki, siarkowodoru a w odpowiednich warunkach też dwutlenku węgla. Jest to o tyle ważne, że nawet niewielkie ilości wody mogą zapychać instalacje podczas przetaczania gazu skroplonego, oraz wpływają korozyjnie na gazociągi.
Odmiany o porach 10-15 A mogą oddzielać węglowodory aromatyczne od ciekłych węglowodorów, a także służyć do rozdziału gazów. Odmiany mezoporowe, powyżej 100 A, mogą być użyte do rozdziału biomolekuł i krótkich peptydów.
Sita o odpowiednio dobranym składzie działają też jako wymieniacze jonowe, mogą pochłaniać z wody i ścieków metale ciężkie, chętnie też chłoną amoniak i jony amonowe.
Obok granulek żelu krzemionkowego sita molekularne są też jednymi z najczęściej używanych pochłaniaczy wilgoci w opakowaniach leków, żywności i elektroniki.
Jako materiał dla wytwarzania sit molekularnych najczęściej używa się zeolitów, bądź to naturalnych bądź otrzymywanych sztucznie. Sama nazwa "zeolit" znaczy dosłownie "wrzący kamień" i wywodzi się z ciekawej właściwości zbitych form. Aby z uwodnionego zeolitu usunąć wodę musimy go ogrzewać do odpowiednio dużej temperatury przez pewien czas. Jak zauważył pod koniec XIX wieku szwedzki mineralog Axel Frederik Cronstedt, proces odwrotny po polaniu wodą dobrze wysuszonego minerału przebiegał z wydzieleniem na tyle dużej ilości ciepła, że powstawała para a woda którą go polano zapieniła się.
Zeolity powstają najczęściej w skałach wulkanicznych i piroklastycznych w wyniku reakcji roztworów bogatych w krzem, glin i kationy alkaliczne z zasadami, często w warunkach hydrotermalnych. Krystalizują w pustkach skalnych i kanałach tworząc skupienia włókniste, szczotkowate lub kuliste. Mogą też powstawać jako spoiwo między ziarnami osadów zagrzebanych na dużej głębokości. Obecnie najwięcej zeolitów wydobywa się w Chinach, Korei Południowej i Japonii, w Europie najwięcej wydobywa ich Słowacja.
Jednak naturalne zeolity nie nadają się do niektórych zastosowań, głównie z powodu obecności zanieczyszczeń, stąd też zaczęto produkować je syntetycznie.
Produkcja generalnie rzecz biorąc jest dość prosta - strukturalnie są to klatkowe glinokrzemiany z domieszką kationów metali alkalicznych. Do syntezy bierze się więc żel wodny zawierający tlenek glinu i łączy ze szkłem wodnym czyli rozpuszczalnym w wodzie krzemianem sodu. Mieszaninę alkalizuje się wodorotlenkiem sodu lub potasu aby spolimeryzować powstające glinokrzemiany. Wielkość i układ porów zależy od rodzaju kationu alkalicznego, stającego się "rusztowaniem" dla pierścienia glinokrzemianowego odpowiedniej wielkości, toteż mieszanina domieszkowana jest odpowiednimi kationami, w tym także organicznymi jak tetraetyloamoniowy.
Teraz gęstniejący żel jest mieszany i ogrzewany w odpowiednich warunkach. Przy czym te "odpowiednie warunki" to w istocie klucz do sukcesu. Proces nie może przebiegać zbyt szybko bo powstaną nam po prostu zbite kryształy. Zależnie od stosunku krzemu do glinu, obecności metali alkalicznych, odczynu mieszaniny, rodzaju kationu stanowiącego wzorzec, szybkości procesowania, temperatury i innych czynników otrzymujemy zeolity o różnych strukturach. Jak na razie opisano ponad 250 struktur zeolitowych a wciąż nie jest to koniec.
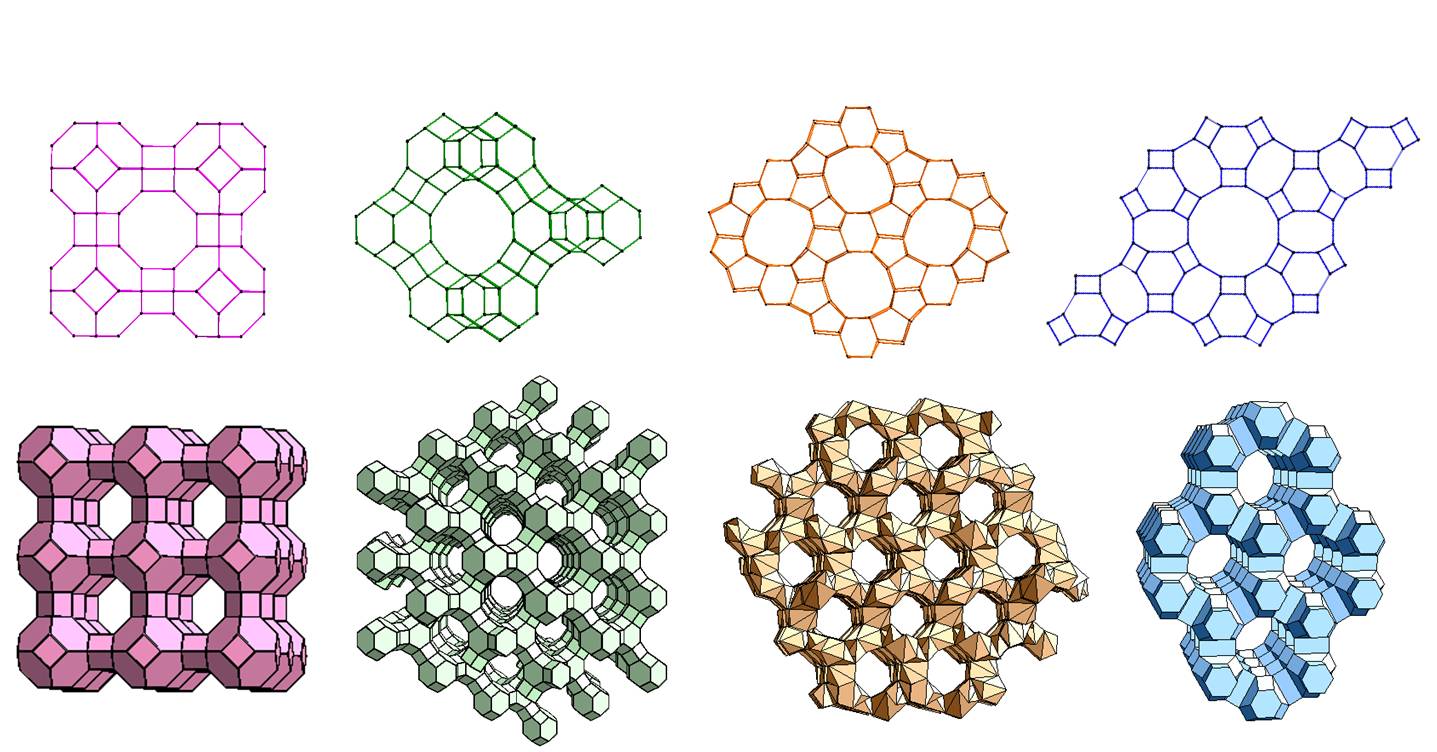
Atomy podczas krystalizacji organizują się w klatkowate "bloczki" z których układana jest sieć. Połączone wielościany o strukturze sodalitu tworzą pomiędzy sobą kanały złożone z pierścieni. Rodzaj struktury determinuje wielkość pierścieni a co za tym idzie wielkość porów.
Po przeprowadzeniu procesu w "odpowiednich" warunkach otrzymujemy wilgotną masę drobnych cząstek zeolitu, która następnie jest granulowana lub wyciskana do formy pręcików i suszona.
Oprócz usuwania wody i innych małocząsteczkowych zanieczyszczeń zeolity znalazły szerokie zastosowanie w zmiękczaniu wody, mogą bowiem pochłaniać i wiązać jony wapnia i magnezu. Akwaryści powinni kojarzyć zeolity w takim zastosowaniu. Znaleźć je możemy w ekologicznych proszkach do prania, gdzie zastępują używane zwykle do zmiękczania fosforany, które trafiając do ścieków wywoływały przenawożenie wód i zakwity glonów. Granulki sit molekularnych są też używane do wzbogacania podłoża, długo bowiem trzymają wilgoć oraz mogą stopniowo uwalniać wchłonięte nawozy.
Inne zastosowanie to katalizatory zwłaszcza w krakingu ropy naftowej. Podejmowane są też próby użycia jako nośniki leków. Ze względu na wysoką energię hydratacji i możliwość zregenerowania wilgotnych sit, zaczęto używać ich także do długotrwałego przechowywania ciepła - sita są suszone przy pomocy ciepła na przykład z kolektorów słonecznych. Zamknięte w szczelnym opakowaniu nie tracą mogą być przechowywane dość długo, a pod wpływem wody ponownie wydzielają ciepło.
Jak jednak mają się te właściwości do zastosowania sit w laboratoriach podczas ogrzewania cieczy?
Stan wrzenia to sytuacja gdy ciecz pod wpływem wysokiej temperatury jest w stanie przechodzić w parę w całej objętości, wytwarzając bąble gazu. W praktyce jednak powstanie pęcherzyka ot tak wewnątrz cieczy jest mało prawdopodobne. Najpierw cząsteczki cieczy muszą zostać rozepchane na boki, gdy utworzy się faza gazowa na pęcherzyk działa zarówno ciśnienie hydrostatyczne jak i napięcie powierzchniowe. W efekcie bardzo małe pęcherzyki odczuwają ciśnienie większe od atmosferycznego, to hamuje parowanie wody do wnętrza pęcherzyka a ten może zaniknąć zanim nie stanie się na tyle duży aby wypłynąć na powierzchnię.
Sytuacja zostaje bardzo ułatwiona gdy podgrzana woda zetknie się z nierówną, chropowatą powierzchnią, wtedy ciśnienie działa na powstający przylegający pęcherzyk tylko od jednej strony, dzięki czemu łatwiej jest mu urosnąć. Analogiczna sytuacja dotyczy wydzielania się gazu z wody mineralnej - pęcherzyki powstają na ściankach i wybiegają stale z pewnych sprzyjających punktów.
Inną sytuacją która bardzo ułatwia wrzenie są bąbelki powietrza, stanowiące "zarodek" bąbelków pary. W przypadku materiałów porowatych mogą być to zarówno bąbelki przyczepione do nierównej powierzchni jak i zawarte wewnątrz materiału, stąd właśnie użycie różnych porowatych materiałów w charakterze "kamyków wrzennych". Mogą być to kawałki porcelany (na pracowni magisterskiej używałem drobnych okruchów rozbitej filiżanki), mogą to być granulki ceramiczne i mogą to być też sita molekularne, które zawsze gdzieś tam stoją na pracowni.
A dlaczego w takim razie musimy ułatwiać wrzenie?
Cóż, to utrudnienie powstawania pierwszych pęcherzyków powoduje, że gdy podgrzewana ciecz jest bardzo czysta i ogrzewamy ją w gładkim naczyniu, możliwe staje się jej przegrzanie powyżej temperatury normalnego wrzenia. Wodę można w ten sposób ogrzać do temperatury 120-130 *C, w sprzyjających warunkach i przy szybkim ogrzewaniu aż do 160 stopni.
W takiej sytuacji drobne zaburzenie, w rodzaju pierwszego pęcherzyka, zamieszania czy wibracji może spowodować dość gwałtowne zawrzenie, często połączone ze spienieniem się i wychlapaniem naszej cieczy. Pół biedy gdy ogrzewana mieszanina pójdzie chłodnicą, ale równie dobrze może prysnąć na rękę eksperymentatora. Problem ten upowszechnił się w ostatnim czasie wraz z mikrofalówkami - wiele osób używa ich do podgrzewania wody na herbatę. Jeśli użyją do tego czystej wody i wstawią wodę w gładkiej szklance, woda może nie zawrzeć mimo, że będzie bardzo gorąca. Wrzucenie do niej teraz herbaty i cukru może spowodować wytryśnięcie z kubka i poparzenia.
Bez kamyków wrzennych ciecze wrą nieregularnie, z uderzeniami gwałtowniejszych wrzeń co jakiś czas, i właśnie dlatego dla bezpieczeństwa i większej kontroli nad procesem należy wrzucać do kolby dwie-trzy granulki sit lub kawałki porcelany.
Ja pierwszy raz spotkałem się z tym (tak, żebym sam coś z tym robił) dopiero na stażu w pewnej firmie biotechnologicznej, na 3 roku studiów.
OdpowiedzUsuńWarto wspomnieć o jeszcze jednym, ciekawym zastosowaniu sit molekularnych. To urządzenia medyczne, koncentratory tlenu, które np. w warunkach domowych, dzięki przepuszczeniu powietrza przez takie sito oddzielają tlen od azotu, koncentrując go do stężenia powyżej 90%. "Skoncentrowany" tlen podawany jest potrzebującym takiego leczenia pacjentom.
OdpowiedzUsuńCzy można prosić o źródło informacji? :)
OdpowiedzUsuńchodzi o koncentratory tlenu?
Usuńhttps://en.wikipedia.org/wiki/Oxygen_concentrator
Witam.
OdpowiedzUsuńCzy sito molekularne lepiej się sprawdzi jako filtr powietrza niż węgiel aktywny z metali ciężkich?
Podejrzewam że nie. Metale ciężkie w powietrzu występują najczęściej jako pyły, jedynie rtęć może być gazową parą. Dlatego najlepsze są po prostu materiały pyłochlonne. Węgiel ma za zadanie pochłaniać z powietrza lotne związki organiczne i tutaj jest o tyle lepszy od sit, że jest lżejszy. Sita są natomiast lepsze do pochłaniania soli metali ciężkich z wody.
Usuń