Dwa lata temu opisałem w wielkanocnym wpisie jakie są naturalne metody barwienia pisanek i jakie związki za to odpowiadają. W tym roku zatem opiszę te sztuczne barwniki.
Wprawdzie różni producenci produkują tego typu barwniki, ale jak zauważyłem, praktycznie wszyscy używają tych samych, więc opis na podstawie składu barwników które mam w domu, powinien być reprezentatywny.
Czerwony
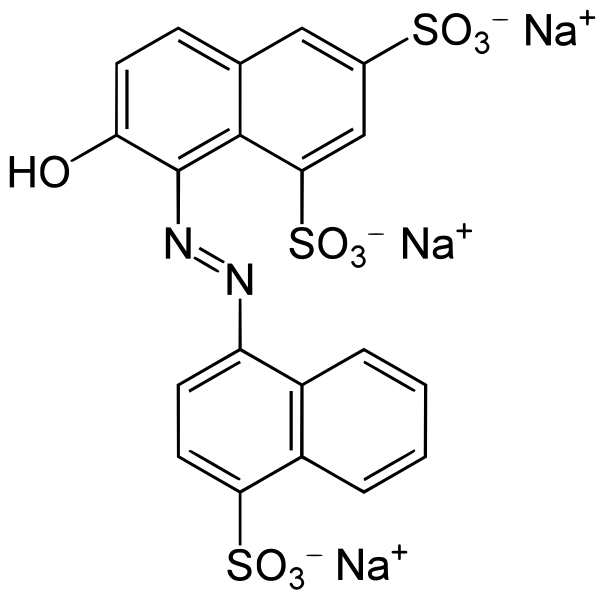
W moim zestawie za czerwień odpowiada E 124 czyli czerwień koszenilowa. To dość skomplikowany związek:
Dwie cząsteczki pochodnych naftalenu połączone grupą azową -N=N-. Grupa ta jest silnym chromoforem, a więc ugrupowaniem nadającym barwę, a jej kolor wzmacniają duże cząsteczki aromatyczne.
Wszystkie barwniki azowe mogą wywoływać uczulenia, u osób nadwrażliwych na salicylany zwiększają objawy a u astmatyków zwiększają wydzielanie histaminy. Z tego powodu ich użycie w żywności jest coraz bardziej ograniczane a normy zawartości systematycznie obniżane.
Różowy
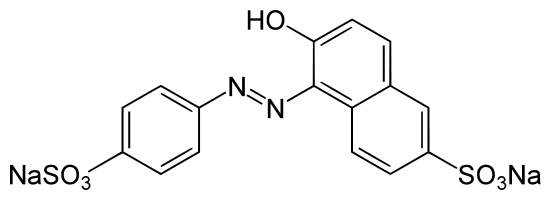
W niektórych zestawach kolor różowy jest otrzymywany przez dodatek amarantu czyli E-123, kolejnego barwnika azowego. Ze względu na częste doniesienia o reakcjach nadwrażliwości jest coraz rzadziej używany w przemyśle spożywczym, podbarwia kawior, galaretki w proszku i napoje alkoholowe. Jest podejrzewany o rakotwórczość ale nie potwierdzono tego u ludzi.
Żółty
W moim zestawie znajdują się dwa żółte barwniki. Pierwszy to żółcień pomarańczowa czyli E 110 o kolorze bliższym pomarańczy, także będąca barwnikiem azowym:
Podobnie jak inne tego typu związki może wywoływać uczulenia i pokrzywki, u nadwrażliwych na salicylany daje reakcję. Jest podejrzewana o rakotwórczość ale nie wykazano tego u ludzi, mimo tego wiele krajów jej nie stosuje. Używa się jej do podbarwiania słodyczy i żywności która musi być podgrzewana, jednak coraz rzadkiej. Kiedyś była często stosowana do dożółcania margaryny.
Znalazłem informację, że stężone roztwory wodne przybierają w pewnych temperaturach formę ciekłego kryształu.
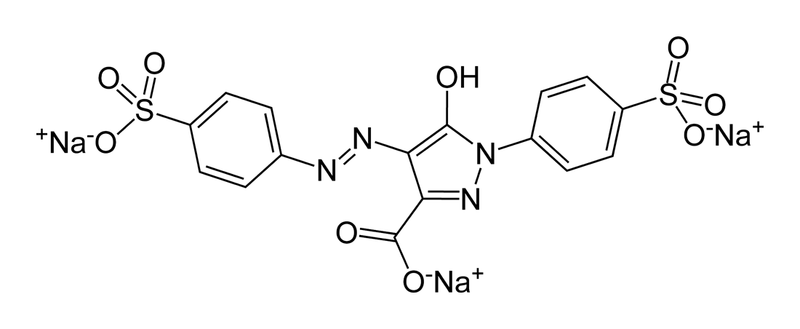
Drugi barwnik to tartrazyna, czyli E 102, mająca dość ciekawą budowę:
Jest to także barwnik azowy z grupami aromatycznymi, ale także pierścieniem diazolowym. Charakteryzuje się dużą siłą barwiącą. Pojawia się w szerokiej gamie produktów, zwłaszcza napojach i słodyczach, choć w ostatnich latach jest wycofywania. Używa się jej też w kosmetykach i jako barwnika do wełny.
Może wywoływać te same problemy zdrowotne jak i pozostałe barwniki azowe - pokrzywki, uczulenia, nadwrażliwość itp ale też migreny. Wydaje się, że u pewnych ludzi występuje specyficzna nadwrażliwość konkretnie na tą substancję, także u tych którzy nie wykazują objawów na inne barwniki azowe.
Z tego co czytałem, niektóre zestawy zawierają jeszcze żółć chinolinową czyli E 104, także barwnik azowy, inne też kurkuminę.
Niebieski
Niebieskim barwnikiem jest tu błękit brylantowy, czyli E 133, nie jest to tym razem barwnik azowy:
Jednak grupy sulfonowe przy pierścieniach aromatycznych powodują, że także może wywoływać nadwrażliwość. Uważany jednak za bezpieczny z powodu bardzo nikłego wchłaniania. Jest często stosowany w napojach i słodyczach.
Możliwy do stosowania jest też indygokarmin E 132, pochodna pigmentu indygo (tego od dżinsów), kiedyś o nim pisałem. Nie jest barwnikiem azowym, nie wywołuje uczuleń i należy do najmniej szkodliwych substancji barwiących, jest bowiem bardzo szybko wydalany - na tyle szybko, że może zabarwić mocz na niebiesko.
Nie wiem natomiast czy w zestawach używa się czerni brylantowej - barwnika o intensywnym, niebiesko-fioletowym kolorze
Zielony
Mój zestaw nie zawierał żadnego specyficznego barwnika zielonego. Zielony był zapewne otrzymany ze zmieszania błękitu brylantowego i tartrazyny. W zasadzie możliwe jest użycie w niektórych zestawach E140 czyli chlorofilu lub lepiej rozpuszczalnej E 141 czyli chlorofiliny miedziowej, barwników pochodzenia naturalnego które spotykałem w zestawach barwników spożywczych do deserów.
Jak zatem widzicie, barwniki do jaj to kawał chemii. Czy wobec tego są groźne? Raczej nie - nie wnikają do wnętrza jajka, lecz pozostają związane w skorupce - a tą zdejmujemy i wyrzucamy. Jeśli zaś ktoś ma obawy to powinien od teraz pamiętać, by niezużytych barwników do jaj nie używać do innych rzeczy - a już parę razy czytałem o barwieniu nimi domowych ciast i lukrów, które się przecież spożywa w całości.
Post scriptum:
Znalazłem wynik ciekawego badania - analitycy ze Zgierza przebadali w 2009 roku komercyjne zestawy do barwienia przy pomocy chromatografii cienkowarstwowej. Wykazali, że na 9 przebadanych zestawów, trzy nie zawierały deklarowanych barwników, bądź zawierały w śladowych ilościach, a głównymi składnikami barwiącymi były barwniki do wełny, niedopuszczone do barwienia żywości. Opis badań jest dosyć przystępny:
http://zgierz.impib.pl/images/pdf/181.pdf
informacje
czwartek, 17 kwietnia 2014
piątek, 11 kwietnia 2014
Dzień pracy na pracowni
Moje wpisy na temat przeprowadzania syntez zapewne dają już jakieś pojęcie o tym co też takiego robi się w laboratorium, jest to jednak w zasadzie skrót wydarzeń, ograniczony do jednego wątku. A jak wygląda dzień na pracowni?
Od pewnego czasu ustalił mi się stały rytm pracy, porządkujący dni. Ponieważ najważniejsze jest dla mnie przetestowanie ligandów w reakcji Henry'ego, zwykle wstawiam jedną lub dwie, ostatnio cztery, w czwartek lub piątek. Ponieważ reakcja ma trwać cztery doby, decyduje ona o planie reszty tygodnia.
Tak więc w poniedziałek przychodzę na krótko, aby zdjąć z mieszadeł wstawione reakcje, i odparować rozpuszczalnik. Zamknięte korkiem i zaparafilmowane kolbki wstawiam do lodówki, żeby produkt się nie rozkładał. Potem mam jeszcze dwa seminaria, więc nic więcej na pracowni nie robię. We wtorek i środę rozdzielam na kolumnie mieszaniny poreakcyjne, odparowuję frakcje z produktami i wstawiam do zamrażarki. W czwartek nad ranem wstawiam początek reakcji - ligand rozpuszczony w izopropanolu i z dodaną solą miedzi. Całość ma się tak mieszać cztery godziny, więc w tym czasie zwykle mierzę skręcalność optyczną oczyszczonych wcześniej produktów. Po upływie czterech godzin dodaję do kolbek substraty i mam wolne.
W piątki albo dokańczam rozdział mieszanin, albo mierzę skręcalności albo mam wolne, zależnie od tego jak się wyrobiłem w tygodniu.
A jak wygląda przykładowy dzień?
Wstaję rano. Teoretycznie na pracowni powinieniem być około 8:30, ale traktuję te "około" dosyć swobodnie, toteż zwykle zjawiam się za kilka minut dziewiąta.
Zaglądam do zeszytu co też mi zostało na ten dzień. Aha... jeszcze jedna mieszanina do rozdziału. Pytam dr Wolińską czy ma może wzorzec produktu do porównania. Dostawszy go robię płytkę TLC w odpowiednim eluencie. Czasem wynik jest bardzo ładny - duża, wyraźna plama produktu. Czasem produkt pojawia się w ilościach śladowych. W przypadku jednego aldehydu nie pojawił się w ogóle, mimo dwukrotnego powtórzenia reakcji. Nie wiem czemu.
Zaczynam więc przygotowywać kolumnę - najpierw watka na dno, potem robię "błotko" krzemionki z eluentem, nalewam, popycham pompką aby się żel dobrze osadził. Mieszaninę poreakcyjną mającą postać brązowego osadu lub oleju rozuszczam w chlorku metylu, i dodaję nieco suchej krzemionki. Po odparowaniu w wyparce otrzymuję mieszaninę reakcyjną wchłoniętą w żel.
Taką sypką mieszaninę nasypuję na początek kolumny, zalewam eluentem, stukam jeszcze aby wyszły pęcherzyki powietrza, po czym nakładam zbiornik, mocuję pompkę i zaczynam chromatografowanie. Zwykle jest wówczas tuż przed dziesiątą.
Na pracowni oprócz mnie jest jeszcze dwóch chłopaków - jeden zajmuje się podobnym ligandem ale z podstawionymi innymi grupami, drugi najmuje się ligandami z funkcją N-tlenkową, ostatnio też pochodną nikotyny. Do tego dr Wolińska, nasza promotor, dr Ławecka zajmująca się związkami siarki, pani asystentka i czasem zachodzą do nas z pracowni na przeciwko skorzystać z wyparki. Trzeba mieć niezły refleks by nie zderzać się na skrzyżowaniu przejść między stołami, gdy jeden odchodzi ze swej kolumny by na płytce sprawdzić kroplę frakcji pod lampą UV (postawioną strategicznie pośrodku), a drugi idzie z kolbką do wyparki i trzeci wraca od wagi.
Zwykle w ciągu dnia ktoś z nas,wstawia do destylacji techniczny rozpuszczalnik, aby mieć czysty do użytku, albo heksan albo chlorek metylenu albo aceton, czasem trzy na raz. Czasem oddaje się próbki na badania NMR i po pewnym czasie odbiera widma.
Tak więc kolumnuję. Eluent zwykle jest tak dobrany, aby Rf na płytce nie przekraczał 0,6 toteż co prawda na kolumnie przebiega to nieco inaczej, ale zanim pierwszy składnik pojawi się w wycieku zwykle trochę to trwa. Czasem zostawiam kolumnę żeby sobie kapała i kupuję kanapkę w bufecie, i wracam przed skapaniem pierwszej substancji.
Z reguły produkt o jaki mi chodzi jest drugą lub trzecią substancją w kolejności, nie zawsze jest jednak naocznie zauważalny na kolumnie (koledzy niekiedy zajmują się kolumnami całkiem białymi, to jest mieszankami z bezbarwnym produktem i zanieczyszczeniami). Zbieram przynajmniej trzy frakcje i sprawdzam na płytce w porównaniu ze wzorcem. Frakcje 1,2,3,4 - aha, to jeszcze nie to.
Nie lubię zupełnej ciszy podczas pracy, więc paradoksalnie żeby się nie rozpraszać zwykle kładę obok komórkę z włączoną jakąś muzyką, czasem z radiem, a bez tego sam sobie coś nucę. Ostatnio przyszedł mi do głowy fajny swingowy rytm, szkoda że na niczym nie gram. I tak to mi płynie - pompką popycham eluent dla szybszego przepływu, ale też nie za szybko. I sprawdzam dalej.
Frakcje 5,6,7 jeszcze nie to, frakcja 8 - produkt i zanieczyszczenie przednie, aha to teraz zbierać mniejsze frakcje. Frakcja 9 produkt czysty, frakcja 10 i 11 też, we frakcji 12 pojawia się zanieczyszczenie tylne, ale produktu są już tylko ślady. Sprawdzam jeszcze jedną-dwie frakcje tyłu aby upewnić się czy na pewno produkt już nie leci. Raz zdarzyło się że produkt wykrystalizował i zamienił się kolejnością z zanieczyszczeniami - pierwsza frakcja czysty produkt, potem pięć frakcji zanieczyszczeń z produktem i na koniec jedna frakcja czystego produktu.
Więc dobrze, mam kilka frakcji czystych, zlewam je zatem i odparowuję w jednej kolbce, wcześniej na sucho zważonej. Gdy mi się odparowuje schodzę do bufetu po cośtam, batonik albo gorącą herbatę.
Na koniec otrzymuję odrobinę żółtawego osadu lub olejku, ważę i porównuję wagi. Aha, męczę się cztery godziny z kolumną i mam 15 mg produktu, fajnie.
Bywa lepiej, bywa gorzej. Czasem jest to koło 100 mg, raz zdarzyło się odzyskać 7 mg. Wtedy śladowe ilości produktu tak rozmyły się na kolumnie, że żeby upewnić się czy cokolwiek mi skapuje musiałem wstępnie zagęszczać frakcje. Innym razem produkt był w ultrafiolecie niewidoczny, rozwiniętą płytkę wywoływałem jodem.
Kolumnę kończę ok 13-14, czasem później gdy z konieczności muszę użyć słabego eluentu, raz kończyłem koło 19 wieczór. Na sąsiedniej pracowni zdarzyło się komuś kolumnować trzy tygodnie. Odparowany produkt wsadzam z kolbką do zamrażalnika. Myję kolbki po frakcjach, wywalam żel z kolumny i myję ją. Zlewam z odbieralników przedestylowane rozpuszczalniki jeśli nie zrobili tego koledzy. Zakręcam wodę i mogę wychodzić.
Jeśli jest dobra pogoda robię jeszcze sobie krótki spacer.
I cóż. Zbieram dane o wydajności i nadmiarach enancjometrycznych, widma NMR, widma masowe, wszystko się przyda do pracy. Przeglądam literaturę, zaglądam do starych prac. Będę pisał.
Od pewnego czasu ustalił mi się stały rytm pracy, porządkujący dni. Ponieważ najważniejsze jest dla mnie przetestowanie ligandów w reakcji Henry'ego, zwykle wstawiam jedną lub dwie, ostatnio cztery, w czwartek lub piątek. Ponieważ reakcja ma trwać cztery doby, decyduje ona o planie reszty tygodnia.
Tak więc w poniedziałek przychodzę na krótko, aby zdjąć z mieszadeł wstawione reakcje, i odparować rozpuszczalnik. Zamknięte korkiem i zaparafilmowane kolbki wstawiam do lodówki, żeby produkt się nie rozkładał. Potem mam jeszcze dwa seminaria, więc nic więcej na pracowni nie robię. We wtorek i środę rozdzielam na kolumnie mieszaniny poreakcyjne, odparowuję frakcje z produktami i wstawiam do zamrażarki. W czwartek nad ranem wstawiam początek reakcji - ligand rozpuszczony w izopropanolu i z dodaną solą miedzi. Całość ma się tak mieszać cztery godziny, więc w tym czasie zwykle mierzę skręcalność optyczną oczyszczonych wcześniej produktów. Po upływie czterech godzin dodaję do kolbek substraty i mam wolne.
W piątki albo dokańczam rozdział mieszanin, albo mierzę skręcalności albo mam wolne, zależnie od tego jak się wyrobiłem w tygodniu.
A jak wygląda przykładowy dzień?
Wstaję rano. Teoretycznie na pracowni powinieniem być około 8:30, ale traktuję te "około" dosyć swobodnie, toteż zwykle zjawiam się za kilka minut dziewiąta.
Zaglądam do zeszytu co też mi zostało na ten dzień. Aha... jeszcze jedna mieszanina do rozdziału. Pytam dr Wolińską czy ma może wzorzec produktu do porównania. Dostawszy go robię płytkę TLC w odpowiednim eluencie. Czasem wynik jest bardzo ładny - duża, wyraźna plama produktu. Czasem produkt pojawia się w ilościach śladowych. W przypadku jednego aldehydu nie pojawił się w ogóle, mimo dwukrotnego powtórzenia reakcji. Nie wiem czemu.
Zaczynam więc przygotowywać kolumnę - najpierw watka na dno, potem robię "błotko" krzemionki z eluentem, nalewam, popycham pompką aby się żel dobrze osadził. Mieszaninę poreakcyjną mającą postać brązowego osadu lub oleju rozuszczam w chlorku metylu, i dodaję nieco suchej krzemionki. Po odparowaniu w wyparce otrzymuję mieszaninę reakcyjną wchłoniętą w żel.
Taką sypką mieszaninę nasypuję na początek kolumny, zalewam eluentem, stukam jeszcze aby wyszły pęcherzyki powietrza, po czym nakładam zbiornik, mocuję pompkę i zaczynam chromatografowanie. Zwykle jest wówczas tuż przed dziesiątą.
Na pracowni oprócz mnie jest jeszcze dwóch chłopaków - jeden zajmuje się podobnym ligandem ale z podstawionymi innymi grupami, drugi najmuje się ligandami z funkcją N-tlenkową, ostatnio też pochodną nikotyny. Do tego dr Wolińska, nasza promotor, dr Ławecka zajmująca się związkami siarki, pani asystentka i czasem zachodzą do nas z pracowni na przeciwko skorzystać z wyparki. Trzeba mieć niezły refleks by nie zderzać się na skrzyżowaniu przejść między stołami, gdy jeden odchodzi ze swej kolumny by na płytce sprawdzić kroplę frakcji pod lampą UV (postawioną strategicznie pośrodku), a drugi idzie z kolbką do wyparki i trzeci wraca od wagi.
Zwykle w ciągu dnia ktoś z nas,wstawia do destylacji techniczny rozpuszczalnik, aby mieć czysty do użytku, albo heksan albo chlorek metylenu albo aceton, czasem trzy na raz. Czasem oddaje się próbki na badania NMR i po pewnym czasie odbiera widma.
Tak więc kolumnuję. Eluent zwykle jest tak dobrany, aby Rf na płytce nie przekraczał 0,6 toteż co prawda na kolumnie przebiega to nieco inaczej, ale zanim pierwszy składnik pojawi się w wycieku zwykle trochę to trwa. Czasem zostawiam kolumnę żeby sobie kapała i kupuję kanapkę w bufecie, i wracam przed skapaniem pierwszej substancji.
Z reguły produkt o jaki mi chodzi jest drugą lub trzecią substancją w kolejności, nie zawsze jest jednak naocznie zauważalny na kolumnie (koledzy niekiedy zajmują się kolumnami całkiem białymi, to jest mieszankami z bezbarwnym produktem i zanieczyszczeniami). Zbieram przynajmniej trzy frakcje i sprawdzam na płytce w porównaniu ze wzorcem. Frakcje 1,2,3,4 - aha, to jeszcze nie to.
Nie lubię zupełnej ciszy podczas pracy, więc paradoksalnie żeby się nie rozpraszać zwykle kładę obok komórkę z włączoną jakąś muzyką, czasem z radiem, a bez tego sam sobie coś nucę. Ostatnio przyszedł mi do głowy fajny swingowy rytm, szkoda że na niczym nie gram. I tak to mi płynie - pompką popycham eluent dla szybszego przepływu, ale też nie za szybko. I sprawdzam dalej.
Frakcje 5,6,7 jeszcze nie to, frakcja 8 - produkt i zanieczyszczenie przednie, aha to teraz zbierać mniejsze frakcje. Frakcja 9 produkt czysty, frakcja 10 i 11 też, we frakcji 12 pojawia się zanieczyszczenie tylne, ale produktu są już tylko ślady. Sprawdzam jeszcze jedną-dwie frakcje tyłu aby upewnić się czy na pewno produkt już nie leci. Raz zdarzyło się że produkt wykrystalizował i zamienił się kolejnością z zanieczyszczeniami - pierwsza frakcja czysty produkt, potem pięć frakcji zanieczyszczeń z produktem i na koniec jedna frakcja czystego produktu.
Więc dobrze, mam kilka frakcji czystych, zlewam je zatem i odparowuję w jednej kolbce, wcześniej na sucho zważonej. Gdy mi się odparowuje schodzę do bufetu po cośtam, batonik albo gorącą herbatę.
Na koniec otrzymuję odrobinę żółtawego osadu lub olejku, ważę i porównuję wagi. Aha, męczę się cztery godziny z kolumną i mam 15 mg produktu, fajnie.
Bywa lepiej, bywa gorzej. Czasem jest to koło 100 mg, raz zdarzyło się odzyskać 7 mg. Wtedy śladowe ilości produktu tak rozmyły się na kolumnie, że żeby upewnić się czy cokolwiek mi skapuje musiałem wstępnie zagęszczać frakcje. Innym razem produkt był w ultrafiolecie niewidoczny, rozwiniętą płytkę wywoływałem jodem.
Kolumnę kończę ok 13-14, czasem później gdy z konieczności muszę użyć słabego eluentu, raz kończyłem koło 19 wieczór. Na sąsiedniej pracowni zdarzyło się komuś kolumnować trzy tygodnie. Odparowany produkt wsadzam z kolbką do zamrażalnika. Myję kolbki po frakcjach, wywalam żel z kolumny i myję ją. Zlewam z odbieralników przedestylowane rozpuszczalniki jeśli nie zrobili tego koledzy. Zakręcam wodę i mogę wychodzić.
Jeśli jest dobra pogoda robię jeszcze sobie krótki spacer.
I cóż. Zbieram dane o wydajności i nadmiarach enancjometrycznych, widma NMR, widma masowe, wszystko się przyda do pracy. Przeglądam literaturę, zaglądam do starych prac. Będę pisał.
wtorek, 8 kwietnia 2014
Azot Kjeldahla
Białka z jakich zbudowane są żyjące organizmy, składają się z aminokwasów, zawierających azot. Chcąc więc oznaczyć zawartość białka w pożywieniu mierzy się zazwyczaj po prostu zawartość azotu. Metodę tą wymyślił duński chemik pracujący na potrzeby browarów - zawartość białka w ziarnie przekłada się na właściwości słodu a te na jakość piwa.
Sama idea jest dosyć prosta - próbkę żywności roztwarza się w kwasie siarkowym w wysokiej temperaturze. W takich warunkach białka, skrobia i większość innych substancji ulegną zniszczeniu, zaś azot pochodzący z amin, głównie tych w białkach, ulegnie zamianie w siarczan amonu.
NR'+ H2SO4 → (NH4)2SO4 + CO2 + H2O
Po zalkalizowaniu roztworu mocną zasadą, siarczan amonu rozłoży się z wydzieleniem amoniaku:
(NH4)2SO4 + 2NaOH → Na2SO4 + 2H2O + 2NH3
Amoniak jest bardzo lotny więc podczas gotowania roztworu odparuje i wraz z parą wodną będzie skraplany w chłodnicy. Rozpuszczony w wykroplinach amoniak musi być teraz schwycony w roztworze. W tym celu skropliny wprowadza się do odbieralnika z kwasem borowym, będącym stosunkowo słabym kwasem. Zobojętnianie kwasu zmienia odczyn i kolor wskaźnika. Pochłoniętą ilość amoniaku odmiareczkowuje się kwasem. Proste.
Nie pamiętam czy sami mineralizowaliśmy próbkę prezed ćwiczeniem, chyba korzystałem z roztworu już przygotowanego. Mętna zalkalizowana próbka gotowała się cały czas:
Aparatura była skonstruowana trochę nieklasycznie:
Odbieralnikiem była zwykła kolbka z mianowanym roztworem kwasu borowego i z dodatkiem odczynnika Tashiro, czyli mieszaniny wskaźników - czerwieni i błękitu metylenowych. W miarę wykraplania amoniaku zawartośc stawała się zielona:
Aby po przemiareczkowaniu zasadą powrócić do głębokiego fioletu:
W tym przypadku azotu było niewiele.
Sama matoda jest dosyć dokładna, ale tak wyznaczoną zawartość białka mogą podwyższać inne substancje też uwalniające azot w formie soli amonowych. Znanym przykładem jest melamina, nagminnie używana przez nieuczciwych producentów do zawyżania zawartości białka w mleku lub paszach. Właśnie to było powodem niedawnego skandalu w Chinach gdzie wypuszczenie na rynek chrzczonego melaminą mleka w proszku spowodowało zatrucie tysięcy niemowląt.
środa, 2 kwietnia 2014
Nietypowe minerały
Kilka przykładów minerałów, które zdecydowanie wyróżniają się spośród reszty.
Arkanit
Minerał zawiera w sumie dosyć pospolite pierwiastki, jest to bowiem po prostu krystaliczny siarczan potasu, jest jednak minerałem rzadkim - znajduje się go na terenach hydrotermalnych, na przykład w Lacjum we Włoszech, w pobliżu złóż guano ale też w jaskiniach. Po raz pierwszy opisany jako kryształy na drewnianych podkładach toru wagoników w nieczynnej kopalni, został znaleziony w zaledwie kilku jaskiniach na świecie.
Jego nazwa bierze się z łacińskiego Arcanum co oznacza tajemnicę i nawiązuje zapewne do nie zbyt chętnego pojawiania się na powierzchni. Nazwa ta spodobała się fantastom, i pojawia się w kilku grach komputerowych, jako magiczny, cenny materiał.
Graczy jednak zapewne nie ucieszy wiadomość, że w jaskiniach arkanit powstaje z odparowywania nietoperzego moczu.
Urycyt
Innym minerałem którego powstanie wiąże się z moczem zwierzęcym, jest urycyt, czyli po prostu krystaliczny mocznik. Występuje w jaskiniach suchego klimatu
Karpatyt
Minerał organiczny stanowiący naturalną formę koronenu - węglowodoru aromatycznego w formie pierścienia złożonego z pierścieni benzenowych.
Po raz pierwszy opisany na Ukrainie, znany też ze Słowacji, został nazwany od gór Karpat. Ma postać żółtych igieł i dość wyraźnie świeci w ultrafiolecie na jasno niebiesko.
Sam węglowodór budzi zainteresowanie chemików ze względu na skłonność do samoorganizacji w kolumny ustawionych na płask cząsteczek, jak stos talerzy, co może znaleźć zastosowanie w chemii supramolekularnej.
Minerały płonących hałd
Zapłon skały płonnej wewnątrz pokopalnianej hałdy wywołuje powstanie specyficznych warunków, przypominających tereny wulkaniczne, zaś w miejscach gdzie z wnętrza hałdy wydobywają się gorące gazy, może dochodzić do krystalizacji nietypowych minerałów.
Hałdy zawierające siarczki mogą w ten sposób wytworzyć siarkę rodzimą, te powęglowe także minerały amoniaku, jak siarczan glinowo-amonowy czyli Czermigit, stanowiący naturalną formę ałunu amonowego. Bardzo nietypowym minerałem jest Kladnoit, znaleziony po raz pierwszy w czeskim Kladnie, stanowiący skrystalizowany ftalimid, ważny odczynik w chemii organicznej. Ma postać przezroczystych płatków:
Towarzyszy mu niekiedy Hoelit, czyli 9,10 antrachinon, związek stanowiący prekursor barwników alizarynowych:
Ponieważ łatwo zamienia się w formę fenolową może stanowić dobry reduktor. Jest też używany w przemysłowej produkcji wody utlenionej. Jako minerał przybiera postać żółtych igieł:
Podobny minerał tworzy acetamid, czyli amid kwasu octowego.
Abelsonit
Jedyny minerał porfiryny.
Porfiryny to ważna grupa związków zawierający obszerny pierścień z czterech cząsteczek pirolu, skierowanych atomami azotu do środka. Pierścień chętnie tworzy kompleksy z atomami metalu, co ma znaczenie dla właściwości związku - porfiryna kompleksująca żelazo to hem, stanowiący aktywnie przenoszącą tlen częścią hemoglobiny we krwi. Chloryna kompleksująca magnez to chlorofil, zielony barwnik roślin. A Abelsonit to krystaliczny kompleks z niklem:
Porfiryny są na tyle trwałe, że często pozostają nierozłożone w pozostałościach po rozpadzie materii roślinnej. Wykrywa się je w torfie, węglu a zwłaszcza w ropie i asfalcie. Częściowo shydrolizowany chlorofil może rozpuszczać się w wodzie i w zetknięciu z solami niklu tworzyć ten specyficzny minerał. Ma postać czerwonych lub pomarańczowych igieł.
Mellit
Mellit nazywany jest też miodowym kamieniem. Ma postać charakterystycznych kryształków powstających w pobliżu złóż węgla brunatnego. Nietypowy jest jego skład - to sól glinowa kwasu melitowego, będącego pochodną benzenu z kwasową grupą karboksylową przy każdym węglu:
Diomignit
Jedyny dotychczas uznany płynny minerał. Ma postać mikroskopijnych płynnych inkluzji wewnątrz kryształów spodumenu i berylu, chemicznie rzecz biorąc to tetraboran litu.
Arkanit
Minerał zawiera w sumie dosyć pospolite pierwiastki, jest to bowiem po prostu krystaliczny siarczan potasu, jest jednak minerałem rzadkim - znajduje się go na terenach hydrotermalnych, na przykład w Lacjum we Włoszech, w pobliżu złóż guano ale też w jaskiniach. Po raz pierwszy opisany jako kryształy na drewnianych podkładach toru wagoników w nieczynnej kopalni, został znaleziony w zaledwie kilku jaskiniach na świecie.
Jego nazwa bierze się z łacińskiego Arcanum co oznacza tajemnicę i nawiązuje zapewne do nie zbyt chętnego pojawiania się na powierzchni. Nazwa ta spodobała się fantastom, i pojawia się w kilku grach komputerowych, jako magiczny, cenny materiał.
Graczy jednak zapewne nie ucieszy wiadomość, że w jaskiniach arkanit powstaje z odparowywania nietoperzego moczu.
Urycyt
Innym minerałem którego powstanie wiąże się z moczem zwierzęcym, jest urycyt, czyli po prostu krystaliczny mocznik. Występuje w jaskiniach suchego klimatu
Karpatyt
Minerał organiczny stanowiący naturalną formę koronenu - węglowodoru aromatycznego w formie pierścienia złożonego z pierścieni benzenowych.
Po raz pierwszy opisany na Ukrainie, znany też ze Słowacji, został nazwany od gór Karpat. Ma postać żółtych igieł i dość wyraźnie świeci w ultrafiolecie na jasno niebiesko.
Sam węglowodór budzi zainteresowanie chemików ze względu na skłonność do samoorganizacji w kolumny ustawionych na płask cząsteczek, jak stos talerzy, co może znaleźć zastosowanie w chemii supramolekularnej.
Minerały płonących hałd
Zapłon skały płonnej wewnątrz pokopalnianej hałdy wywołuje powstanie specyficznych warunków, przypominających tereny wulkaniczne, zaś w miejscach gdzie z wnętrza hałdy wydobywają się gorące gazy, może dochodzić do krystalizacji nietypowych minerałów.
Hałdy zawierające siarczki mogą w ten sposób wytworzyć siarkę rodzimą, te powęglowe także minerały amoniaku, jak siarczan glinowo-amonowy czyli Czermigit, stanowiący naturalną formę ałunu amonowego. Bardzo nietypowym minerałem jest Kladnoit, znaleziony po raz pierwszy w czeskim Kladnie, stanowiący skrystalizowany ftalimid, ważny odczynik w chemii organicznej. Ma postać przezroczystych płatków:
Towarzyszy mu niekiedy Hoelit, czyli 9,10 antrachinon, związek stanowiący prekursor barwników alizarynowych:
Ponieważ łatwo zamienia się w formę fenolową może stanowić dobry reduktor. Jest też używany w przemysłowej produkcji wody utlenionej. Jako minerał przybiera postać żółtych igieł:
Podobny minerał tworzy acetamid, czyli amid kwasu octowego.
Abelsonit
Jedyny minerał porfiryny.
Porfiryny to ważna grupa związków zawierający obszerny pierścień z czterech cząsteczek pirolu, skierowanych atomami azotu do środka. Pierścień chętnie tworzy kompleksy z atomami metalu, co ma znaczenie dla właściwości związku - porfiryna kompleksująca żelazo to hem, stanowiący aktywnie przenoszącą tlen częścią hemoglobiny we krwi. Chloryna kompleksująca magnez to chlorofil, zielony barwnik roślin. A Abelsonit to krystaliczny kompleks z niklem:
Porfiryny są na tyle trwałe, że często pozostają nierozłożone w pozostałościach po rozpadzie materii roślinnej. Wykrywa się je w torfie, węglu a zwłaszcza w ropie i asfalcie. Częściowo shydrolizowany chlorofil może rozpuszczać się w wodzie i w zetknięciu z solami niklu tworzyć ten specyficzny minerał. Ma postać czerwonych lub pomarańczowych igieł.
Mellit
Mellit nazywany jest też miodowym kamieniem. Ma postać charakterystycznych kryształków powstających w pobliżu złóż węgla brunatnego. Nietypowy jest jego skład - to sól glinowa kwasu melitowego, będącego pochodną benzenu z kwasową grupą karboksylową przy każdym węglu:
Diomignit
Jedyny dotychczas uznany płynny minerał. Ma postać mikroskopijnych płynnych inkluzji wewnątrz kryształów spodumenu i berylu, chemicznie rzecz biorąc to tetraboran litu.
Subskrybuj:
Komentarze (Atom)