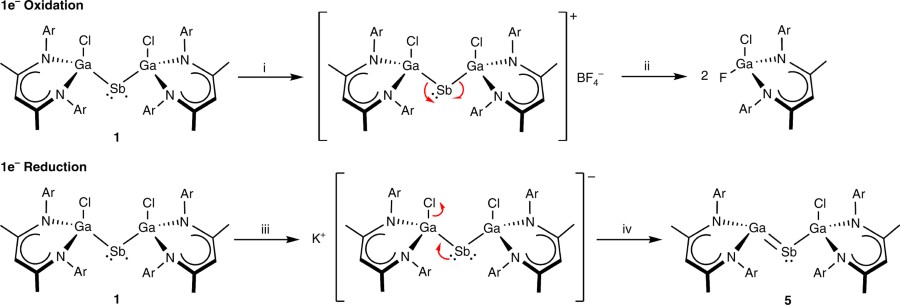
TNT czyli trinitrotoluen, to dość stary związek, wciąż używany jako materiał wybuchowy ze względu na stabilność termiczną, niską wrażliwość na uderzenia oraz stosunkowo łatwe przerabianie w stanie stopionym. Niestety przy okazji jest toksyczny i wolno ulega degradacji w przyrodzie. Ostatnio doniesiono o odkryciu nowego materiału, który zachowując podobną stabilność i łatwotopliwość co TNT, a przy tym jest od niego silniejszy i mniej toksyczny.
Zaprezentowany związek to znitrowany bis-oksadiazol. Zmierzona siła wybuchowa jest około 50% większa niż TNT.[1]
Dagerotypy na nowo odczytane
Dagerotypia była pierwszą stosowaną praktycznie techniką fotograficzną rozwijaną od lat 30. XIX wieku. Potem wprawdzie wyparła ją technika kolodionowa, ale do tego czasu utrwalono degerotypowo wiele miejsc i osób, których nie dało się ponownie sfotografować. Dagerotyp był trwałym obrazem otrzymywanym na metalowej płytce, zwykle posrebrzanej miedzi. Gładką, dobrze wypolerowaną płytkę uczulano w oparach jodu lub bromu, przez co na powierzchni powstawała stała warstewka soli srebra. Następnie płytkę umieszczano w aparacie.
Ze względu na stosunkowo małą czułość suchego związku, oraz dość ciemne obiektywy (przez problemy z uzyskaniem dobrej ostrości wymagane było użycie wąskiej przesłony) naświetlanie mogło trwać dość długo. Na samym początku wykonanie zdjęcia portretowego wymagało siedzenia nieruchomo przez 15-20 minut, czasem dłużej, w ostrym, jasnym świetle. Na takich portretach często więc widać podpórki o które opierano głowę i ręce przez stosowny czas. Później lepsze, jaśniejsze obiektywy i modyfikacje chemiczne, umożliwiły skrócenie czasów, ale wciąż była to technika nadająca się do raczej statycznych ujęć.
Naświetlona płytka była wywoływana w oparach rtęci, która ujawniała ciemnym kolorem miejsca, na które padało światło. Podczas naświetlania część halogenku redukowała się do metalicznego srebra; rtęć tworzyła z tymi cząsteczkami amalgamat, o cząstkach większych rozmiarów, co ujawniało czarny obraz. Na koniec należało jeszcze utrwalić zdjęcie poprzez wypłukanie nienaświetlonego jodku srebra, który dociemniłby jasne miejsca, używano do tego tiosiarczanu sodu.
Otrzymywano w ten sposób pozytywowy obraz na metalicznym tle, którego nie dało się kopiować, zatem każdy dagerotyp był w pewnym sensie unikatowym egzemplarzem. Przy dobrych ustawieniach obiektywu pozwalał na uzyskanie wysokiej rozdzielczości obrazu.
Niestety po upływie bardzo wielu lat zauważalna stała się stopniowa degradacja obrazu, przez co wiele najstarszych dagerotypów, zwłaszcza tych przechowywanych w złych warunkach, jest już właściwie niewidocznych. Z jednej strony miejsca jasne są przyciemniane przez tworzenie się siarczków i tlenków na powierzchni srebra, z drugiej odparowywanie rtęci z amalgamatu rozjaśnia ciemne partie.
W ostatniej publikacji z Nature, grupa kanadyjskich badaczy z University of Western Ontario postanowiła przyjrzeć się nalotom na dagerotypach od strony chemicznej. Przy pomocy mikroskopowej fluorescencji rentgenowskiej byli w stanie określić skład i grubość warstw na powierzchni płytki, znajdując nakładające się osady organiczne, produkty utlenienia czy produkty reakcji podłoża ze szklanymi płytkami, którymi zakrywano dagerotypy, oraz ślady rtęci z pierwotnego obrazu. Spektroskop skanował płytkę z rozdzielczością 10 mikrometrów, co po nastawieniu promieniowania na długość fali najsilniej pochłanianą przez rtęć umożliwiło odtworzenie obrazu z całkiem niezłą jakością. Na dwóch przebadanych zdjęciach, na których gołym okiem widać było zarys postaci, ujawniono portrety mężczyzny i kobiety.
Przy okazji stwierdzono, że zasadniczo cząstki amalgamatu w dużej mierze dobrze się zachowały, potencjalnie więc płytkę dałoby się oczyścić z innych osadów bez niszczenia obrazu, po dobraniu odpowiednich odczynników. [2]
---------
[1] Pablo E. Guzmàn et al. Bis(1,2,4-oxadiazole)bis(methylene) Dinitrate: A High-Energy Melt-Castable Explosive and Energetic Propellant Plasticizing Ingredient. Organic Process Research & Development, 2018; 22 (6):
[2] Kozacuk, Madalena S., Tsun-Kong Sham, Ronald R. Martin, Andrew J. Nelson, Ian Coulthard, John P. McElhone. “Recovery of Degraded-Beyond-Recognition 19th Century Daguerreotypes with Rapid High Dynamic Range Elemental X-ray Fluorescence Imaging of Mercury L Emmission.” Scientific Reports