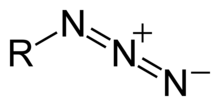Z czym można pracować i co nie jest naj
Jedną z maksym przypisywanych Einsteinowi jest ta o przekazywaniu informacji, mówiąca że należy upraszczać jak można, ale nie bardziej. Bo jeśli coś uprościmy za bardzo, możemy wprowadzić inną osobę w błąd.
Ten problem dotyczy Polonu-210 opisanego przez autora jako "najbardziej promieniotwórcza substancja znana Ludzkości". Jak tłumaczy w komentarzach, wybrał tą substancję, bo jest dostępna w stosunkowo dużych ilościach, silnie radioaktywna i ma na tyle długi czas półrozpadu, że człowiek zdąży się nią zatruć. Ale o tym w filmie nie wspomina. Widz dostaje tylko prosty przekaz "Polon-210 jest najbardziej promieniotwórczy w ogóle", co nie jest prawdą.
Zgodnie z definicją aktywności promieniotwórczej, jest to szybkość z jaką następują rozpady promieniotwórcze. Największą aktywność mają te z najkrótszymi czasami półrozpadu i małymi masami, z czego wynika że najbardziej promieniotwórczą substancją jest Wodór-7 o czasie półtrwania 2,3×10−23 s i masie 8 unitów.
Tak że akurat Polon-210 byłby raczej "najbardziej promieniotwórczą substancją z jaką można się zetknąć" w tym znaczeniu, że jest stosunkowo dostępny i niektórzy muszą z nim pracować - choć można spekulować czy przypadkiem bardziej szkodliwy nie jest ameryk-243, spotykany w czujnikach dymu, który jest wytwarzany w większych ilościach a oprócz mało przenikliwego promieniowania alfa, produkuje też wysokoenergetyczne promienie gamma.
Podobny problem dotyczy "najbardziej palnej substancji" czyli trifluorku chloru, bo przecież fluorek ten sam w sobie nie jest specjalnie palny - jest natomiast silnym środkiem zapalającym, powodującym zapłon innych substancji z którymi się zetknie, a przy tym przeżerający substancje niepalne.
Myślę, że wśród najbardziej palnych substancji na pewno znajduje się silan, czyli krzemowy analog metanu. Duże powinowactwo krzemu do tlenu i ujemna jonizacja wodoru powodują, że w mieszance z tlenem ulega samozapłonowi w temperaturach około -100 °C, przy czym różne prace podają różne dane, w jednej opisano zapłon mieszanki z powietrzem w temperaturze -162 °C[1] Natomiast silniejszym od trifluorku chloru środkiem utleniającym i zapalającym inne substancje jest zapewne difluorek ditlenu, potrafiący zapalić stały metan w temperaturze 90 K.[2]
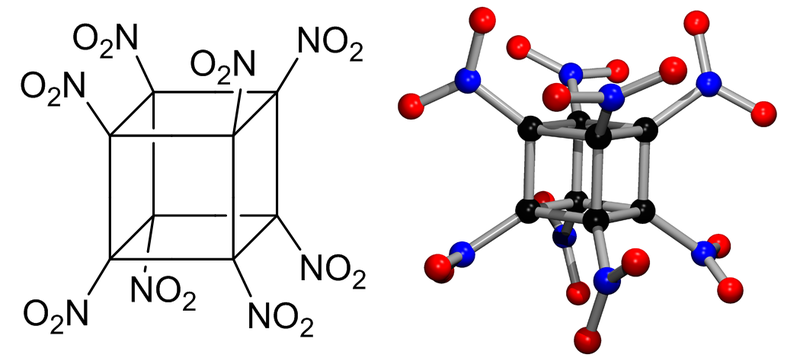
Inny problem dotyczy pozostałych substancji - tematem filmu są substancje "z którymi wolelibyście nie pracować" bo są niebezpieczne, trudne do obsługi, groźne jeśli się z nimi zetknąć. Tylko że w tym kontekście materiał wybuchowy oktanitrokuban pomimo swej niesamowitej siły wybuchowej zupełnie do zestawienia nie pasuje, jest bowiem stosunkowo bezpieczny - nie wybucha pod wpływem wstrząsów, nie powinien eksplodować nawet po uderzeniu młotkiem, dopiero wybuch spłonki inicjującej wywołuje eksplozję. Osobiście wolałbym pracować z nim, niż z na przykład chloranem potasu (jest ciekawszy).
Dlatego do zestawienia pasuje właściwie tylko batrachotoksyna, dwucyjan i ten bardzo azotowy materiał wybuchowy, eksplodujący spontanicznie.
Trochę zdziwiło mnie zatem, że autor filmu zapomniał o kilku innych substancjach, które warto tu pokrótce opisać.
Z czym ja wolałbym jako chemik nie pracować:
1. Diselenek węgla
Analog dwusiarczku węgla, przydatny w niektórych syntezach. A przy tym związek niesamowicie wprost śmierdzący. Po tym jak w 1936 roku otrzymano go po raz pierwszy, konieczna była ewakuacja najbliższej miejscowości, leżącej po zawietrznej stronie laboratorium. Jest lotny, łatwo przenika przez gumę i wchłania się do organizmu, łatwo przenika przez błony komórkowe i jest neurotoksyczny. Chemik pracujący z tym związkiem przez dłuższy czas otoczony byłby banieczką nieznośnego zapachu i bez wątpienia znalazłby wolne miejsce w tramwaju.
Podobne efekty mogą dawać też inne związki selenoorganiczne, jak selenol, analog etanolu, czy selenofenol.
Nie chcę zostać na kilka tygodni człowiekiem-skunksem, więc pracy z tym związkiem będę unikał.
2. Dimetylortęć
Jedna z najsilniejszych znanych trucizn. Dawka śmiertelna dla człowieka właściwie nie jest znana, estymuje się ją na podstawie kilku wypadków śmiertelnych. Znanym przypadkiem było zatrucie badaczki Karen Wetterhahn, której na rękawiczki rozprysnęło się ok. 0,05 ml substancji. Przeniknęła przez rękawiczki i w krótkim czasie wchłonęła się przez skórę w ilości wystarczającej do zabicia. Z batrachotoksyną czy jeszcze silniejszą ciguarotoksyną można w miarę bezpieczne pracować, z dimetylortęcią nie jest już tak dobrze.
Tak że jeśli na prawdę nie będzie mi to do czegoś potrzebne, wolę z tą substancją nie pracować.
3. Benzo-a-piren
Jeden z najważniejszych wielopierścieniowych węglowodorów aromatycznych (WWA) będących rakotwórczymi składnikami dymu. Metabolity benzo-a-pirenu łączą się z DNA wywołując mutacje. Spożyty wywołuje raka żołądka i jelit, obecność w powietrzu sprzyja nowotworom płu, a zanieczyszczenie skóry może wywołać raka skóry. W niektórych badaniach już jednokrotna iniekcja podskórna ekstraktu zwierającego WWA wywoływała nowotwory u badanych zwierzat.
Tak że pracy nad tym związkiem czystym, lub w ekstraktach wolałbym też unikać.
4. Gaz musztardowy
Środek bojowy będący silnym środkiem alkilującym. Wywołuje silne oparzenia skóry które ujawniają się nawet dobę po kontakcie z substancją, wchłonięty drogą inhalacyjną daje objawy zatrucia z dużym opóźnieniem, od 4 do 6 godzin dla małych dawek (dla dużych natychmiastowo). Jest potwierdzonym środkiem rakotwórczym.
Tak więc pragnącym zachować zdrowie i ładną twarz też radzę unikać styczności z tą substancją
5. Azydek sodu
Sól kwasu azotowodorowego, zawierająca trzy połączone atomy azotu. Azydki nieorganiczne zwykle są stosowane w syntezie azydków organicznych, oraz 1,2,3 triazyn, ewentualnie tetrazolu. Niestety azydki są związkami nietrwałymi i bardzo silnie trującymi, porównywalnie z cyjankami. Chętnie hydrolizują do azotowodoru, gazu bardziej toksycznego niż tlenek węgla, który w śladowych, niewyczuwalnych stężeniach jest w stanie wywołać zatrucie. Ekspozycja wywołuje mdłości, bóle głowy, uszkodzenie włókien nerwowych, zaburzenia oddychania zaś działaniem długofalowym po zatruciu jest uszkodzenie wątroby i jąder. Zatrucia tym związkiem wśród chemików są notowane dość często.
Przy ogrzewaniu potrafią eksplodować. Z jonami metali ciężkich tworzą wrażliwe na wstrząsy i nacisk azydki, używane czasem jeszcze w spłonkach.
Tak więc z tymi związkami bez konieczności też dobrze by było nie pracować
6. Siarczan niklu
Ten związek jest akurat stosunkowo często spotykany w laboratoriach chemii nieorganicznej. Jego głównym niebezpieczeństwem jest łatwość wywoływania alergii - powtarzalny kontakt ze związkiem skutkuje rozwinięciem się alergii na nikiel i kilkunastu procent ludzi. A zaistnienie takiej alergii może potem poważnie utrudniać życie, w związku z występowaniem niklu w wielu stopach metali używanych w elektronice czy medycynie.
------
[1] http://cdn.intechopen.com/pdfs-wm/24448.pdf
[2] http://pubs.acs.org/doi/abs/10.1021/ja00893a004