Plotki o alkoholu w proszku krążyły już od dawna, ale dopiero w ostatnich latach produkt tego typu pojawił się na międzynarodowym rynku. Czytający te doniesienia z pewnością zastanawiali się jakiej to nietypowej chemii musiano użyć, aby zatrzymać w sypkiej postaci tak lotny związek jak alkohol etylowy.
Związek jaki został tu użyty rzeczywiście jest ciekawy, ale równocześnie bardzo prosty - w zasadzie zwykła skrobia, tylko zawinięta w małe kółko...
Omawiałem już tu kiedyś nietypowe połączenia cząsteczek "połączonych acz nie powiązanych" gdzie geometria powodowała, że dwie osobne cząsteczki tworzyły nierozerwalny układ. Teraz zajmę się przypadkiem słabszego powiązania - związku inkluzyjnego, będącego formą kompleksów typu gość-gospodarz.
W połączeniu tego rodzaju cząsteczka większa, nazywana gospodarzem, tworzy "wnękę" której kształt i rozmiar pasują do mniejszej cząsteczki "gościa". Mniejsza cząsteczka wsuwa się w większą, zagłębia we wnękę a gdy już się tam dobrze umości oddziaływania między nią a cząsteczką gospodarza tworzą kompleks, w wielu przypadkach zaskakująco trwały. Wnęka gospodarza może też nie istnieć w związku samotnym, lecz powstaje wskutek przyjmowania odpowiedniej konformacji owijającej go wokół gościa. Brzmi to bardzo intymnie.
W przypadku inkluzji, cząsteczka gospodarza tworzy wnękę na tyle dużą, że goszcząca w niej molekuła jest niemal całkiem odizolowana od środowiska zewnętrznego. Powstałe połączenie często ma inne właściwości niż związki osobne - jeśli w normalnej sytuacji "gość" jest nierozpuszczalny w danym rozpuszczalniku, a "gospodarz" jest, to stworzony kompleks prawdopodobnie będzie się rozpuszczał.
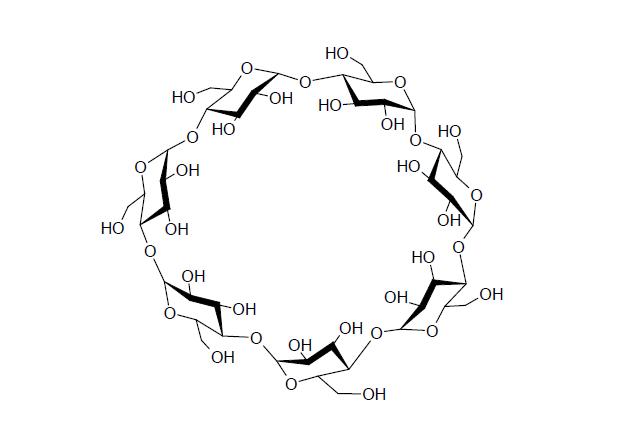
Spośród różnych znanych układów, najbardziej popularnymi i najdłużej badanymi są cyklodekstryny. Są to fragmenty łańcucha skrobi, zamknięte w formę małych pierścieni, zawierających od 6 do ponad 30 członów glukozy połączonych wiązaniami glikozydowymi poprzez tlen.
Po raz pierwszy cyklodeksytryny opisano w 1891 roku jako substancję wytwarzaną przez bakterie z rodzaju Bacillus, gdy w latach 30. zorientowano się w ich pierścieniowej budowie, szybko zaczęto badać kompleksy tworzone z małymi cząsteczkami organicznymi. Po odkryciu, że bakterie Bacillus wytwarzają cyklodekstryny ze skrobi przy pomocy specjalnego enzymu cykloglukotransferazy, zaczęto produkować je na większą skalę, traktując skrobię lub dekstrynę tymże enzymem wyizolowanym z bakterii. Długie na kilkaset lub kilkadziesiąt członów - cząstek glukozy - łańcuchy skrobi są rozcinane na krótsze fragmenty i łączone w pierścienie. Zwykle izoluje się trzy najważniejsze frakcję - alfa składającą się z 6 glukoz, beta złożoną z 7 glukoz i gamma złożoną z ośmiu glukoz. Użycie enzymów z różnych gatunków bakterii pozwala na otrzymanie także większych pierścieni, do ok. 36 glukoz.
Cyklodekstryny przyjmują szczególną, nie płaską geometrię - płaszczyzny pierścieni glukozy budujących okrąg nachylają się ku sobie, przez co związek przyjmuje formę zbliżoną do ściętego stożka, lub też, jak to się często określa, do kubka z obciętym dnem. W takim układzie po stronie szerszego otworu zagęszczają się grupy hydroksylowe, przez co od tej strony cząsteczka jest hydrofilowa, natomiast po stronie otworu węższego, grupy hydroksylowe odginają się na zewnątrz, zaś okolice tego otworu i wnętrze nabierają charakteru hydrofobowego:
Dla zdolności kompleksowania ma to dość istotne znaczenie - cząsteczki organiczne na tyle małe aby zmieścić się we wnęce cyklodekstryny i mające właściwości hydrofobowe będą chętnie wnikać do środka. Duże cząsteczki hydrofilowe nie będą wnikały, ale mogą oddziaływać z zagęszczonymi grupami hydroksylowymi na obrzeżu. Cząsteczki mające fragmenty hydrofobowe i hydrofilowe będą częściowo wsuwać się a częściowo wystawać.
Alfa cyklodekstryna tworzy "kubek" o wysokości 0,78 nanometrów i średnicy wewnętrznej 0,57 nm; beta cyklodekstryna przy tej samej wysokości ma wnękę o średnicy 0,78 nm a gamma 0,95. Wielkości tych wnęk determinują rodzaj cząsteczek które mogą do nich wniknąć - zbyt duże się nie zmieszczą, zaś bardzo małe będą słabiej oddziaływały.
Jeśli chodzi o rodzaj sił wciągających cząsteczki do wnętrza cyklodekstryny, to oprócz sił van deer Walsa znaczenie ma tu też adsorbcja hydrofobowa. Cząsteczka hydrofobowa słabo oddziałuje z wodą i podobnymi do niej rozpuszczalnikami, efekty oddziaływań między cząsteczkami wody prowadzą do odpychania grupy hydrofobowej. W tej sytuacji cząsteczki hydrofobowe będą dążyły do utworzenia agregatów, zaś w naszym przypadku mała cząsteczka hydrofobowa będzie wpychana do mającego takie właściwości wnętrza cyklodekstryny.
Cząsteczki zawierające fragmenty z elektroujemnymi niemetalami mogą dodatkowo tworzyć wiązania wodorowe z grupami -OH na obrzeżu. Ponadto możliwe jest tworzenie kompleksów koordynacyjnych. Cyklodekstryny to jedne z nielicznych cząsteczek organicznych kompleksujących aniony. Gdy hydrofobowa cząsteczka jest dłuższa niż wynosi głębokość pierścienia, możliwe jest dołączenie drugiego. Tak powstały kompleks o stosunku 1:2 nazywa się molekularną kapsułką lub też niezupełnie poprawnie, mikrokapsułką.
Wykazano powstawanie kompleksów z bardzo dużą ilością cząsteczek organicznych i nieorganicznych, nieraz całkiem sporych, na przykład fullereny, i szybko zaczęto ten fakt wykorzystywać. Zamknięte w molekularnej kapsułce związki przechodzą do roztworu w wodzie oraz są w pewnym stopniu chronione przed zewnętrznymi wpływami, stąd chętne użycie cyklodekstryn jako nośnika substancji zapachowych i smakowych dodawanych do żywności. Sama cyklodekstryna ma na liście dodatków oznaczenie E459. Może być też używana do stabilizacji składników odżywczych i witamin, chroniąc je przed utlenieniem w żywności suchej. Udało się w ten sposób stworzyć rozpuszczalną formę kurkuminy, która w normalnych warunkach jest słabo rozpuszczalna.
Zastosowania medyczne
Jednym z ciekawszych przypadków takiego kompleksowania, który znalazł zastosowanie w medycynie, jest tworzenie połączeń z cholesterolem. Cząsteczka cholesterolu jest generalnie hydrofobowa i słabo rozpuszczalna w wodzie natomiast dobrze w tłuszczach. Jej rozmiar i kształt idealnie pasuje do alfa-cyklodekstryny. Po dodaniu cyklodekstryn do żywności duża część cholesterolu zostaje związana co utrudnia jego wchłanianie. W taki sposób produkuje się jedzenie niskocholesterolowe.
Obecnie testuje się pochodne cyklodekstryn jako lek na chorobę Niemanna-Picka typu C. Choroba ta, wywołana pewnymi mutacjami, powoduje zaburzenia w transporcie substancji do komórek, wywołując gromadzenie się cholesterolu w lizosomach i sfingolipidów w neuronach. Prowadzi to do zaburzeń czynności wątroby i trzustki, oraz objawów neurologicznych, w przypadku dzieci wywołujących niepełnosprawność i opóźnienie umysłowe, a w przypadku osób starszych szybko postępującą demencję, głuchotę, zaburzenia psychiczne, padaczki. Podobieństwo objawów powoduje, że czasem nazywa się ją "dziecięcym Alzheimerem".
W 2009 roku zezwolono na eksperymentalne użycie hydroksypropylowej pochodnej beta-cyklodekstryny do łagodzenia przebiegu choroby u sióstr bliźniaczek[1], gdyż usuwa cholesterol z lizosomów, co powinno ograniczyć postęp choroby. Potem zastosowano ją jeszcze u kilkunastu pacjentów ale nie ma jeszcze ostatecznych wniosków na ile jest to sposób skuteczny. Pewne niedawne badanie na kilku pacjentach sugeruje spowolnienie rozwoju choroby. [2] Substancja jest w takich zastosowaniu podawana w formie roztworu do płynu mózgowo-rdzeniowego.
Inny przykład to Sugammadeks, lek odwracający blokadę mięśniowo-nerwową u osób którym podano leki zwiotczające na przykład przy znieczuleniu ogólnym. Jest to cząsteczka gamma-cyklodekstryny zmodyfikowana przez dodanie grup sulfanylopropionowych. Rodzaj grup i ich długość dobrano tak, aby cząsteczka idealnie pasowała do środka zwiotczającego rokuronium. Początkowo miał to być nośnik leku ułatwiający rozpuszczanie w wodzie, ale po stwierdzeniu wyjątkowo dużej siły kompleksowania, zaczęto stosować zmodyfikowaną cyklodekstrynę do usuwania środka z ustroju. Po wstrzyknięciu do krwioobiegu, sugammadeks kompleksuje rokuronium, w związku z tym związek ten zaczyna być oddawany przez tkanki co znosi działanie zwiotczające.
A co z alkoholem?
Etanol jest małą cząsteczką organiczną z jednym końcem o pewnych właściwościach lipofilowych, i już dawno stwierdzono, że w odpowiednich warunkach możliwe jest stworzenie połączenia inkluzyjnego z cyklodeksytryną, które jednak rozpadało się pod wpływem wody. Pierwsze próby zastosowań spożywczych miały miejsce w latach 70. ale najwyraźniej nie były zbyt udane, dlatego dla przeciętnego konsumenta wynalazek zaistniał dopiero w ostatnich latach. Najczęściej spotykane użycie, to napoje typu "grzaniec" - te dostępne na polskim rynku zawierają enkapsulowany alkohol w ilości odpowiadającej stężeniu 0,5% w gotowym napoju (w zasadzie więc są to ilości dla aromatu).
W Europie dostępne są napoje w proszku o smaku szampana czy wina z dodatkiem alkoholu w ilości wystarczającej, aby się upić.
Proszek taki składa się z drobnych cząstek zawierających wewnątrz masę kompleksu cyklodekstryna-alkohol, otoczoną warstewką ochronną liniowych dekstryn, chroniących wnętrze przed parowaniem. Pył może zawierać do 30% alkoholu.
Cyklodekstryny spożyte doustnie nie wywołują szkodliwych skutków, są częściowo trawione tak samo jak zwykła skrobia. Ze względu na rozmiar cząsteczek nie są wchłaniane do organizmu. Testuje się je jako środek obniżający poziom cholesterolu, zażywany w dawkach kilkugramowych.[3]
---------
* https://en.wikipedia.org/wiki/Alcohol_powder
* https://en.wikipedia.org/wiki/Cyclodextrin
[1] http://addiandcassi.com/walgreens-support-twins-niemann-pick-type-receive-cyclodextrin-treatments-home/
[2] https://www.sciencedaily.com/releases/2017/08/170810192740.htm
[3] https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4941029/
informacje
Pokazywanie postów oznaczonych etykietą lista E. Pokaż wszystkie posty
Pokazywanie postów oznaczonych etykietą lista E. Pokaż wszystkie posty
poniedziałek, 23 października 2017
wtorek, 19 stycznia 2016
To jest złe, bo w przemyśle...
Witam. Jakiś czas mnie tu nie było, różne rzeczy zaprzątały mi głowę.
Kilkakrotnie już pisałem o różnych formach błędnego rozumienia chemii w mediach, tym razem zajmę się dość charakterystycznym sposobem argumentacji (argumentum ad sumptum) uzasadniającej szkodliwość jakiejś substancji na zasadzie "to musi być świństwo, skoro w przemyśle używa się tego do produkcji czegoś, co wiemy że jest szkodliwe".
Najczęściej argumentuje się w ten sposób szkodliwość dodatków żywnościowych, czego charakterystyczny przykład znalazłem niedawno na stronie o charakterystycznym tytule "Smakuje czy truje" która w zamierzeniu ma obalać mity dietetyczne, tymczasem całkiem nieźle idzie jej ich tworzenie, jak choćby w artykule o składnikach lodów[1]. Artykuł zaczyna się od stwierdzenia, że lody zawierają dużo emulgatorów i sztucznych barwników, które mają wpływ na nasze zdrowie. Aby to udowodnić najpierw wymienia kilka dodatków nieszkodliwych, jak guma guar czy mączka chleba świętojańskiego, a potem kilka dodatków które wzbudzają wątpliwości.
Przy czym trudno dokładnie stwierdzić co dokładnie wzbudza te wątpliwości, w podanej liście zastosowano bowiem wspomniany "argument z użytku" uważając, że już samo to, bez sprawdzania innych danych, świadczy o tych dodatkach:
Problem z taką argumentacją polega na tym, że wiele substancji ma gdzieś w przemyśle zastosowania o jakich nigdy byśmy nie pomyśleli, ale samo to nic nam nie mówi na temat tej substancji.
Woda jest składnikiem ścieków, używa się jej do produkcji leków psychotropowych, jest zawarta w komórkach rakowych a w średniowieczu była narzędziem tortur, co świadczy tylko o jej wszechstronnych zastosowaniach. Oleje roślinne mogą posłużyć do produkcji środków wybuchowych. Niektóre składniki popularnych przypraw służą do otrzymywania narkotyków, inne do wypełnień dentystycznych. Olejek eteryczny ze skórki pomarańczy jest dobrym rozpuszczalnikiem do niektórych tworzyw sztucznych, ze względu na ilość przetwarzanych pomarańczy względnie tanim*. Olejek lawendowy przez wiele wieków był używany do rozcieńczania farb olejnych.
Dyskusja na temat substancji powinna być więc merytoryczna i opierać się o to jaka konkretnie jest to substancja i o jakich ilościach mowa. Bez tego pusta lista przemysłowych zastosowań staje się straszeniem czytelnika, obliczonym na to, że przecież i tak nikt nie sprawdzi.
Zajrzyjmy więc na powyższą listę i zobaczmy czym są wymienione składniki:
Piperonal to inaczej heliotropina, ładnie pachnący związek występujący w wielu kwiatach i roślinach aromatycznych, w tym głównie w lasce wanilii, kwiatach fiołka pachnącego i czarnym pieprzu od którego wywiedziono jego nazwę. Przemysłowo otrzymuje się go albo z utlenienia safrolu, związku o zapachu gałki muszkatołowej wyodrębnianego z owoców sassafrasu, albo z katecholu. Używany jest do produkcji perfum i nawaniaczy powietrza, w lodach stanowi zapewne składnik zapachu.
Czy jest używany na wszy? Owszem, wszy nie lubią jego zapachu i dlatego nie żerują w miejscach posmarowanych preparatem w tym związkiem. Istnieje wiele pachnących substancji których zapachu wszy nie lubią, jak choćby wanilina. Piperonal jest używany głównie dlatego, bo jest nietoksyczny i można go użyć w dużym rozcieńczeniu. [2] Na podobnej zasadzie linalol odstrasza komary, a jakoś nikt nie panikuje, że produkty aromatyzowane trawą cytrynową "zawierają repelent ".
Octan etylu - to ester kwasu octowego i alkoholu etylowego, ma zapach owocowy, w stanie czystym używany jako rozpuszczalnik, na przykład w bezacetonowych rozpuszczalnikach do paznokci. W niewielkich ilościach składnik aromatów owocowych.
Octan benzylu - ester o zapachu jaśminowym, a nie truskawkowym. Oleista ciecz, może być użyty jako rozpuszczalnik do modyfikowanej celulozy, octanu i azotanu, w zastępstwie do eteru.
Aldehyd masłowy - oleista ciecz o ostrym zapachu, w mniejszym stężeniu podobnym do czekolady, jeden ze składników olejku lawendowego, łatwo utlenia się do kwasu masłowego. Nietoksyczny. Polimeryzuje i stąd zapewne odniesienie do jakichś klejów.
Aldehyd C17 - czyli 3-fenyloglicydan etylu, środek zapachowy o intensywnym owocowym zapachu[3]. Jego pochodna 3-metylowa to tak zwany aldehyd truskawkowy, składnik zapachu truskawek. Nie znalazłem natomiast potwierdzenia, że ten konkretnie związek jest używany do produkcji gumy. Prawdopodobnie chodziło o to, że glicydany, będące epoksydami, mogą służyć do produkcji żywic i polimerów, jednak ten konkretny jest zużywany raczej jako składnik aromatów.
Aldehyd C18 - czyli gamma nonalakton, nazywany też laktonem kokosowym, to środek zapachowy o zapachu słodko-kokosowym, będący laktonem kwasu pelargonowego.[4] Nie wiem natomiast o jaki detergent produkowany z tego związku chodzi. Albo o których z sulfonianów, albo o eter poliglikolowy, w każdym razie związek sam w sobie detergentem nie jest.
Jak więc widać te straszne zastosowania wynikają albo z tego, że związek może rozpuszczać w sobie inne substancje, albo stąd, bo jego pochodne są do czegoś używane
----------
* Jedząc pomarańcze weźcie kawałek skórki i zegnijcie go w palcach, aby prysnął olejek. Jeśli napryskacie go na styropian, okaże się, że olejek pomarańczowy dobrze go rozpuszcza.
[1] http://smakujeczytruje.pl/przeczytaj-zanim-zjesz-kolejnego-loda/
[2] http://phthiraptera.info/Publications/45246.pdf
[3] http://www.prasadorganics.com/files/fruity/c17.pdf
[4] http://www.thegoodscentscompany.com/data/rw1000532.html
Kilkakrotnie już pisałem o różnych formach błędnego rozumienia chemii w mediach, tym razem zajmę się dość charakterystycznym sposobem argumentacji (argumentum ad sumptum) uzasadniającej szkodliwość jakiejś substancji na zasadzie "to musi być świństwo, skoro w przemyśle używa się tego do produkcji czegoś, co wiemy że jest szkodliwe".
Najczęściej argumentuje się w ten sposób szkodliwość dodatków żywnościowych, czego charakterystyczny przykład znalazłem niedawno na stronie o charakterystycznym tytule "Smakuje czy truje" która w zamierzeniu ma obalać mity dietetyczne, tymczasem całkiem nieźle idzie jej ich tworzenie, jak choćby w artykule o składnikach lodów[1]. Artykuł zaczyna się od stwierdzenia, że lody zawierają dużo emulgatorów i sztucznych barwników, które mają wpływ na nasze zdrowie. Aby to udowodnić najpierw wymienia kilka dodatków nieszkodliwych, jak guma guar czy mączka chleba świętojańskiego, a potem kilka dodatków które wzbudzają wątpliwości.
Przy czym trudno dokładnie stwierdzić co dokładnie wzbudza te wątpliwości, w podanej liście zastosowano bowiem wspomniany "argument z użytku" uważając, że już samo to, bez sprawdzania innych danych, świadczy o tych dodatkach:
Tekst krąży w internecie od paru lat, czasem wyłaniając się w mniej lub bardziej sensacyjnego formie, na przykład w zeszłym roku pod tytułem "środek na wszy w lodach". No bo jeśli nie chce się dyskutować o tym czym są te substancje, najlepiej wywołać skojarzenie z czymś obrzydliwym.Szczególnie uważaj na takie składniki, jak:– aldehyd C-17 – nadaje lodom smak wiśniowy, w przemyśle używany do produkcji barwników i gumy– aldehyd C-18 – nadaje lodom smak czekoladowy, w przemyśle używany jest do produkcji płynów do mycia naczyń i innych detergentów,– aldehyd masłowy – nadaje lodom smak orzechowy, w przemyśle stosowany jest do produkcji klejów kauczukowych,– octan benzylu – nadaje lodom smak truskawkowy, rozpuszczalnik azotanów,– octan etylu – nadaje lodom smak ananasowy, w przemyśle używany do czyszczenia skór,– piperonal – nadaje lodom smak waniliowy, stosowany w przemyśle perfumeryjnym i jako środek do zwalczania wszy.
Problem z taką argumentacją polega na tym, że wiele substancji ma gdzieś w przemyśle zastosowania o jakich nigdy byśmy nie pomyśleli, ale samo to nic nam nie mówi na temat tej substancji.
Woda jest składnikiem ścieków, używa się jej do produkcji leków psychotropowych, jest zawarta w komórkach rakowych a w średniowieczu była narzędziem tortur, co świadczy tylko o jej wszechstronnych zastosowaniach. Oleje roślinne mogą posłużyć do produkcji środków wybuchowych. Niektóre składniki popularnych przypraw służą do otrzymywania narkotyków, inne do wypełnień dentystycznych. Olejek eteryczny ze skórki pomarańczy jest dobrym rozpuszczalnikiem do niektórych tworzyw sztucznych, ze względu na ilość przetwarzanych pomarańczy względnie tanim*. Olejek lawendowy przez wiele wieków był używany do rozcieńczania farb olejnych.
Dyskusja na temat substancji powinna być więc merytoryczna i opierać się o to jaka konkretnie jest to substancja i o jakich ilościach mowa. Bez tego pusta lista przemysłowych zastosowań staje się straszeniem czytelnika, obliczonym na to, że przecież i tak nikt nie sprawdzi.
Zajrzyjmy więc na powyższą listę i zobaczmy czym są wymienione składniki:
Piperonal to inaczej heliotropina, ładnie pachnący związek występujący w wielu kwiatach i roślinach aromatycznych, w tym głównie w lasce wanilii, kwiatach fiołka pachnącego i czarnym pieprzu od którego wywiedziono jego nazwę. Przemysłowo otrzymuje się go albo z utlenienia safrolu, związku o zapachu gałki muszkatołowej wyodrębnianego z owoców sassafrasu, albo z katecholu. Używany jest do produkcji perfum i nawaniaczy powietrza, w lodach stanowi zapewne składnik zapachu.
Czy jest używany na wszy? Owszem, wszy nie lubią jego zapachu i dlatego nie żerują w miejscach posmarowanych preparatem w tym związkiem. Istnieje wiele pachnących substancji których zapachu wszy nie lubią, jak choćby wanilina. Piperonal jest używany głównie dlatego, bo jest nietoksyczny i można go użyć w dużym rozcieńczeniu. [2] Na podobnej zasadzie linalol odstrasza komary, a jakoś nikt nie panikuje, że produkty aromatyzowane trawą cytrynową "zawierają repelent ".
Octan etylu - to ester kwasu octowego i alkoholu etylowego, ma zapach owocowy, w stanie czystym używany jako rozpuszczalnik, na przykład w bezacetonowych rozpuszczalnikach do paznokci. W niewielkich ilościach składnik aromatów owocowych.
Octan benzylu - ester o zapachu jaśminowym, a nie truskawkowym. Oleista ciecz, może być użyty jako rozpuszczalnik do modyfikowanej celulozy, octanu i azotanu, w zastępstwie do eteru.
Aldehyd masłowy - oleista ciecz o ostrym zapachu, w mniejszym stężeniu podobnym do czekolady, jeden ze składników olejku lawendowego, łatwo utlenia się do kwasu masłowego. Nietoksyczny. Polimeryzuje i stąd zapewne odniesienie do jakichś klejów.
Aldehyd C17 - czyli 3-fenyloglicydan etylu, środek zapachowy o intensywnym owocowym zapachu[3]. Jego pochodna 3-metylowa to tak zwany aldehyd truskawkowy, składnik zapachu truskawek. Nie znalazłem natomiast potwierdzenia, że ten konkretnie związek jest używany do produkcji gumy. Prawdopodobnie chodziło o to, że glicydany, będące epoksydami, mogą służyć do produkcji żywic i polimerów, jednak ten konkretny jest zużywany raczej jako składnik aromatów.
Aldehyd C18 - czyli gamma nonalakton, nazywany też laktonem kokosowym, to środek zapachowy o zapachu słodko-kokosowym, będący laktonem kwasu pelargonowego.[4] Nie wiem natomiast o jaki detergent produkowany z tego związku chodzi. Albo o których z sulfonianów, albo o eter poliglikolowy, w każdym razie związek sam w sobie detergentem nie jest.
Jak więc widać te straszne zastosowania wynikają albo z tego, że związek może rozpuszczać w sobie inne substancje, albo stąd, bo jego pochodne są do czegoś używane
----------
* Jedząc pomarańcze weźcie kawałek skórki i zegnijcie go w palcach, aby prysnął olejek. Jeśli napryskacie go na styropian, okaże się, że olejek pomarańczowy dobrze go rozpuszcza.
[1] http://smakujeczytruje.pl/przeczytaj-zanim-zjesz-kolejnego-loda/
[2] http://phthiraptera.info/Publications/45246.pdf
[3] http://www.prasadorganics.com/files/fruity/c17.pdf
[4] http://www.thegoodscentscompany.com/data/rw1000532.html
wtorek, 5 maja 2015
Czarne czy zielone?
Zaszedłem do sklepu aby przy okazji innych zakupów kupić też oliwki. Wybrałem słoiczek czarnych i oczywiście pierwsze co zrobiłem, to zajrzałem na masę netto i na skład. A tam oprócz soli i innych typowych składników zalewy, znalazłem też "stabilizator - glukonian żelazawy". Stabilizator czego? - zaciekawiłem się. A no stabilizator czarnej barwy.
Oliwka europejska to gatunek typowo śródziemnomorski. Jest wiecznie zielonym, niskim drzewem, często przybierającym formy krzewiaste. Za sprawą silnego systemu korzeniowego, dużej zdolności regeneracji i wolnego wzrostu może żyć długo, nawet ponad tysiąc lat. Owocem oliwki jest pestkowiec o tłustym miąższu otaczającym dużą pestkę. Większość światowych zbiorów jest przetwarzana na cenioną w kuchni oliwę, zdecydowanie mniejsza trafia na nasze stoły w formie zamarynowanej w soli lub occie.
I tutaj właśnie zaczyna się interesująca nas kwestia - owoc oliwki po zupełnym dojrzeniu ma kolor ciemnofioletowy, jednak większość oliwek zbiera się gdy są jeszcze zielone, niedojrzałe, głownie ze względu na lepszy smak. Skąd więc oliwka czarna?
Różne źródła różnie to podawały, ale wydaje się że są dwa typy - zebrane oliwki mogą być poddawane dalszej fermentacji, podczas której ciemnieją. Wydaje się jednak, że częściej poddawane są specjalnemu procesowi, polegającym na macerowaniu w alkalicznej zalewie z dodatkiem soli żelaza i przedmuchiwanej powietrzem. W alkalicznym środowisku związane polifenole w skórce oliwki ulegają uwolnieniu i mogą być utleniane przez powietrze do form ciemno zabarwionych. Sole żelaza dodatkowo tworzą z polifenolami ciemne kompleksy - opisałem to kiedyś w artykule o atramencie z dębowych galasów. W efekcie zielona oliwka staje się czarna.[1]
Identyczne procesy zachodzą podczas fermentacji, tutaj są jednak szybsze i dają równomierny kolor. Nawiasem mówiąc zielone oliwki są chronione przez dostępem powietrza aby same nie zaczęły ciemnieć - stąd zwykle zalewa zawiera kwas askorbinowy jako przeciwutleniacz.
Dodatek soli żelaza do zalewy utrwala kolor czarnych oliwek i zapobiega odbarwieniom. Ale czy wobec tego - zastanowią się niektórzy - czy przypadkiem aby taka czerniona oliwka nie jest szkodliwa? Wydaje się, że nie - sam owoc mógł wchłonąć nieco żelaza. Glukonian żelazawy jest natomiast solą nieszkodliwą - stanowi połączenie żelaza z pochodną glukozy, kwasem glukonowym. Połączenie to charakteryzuje się tym, że w takiej formie żelazo jest stosunkowo dobrze przyswajalne, stąd też używa się do w suplementach do leczenia anemii. Dopiero dość duże dawki mogą wywołać biegunki i podrażnienia, co związane jest z toksycznym działaniem samego żelaza.[2]
W anglojęzycznym internecie zauważyć można charakterystyczną pomyłkę - otóż wiele osób widząc nazwę "gluconate" sądzi, że jest to składnik zawierający gluten. A to nie prawda.
Wygląda na to, że sprzedawane w sklepach oliwki, nie są tak czarne jak to by się wydawało.
-------
[1] http://www.oliveoilsource.com/asktheexpert/are-olives-dyed-make-them-black
[2] http://en.wikipedia.org/wiki/Iron%28II%29_gluconate
Oliwka europejska to gatunek typowo śródziemnomorski. Jest wiecznie zielonym, niskim drzewem, często przybierającym formy krzewiaste. Za sprawą silnego systemu korzeniowego, dużej zdolności regeneracji i wolnego wzrostu może żyć długo, nawet ponad tysiąc lat. Owocem oliwki jest pestkowiec o tłustym miąższu otaczającym dużą pestkę. Większość światowych zbiorów jest przetwarzana na cenioną w kuchni oliwę, zdecydowanie mniejsza trafia na nasze stoły w formie zamarynowanej w soli lub occie.
I tutaj właśnie zaczyna się interesująca nas kwestia - owoc oliwki po zupełnym dojrzeniu ma kolor ciemnofioletowy, jednak większość oliwek zbiera się gdy są jeszcze zielone, niedojrzałe, głownie ze względu na lepszy smak. Skąd więc oliwka czarna?
Różne źródła różnie to podawały, ale wydaje się że są dwa typy - zebrane oliwki mogą być poddawane dalszej fermentacji, podczas której ciemnieją. Wydaje się jednak, że częściej poddawane są specjalnemu procesowi, polegającym na macerowaniu w alkalicznej zalewie z dodatkiem soli żelaza i przedmuchiwanej powietrzem. W alkalicznym środowisku związane polifenole w skórce oliwki ulegają uwolnieniu i mogą być utleniane przez powietrze do form ciemno zabarwionych. Sole żelaza dodatkowo tworzą z polifenolami ciemne kompleksy - opisałem to kiedyś w artykule o atramencie z dębowych galasów. W efekcie zielona oliwka staje się czarna.[1]
Identyczne procesy zachodzą podczas fermentacji, tutaj są jednak szybsze i dają równomierny kolor. Nawiasem mówiąc zielone oliwki są chronione przez dostępem powietrza aby same nie zaczęły ciemnieć - stąd zwykle zalewa zawiera kwas askorbinowy jako przeciwutleniacz.
Dodatek soli żelaza do zalewy utrwala kolor czarnych oliwek i zapobiega odbarwieniom. Ale czy wobec tego - zastanowią się niektórzy - czy przypadkiem aby taka czerniona oliwka nie jest szkodliwa? Wydaje się, że nie - sam owoc mógł wchłonąć nieco żelaza. Glukonian żelazawy jest natomiast solą nieszkodliwą - stanowi połączenie żelaza z pochodną glukozy, kwasem glukonowym. Połączenie to charakteryzuje się tym, że w takiej formie żelazo jest stosunkowo dobrze przyswajalne, stąd też używa się do w suplementach do leczenia anemii. Dopiero dość duże dawki mogą wywołać biegunki i podrażnienia, co związane jest z toksycznym działaniem samego żelaza.[2]
W anglojęzycznym internecie zauważyć można charakterystyczną pomyłkę - otóż wiele osób widząc nazwę "gluconate" sądzi, że jest to składnik zawierający gluten. A to nie prawda.
Wygląda na to, że sprzedawane w sklepach oliwki, nie są tak czarne jak to by się wydawało.
-------
[1] http://www.oliveoilsource.com/asktheexpert/are-olives-dyed-make-them-black
[2] http://en.wikipedia.org/wiki/Iron%28II%29_gluconate
poniedziałek, 16 lutego 2015
Chemia bardzo tłustego pączka, czyli o niemożebnie długim składzie słów kilka
Z okazji Tłustego Czwartku w mediach wypłynęła sprawa pewnych pączków, opatrzonych w sklepie niemożebnie długą listą składników. I oczywiście zaraz popłynęły komentarze "zaraz będziemy świecić", "ale syf", "tam jest cała tablica mendelejewa" czy nawet stary szlagier używany w każdej dyskusji o jedzeniu "myślicie że skąd teraz tyle chorób?".
No cóż. Odkrycie że pączek nie składa się po prostu z pączka, dla wielu może być zaskakujące, jednak wczytując się w artykuły o tym znalezisku zauważyłem, że nikt nie podał merytorycznych argumentów. Zamiast "ten pączek jest zły bo zawiera składnik X którzy szkodzi" cała argumentacja we wszystkich artykułach opiera się na stwierdzeniu "to musi być złe bo ma tak dużo składników". I dla wielu zatrzymywanie się na tym etapie jest wystarczające - na Facebookowym profilu Czytamy Etykiety omawianie składu zaczyna się od oglądania etykiety i koniec, już można komentować że syf, że złe, że można popić płynem do naczyń.
No to teraz przeprowadźmy merytoryczny rozbiór pączka na składniki.
Na początku wyjaśnienie - producent podał pełny skład produktu, ze składnikami wedle malejącego udziału z podziałem na poszczególne części. Pączek zawiera w sobie właściwe ciasto, czekoladowe nadzienie i polewę czekoladową czarną. Każda z tych składowych ma swoje własne składniki, które muszą zostać wymienione osobno, nawet jeśli się powtarzają. Z pobieżnego przeglądu można wychwycić, że w składzie wymieniającym składniki tych trzech substancji składających na pączek woda pojawia się trzy razy, utwardzone tłuszcze roślinne trzy razy, sól dwa razy, sorbinian dwa razy, cukier trzy razy, kwas cytrynowy trzy razy...
To trochę tak jakbyście chcieli sprzedawać domowe ciasteczka z dżemem i czekoladą i musieli dodać skład w którym zmuszeni byście byli wymienić nie tylko wszystkie składniki ciasta, ale jeszcze wszystkie składniki dżemu i wszystkie składniki czekolady, nawet gdy się będą powtarzać. Wtedy też wam wyjdzie bardzo długa lista.*
No ale może po kolei. Najpierw idą składniki ciasta, począwszy od mąki, aż dochodzimy do margaryny 80% i dalej wymienione mamy składniki margaryny użytej do ciasta aż do pozycji "mieszanka tokoferoli" potem znów dalsze składniki ciasta, których było mniej niż margaryny, w tym ponownie sól, aż do aromatu.
Potem idą składniki nadzienia czekoladowego, począwszy od wody a skończywszy na polisorbacie, i na koniec składniki polewy. I jeszcze lista alergenów. Rozpatrzmy więc składniki osobno:
1. Ciasto
*Mąka pszenna - jakieś zastrzeżenia?
*Masa jajowa płynna pasteryzowana - Ten tajemniczo brzmiący składnik, jest dokładnie tym co pierwsze przychodzi na myśl. To po prostu białko i żółtko zmiksowane razem i zapasteryzowane. Jak podaje na swojej stronie jeden z producentów masy, jej produkcja opiera się na następujących etapach: wybijanie świeżych jaj kurzych, filtrowanie, pasteryzacja, schładzanie [1]. Żadnych dodatków, konserwantów, barwników itp. Jakieś zastrzeżenia?
*Cukier
*Drożdże
(margaryna osobno)
*substancja konserwująca kwas sorbowy - konserwant pochodzący z owoców jarzębiny, zapobiega wzrostowi pleśni a także pałeczki jadu kiełbasianego, może wywoływać alergie na skórze natomiast nie jest szkodliwy wewnętrznie (zatem pamiętajcie - nie smarujcie się ciastem od pączka)
* regulator kwasowości kwas cytrynowy - nieszkodliwy
* barwnik annato - jest to barwnik naturalny, wyciąg z osnówek nasion Arnoty właściwej, tropikalnego krzewu z ameryki południowej, zawierający karotenoidy i terpenoidy. Pozwala uzyskać kolor od żółtego do czerwono-pomarańczowego, zwykle używany do serów, tu zapewne w śladowych ilościach dla nadania ciastu kremowego odcienia. W dużych ilościach może wywoływać alergie, dlatego normy są bardzo wyśrubowane.
* woda
*sól
* mleko w proszku
* polepszacz E 407 - Karagen, substancja żelująca otrzymywana z czerwonych krasnorostów. Głównym składnikiem jest polisacharyd o bardzo dużej ilości grup sulfonowych. Zwiększa lepkość i spowalnia sedymentację. ze względu na grupy sulfonowe może wywoływać reakcje u uczulonych na siarczyny. Jest składnikiem kontrowersyjnym - niektóre badania wskazują że ma wpływ na rozwój raka jelita grubego. Ponieważ jednak inne badania tego efektu nie wykazują, formalnie nie jest na liście kancerogenów.
* Aromat - ?
1.a Margaryna 80%
* Oleje roślinne i tłuszcze roślinne utwardzone
* woda
* emulgatory, mono i dwuglicerydy kwasów tłuszczowych - pochodna tłuszczów. Zwykłe tłuszcze składają się z gliceryny, alkoholu trójwodorotlenowego, połączonego wiązaniami estrowymi z trzema cząsteczkami kwasów tłuszczowych. W wyniku częściowej hydrolizy kwasem lub enzymem, otrzymnujemu mono gliceryd z jednym kwasem tłuszczowym i dwiema wolnymi grupami hydroksylowymi gliceryny, lub diglicerydy z dwoma kwasami tłuszczowymi.
Póki wszystkie trzy miejsca w glicerynie są zajęte, tłuszcz jest hydrofobowy, czyli niechętnie styka się i miesza z wodą. Częściowo zhydrolizowany tłuszcz z wolnymi miejscami zachowuje się inaczej - jest łatwo zwilżalny, pozwala wodzie tworzyć ścisłą warstewkę na powierzchni kropli i wchłania pewną ilość wody. Dodany do zwykłego tłuszczu ułatwia tworzenie emulsji, i dlatego jest dodany do margaryny aby się nie rozdzielała.
Takie mono i diglicerydy nie są szkodliwe. Powstają w naszych jelitach podczas trawienia tłuszczu, i w pewnym stopniu ułatwiają ten proces, właśnie przez tworzenie emulsji.
* Lecytyna - Kolejny emulgator. Naturalny fosfolipid otrzymywany albo z jaj kurzych, albo soi albo z rzepaku. W pewnym sensie jest to pochodna diglicerydów, zawierająca resztę fosforanową i cholinę. Pomaga w tworzeniu emulsji i mieszaniu tłuszczy z wodą. Nieszkodliwa, składnik naszego organizmu głównie w układzie nerwowym.
*sól 0,5%
*przeciwutleniacz palmitynian askorbylu - ta trudna chemiczna nazwa opisuje nietypowe połączenie. Jest to ester kwasu tłuszczowego, konkretnie kwasu palmitynowego, z kwasem askorbinowym, czyli witaminą C. Dzięki takiej formie witamina staje się rozpuszczalna w tłuszczach, dzięki czemu zapobiega ich utlenieniu i jełczeniu. Nieszkodliwa, podczas trawienia jest rozkładana na składowe.
* mieszanina tokoferoli - tokoferole to witamina E. Naturalna forma występująca w tłuszczach to mieszanka ośmiu podobnych związków. Są antyoksydantami wymiatającymi wolne rodniki i zapobiegającymi utlenianiu tłuszczy, stąd zastosowanie do utrwalania margaryn i majonezów.
2. Nadzienie czekoladowe
* woda
* syrop glukozowy
* cukier
* skrobia modyfikowana 2,5% - nie podano która konkretnie skrobia modyfikowana, w każdym bądź razie składnik nieszkodliwy, zagęstnik
* kakao niskotłuszczowe w proszku
* olej palmowy
* zagęstniki: celuloza E 460
* karboksymetyloceluloza E 466 - pochodna celulozy podstawiona kwasem octowym z wolną grupą karboksylową. Rozpuszczalna w wodzie, zwiększa lepkość roztworów. Nieszkodliwa, choć w dużych ilościach może powodować wzdęcia.
* karagen - już omówiony
* guma ksantanowa - produkt fermentacji węglowodanów. Zwiększa lepkość roztworów w sposób odporny na zmiany temperatur. Nieszkodliwa, choć w dużych ilościach może wywołać wzdęcia
* regulator kwasowości: lakton kwasu glukonowego. Pochodna glukozy powstająca w wyniku jej utlenienia. Lekko kwaśny, równowaga z kwasem glukonowym powoduje, że działa podobnie do bufora. Nieszkodliwy, jeden z produktów metabolizmu glukozy, przetwarzany tak samo jak ona.
*aromat - ?
* sól
* konserwant - sorbinian potasu - już omówiony
* barwnik dwutlenek tytanu - tak na prawdę pigment. nierozpuszczalny biały proszek, rozpraszający światło. Nie ulega strawieniu, wydalany, nietrujący.
* wanilina
* substancja emulgująca polisorbat 60 - inaczej monooleinian polioksyetylenosorbitolu. Połączenie sorbitolu, zwykle używanego jako słodzik, z kwasem tłuszczowym, w tym przypadku oleinowym. Z czterech grup hydroksylowych sorbitolu, jedna łączy się z kwasem tłuszczowym, zaś pozostałe mają przyłączony łańcuch polieterowy.
Takie połączenie pomaga tłuszczom tworzyć małe kropelki łączące się ze skrobią w jednolitą masę. Pomaga pęcherzykom powietrza przyklejać się do tłuszczu, stąd użycie w produktach spienionych. W lodach spowalnia rozpływanie się. Nieszkodliwy. Podczas trawienia rozpada się na sorbitol, kwasy tłuszczowe i kwas szczawiowy.
Ostatnim składnikiem z podaną ilością była skrobia modyfikowana i było jej 2,5%. Następnie mieliśmy 12 składników. Ponieważ składniki uszeregowano od największej ilości do najmniejszej polisorbatu musi być na prawdę mało.
3. Polewa o smaku czekoladowym
* Cukier
* tłuszcz roślinny częściowo utwardzony
* proszek kakaowy niskotłuszczowy 16%
*miazga kakaowa 1,3%
*emulgatory E 222 - zły numer, dodatek o tym numerze to konserwant wodorosiarczan sodu, konserwujący przetwory owocowe, chodziło zapewne o E 322 czyli lecytynę sojowa, już omówioną
*E 476 - Polirycynoleinian poliglicerolu, pochodna tłuszczu gdzie z kwasem tłuszczowym rycynolowym połączona jest spolimeryzowana gliceryna. Podczas trawienia rozpada się na glicerynę i kwas rycynolowy. U zwierząt duże dawki powiększają wątrobę, u ludzi tego nie stwierdzono. Teoretycznie powinien wywoływać przeczyszczenie po spożyciu większej ilości, ze względu na kwas rycynolowy, ten sam co w oleju rycynowym, ale chyba nie ma bo w produktach tak dużo.
Jest emulgatorem do mas stałych, wiąże tłuszcze krzepnące w temperaturze pokojowej z cząstkami skrobi i cukrem. Chętnie używany w masach czekoladowych gdzie zapobiega oddzielaniu się cząstek kakao. Używany w czekoladach niskotłuszczowych, ma bowiem właściwości podobne do masła kakaowego ale może być użyty w mniejszych ilościach
* Aromat - ?
Uff! Trochę tego było.
Po odjęciu powtarzających się składników zostaje ok. 30. Jeśli nie brać pod uwagę zwyczajnych składników ciast, a więc cukru, mąki, kakao itp.; jeśli odjąć składniki nieszkodliwe jak kwas cytrynowy, lecytyna, glukonolakton itd. to ostatecznie dyskusyjnych pozostaje tylko kilka - kwas sorbowy mogący wywoływać alergie na skórze, barwnik annato mogący wywołać alergię, kontrowersyjny karagen. Składników typowo alergicznych jak soja czy białko jaj nie liczę, bo to nie dodatki.
[Edit: Jak to się potrafi nauka szybko zmieniać. Gdy pisałem artykuł nie było wiadomo nic na temat szkodliwego wpływu emulgatorów. Tymczasem we wczorajszym numerze The Nature ukazał się artykuł o związku niektórych emulgatorów ze stanami zapalnymi jelit. Przebadane emulgatory czyli kaboksymetyloceluloza i polisorbat 80 podawane przez dłuższy czas szczurom, powodowały zmianę składu bakterii jelitowych na taki, który sprzyjał stanom zapalnym. {2}
Jak napisałem, dodatek ten może wywoływać wzdęcia w większych ilościach. Wynika to stąd że mogą go przetwarzać bakterie jelitowe, wydzielając gazy. Najwyraźniej jedne szczepy rosną w ich obecności lepiej od innych, więc gdy jedzenie z dużą ilością tych dodatków stanowi częsty składnik diety, flora bakteryjna jelit się przebudowuje. Stanowiłoby to kolejny argument za tym, aby nie zajadać się pączkami.
Jeśli mechanizm jest rzeczywiście taki, to polirycynooleinian, mono i diglicerydy oraz lecytyna nie powinny wywoływać tego efektu, nie są bowiem trawione przez bakterie jelitowe.]
Zatem teraz jeśli już dyskutować o składzie pączka, to niech to będzie dyskusja o tym czy potrzebny jest tam karagen i czy nie ma aby za dużo tłuszczu, a nie dyskusja o tym, że "to musi być szkodliwe bo ma tyle różnych składników" zupełnie jakby ludzie czytać nie umieli.
-------------
[1] http://www.basso.pl/oferta-masa-jajowa.html
{2} Chassaing, B. et al. Nature http://www.dx.doi.org/10.1038/nature14232 (2015). 25 luty
* Przykładowy przepis (stąd):
" SKŁADNIKI:
- 300g mąki pszennej,
- 150g masła temp. pokojowa,
- 60g cukru pudru,
- 2 żółtka (z wiejskich jajek),
- 1/2 buteleczki aromatu waniliowego,
- 1/2 łyżeczki sody oczyszczonej,
- szczypta soli.
DODATKOWO
- 150g dżemu agrestowego, wysokosłodzonego np. z firmy GIL,
- 100g mlecznej czekolady (jeżeli dzieci lubią lepsza gorzka;))"
Biorąc pod uwagę składniki dżemu wymienione na stronie producenta (link) i składniki czekolady mlecznej (Wedel), gdybyśmy musieli dodać etykietkę ze składnikami własnoręcznie upieczonych domowych ciastek, wyglądałaby tak:
No cóż. Odkrycie że pączek nie składa się po prostu z pączka, dla wielu może być zaskakujące, jednak wczytując się w artykuły o tym znalezisku zauważyłem, że nikt nie podał merytorycznych argumentów. Zamiast "ten pączek jest zły bo zawiera składnik X którzy szkodzi" cała argumentacja we wszystkich artykułach opiera się na stwierdzeniu "to musi być złe bo ma tak dużo składników". I dla wielu zatrzymywanie się na tym etapie jest wystarczające - na Facebookowym profilu Czytamy Etykiety omawianie składu zaczyna się od oglądania etykiety i koniec, już można komentować że syf, że złe, że można popić płynem do naczyń.
No to teraz przeprowadźmy merytoryczny rozbiór pączka na składniki.
Na początku wyjaśnienie - producent podał pełny skład produktu, ze składnikami wedle malejącego udziału z podziałem na poszczególne części. Pączek zawiera w sobie właściwe ciasto, czekoladowe nadzienie i polewę czekoladową czarną. Każda z tych składowych ma swoje własne składniki, które muszą zostać wymienione osobno, nawet jeśli się powtarzają. Z pobieżnego przeglądu można wychwycić, że w składzie wymieniającym składniki tych trzech substancji składających na pączek woda pojawia się trzy razy, utwardzone tłuszcze roślinne trzy razy, sól dwa razy, sorbinian dwa razy, cukier trzy razy, kwas cytrynowy trzy razy...
To trochę tak jakbyście chcieli sprzedawać domowe ciasteczka z dżemem i czekoladą i musieli dodać skład w którym zmuszeni byście byli wymienić nie tylko wszystkie składniki ciasta, ale jeszcze wszystkie składniki dżemu i wszystkie składniki czekolady, nawet gdy się będą powtarzać. Wtedy też wam wyjdzie bardzo długa lista.*
No ale może po kolei. Najpierw idą składniki ciasta, począwszy od mąki, aż dochodzimy do margaryny 80% i dalej wymienione mamy składniki margaryny użytej do ciasta aż do pozycji "mieszanka tokoferoli" potem znów dalsze składniki ciasta, których było mniej niż margaryny, w tym ponownie sól, aż do aromatu.
Potem idą składniki nadzienia czekoladowego, począwszy od wody a skończywszy na polisorbacie, i na koniec składniki polewy. I jeszcze lista alergenów. Rozpatrzmy więc składniki osobno:
1. Ciasto
*Mąka pszenna - jakieś zastrzeżenia?
*Masa jajowa płynna pasteryzowana - Ten tajemniczo brzmiący składnik, jest dokładnie tym co pierwsze przychodzi na myśl. To po prostu białko i żółtko zmiksowane razem i zapasteryzowane. Jak podaje na swojej stronie jeden z producentów masy, jej produkcja opiera się na następujących etapach: wybijanie świeżych jaj kurzych, filtrowanie, pasteryzacja, schładzanie [1]. Żadnych dodatków, konserwantów, barwników itp. Jakieś zastrzeżenia?
*Cukier
*Drożdże
(margaryna osobno)
*substancja konserwująca kwas sorbowy - konserwant pochodzący z owoców jarzębiny, zapobiega wzrostowi pleśni a także pałeczki jadu kiełbasianego, może wywoływać alergie na skórze natomiast nie jest szkodliwy wewnętrznie (zatem pamiętajcie - nie smarujcie się ciastem od pączka)
* regulator kwasowości kwas cytrynowy - nieszkodliwy
* barwnik annato - jest to barwnik naturalny, wyciąg z osnówek nasion Arnoty właściwej, tropikalnego krzewu z ameryki południowej, zawierający karotenoidy i terpenoidy. Pozwala uzyskać kolor od żółtego do czerwono-pomarańczowego, zwykle używany do serów, tu zapewne w śladowych ilościach dla nadania ciastu kremowego odcienia. W dużych ilościach może wywoływać alergie, dlatego normy są bardzo wyśrubowane.
* woda
*sól
* mleko w proszku
* polepszacz E 407 - Karagen, substancja żelująca otrzymywana z czerwonych krasnorostów. Głównym składnikiem jest polisacharyd o bardzo dużej ilości grup sulfonowych. Zwiększa lepkość i spowalnia sedymentację. ze względu na grupy sulfonowe może wywoływać reakcje u uczulonych na siarczyny. Jest składnikiem kontrowersyjnym - niektóre badania wskazują że ma wpływ na rozwój raka jelita grubego. Ponieważ jednak inne badania tego efektu nie wykazują, formalnie nie jest na liście kancerogenów.
* Aromat - ?
1.a Margaryna 80%
* Oleje roślinne i tłuszcze roślinne utwardzone
* woda
* emulgatory, mono i dwuglicerydy kwasów tłuszczowych - pochodna tłuszczów. Zwykłe tłuszcze składają się z gliceryny, alkoholu trójwodorotlenowego, połączonego wiązaniami estrowymi z trzema cząsteczkami kwasów tłuszczowych. W wyniku częściowej hydrolizy kwasem lub enzymem, otrzymnujemu mono gliceryd z jednym kwasem tłuszczowym i dwiema wolnymi grupami hydroksylowymi gliceryny, lub diglicerydy z dwoma kwasami tłuszczowymi.
Póki wszystkie trzy miejsca w glicerynie są zajęte, tłuszcz jest hydrofobowy, czyli niechętnie styka się i miesza z wodą. Częściowo zhydrolizowany tłuszcz z wolnymi miejscami zachowuje się inaczej - jest łatwo zwilżalny, pozwala wodzie tworzyć ścisłą warstewkę na powierzchni kropli i wchłania pewną ilość wody. Dodany do zwykłego tłuszczu ułatwia tworzenie emulsji, i dlatego jest dodany do margaryny aby się nie rozdzielała.
Takie mono i diglicerydy nie są szkodliwe. Powstają w naszych jelitach podczas trawienia tłuszczu, i w pewnym stopniu ułatwiają ten proces, właśnie przez tworzenie emulsji.
* Lecytyna - Kolejny emulgator. Naturalny fosfolipid otrzymywany albo z jaj kurzych, albo soi albo z rzepaku. W pewnym sensie jest to pochodna diglicerydów, zawierająca resztę fosforanową i cholinę. Pomaga w tworzeniu emulsji i mieszaniu tłuszczy z wodą. Nieszkodliwa, składnik naszego organizmu głównie w układzie nerwowym.
*sól 0,5%
*przeciwutleniacz palmitynian askorbylu - ta trudna chemiczna nazwa opisuje nietypowe połączenie. Jest to ester kwasu tłuszczowego, konkretnie kwasu palmitynowego, z kwasem askorbinowym, czyli witaminą C. Dzięki takiej formie witamina staje się rozpuszczalna w tłuszczach, dzięki czemu zapobiega ich utlenieniu i jełczeniu. Nieszkodliwa, podczas trawienia jest rozkładana na składowe.
* mieszanina tokoferoli - tokoferole to witamina E. Naturalna forma występująca w tłuszczach to mieszanka ośmiu podobnych związków. Są antyoksydantami wymiatającymi wolne rodniki i zapobiegającymi utlenianiu tłuszczy, stąd zastosowanie do utrwalania margaryn i majonezów.
2. Nadzienie czekoladowe
* woda
* syrop glukozowy
* cukier
* skrobia modyfikowana 2,5% - nie podano która konkretnie skrobia modyfikowana, w każdym bądź razie składnik nieszkodliwy, zagęstnik
* kakao niskotłuszczowe w proszku
* olej palmowy
* zagęstniki: celuloza E 460
* karboksymetyloceluloza E 466 - pochodna celulozy podstawiona kwasem octowym z wolną grupą karboksylową. Rozpuszczalna w wodzie, zwiększa lepkość roztworów. Nieszkodliwa, choć w dużych ilościach może powodować wzdęcia.
* karagen - już omówiony
* guma ksantanowa - produkt fermentacji węglowodanów. Zwiększa lepkość roztworów w sposób odporny na zmiany temperatur. Nieszkodliwa, choć w dużych ilościach może wywołać wzdęcia
* regulator kwasowości: lakton kwasu glukonowego. Pochodna glukozy powstająca w wyniku jej utlenienia. Lekko kwaśny, równowaga z kwasem glukonowym powoduje, że działa podobnie do bufora. Nieszkodliwy, jeden z produktów metabolizmu glukozy, przetwarzany tak samo jak ona.
*aromat - ?
* sól
* konserwant - sorbinian potasu - już omówiony
* barwnik dwutlenek tytanu - tak na prawdę pigment. nierozpuszczalny biały proszek, rozpraszający światło. Nie ulega strawieniu, wydalany, nietrujący.
* wanilina
* substancja emulgująca polisorbat 60 - inaczej monooleinian polioksyetylenosorbitolu. Połączenie sorbitolu, zwykle używanego jako słodzik, z kwasem tłuszczowym, w tym przypadku oleinowym. Z czterech grup hydroksylowych sorbitolu, jedna łączy się z kwasem tłuszczowym, zaś pozostałe mają przyłączony łańcuch polieterowy.
Takie połączenie pomaga tłuszczom tworzyć małe kropelki łączące się ze skrobią w jednolitą masę. Pomaga pęcherzykom powietrza przyklejać się do tłuszczu, stąd użycie w produktach spienionych. W lodach spowalnia rozpływanie się. Nieszkodliwy. Podczas trawienia rozpada się na sorbitol, kwasy tłuszczowe i kwas szczawiowy.
Ostatnim składnikiem z podaną ilością była skrobia modyfikowana i było jej 2,5%. Następnie mieliśmy 12 składników. Ponieważ składniki uszeregowano od największej ilości do najmniejszej polisorbatu musi być na prawdę mało.
3. Polewa o smaku czekoladowym
* Cukier
* tłuszcz roślinny częściowo utwardzony
* proszek kakaowy niskotłuszczowy 16%
*miazga kakaowa 1,3%
*emulgatory E 222 - zły numer, dodatek o tym numerze to konserwant wodorosiarczan sodu, konserwujący przetwory owocowe, chodziło zapewne o E 322 czyli lecytynę sojowa, już omówioną
*E 476 - Polirycynoleinian poliglicerolu, pochodna tłuszczu gdzie z kwasem tłuszczowym rycynolowym połączona jest spolimeryzowana gliceryna. Podczas trawienia rozpada się na glicerynę i kwas rycynolowy. U zwierząt duże dawki powiększają wątrobę, u ludzi tego nie stwierdzono. Teoretycznie powinien wywoływać przeczyszczenie po spożyciu większej ilości, ze względu na kwas rycynolowy, ten sam co w oleju rycynowym, ale chyba nie ma bo w produktach tak dużo.
Jest emulgatorem do mas stałych, wiąże tłuszcze krzepnące w temperaturze pokojowej z cząstkami skrobi i cukrem. Chętnie używany w masach czekoladowych gdzie zapobiega oddzielaniu się cząstek kakao. Używany w czekoladach niskotłuszczowych, ma bowiem właściwości podobne do masła kakaowego ale może być użyty w mniejszych ilościach
* Aromat - ?
Uff! Trochę tego było.
Po odjęciu powtarzających się składników zostaje ok. 30. Jeśli nie brać pod uwagę zwyczajnych składników ciast, a więc cukru, mąki, kakao itp.; jeśli odjąć składniki nieszkodliwe jak kwas cytrynowy, lecytyna, glukonolakton itd. to ostatecznie dyskusyjnych pozostaje tylko kilka - kwas sorbowy mogący wywoływać alergie na skórze, barwnik annato mogący wywołać alergię, kontrowersyjny karagen. Składników typowo alergicznych jak soja czy białko jaj nie liczę, bo to nie dodatki.
[Edit: Jak to się potrafi nauka szybko zmieniać. Gdy pisałem artykuł nie było wiadomo nic na temat szkodliwego wpływu emulgatorów. Tymczasem we wczorajszym numerze The Nature ukazał się artykuł o związku niektórych emulgatorów ze stanami zapalnymi jelit. Przebadane emulgatory czyli kaboksymetyloceluloza i polisorbat 80 podawane przez dłuższy czas szczurom, powodowały zmianę składu bakterii jelitowych na taki, który sprzyjał stanom zapalnym. {2}
Jak napisałem, dodatek ten może wywoływać wzdęcia w większych ilościach. Wynika to stąd że mogą go przetwarzać bakterie jelitowe, wydzielając gazy. Najwyraźniej jedne szczepy rosną w ich obecności lepiej od innych, więc gdy jedzenie z dużą ilością tych dodatków stanowi częsty składnik diety, flora bakteryjna jelit się przebudowuje. Stanowiłoby to kolejny argument za tym, aby nie zajadać się pączkami.
Jeśli mechanizm jest rzeczywiście taki, to polirycynooleinian, mono i diglicerydy oraz lecytyna nie powinny wywoływać tego efektu, nie są bowiem trawione przez bakterie jelitowe.]
Zatem teraz jeśli już dyskutować o składzie pączka, to niech to będzie dyskusja o tym czy potrzebny jest tam karagen i czy nie ma aby za dużo tłuszczu, a nie dyskusja o tym, że "to musi być szkodliwe bo ma tyle różnych składników" zupełnie jakby ludzie czytać nie umieli.
-------------
[1] http://www.basso.pl/oferta-masa-jajowa.html
{2} Chassaing, B. et al. Nature http://www.dx.doi.org/10.1038/nature14232 (2015). 25 luty
* Przykładowy przepis (stąd):
" SKŁADNIKI:
- 300g mąki pszennej,
- 150g masła temp. pokojowa,
- 60g cukru pudru,
- 2 żółtka (z wiejskich jajek),
- 1/2 buteleczki aromatu waniliowego,
- 1/2 łyżeczki sody oczyszczonej,
- szczypta soli.
DODATKOWO
- 150g dżemu agrestowego, wysokosłodzonego np. z firmy GIL,
- 100g mlecznej czekolady (jeżeli dzieci lubią lepsza gorzka;))"
Biorąc pod uwagę składniki dżemu wymienione na stronie producenta (link) i składniki czekolady mlecznej (Wedel), gdybyśmy musieli dodać etykietkę ze składnikami własnoręcznie upieczonych domowych ciastek, wyglądałaby tak:
Składrazem 24 punkty w spisie. Smacznego.
Ciasto: mąka pszenna, masło, cukier, żółtka jaj kurzych, spulchniacz wodorowęglan sodu (E 500b), wanilina, sól; Dżem agrestowy wysokosłodzony pasteryzowany: pulpa agrestowa z kawałkami owoców, cukier, kwas cytrynowy (E 330), zagęstnik pektyny (E 400); masa czekoladowa: cukier, tłuszcz kakaowy, mleko pełne w proszku, miazga kakaowa, serwatka w proszku, laktoza, białka mleka, miazga z orzechów laskowych, tłuszcz mleczny, emulgator: lecytyna sojowa, aromat. Informacja dla alergików: zawiera jaja, pszenica, białka mleka, laktoza, orzechy laskowe; może zawierać gluten, ślady soi i innych orzechów.
piątek, 28 listopada 2014
Dwie anegdoty o chemikach
Aby przełamać totalny blog-blok, wrzucam na szybko dwie historyjki z cyklu anegdot o chemikach. Już tu pisałem o serendipity - przypadkach doprowadzających do odkryć. Jak się okazuje takich przypadków było w historii znacznie więcej.
Na skutek złej znajomości języka
Język jest w badaniach chemicznych bardzo ważny. Większość publikacji z jakich się korzysta jest w języku angielskim, pewne znaczenie ma może jeszcze niemiecki, i dlatego powinno się te języki znać. Nieporozumienie językowe może bowiem przynieść zaskakujące skutki.
W 1979 roku w Londyńskim Queen Elizabeth College trwały badania nad uzyskiwaniem halogenopochodnych cukrów, mogących mieć właściwości biologiczne. Podejrzewano że pochodne z dużą ilością takich podstawników mogą być przydatne jako środki owadobójcze podobne do DDT. Jednym z takich cukrów była sacharoza czyli cukier stołowy. Posiada ona osiem grup wodorotlenowych które mogą być bez niszczenia cząsteczki zastąpione atomem chloru, dlatego po standardowym chlorowaniu otrzymano mieszaninę podobnych związków z jedną, dwoma, trzema i więcej podstawionych grup w różnym układzie. Po oczyszczeniu poszczególnych związków, prowadzący badania oddał je swojemu magistrantowi, pochodzącemu z Indii Shashikantowi Phadnisowi, polecając ustnie, aby je przetestował.
Doszło tu jednak do nieporozumienia - student zrozumiał nie że związki należy przetestować (testing) tylko posmakować (tasting). Wziął więc łopatką odrobinę na język i wkrótce doniósł osłupiałemu kierownikowi, że jeden z tych związków smakuje niesamowicie słodko. Tak odkryto słodzik sukralozę, ok. 600 razy słodszy od wyjściowej sacharozy i trzy razy od aspartamu. W porównaniu z innymi słodzikami jest bardzo słabo wchłaniany i trwały termicznie, zarazem jednak jako związek chloroorganiczny budzi kontrowersje.[1]
Słodziki mają jakąś specjalną predylekcję do zbiegów okoliczności...
Dlaczego czasem warto zbadać odpady
Charles J. Pedersen pracując w koncernie chemicznym DuPont zajmował się poszukiwaniem nowych związków kompleksujących metale. Zanieczyszczenia jonami metali ciężkich w ropie i paliwach przyspieszały ich utlenianie, a co za tym idzie, pogorszenie jakości. Wymyślił więc związki które tworzyły z jonami żelaza i miedzi dosyć trwałe kompleksy, przerywając utlenianie. W pewnej chwili zainteresował się problemem selektywnego kompleksowania wanadu. Chcąc sprawdzić jaki związek będzie najefektywniej wiązał jego kationy, postanowił zsyntetyzować pochodną katecholu, łącząc ze sobą dwie cząsteczki przez łańcuch diglikolu etylenowego, i pozostawiając wolne dwie grupy hydroksylowe. Rozumował, że powstający mostek eterowy powinien zwiększyć rozstaw między cząsteczkami powstającego fenolu, co jego zdaniem powinno wyraźnie wpłynąć na kompleksowanie wanadu.
Aby połączyć dwie cząsteczki katecholu jednym mostkiem i nie uzyskać polimeru, zabezpieczył jedną z dwóch grup wodorotlenowych tego związku grupą etylową. Następnie przeprowadził reakcję zabezpieczonego związku z chloropochodną diglikolu, spodziewając się uzyskać poszukiwany związek.
Wstawiając reakcję wiedział zarazem, że substrat jest nadal nieco zanieczyszczony wolnym katecholem, uznał jednak że nie przeszkodzi on w reakcji.
Mieszanina poreakcyjna miała postać szarawej, gęstej mazi, którą należało teraz rozdzielić. Gdy rozpuścił ją w metanolu zauważył, że na dnie zebrało się odrobinę białawego osadu. Było to na prawdę niewiele - związek powstał z wydajnością 0,4%, a ponieważ był mało rozpuszczalny, to na pewno nie był to związek poszukiwany. Pedersen zajmował się produkcją określonego związku do określonego celu i nie miał potrzeby wdawać się w szersze analizy. Niemniej zastanowiła go delikatna, włóknista struktura osadu.
Mając na podorędziu spektroskop UV postanowił zbadać czy ma do czynienia z jakimś fenolem - widmo pokazało że musi to być jakaś podstawiona pochodna katecholu. Postanowił dodać nieco wodorotlenku sodu aby zalkalizować roztwór, oczekując że widmo absorpcji albo nie zmieni się, dla związku bez wolnych grup, albo maksimum absorpcji pogłębi się i przesunie się w stronę mniejszych długości fal. Tymczasem jednak zaobserwował dwie zaskakujące rzeczy - widmo nie przesunęło się lecz podzieliło na mniejsze pasma, zaś związek przedtem bardzo słabo rozpuszczający się w metanolu, po zalkalizowaniu rozpuszczał się bardzo chętnie.
Gdyby był to związek fenolowy, zwiększenie rozpuszczalności tłumaczyłoby się tworzeniem soli, fenole są bowiem dosyć kwaśne, jednak widma NMR i w podczerwieni wykluczały taką możliwość. W dodatku jak wykazał, aby zwiększyć rozpuszczalność związku, wystarczała dowolna sól sodu bądź potasu.
Był to zatem związek łączący się z kationami tych metali, choć nie bardzo miał w jaki sposób. Po analizie elementarnej Pedersenowi wyszedł wzór C10H12O3, z czego wynikałaby struktura:
Potem inne badania wykazały jednak że rzeczywista masa cząsteczkowa jest dwa razy większa. A skoro tak musiała to był taka oto piękna struktura:
Tym samym odkrył pierwszy znany eter koronowy.[2]
Nazwa tej grupy związków makrocyklicznych bierze się od struktury, w której możliwa jest konformacja z atomami tlenu skierowanymi w jedną stronę płaszczyzny, niczym szpice w koronie. Mają niesamowite zdolności do kompleksowania - wynaleziony przez Pedersena związek dibenzo-18-korona-6 bardzo selektywnie kompleksuje potas, robiąc to z taką siłą, iż można za jego pomocą oddzielić kationy potasu od innych metali. Inne etery kompleksują sód, wapń czy magnez, każdy z inną siłą, wszystko zależy od wielkości "oczka" które lepiej pasuje do jednych jonów a gorzej do innych. Skompleksowany jon przestaje być reaktywny, dlatego dodatek odpowiedniego związku do badanej mieszaniny, może zamaskować przeszkadzające metale.
Etery takie mogą zmieniać konformację i rozpuszczalność, możliwe jest więc przeprowadzenie normalnie nierozpuszczalnych kationów metali do fazy organicznej. Mogą też przydać się jako katalizatory.
Za badania nad eterami koronowymi, zapoczątkowanymi dokładniejszą analizą odpadowego produktu, Pedersen został w 1987 roku uhonorowany Nagrodą Nobla z Chemii.
------------
[1] http://www.laleva.org/eng/2006/12/the_history_of_splenda_the_bestselling_artificial_sweetener_in_america.html
[2] http://www.nobelprize.org/nobel_prizes/chemistry/laureates/1987/pedersen-lecture.pdf
Na skutek złej znajomości języka
Język jest w badaniach chemicznych bardzo ważny. Większość publikacji z jakich się korzysta jest w języku angielskim, pewne znaczenie ma może jeszcze niemiecki, i dlatego powinno się te języki znać. Nieporozumienie językowe może bowiem przynieść zaskakujące skutki.
W 1979 roku w Londyńskim Queen Elizabeth College trwały badania nad uzyskiwaniem halogenopochodnych cukrów, mogących mieć właściwości biologiczne. Podejrzewano że pochodne z dużą ilością takich podstawników mogą być przydatne jako środki owadobójcze podobne do DDT. Jednym z takich cukrów była sacharoza czyli cukier stołowy. Posiada ona osiem grup wodorotlenowych które mogą być bez niszczenia cząsteczki zastąpione atomem chloru, dlatego po standardowym chlorowaniu otrzymano mieszaninę podobnych związków z jedną, dwoma, trzema i więcej podstawionych grup w różnym układzie. Po oczyszczeniu poszczególnych związków, prowadzący badania oddał je swojemu magistrantowi, pochodzącemu z Indii Shashikantowi Phadnisowi, polecając ustnie, aby je przetestował.
Doszło tu jednak do nieporozumienia - student zrozumiał nie że związki należy przetestować (testing) tylko posmakować (tasting). Wziął więc łopatką odrobinę na język i wkrótce doniósł osłupiałemu kierownikowi, że jeden z tych związków smakuje niesamowicie słodko. Tak odkryto słodzik sukralozę, ok. 600 razy słodszy od wyjściowej sacharozy i trzy razy od aspartamu. W porównaniu z innymi słodzikami jest bardzo słabo wchłaniany i trwały termicznie, zarazem jednak jako związek chloroorganiczny budzi kontrowersje.[1]
Słodziki mają jakąś specjalną predylekcję do zbiegów okoliczności...
Dlaczego czasem warto zbadać odpady
Charles J. Pedersen pracując w koncernie chemicznym DuPont zajmował się poszukiwaniem nowych związków kompleksujących metale. Zanieczyszczenia jonami metali ciężkich w ropie i paliwach przyspieszały ich utlenianie, a co za tym idzie, pogorszenie jakości. Wymyślił więc związki które tworzyły z jonami żelaza i miedzi dosyć trwałe kompleksy, przerywając utlenianie. W pewnej chwili zainteresował się problemem selektywnego kompleksowania wanadu. Chcąc sprawdzić jaki związek będzie najefektywniej wiązał jego kationy, postanowił zsyntetyzować pochodną katecholu, łącząc ze sobą dwie cząsteczki przez łańcuch diglikolu etylenowego, i pozostawiając wolne dwie grupy hydroksylowe. Rozumował, że powstający mostek eterowy powinien zwiększyć rozstaw między cząsteczkami powstającego fenolu, co jego zdaniem powinno wyraźnie wpłynąć na kompleksowanie wanadu.
| Katechol |
Aby połączyć dwie cząsteczki katecholu jednym mostkiem i nie uzyskać polimeru, zabezpieczył jedną z dwóch grup wodorotlenowych tego związku grupą etylową. Następnie przeprowadził reakcję zabezpieczonego związku z chloropochodną diglikolu, spodziewając się uzyskać poszukiwany związek.
Wstawiając reakcję wiedział zarazem, że substrat jest nadal nieco zanieczyszczony wolnym katecholem, uznał jednak że nie przeszkodzi on w reakcji.
Mieszanina poreakcyjna miała postać szarawej, gęstej mazi, którą należało teraz rozdzielić. Gdy rozpuścił ją w metanolu zauważył, że na dnie zebrało się odrobinę białawego osadu. Było to na prawdę niewiele - związek powstał z wydajnością 0,4%, a ponieważ był mało rozpuszczalny, to na pewno nie był to związek poszukiwany. Pedersen zajmował się produkcją określonego związku do określonego celu i nie miał potrzeby wdawać się w szersze analizy. Niemniej zastanowiła go delikatna, włóknista struktura osadu.
Mając na podorędziu spektroskop UV postanowił zbadać czy ma do czynienia z jakimś fenolem - widmo pokazało że musi to być jakaś podstawiona pochodna katecholu. Postanowił dodać nieco wodorotlenku sodu aby zalkalizować roztwór, oczekując że widmo absorpcji albo nie zmieni się, dla związku bez wolnych grup, albo maksimum absorpcji pogłębi się i przesunie się w stronę mniejszych długości fal. Tymczasem jednak zaobserwował dwie zaskakujące rzeczy - widmo nie przesunęło się lecz podzieliło na mniejsze pasma, zaś związek przedtem bardzo słabo rozpuszczający się w metanolu, po zalkalizowaniu rozpuszczał się bardzo chętnie.
Gdyby był to związek fenolowy, zwiększenie rozpuszczalności tłumaczyłoby się tworzeniem soli, fenole są bowiem dosyć kwaśne, jednak widma NMR i w podczerwieni wykluczały taką możliwość. W dodatku jak wykazał, aby zwiększyć rozpuszczalność związku, wystarczała dowolna sól sodu bądź potasu.
Był to zatem związek łączący się z kationami tych metali, choć nie bardzo miał w jaki sposób. Po analizie elementarnej Pedersenowi wyszedł wzór C10H12O3, z czego wynikałaby struktura:
Potem inne badania wykazały jednak że rzeczywista masa cząsteczkowa jest dwa razy większa. A skoro tak musiała to był taka oto piękna struktura:
Tym samym odkrył pierwszy znany eter koronowy.[2]
Nazwa tej grupy związków makrocyklicznych bierze się od struktury, w której możliwa jest konformacja z atomami tlenu skierowanymi w jedną stronę płaszczyzny, niczym szpice w koronie. Mają niesamowite zdolności do kompleksowania - wynaleziony przez Pedersena związek dibenzo-18-korona-6 bardzo selektywnie kompleksuje potas, robiąc to z taką siłą, iż można za jego pomocą oddzielić kationy potasu od innych metali. Inne etery kompleksują sód, wapń czy magnez, każdy z inną siłą, wszystko zależy od wielkości "oczka" które lepiej pasuje do jednych jonów a gorzej do innych. Skompleksowany jon przestaje być reaktywny, dlatego dodatek odpowiedniego związku do badanej mieszaniny, może zamaskować przeszkadzające metale.
Etery takie mogą zmieniać konformację i rozpuszczalność, możliwe jest więc przeprowadzenie normalnie nierozpuszczalnych kationów metali do fazy organicznej. Mogą też przydać się jako katalizatory.
Za badania nad eterami koronowymi, zapoczątkowanymi dokładniejszą analizą odpadowego produktu, Pedersen został w 1987 roku uhonorowany Nagrodą Nobla z Chemii.
------------
[1] http://www.laleva.org/eng/2006/12/the_history_of_splenda_the_bestselling_artificial_sweetener_in_america.html
[2] http://www.nobelprize.org/nobel_prizes/chemistry/laureates/1987/pedersen-lecture.pdf
sobota, 15 marca 2014
Chemik robi galaretki, czyli historia pewnego pomysłu
Pewnego razu wracając z zajęć do akademika zauważyłem w holu kolorowy plakat. Konkurs - brzmiał duży napis. Napój Nowej Generacji - dopisano poniżej. Oczywiście się zainteresowałem.
Konkurs organizowany przez uniwersytet i firmę spożywczą z Siedlec był skierowany do studentów, i kusił całkiem niezłą nagrodą pieniężną, zaś przedmiotem było wymyślenie i zaprezentowanie dodatku do napoju. To mogło by być coś w sam raz dla chemika - uznałem. I zapomniałem o sprawie. Dopiero gdy zostało kilka dni do końca terminu zgłaszania ruszyło mnie, że coś trzeba by spróbować, bo głupio by było nie wystartować.
Regulamin nie określał szczegółowo co ma być tematem konkursu - musiał być to dodatek do napojów, w formie pływających stałych cząstek lub dodatku smakowego. Tylko co też takiego wymyślić, aby było to zarazem oryginalne i łatwe do zrobienia? Pomysłów miałem od groma, jednak jednym z etapów konkursu była prezentacja wykonanego dodatku, więc takie pomysły jak błonnikowe kwiaty rozchylające płatki po położeniu na powierzchni napoju czy musujące kulki nadmuchiwane pianą po zamoknięciu, musiały pójść w odstawkę - w kuchni bym tego nie zrobił.
Plakat konkursowy nasuwał na myśl jakieś kulki, może żelowe. Faktycznie, kuchnia molekularna opierająca się na kulinarnych zastosowaniach zdobyczy nauki potrafi łatwo produkować żelowe kulki nazywane sztucznym kawiorem, z płynnym nadzieniem i twardą powłoczką. Tyle, że jeśli jest to tak znana sprawa, to wielu może wpaść na coś takiego, a przecież pomysły nie powinny się powtarzać - myślałem. Jak nie kulki to co? Po odrzuceniu kostek i trójkątów zdecydowałem się na gwiazdki.
Ale jakie? Powinny mieć ciekawy smak i coś charakterystycznego. Z ćwiczeń z rozpoznawaniem tworzyw sztucznych przez różną pływalność pamiętałem, że gdy gęstość stałego materiału jest podobna do gęstości cieczy, to unosi się on swobodnie wewnątrz cieczy. Zarazem jednak płaskie płatki materiału mają skłonność do układania się poziomo, jak opadający liść. Gdyby zatem - pomyślałem - ustawić je pionowo i równocześnie zawiesić swobodnie, to patrzący z boku na szklankę napoju widziałby dobrze kształt gwiazdki. A to już by było coś.
Jako materiał wybrałem sobie agar, głownie dlatego, że galaretka żelatynowa miewa niekiedy pewien posmak który nie każdemu pasuje, a także dlatego, że agar bardzo szybko zastyga i ma dobrą wydajność (łyżeczka na litr wody). Potem na pierwszym etapie tłumaczyłem też komisji, że taka galaretka byłaby wegetariańska na co coraz więcej osób zwraca uwagę. Tak więc gwiazdki z agaru, ale o jakim smaku? Postanowiłem spróbować czegoś nietypowego - smaku ostrego, konkretnie zaś imbiru. Smak kojarzył się z kolorem czerwonym, stąd projekt czerwonych-ostrych gwiazdek. Na podobnej zasadzie powstały inne typy: zielony-kwaśny i żółty-ananasowy. A jak z tym ustawieniem w zawieszeniu? Najprościej byłoby sprawić, że kształt będzie miał nie równo rozłożony ciężar. Postanowiłem zalewać żel tak, by z jednej strony płat był cieńszy, dzięki temu powinny się ustawiać cięższą połową w dół.
Ale miałem wrażenie, że to może być za mało. Trzeba było dodać do tego coś jeszcze, takiego fajnego, molekularnego a najlepiej chemicznego, żeby się coś działo w tej szklance. Może barwnik który nabiera koloru podczas wytrząsania w shakerze? Albo coś z zapachem? Albo może jeszcze... Pomysł który przyszedł mi do głowy na sam koniec był na tyle ciekawy, że postanowiłem zgłosić go osobno. Były to płatki galaretki, które po wrzuceniu do napoju zmieniają kolor na całkiem inny.
Wiele jest łatwo dostępnych i jadalnych substancji o właściwościach wskaźnika kwasowo-zasadowego. Większość napojów i soków owocowych ma odczyn kwaśny. Postanowiłem zatem przygotować twardą galaretkę zabarwioną takim wskaźnikiem z niewielkim dodatkiem alkalizującej sody oczyszczonej. Po wrzuceniu do napoju żel zakwaszałby się, zmieniając kolor.
Jest kilka takich kuchennych wskaźników. Najlepszym jest wywar z czerwonej kapusty, który zależnie od kwasowości przybiera kolor zielony w mocniejszych, niebieski w słabszych zasadach, w roztworach obojętnych lub lekko kwaśnych fioletowy a w kwaśnych różowy i czerwony. Płat galaretki barwionej kapustą przybierałby więc różne kolory zależnie od rodzaju napoju, stąd też jeden typ dodatku zachowując się różnie dawałby szeroki wachlarz efektów. Sami zresztą zobaczcie:
Płatki niebieskie to kolor surowego żelu o alkalicznym odczynie, różowe wyciągnąłem z soku pomarańczowego parę minut po dodaniu. Różnica koloru jest bardzo wyraźna.
Inny typ byłby zabarwiany wywarem z czarnych jagód, tutaj próbka:
Zielone płatki przed wrzuceniem, różowe po wyciągnięciu z napoju. Jeszcze inny typ byłby zabarwiany hibiskusem, który zmienia kolor w taki sam sposób.
Tak więc pomysł miałem a pierwsze próby pokazały, że się sprawdza. Teraz należało wysłać zgłoszenie. Zrobiłem to w ostatnim dniu terminu, tuż przed zamknięciem poczty i z zaaferowania wpisałem błędny adres. Tak to niestety ze mną jest że wiele robię na ostatnią chwilę, nie mogąc przedtem się zmobilizować. List jakoś jednak doszedł na miejsce i na tydzień przed pierwszym etapem, w połowie stycznia, dostałem zawiadomienie gdzie to i o której mam się prezentować. Przygotowałem prezentacje multimedialne, po czym zakasałem rękawy i zabrałem się do wyrobu. Najpierw sporządziłem wywar ze świeżego imbiru, a gdy był dostatecznie szczypiący, dodałem torebkę herbaty hibiskusowej. Gdy się naciągnęła dosypałem agaru.
Agar kupiłem w sklepie ze zdrową żywnością. Miał postać kremowego proszku bez smaku, nie rozpuszczalnego w zimnej wodzie i powoli w gorącej.
Następnie wylałem roztwór na plastikowy talerzyk, lekko go przechylając. Żel zastygł w krótkim czasie, praktycznie zaraz po ochłodzeniu, dzięki czemu w jeden wieczór wykonałem kilka prób z różnym składem.
W zasadzie największy problem sprawiło mi wycięcie gwiazdki, nie mam bowiem zbyt dużych zdolności manualnych, jakoś sobie jednak poradziłem.
W podobny sposób zrobiłem żel zabarwiany kapustą, tylko bez imbiru. Ciekawe zresztą jak czuły okazał się wskaźnik - barwa zmieniała się po dodaniu cukru, zawierającego alkaliczne domieszki, jak i po dodaniu agaru, będącego substancją lekko kwaśną (agar zawiera 0,3% grup sulfonowych i stanowi naturalny kationit). Małe próbki zapakowałem w pojemniki aby pokazać na pierwszym etapie.
Jak to wyglądało? Całkiem spokojnie, wręcz kameralnie. Uczestnicy, których było około dziesięciu, po kolei prezentowali się przed komisją w pustej sali. Następnie powiedziano nam że w razie czego dostaniemy informację i tyle. W sumie podszedłem do tego na luzie. Więc czekałem.
Informacja o drugim, finałowym etapie, pojawiła pod koniec lutego. Termin wyznaczono na 11 marca, do finału zakwalifikowało się pięć osób, w tym ja. Fajnie. Przygotowywałem się przez ten czas, a w przeddzień, oczywiście bardzo późną nocą więc na ostatnią chwilę, przygotowałem jeszcze raz gwiazdki i zmiennobarwne płatki.
Z gwiazdkami był zresztą problem. Gdy w kuchni dobierałem dla nich gęstość, miałem na podorędziu jeden sok, nieco mętny, przez co efekt był słabo widoczny:
Więc idąc na konkurs kupiłem drugi sok, przezroczysty. Był też jednak gęstszy i gwiazdki w nim pływały po wierzchu. Musiałem rozcieńczyć. Od przygotowania stanowiska do właściwej prezentacji pomysłu minęła prawie godzina, przez ten czas gwiazdki straciły część barwnika, zarazem wchłaniając z napoju więcej cukru i teraz dla odmiany opadły na dno. Musiałem więc odlewać i dolewać żeby złapać gęstość dzięki której unosiły się swobodnie pośrodku szklanki
Jak wyglądały prezentacje innych? Pozostali uczestnicy właściwie skupili się na wymyśleniu nowego napoju a nie dodatku. Martyna Chromińska studiująca dietetykę zaproponowała ciekawy sok warzywny, zawierający głownie buraka ćwikłowego i słodzony wyciągiem ze Stewii, który jest znacznie bardziej słodszy od cukru, nie dorzucając jednak kalorii. Takie połączenie było więc zarówno smacznie dzięki słodyczy zabijającej ziemiste posmaki warzyw, ale zarazem bez cukru, stanowiąc bardzo dobry pomysł.
Bardzo dobra była też propozycja Joanny Szczepańskiej z pedagogiki, aby stworzyć koktajl warzywno-owocowy, zawierający brokuły, ale też jabłko, marchewkę, szpinak i sok pomarańczowy, dając tym samym nietypowe połączenie. Na tym etapie konkursu należało zareklamować produkt przed publicznością, nijako sprzedać swój pomysł, kiedy więc na swej prezentacji opisała jak to podczas praktyk w przedszkolu wpadła na pomysł aby dzieci zjadały więcej warzyw, gdy opisała jak to mali wychowankowie po kilku łyczkach zielonego napoju prosili o więcej i gdy wreszcie próbowała włączyć filmik pokazujący z jaką radością i ochotą dzieci wypijają unikalną mieszankę ze zmiksowanymi brokułami - szczerze mówiąc aż skręcało mnie w środku bo prezentowało się to bardzo dobrze i obawiałem się, czy aby ta propozycja nie będzie tą najlepszą.
Kolejny był pomysł matematyczki Barbry Rozwadowskiej, polegający na nalewaniu syropu miętowego na dno szklanki ze Sprite i dodawaniu kolorowej posypki. Cząstki posypki opadały aż do granicy faz, pojawiały się na nich pęcherzyki gazu, które podnosiły je do góry. W ten sposób w szklance następowała ciągła cyrkulacja kolorowych cząstek. Piąta uczestniczka z trzema propozycjami nie przyszła, nie wiem nawet jakie były jej pomysły.
Po prezentacji obejrzeliśmy krótki dokument na temat sponsorującej konkurs firmy spożywczej, potem wysłuchaliśmy krótkiego wykładu pani profesor Chruściel o nanocząstkach w żywności, az przyszło do ogłoszenia wyników.
Piąte miejsce zajął pomysł napoju ze stewią, dla pocieszenia uczestniczka dostała nagrodę publiczności. Czwarte miejsce dostał napój z kolorowa posypką. Trzecie miejsce... Nie chcę wyjść na samochwała, ale trzecie miejsce otrzymałem ja, za pomysł zmiennobarwnych płatków.
Drugie miejsce zdobył tak zachwalany pomysł napoju brokułowego, tymczasem jeśli chodzi o pierwsze, to tu się zdziwiłem - pięć miejsc i tylko czterech uczestników? Czyżby zatem... I choć wydawało się to niemożliwe, pierwsze miejsce zająłem ja. Czego jak czego ale dwóch nagród się nie spodziewałem.
W sumie trochę zaskakujące że najbardziej spodobały się gwiazdki a mniej zmiennobarwne kwadraciki, gdy tymczasem to z tymi drugimi wiązałem większe nadzieje.
I co dalej? Cóż, ja odbiorę nagrodę zaś prawa do produkcji przejmie firma i być może wdroży, kto wie zatem czy za jakiś czas nie zobaczycie w sklepach czegoś co zaprojektowałem.Dwa lata temu w konkursie wygrała propozycja jogurtu z suszonymi pomidorami i podobno niedługo ma być wypuszczony na rynek.
Konkurs organizowany przez uniwersytet i firmę spożywczą z Siedlec był skierowany do studentów, i kusił całkiem niezłą nagrodą pieniężną, zaś przedmiotem było wymyślenie i zaprezentowanie dodatku do napoju. To mogło by być coś w sam raz dla chemika - uznałem. I zapomniałem o sprawie. Dopiero gdy zostało kilka dni do końca terminu zgłaszania ruszyło mnie, że coś trzeba by spróbować, bo głupio by było nie wystartować.
Regulamin nie określał szczegółowo co ma być tematem konkursu - musiał być to dodatek do napojów, w formie pływających stałych cząstek lub dodatku smakowego. Tylko co też takiego wymyślić, aby było to zarazem oryginalne i łatwe do zrobienia? Pomysłów miałem od groma, jednak jednym z etapów konkursu była prezentacja wykonanego dodatku, więc takie pomysły jak błonnikowe kwiaty rozchylające płatki po położeniu na powierzchni napoju czy musujące kulki nadmuchiwane pianą po zamoknięciu, musiały pójść w odstawkę - w kuchni bym tego nie zrobił.
Plakat konkursowy nasuwał na myśl jakieś kulki, może żelowe. Faktycznie, kuchnia molekularna opierająca się na kulinarnych zastosowaniach zdobyczy nauki potrafi łatwo produkować żelowe kulki nazywane sztucznym kawiorem, z płynnym nadzieniem i twardą powłoczką. Tyle, że jeśli jest to tak znana sprawa, to wielu może wpaść na coś takiego, a przecież pomysły nie powinny się powtarzać - myślałem. Jak nie kulki to co? Po odrzuceniu kostek i trójkątów zdecydowałem się na gwiazdki.
Ale jakie? Powinny mieć ciekawy smak i coś charakterystycznego. Z ćwiczeń z rozpoznawaniem tworzyw sztucznych przez różną pływalność pamiętałem, że gdy gęstość stałego materiału jest podobna do gęstości cieczy, to unosi się on swobodnie wewnątrz cieczy. Zarazem jednak płaskie płatki materiału mają skłonność do układania się poziomo, jak opadający liść. Gdyby zatem - pomyślałem - ustawić je pionowo i równocześnie zawiesić swobodnie, to patrzący z boku na szklankę napoju widziałby dobrze kształt gwiazdki. A to już by było coś.
Jako materiał wybrałem sobie agar, głownie dlatego, że galaretka żelatynowa miewa niekiedy pewien posmak który nie każdemu pasuje, a także dlatego, że agar bardzo szybko zastyga i ma dobrą wydajność (łyżeczka na litr wody). Potem na pierwszym etapie tłumaczyłem też komisji, że taka galaretka byłaby wegetariańska na co coraz więcej osób zwraca uwagę. Tak więc gwiazdki z agaru, ale o jakim smaku? Postanowiłem spróbować czegoś nietypowego - smaku ostrego, konkretnie zaś imbiru. Smak kojarzył się z kolorem czerwonym, stąd projekt czerwonych-ostrych gwiazdek. Na podobnej zasadzie powstały inne typy: zielony-kwaśny i żółty-ananasowy. A jak z tym ustawieniem w zawieszeniu? Najprościej byłoby sprawić, że kształt będzie miał nie równo rozłożony ciężar. Postanowiłem zalewać żel tak, by z jednej strony płat był cieńszy, dzięki temu powinny się ustawiać cięższą połową w dół.
Ale miałem wrażenie, że to może być za mało. Trzeba było dodać do tego coś jeszcze, takiego fajnego, molekularnego a najlepiej chemicznego, żeby się coś działo w tej szklance. Może barwnik który nabiera koloru podczas wytrząsania w shakerze? Albo coś z zapachem? Albo może jeszcze... Pomysł który przyszedł mi do głowy na sam koniec był na tyle ciekawy, że postanowiłem zgłosić go osobno. Były to płatki galaretki, które po wrzuceniu do napoju zmieniają kolor na całkiem inny.
Wiele jest łatwo dostępnych i jadalnych substancji o właściwościach wskaźnika kwasowo-zasadowego. Większość napojów i soków owocowych ma odczyn kwaśny. Postanowiłem zatem przygotować twardą galaretkę zabarwioną takim wskaźnikiem z niewielkim dodatkiem alkalizującej sody oczyszczonej. Po wrzuceniu do napoju żel zakwaszałby się, zmieniając kolor.
Jest kilka takich kuchennych wskaźników. Najlepszym jest wywar z czerwonej kapusty, który zależnie od kwasowości przybiera kolor zielony w mocniejszych, niebieski w słabszych zasadach, w roztworach obojętnych lub lekko kwaśnych fioletowy a w kwaśnych różowy i czerwony. Płat galaretki barwionej kapustą przybierałby więc różne kolory zależnie od rodzaju napoju, stąd też jeden typ dodatku zachowując się różnie dawałby szeroki wachlarz efektów. Sami zresztą zobaczcie:
Inny typ byłby zabarwiany wywarem z czarnych jagód, tutaj próbka:
Zielone płatki przed wrzuceniem, różowe po wyciągnięciu z napoju. Jeszcze inny typ byłby zabarwiany hibiskusem, który zmienia kolor w taki sam sposób.
Tak więc pomysł miałem a pierwsze próby pokazały, że się sprawdza. Teraz należało wysłać zgłoszenie. Zrobiłem to w ostatnim dniu terminu, tuż przed zamknięciem poczty i z zaaferowania wpisałem błędny adres. Tak to niestety ze mną jest że wiele robię na ostatnią chwilę, nie mogąc przedtem się zmobilizować. List jakoś jednak doszedł na miejsce i na tydzień przed pierwszym etapem, w połowie stycznia, dostałem zawiadomienie gdzie to i o której mam się prezentować. Przygotowałem prezentacje multimedialne, po czym zakasałem rękawy i zabrałem się do wyrobu. Najpierw sporządziłem wywar ze świeżego imbiru, a gdy był dostatecznie szczypiący, dodałem torebkę herbaty hibiskusowej. Gdy się naciągnęła dosypałem agaru.
Agar kupiłem w sklepie ze zdrową żywnością. Miał postać kremowego proszku bez smaku, nie rozpuszczalnego w zimnej wodzie i powoli w gorącej.
Następnie wylałem roztwór na plastikowy talerzyk, lekko go przechylając. Żel zastygł w krótkim czasie, praktycznie zaraz po ochłodzeniu, dzięki czemu w jeden wieczór wykonałem kilka prób z różnym składem.
W zasadzie największy problem sprawiło mi wycięcie gwiazdki, nie mam bowiem zbyt dużych zdolności manualnych, jakoś sobie jednak poradziłem.
W podobny sposób zrobiłem żel zabarwiany kapustą, tylko bez imbiru. Ciekawe zresztą jak czuły okazał się wskaźnik - barwa zmieniała się po dodaniu cukru, zawierającego alkaliczne domieszki, jak i po dodaniu agaru, będącego substancją lekko kwaśną (agar zawiera 0,3% grup sulfonowych i stanowi naturalny kationit). Małe próbki zapakowałem w pojemniki aby pokazać na pierwszym etapie.
Jak to wyglądało? Całkiem spokojnie, wręcz kameralnie. Uczestnicy, których było około dziesięciu, po kolei prezentowali się przed komisją w pustej sali. Następnie powiedziano nam że w razie czego dostaniemy informację i tyle. W sumie podszedłem do tego na luzie. Więc czekałem.
Informacja o drugim, finałowym etapie, pojawiła pod koniec lutego. Termin wyznaczono na 11 marca, do finału zakwalifikowało się pięć osób, w tym ja. Fajnie. Przygotowywałem się przez ten czas, a w przeddzień, oczywiście bardzo późną nocą więc na ostatnią chwilę, przygotowałem jeszcze raz gwiazdki i zmiennobarwne płatki.
Z gwiazdkami był zresztą problem. Gdy w kuchni dobierałem dla nich gęstość, miałem na podorędziu jeden sok, nieco mętny, przez co efekt był słabo widoczny:
Więc idąc na konkurs kupiłem drugi sok, przezroczysty. Był też jednak gęstszy i gwiazdki w nim pływały po wierzchu. Musiałem rozcieńczyć. Od przygotowania stanowiska do właściwej prezentacji pomysłu minęła prawie godzina, przez ten czas gwiazdki straciły część barwnika, zarazem wchłaniając z napoju więcej cukru i teraz dla odmiany opadły na dno. Musiałem więc odlewać i dolewać żeby złapać gęstość dzięki której unosiły się swobodnie pośrodku szklanki
Jak wyglądały prezentacje innych? Pozostali uczestnicy właściwie skupili się na wymyśleniu nowego napoju a nie dodatku. Martyna Chromińska studiująca dietetykę zaproponowała ciekawy sok warzywny, zawierający głownie buraka ćwikłowego i słodzony wyciągiem ze Stewii, który jest znacznie bardziej słodszy od cukru, nie dorzucając jednak kalorii. Takie połączenie było więc zarówno smacznie dzięki słodyczy zabijającej ziemiste posmaki warzyw, ale zarazem bez cukru, stanowiąc bardzo dobry pomysł.
Bardzo dobra była też propozycja Joanny Szczepańskiej z pedagogiki, aby stworzyć koktajl warzywno-owocowy, zawierający brokuły, ale też jabłko, marchewkę, szpinak i sok pomarańczowy, dając tym samym nietypowe połączenie. Na tym etapie konkursu należało zareklamować produkt przed publicznością, nijako sprzedać swój pomysł, kiedy więc na swej prezentacji opisała jak to podczas praktyk w przedszkolu wpadła na pomysł aby dzieci zjadały więcej warzyw, gdy opisała jak to mali wychowankowie po kilku łyczkach zielonego napoju prosili o więcej i gdy wreszcie próbowała włączyć filmik pokazujący z jaką radością i ochotą dzieci wypijają unikalną mieszankę ze zmiksowanymi brokułami - szczerze mówiąc aż skręcało mnie w środku bo prezentowało się to bardzo dobrze i obawiałem się, czy aby ta propozycja nie będzie tą najlepszą.
Kolejny był pomysł matematyczki Barbry Rozwadowskiej, polegający na nalewaniu syropu miętowego na dno szklanki ze Sprite i dodawaniu kolorowej posypki. Cząstki posypki opadały aż do granicy faz, pojawiały się na nich pęcherzyki gazu, które podnosiły je do góry. W ten sposób w szklance następowała ciągła cyrkulacja kolorowych cząstek. Piąta uczestniczka z trzema propozycjami nie przyszła, nie wiem nawet jakie były jej pomysły.
Po prezentacji obejrzeliśmy krótki dokument na temat sponsorującej konkurs firmy spożywczej, potem wysłuchaliśmy krótkiego wykładu pani profesor Chruściel o nanocząstkach w żywności, az przyszło do ogłoszenia wyników.
Piąte miejsce zajął pomysł napoju ze stewią, dla pocieszenia uczestniczka dostała nagrodę publiczności. Czwarte miejsce dostał napój z kolorowa posypką. Trzecie miejsce... Nie chcę wyjść na samochwała, ale trzecie miejsce otrzymałem ja, za pomysł zmiennobarwnych płatków.
Drugie miejsce zdobył tak zachwalany pomysł napoju brokułowego, tymczasem jeśli chodzi o pierwsze, to tu się zdziwiłem - pięć miejsc i tylko czterech uczestników? Czyżby zatem... I choć wydawało się to niemożliwe, pierwsze miejsce zająłem ja. Czego jak czego ale dwóch nagród się nie spodziewałem.
W sumie trochę zaskakujące że najbardziej spodobały się gwiazdki a mniej zmiennobarwne kwadraciki, gdy tymczasem to z tymi drugimi wiązałem większe nadzieje.
I co dalej? Cóż, ja odbiorę nagrodę zaś prawa do produkcji przejmie firma i być może wdroży, kto wie zatem czy za jakiś czas nie zobaczycie w sklepach czegoś co zaprojektowałem.Dwa lata temu w konkursie wygrała propozycja jogurtu z suszonymi pomidorami i podobno niedługo ma być wypuszczony na rynek.
piątek, 2 listopada 2012
Modyfikowana ale nie tak
Pojawia się w zupkach chińskich, budyniach, sosach w proszku, jogurtach, kisielkach i wszelkich innych produktach wymagających zagęszczenia; tym jednak co budzi obawy nie jeśli oznaczenie E lecz rozwinięcie nazwy, mówiące o tym że jest to nie zwyczajna skrobia, ale modyfikowana. A modyfikowane coś w jedzeniu, to na pewno jakiś szkodliwy gen - myśli niezorientowany konsument. I myli się całkowicie.
Temat GMO (genetycznie modyfikowane organizmy) budzi dziś dużo kontrowersji. Kwestii tego na ile roszczenia spierających się grup są zasadne, nie będę tutaj rozstrzygał, niech to robią inni. Kontrowersje z tym związane są jednak często przenoszone na całkiem inne produkty i substancje, które jedynie kojarzą się z GMO. Dziś o modyfikacje podejrzewane jest wszystko co bierze się z soi, z lecytyną sojową włącznie. Na podobnej zasadzie dostaje się też modyfikowanej skrobi, której obecność w pożywieniu jest często powodem skarg na producentów. Przykład mamy tutaj - jako produkty GMO wyliczono wszystkie ze skrobią modyfikowaną. Nieco inną wersję znajdziemy na tym blogu - autorka wprawdzie sprawdziła, że chodzi tu o inną modyfikację, ale uważa termin za kamuflaż dla "skrobi modyfikowanej genetycznie" z której tylko i wyłącznie ma się produkować ten zagęstnik. W czym i kto nie ma racji objaśniam poniżej.
Skrobia, chemicznie rzecz ujmując, jest jednym z najpospolitszych naturalnych polimerów, stanowiąc energetyczny zapas dla roślin. Jej długie łańcuchy są zbudowane z połączonych cząsteczek glukozy:
połączonych wiązaniem α-1,4-glikozydowym. Jedna cząsteczka skrobi może się składać z od kilku setek do ponad tysiąca członów glukozowych. Zasadniczo dzieli się na dwie frakcję - amylozę składającą się wyłącznie z pojedynczych, prostych łańcuchów, i amylopektynę, której łańcuchy są w wielu miejscach rozgałęzione.
Ta różnica budowy ma istotne znaczenie dla właściwości - prosta amyloza jest nierozpuszczalna w zimnej wodzie, natomiast rozpuszcza się w gorącej. Amylopektyna częściowo rozpuszcza się w zimnej wodzie, silnie pęczniejąc i odpowiadając za kleistość mokrej skrobi.
Stanowi podstawowy składnik wielu produktów spożywczych i często jest do nich dodawana jako zagęstnik, jednak jej właściwości nie zawsze są odpowiednie. Dlatego poddaje się ją modyfikacjom, zmieniając długość i kształt cząsteczek, lub doczepiając do nich różne grupy, wpływające na zachowanie się w żywności. Jakie są to przemiany?
Najprostsza polega na częściowej hydrolizie, to jest rozdzieleniu długich łańcuchów na części, pod wpływem enzymów, podwyższonej temperatury lub kwasów. Takie kawałki nazywane dekstrynami, mające po kilkanaście członów glukozy, są już rozpuszczalne w wodzie, tworząc lepkie roztwory i zastępując gumę arabską. Dekstryny powstają między innymi podczas wypieku chleba, odpowiadając za właściwości lekko słodkawej, chrupiącej skórki. Dekstryny są też składnikami klejów, jak choćby używany dawniej klej z prażonych kasztanów. Istnieje kilka typów dekstryn, te hydrolizowane kwasami są oznaczane jako E 1400, hydrolizowane enzymatycznie jako E 1405.
Inne modyfikacje polegają na potraktowaniu skrobi kwasami (E 1401) lub zasadami (E1402) które też rozbijają łańcuchy, ale na dłuższe cząsteczki, mające po kilkadziesiąt do stu członów. Te odmiany są już słabo rozpuszczalne w zimnej wodzie. Działając na skrobię utleniaczami, otrzymuje się s. utlenioną lub bieloną zawierającą grupy karboksylowe, zależnie od użytego utleniacza jest to E 1403 dla wody utlenionej, i E 1404 dla chloranu sodu. Tak zmieniona skrobia tworzy miękkie żele podobne do żelatynowych. Wszystkie te odmiany po spożyciu rozkładają się tak samo jak zwykła skrobia, tworząc glukozę.
Inne modyfikacje polegają na podstawieniu grup wodorotlenowych odpowiednimi podstawnikami. Traktując skrobię kwasem fosforowym, można uzyskać produkt częściowo podstawiony resztą fosforanową (E 1410) lub usieciowany (E 1412) lub usieciowany i podstawiony (E 1413). Ta pierwsza odmiana charakteryzuje się niską skłonnością do retrogradacji - procesu powodującego wypychanie wody z żelu skrobiowego i tworzenie zwartych agregatów o krystalicznej strukturze. Zretrogradowana skrobia jest twarda i gorzej trawiona, dla przemysłu spożywczego większe znaczenie ma jednak to, że proces retrogradacji zmienia właściwości produktu, który staje się mniej sprężysty. Odpowiada między innymi za przemiany powodujące czerstwienie pieczywa. Odmiany usieciowane tworzą żele twarde, rozpływające się w wyższych temperaturach, odporne na przemrożenie.
Jak łatwo się domyśleć, w odróżnieniu od poprzednich odmian, skrobia fosforyzowana rozkłada się z wydzieleniem reszt fosforanowych, te zaś mają już pewien wpływ na organizm. Nadmiar fosforu w takiej formie zaburza wchłanianie wapnia, zwiększając skłonność do osteoporozy. Z drugiej strony zawartość reszt fosforanowych w modyfikowanej skrobi nie może przekraczać 0,04% (ograniczenie prawne) a zazwyczaj osiąga 0,01%, trudno zatem aby doznać nadmiaru tylko tą drogą i więcej zaszkodzić może wypicie coca-coli - choć warto uwzględniać i tę ilość wobec całkowitej ilości w pozostałych produktach. Odgórnie ustalono limit zawartości w produktach dla niemowląt na 20 g/kg produktu.
Kolejne modyfikacje polegają na przyłączeniu do skrobi reszt kwasów organicznych. Jeśli potraktować ją bezwodnikiem octowym, otrzymamy skrobię acetylowaną (E 1420) tworzącą miękkie, przezroczyste żele w niskich temperaturach. Ten podstawowy typ, ma różne odmiany, na przykład acetylowana skrobia utleniona (E 1451), acetylowany fosforan skrobiowy (E 1414), czy acetylowany adypinian skrobiowy (E 1422) tworzący żele w warunkach silnie kwaśnych, podobnie do naturalnych pektyn.
Te odmiany rozkładają się z wydzieleniem kwasu octowego, który jest nieszkodliwy, jednak ze względu na możliwe działanie drażniące ustalono limit zawartości w produktach dla niemowląt na maksymalną zawartość 50g/kg produktu[1]
Najbardziej skomplikowaną nazwę ma E 1450 - oktenylobursztynian skrobiowy - o którym zarazem najtrudniej było mi coś znaleźć. Jest to ester w którym do pierścienia glukozy dołączono kwas zawierający dwie grupy karboksylowe i wyglądający jak pochodna kwasu bursztynowego, podstawionego oktenem - stąd zawiła nazwa (podejrzewam że równie dobrze można by go nazwać kwasem 2-acetylodek-7-enowym)
Tak duża grupa organiczna powoduje że skrobia może przylepiać się do tłuszczu na granicy faz woda-tłuszcz, stąd też używa się jej do zagęszczania majonezów, musztard i kremów. Podczas rozkładu w organizmie cała ta grupa odszczepia się i jak się wydaje, jest wydalana z moczem. Znalałem tylko jeden przegląd badań na ten temat [2], w którym nie stwierdzono negatywnych wpływów na dwa kolejne pokolenia szczurów, których dieta zawierała nawet 30% tej modyfikacji. Jedynym negatywnym wpływem był niedobór magnezu wywołany tak ubogą dietą.
Sole glinowe tego związku są używane w pudrach do ciała i jako stabilizatory w tabletkach.
Kolejną zawiłą modyfikacją jest hydroksypropyloskrobia (E 1440 lub HPS) i jej kombinacje: z fosforanem (E 1442) i z gliceryną( E 1441). Otrzymuje się ją traktując substrat naturalny tlenkiem propylenu - epoksydem z trójkątnym mostkiem tlenowym, który łatwo się otwiera, przyłączając się do innych cząsteczek. Zależnie od stopnia podstawienia otrzymany produkt ma różne właściwości. Odmiany używane w przemyśle spożywczym zawierają do 60% podstawionych grup, tworzą żele o dobrym połysku, wytrzymałe na zamrażanie, stąd niekiedy pokrywa się nimi mrożone owoce aby spowolnić powierzchniowe utlenianie, a ponadto zagęszcza lody i ciasta mrożone. Zwykle też zastępuje się nimi mączkę chleba świętojańskiego. Stanowi też materiał rozpuszczających się w żołądku kapsułek na leki, zastępując używaną wcześniej żelatynę.
Podczas trawienia rozkłada się na glukozę i glikol propylowy - który z kolei utlenia się do nieszkodliwego kwasu pirogronowego lub mlekowego. Mimo to wygląda na to, że może podrażniać jelita, skłaniając je do bardziej intensywnego wydalania. Krótko mówiąc może wywołać rozwolnienie. Potwierdzają to badania - u szczurów które zjadały karmę zawierającą 50% związku pojawiała się biegunka, w innym badaniu pojawiła się przy ilości 30% karmy; w badaniu na ludziach ochotnikach biegunka pojawiała się przy dawce 60 g dziennie. Zarazem nie stwierdzono negatywnych zmian w układzie krążenia, nerwowym i trawiennym u szczurów, psów i świń zjadających ten związek przez okres od kilku do kilkunastu tygodni, podobnie jak u szczurów karmionych nim przez 2 lata, a w pewnym badaniu nie wykazano negatywnych i dziedzicznych zmian u trzech kolejnych pokoleń szczurów karmionych tym związkiem.[3] Zatem właściwie tylko biegunka przy spożyciu dużej ilości, może być uważana za jakiś wpływ zdrowotny.
Nie takie więc te dodatki straszne, jak by to mogło wynikać z długich nazw. Dla mnie bardziej istotne jest jednak to, gdzie są one stosowane i w jakich ilościach. 30 lat temu śmietana utwardzana mąką byłaby brana za oszustwo, a jednak dziś trafiają się produkty tego typu zagęszczane modyfikowaną skrobią, i w zasadzie nikt nie widzi w tym niczego złego. Skrobia dziś zagęszcza kremy, utwardza wędliny, nabłyszcza warzywa, usztywnia mocno rozpulchnione pieczywo, a nawet zastępuje tłuszcz w produktach dietetycznych, i białko w serze do posypywania pizzy. Jest wypełniaczem w jedzeniu, a sama nie ma zbyt dużej wartości dietetycznej.
Natomiast co ze skrobią GMO? No cóż, cząsteczka skrobi nie posiada własnego DNA, zatem nie ma czegoś takiego jak "skrobia genetycznie modyfikowana" - i to skrobia i to, chemicznie cząsteczki z różnych roślin niczym się między sobą nie różnią. Nie wiem zresztą czym miałyby się różnić w przypadku pochodzenia od roślin, których modyfikacje nie dotyczyły skrobi.
Gdyby zaś materiał początkowy był zanieczyszczony na przykład białkiem roślin modyfikowanych, to wszystkie przemiany którym poddaje się skrobię, a więc traktowanie kwasami, temperaturą, bezwodnikami i innymi upochodniaczami, spowodowałyby jego rozkład, a co za tym idzie unieczynnienie. Ot i cała zagadka.
------
* Od strony technicznej modyfikowanie skrobi wygląda tak
[1] http://www.zusatzstoffe-online.de/zusatzstoffe/313.e1420_acetylierte_st%E4rke.html
[2] http://www.inchem.org/documents/jecfa/jecmono/v17je21.htm
[3] http://www.inchem.org/documents/jecfa/jecmono/v05je70.htm
Temat GMO (genetycznie modyfikowane organizmy) budzi dziś dużo kontrowersji. Kwestii tego na ile roszczenia spierających się grup są zasadne, nie będę tutaj rozstrzygał, niech to robią inni. Kontrowersje z tym związane są jednak często przenoszone na całkiem inne produkty i substancje, które jedynie kojarzą się z GMO. Dziś o modyfikacje podejrzewane jest wszystko co bierze się z soi, z lecytyną sojową włącznie. Na podobnej zasadzie dostaje się też modyfikowanej skrobi, której obecność w pożywieniu jest często powodem skarg na producentów. Przykład mamy tutaj - jako produkty GMO wyliczono wszystkie ze skrobią modyfikowaną. Nieco inną wersję znajdziemy na tym blogu - autorka wprawdzie sprawdziła, że chodzi tu o inną modyfikację, ale uważa termin za kamuflaż dla "skrobi modyfikowanej genetycznie" z której tylko i wyłącznie ma się produkować ten zagęstnik. W czym i kto nie ma racji objaśniam poniżej.
Skrobia, chemicznie rzecz ujmując, jest jednym z najpospolitszych naturalnych polimerów, stanowiąc energetyczny zapas dla roślin. Jej długie łańcuchy są zbudowane z połączonych cząsteczek glukozy:
połączonych wiązaniem α-1,4-glikozydowym. Jedna cząsteczka skrobi może się składać z od kilku setek do ponad tysiąca członów glukozowych. Zasadniczo dzieli się na dwie frakcję - amylozę składającą się wyłącznie z pojedynczych, prostych łańcuchów, i amylopektynę, której łańcuchy są w wielu miejscach rozgałęzione.
Ta różnica budowy ma istotne znaczenie dla właściwości - prosta amyloza jest nierozpuszczalna w zimnej wodzie, natomiast rozpuszcza się w gorącej. Amylopektyna częściowo rozpuszcza się w zimnej wodzie, silnie pęczniejąc i odpowiadając za kleistość mokrej skrobi.
Stanowi podstawowy składnik wielu produktów spożywczych i często jest do nich dodawana jako zagęstnik, jednak jej właściwości nie zawsze są odpowiednie. Dlatego poddaje się ją modyfikacjom, zmieniając długość i kształt cząsteczek, lub doczepiając do nich różne grupy, wpływające na zachowanie się w żywności. Jakie są to przemiany?
Najprostsza polega na częściowej hydrolizie, to jest rozdzieleniu długich łańcuchów na części, pod wpływem enzymów, podwyższonej temperatury lub kwasów. Takie kawałki nazywane dekstrynami, mające po kilkanaście członów glukozy, są już rozpuszczalne w wodzie, tworząc lepkie roztwory i zastępując gumę arabską. Dekstryny powstają między innymi podczas wypieku chleba, odpowiadając za właściwości lekko słodkawej, chrupiącej skórki. Dekstryny są też składnikami klejów, jak choćby używany dawniej klej z prażonych kasztanów. Istnieje kilka typów dekstryn, te hydrolizowane kwasami są oznaczane jako E 1400, hydrolizowane enzymatycznie jako E 1405.
Inne modyfikacje polegają na potraktowaniu skrobi kwasami (E 1401) lub zasadami (E1402) które też rozbijają łańcuchy, ale na dłuższe cząsteczki, mające po kilkadziesiąt do stu członów. Te odmiany są już słabo rozpuszczalne w zimnej wodzie. Działając na skrobię utleniaczami, otrzymuje się s. utlenioną lub bieloną zawierającą grupy karboksylowe, zależnie od użytego utleniacza jest to E 1403 dla wody utlenionej, i E 1404 dla chloranu sodu. Tak zmieniona skrobia tworzy miękkie żele podobne do żelatynowych. Wszystkie te odmiany po spożyciu rozkładają się tak samo jak zwykła skrobia, tworząc glukozę.
Inne modyfikacje polegają na podstawieniu grup wodorotlenowych odpowiednimi podstawnikami. Traktując skrobię kwasem fosforowym, można uzyskać produkt częściowo podstawiony resztą fosforanową (E 1410) lub usieciowany (E 1412) lub usieciowany i podstawiony (E 1413). Ta pierwsza odmiana charakteryzuje się niską skłonnością do retrogradacji - procesu powodującego wypychanie wody z żelu skrobiowego i tworzenie zwartych agregatów o krystalicznej strukturze. Zretrogradowana skrobia jest twarda i gorzej trawiona, dla przemysłu spożywczego większe znaczenie ma jednak to, że proces retrogradacji zmienia właściwości produktu, który staje się mniej sprężysty. Odpowiada między innymi za przemiany powodujące czerstwienie pieczywa. Odmiany usieciowane tworzą żele twarde, rozpływające się w wyższych temperaturach, odporne na przemrożenie.
Jak łatwo się domyśleć, w odróżnieniu od poprzednich odmian, skrobia fosforyzowana rozkłada się z wydzieleniem reszt fosforanowych, te zaś mają już pewien wpływ na organizm. Nadmiar fosforu w takiej formie zaburza wchłanianie wapnia, zwiększając skłonność do osteoporozy. Z drugiej strony zawartość reszt fosforanowych w modyfikowanej skrobi nie może przekraczać 0,04% (ograniczenie prawne) a zazwyczaj osiąga 0,01%, trudno zatem aby doznać nadmiaru tylko tą drogą i więcej zaszkodzić może wypicie coca-coli - choć warto uwzględniać i tę ilość wobec całkowitej ilości w pozostałych produktach. Odgórnie ustalono limit zawartości w produktach dla niemowląt na 20 g/kg produktu.
Kolejne modyfikacje polegają na przyłączeniu do skrobi reszt kwasów organicznych. Jeśli potraktować ją bezwodnikiem octowym, otrzymamy skrobię acetylowaną (E 1420) tworzącą miękkie, przezroczyste żele w niskich temperaturach. Ten podstawowy typ, ma różne odmiany, na przykład acetylowana skrobia utleniona (E 1451), acetylowany fosforan skrobiowy (E 1414), czy acetylowany adypinian skrobiowy (E 1422) tworzący żele w warunkach silnie kwaśnych, podobnie do naturalnych pektyn.
Te odmiany rozkładają się z wydzieleniem kwasu octowego, który jest nieszkodliwy, jednak ze względu na możliwe działanie drażniące ustalono limit zawartości w produktach dla niemowląt na maksymalną zawartość 50g/kg produktu[1]
Najbardziej skomplikowaną nazwę ma E 1450 - oktenylobursztynian skrobiowy - o którym zarazem najtrudniej było mi coś znaleźć. Jest to ester w którym do pierścienia glukozy dołączono kwas zawierający dwie grupy karboksylowe i wyglądający jak pochodna kwasu bursztynowego, podstawionego oktenem - stąd zawiła nazwa (podejrzewam że równie dobrze można by go nazwać kwasem 2-acetylodek-7-enowym)
Tak duża grupa organiczna powoduje że skrobia może przylepiać się do tłuszczu na granicy faz woda-tłuszcz, stąd też używa się jej do zagęszczania majonezów, musztard i kremów. Podczas rozkładu w organizmie cała ta grupa odszczepia się i jak się wydaje, jest wydalana z moczem. Znalałem tylko jeden przegląd badań na ten temat [2], w którym nie stwierdzono negatywnych wpływów na dwa kolejne pokolenia szczurów, których dieta zawierała nawet 30% tej modyfikacji. Jedynym negatywnym wpływem był niedobór magnezu wywołany tak ubogą dietą.
Sole glinowe tego związku są używane w pudrach do ciała i jako stabilizatory w tabletkach.
Kolejną zawiłą modyfikacją jest hydroksypropyloskrobia (E 1440 lub HPS) i jej kombinacje: z fosforanem (E 1442) i z gliceryną( E 1441). Otrzymuje się ją traktując substrat naturalny tlenkiem propylenu - epoksydem z trójkątnym mostkiem tlenowym, który łatwo się otwiera, przyłączając się do innych cząsteczek. Zależnie od stopnia podstawienia otrzymany produkt ma różne właściwości. Odmiany używane w przemyśle spożywczym zawierają do 60% podstawionych grup, tworzą żele o dobrym połysku, wytrzymałe na zamrażanie, stąd niekiedy pokrywa się nimi mrożone owoce aby spowolnić powierzchniowe utlenianie, a ponadto zagęszcza lody i ciasta mrożone. Zwykle też zastępuje się nimi mączkę chleba świętojańskiego. Stanowi też materiał rozpuszczających się w żołądku kapsułek na leki, zastępując używaną wcześniej żelatynę.
Podczas trawienia rozkłada się na glukozę i glikol propylowy - który z kolei utlenia się do nieszkodliwego kwasu pirogronowego lub mlekowego. Mimo to wygląda na to, że może podrażniać jelita, skłaniając je do bardziej intensywnego wydalania. Krótko mówiąc może wywołać rozwolnienie. Potwierdzają to badania - u szczurów które zjadały karmę zawierającą 50% związku pojawiała się biegunka, w innym badaniu pojawiła się przy ilości 30% karmy; w badaniu na ludziach ochotnikach biegunka pojawiała się przy dawce 60 g dziennie. Zarazem nie stwierdzono negatywnych zmian w układzie krążenia, nerwowym i trawiennym u szczurów, psów i świń zjadających ten związek przez okres od kilku do kilkunastu tygodni, podobnie jak u szczurów karmionych nim przez 2 lata, a w pewnym badaniu nie wykazano negatywnych i dziedzicznych zmian u trzech kolejnych pokoleń szczurów karmionych tym związkiem.[3] Zatem właściwie tylko biegunka przy spożyciu dużej ilości, może być uważana za jakiś wpływ zdrowotny.
Ziarna skrobi pszenicznej barwione jodem. Powiększenie ok. 500 razy
Nie takie więc te dodatki straszne, jak by to mogło wynikać z długich nazw. Dla mnie bardziej istotne jest jednak to, gdzie są one stosowane i w jakich ilościach. 30 lat temu śmietana utwardzana mąką byłaby brana za oszustwo, a jednak dziś trafiają się produkty tego typu zagęszczane modyfikowaną skrobią, i w zasadzie nikt nie widzi w tym niczego złego. Skrobia dziś zagęszcza kremy, utwardza wędliny, nabłyszcza warzywa, usztywnia mocno rozpulchnione pieczywo, a nawet zastępuje tłuszcz w produktach dietetycznych, i białko w serze do posypywania pizzy. Jest wypełniaczem w jedzeniu, a sama nie ma zbyt dużej wartości dietetycznej.
Natomiast co ze skrobią GMO? No cóż, cząsteczka skrobi nie posiada własnego DNA, zatem nie ma czegoś takiego jak "skrobia genetycznie modyfikowana" - i to skrobia i to, chemicznie cząsteczki z różnych roślin niczym się między sobą nie różnią. Nie wiem zresztą czym miałyby się różnić w przypadku pochodzenia od roślin, których modyfikacje nie dotyczyły skrobi.
Gdyby zaś materiał początkowy był zanieczyszczony na przykład białkiem roślin modyfikowanych, to wszystkie przemiany którym poddaje się skrobię, a więc traktowanie kwasami, temperaturą, bezwodnikami i innymi upochodniaczami, spowodowałyby jego rozkład, a co za tym idzie unieczynnienie. Ot i cała zagadka.
------
* Od strony technicznej modyfikowanie skrobi wygląda tak
[1] http://www.zusatzstoffe-online.de/zusatzstoffe/313.e1420_acetylierte_st%E4rke.html
[2] http://www.inchem.org/documents/jecfa/jecmono/v17je21.htm
[3] http://www.inchem.org/documents/jecfa/jecmono/v05je70.htm
piątek, 19 października 2012
Kwasek śmierci i inne bzdury
Kwas cytrynowy należy do najczęstszych stosowanych dodatków żywnościowych, również przez nas samych w domowym zakresie. Nic więc dziwnego że znalazł się na celowników internetowych panikarzy, do wszystkiego co oznaczone literką E podchodzących jak diabeł do wody być może święconej. Co zaskakujące, dokładnie przeciwny stosunek mają do obfitujących w ten związek owoców cytrusowych, stanowiących częsty składnik mikstur detoksykacyjnych.
Swoistą kwintesencję krążących po internecie plotek stanowi artykuł z Astromarii, który będę dalej selektywnie cytował:
Kwasy hamują proces utleniania, a więc są naturalnymi konserwantami. Naturalne kwasy występują w wielu produktach spożywczych, takich jak kiszonki oraz przetwory mleczne i owocowe. Ale władza uznała, że tamte kwasy nie wystarczą, konieczny jest jeszcze jeden. Mało tego, według nich zakwaszania wymagają również te wyroby, które z natury kwaśne nie są (a więc praktycznie wszystkie). Mogliby oczywiście wybrać kwas askorbinowy, który nie dość, że jest tani, to jeszcze zdrowy (witamina C), ale dziwnym trafem wybrali nienaturalny i pozbawiony wartości zdrowotnych kwasek cytrynowy i przekonali producentów, że jest on niezbędny i trzeba go sypać wszędzie, nawet tam, gdzie jest już i tak wystarczająco kwaśno. I mimo, że ma on właściwości konserwujące (po to przecież jest dodawany) ładują do wszystkiego jeszcze różne benzoesany i inne konserwanty.A więc dla porządku:
Wbrew ładnie brzmiącej nazwie kwasek cytrynowy nie ma nic wspólnego ani z naturą, ani z cytrynami, chociaż w swojej naturalnej postaci występuje w wielu owocach, w tym również w cytrynach. Spełnia on również ważną rolę w metabolizmie organizmów żywych (cykl Krebsa). Jednak ten stosowany w przemyśle spożywczym jest czysto syntetyczną substancją, otrzymywaną głównie przez fermentację cukru za pomocą kultur kropidlaka Aspergillus niger. Kropidlak ten jest bardzo niebezpieczną dla zdrowia pleśnią, powodującą wiele poważnych chorób.[1]
Kwas cytrynowy to stosunkowo pospolity w przyrodzie kwas organiczny, zawierający trzy grupy karboksylowe. Zgodnie z nazwą występuje w cytrynach. Pierwsza wzmianka o kwaśnych właściwościach ich soku pochodzi z VIII wieku z pism Gebera, jednak właściwy związek za to odpowiedzialny, wyizolował dopiero w 1784 Carl Scheele. Przez długi czas produkowano go z soków owocowych, do czasu aż w 1893 roku odkryto, że powstaje jako produkt metabolizmu pewnych gatunków pleśni, podobnie jak kwasy mlekowy, octowy i propionowy w pewnych typach fermentacji. Synteza tą metodą rozpoczęła się jednak niemal trzydzieści lat później. Najczęściej stosowany jest szczep Aspergillus niger, zaś pożywką jest nierafinowany cukier, melasa, syrop kukurydziany lub nawet nieprzetworzony sok z buraków cukrowych.
Gdy stężenie kwasu w pożywce wzrasta do odpowiedniego poziomu, dodaje się do niej mleka wapiennego, wytrącając cytrynian wapnia. Po odsączeniu traktowany jest kwasem siarkowym, zaś z zakwaszonego roztworu krystalizuje czysty kwas cytrynowy.
 |
| Mojej hodowli kryształy kwasu cytrynowego, o czym pisałem tu. |
Dlaczego dodaje się go do jedzenia? Głównie dla uzyskania odpowiedniego smaku, w czym jest o tyle lepszy od octu, że nie posiada własnego zapachu. Zakwaszając produkt przedłuża jego trwałość, i to na dwa sposoby - większość bakterii nie rozwija się w kwaśnym środowisku. Poza tym niskie pH zasadniczo przeszkadza reakcjom utlenienia, a właśnie one odpowiadają za większość reakcji rozkładu żywności. Dodatkowo w przypadku produktów nieprzetworzonych zakwaszenie unieczynnia enzymy degradujące, o czym każdy się nieraz przekonał, próbując powstrzymać brązowienie ziemniaków lub jabłek.
No dobra - a kwas askorbinowy? Witamina C to cenny przeciwutleniacz, w większości przypadków dodaje się ją nie jako środek wzbogacający, ale właśnie dla przedłużenia trwałości, ma jednak dwie wady - jest słabym kwasem i za łatwo się utlenia. Z tego powodu niektóre produkty mogą szybko ją utracić, co zmniejszy ich wartość zdrowotną. Można jednak spowolnić ten proces stwarzając dogodne warunki. Na przykład przez zakwaszenie.
Natomiast co do kwestii naturalności związku - producent który go dodaje może potem napisać na opakowaniu, że produkt nie zawiera sztucznych konserwantów. Związek syntetyczny to taki, który otrzymano drogą przemian chemicznych z prostych substratów, na przykład w tym przypadku z propanu, tymczasem tutaj mamy do czynienia ze związkiem wytworzonym przez pewne organizmy żywe. Nie są to może cytryny ale fabryka chemiczna też nie.
I proszę mi nie mówić, że cytryny są zdrowe. Oczywiście, że są. Zawierają kwas cytrynowy, ale naturalny, a oprócz niego witaminy, enzymy, sole mineralne i inne zdrowe składniki, które razem działają zbawiennie na nasze zdrowie. Owoce są dziełem natury, są harmonijną całością, a zawarte w nich składniki chemiczne są doskonale przyswajane przez nasze organizmy[2]Tylko czymże naturalny kwas, wytworzony przez taki organizm żywy jaki cytryna, różni się od kwasu rzekomo syntetycznego, wytworzonego przez organizm żywy kropidlaka? Związek ten nie ma odmian prawo i lewoskrętnej ani jakiejś unikalnej struktury, na co niekiedy powołują się producenci różnych suplementów.
Dlaczego jest szkodliwy? Z prostej przyczyny – kwas cytrynowy zakłóca przewodnictwo elektrochemiczne w naszych komórkach mózgowych i zmienia w nich reakcje chemiczne. Dodając kwasek do potraw i napojów (również dla niemowląt i małych dzieci) ktoś sprytnie zmienia nas w bezmyślne baranki. Wiemy nie od dziś, że władza nie lubi inteligentnych obywateli, bo takimi trudno jest rządzić, szczególnie, że władza sama nie grzeszy inteligencją i doskonale zdaje sobie z tego sprawę.[3]Kwestia szkodliwego wpływu na mózg, pojawia się w tego typu tekstach co i rusz, nigdzie jednak nie podano kto to zbadał, jak i kiedy. Astromaria powołuje się na jakichś dwóch lekarzy, tylko nie chce podać jakich. Musiałem więc sam grzebnąć.
Wedle raportu SIDS z 2000 roku toksyczność związku jest bardzo niska, LD w badaniach na szczurach wyniosła 1200mg/kg/dzień, czyli 1,2 grama na kilogram masy ciała. Dla człowieka ważącego 60 kg odpowiada to całkowitej dawce 80g związku. Nie wykazano w jego przypadku rakotwórczości ani nie jest o to podejrzewany. To samo tyczy się mutagenności i teratogenności. Nie stwierdzono aby był alergenem, choć wywołuje podrażnienia błon śluzowych i oczu. U osób zawodowo stykających się na co dzień z tym związkiem, podrażnienia mogą rozwinąć się w zapalenie skóry. W dwóch kolejnych pokoleniach szczurów zażywających karmę z 1% związku, nie stwierdzono deformacji. Nefrotoksyczności nie potwierdzono. [4] Jak to już opisywałem, kwas cytrynowy zwiększa wchłanianie aluminium z pożywienia, wygląda jednak że może to działać też w drugą stronę - zażywanie większych dawek prowokuje zwiększone wydalanie glinu z organizmu[5]. Stała obecność kwasu w diecie zapobiega kamicy nerkowej związanej z solami wapnia[6]
Zresztą kwas cytrynowy występuje naturalnie w naszym organizmie. Powstaje podczas metabolizmu jako jeden z elementów Cyklu Krebsa, mającego wytworzyć energię komórce. Każdy go ma w sobie.
Co ciekawsze, obecność kwasu wcale nie przeszkadza wielu specjalistom od alternatywnej medycyny polecać częste spożywanie cytryn. Jest elementem kuracji oczyszczającej Tombaka, podczas której w ciągu dwóch tygodni spożywa się sok z łącznie 200 cytryn[7]. Sam Tombak pisze coś o unikalnych właściwościach soli cytrynowych, ale jak to zwykle u niego, nie wiadomo skąd mu to wiadomo. Inna wersja to zażywanie mieszanki oliwy z sokiem cytrynowym. W dodatku sok z cytryny ma w jakiś paradoksalny sposób sprzyjać powstawaniu w organizmie odczynu zasadowego, co podobno też przynosić jakieś tam korzyści. A to wszystko za sprawą tego całego okropnego kwasu cytrynowego....
Jak się wydaje całe zamieszanie ma swe źródło w krążącej po świecie od połowy lat 70. "liście z Villejuif" - anonimowego tekstu ostrzegającego przed szkodliwymi dodatkami do żywności. Najgorszym, silnie rakotwórczym, miał być E 330 czyli właśnie kwas cytrynowy. Lista, w formie listów-łańcuszków rozlała się na cały świat, rozprzestrzeniana w formie zaraźliwego, bardzo wiarygodnie brzmiącego memu. Wkrótce zresztą objawiła się siła obaw zdrowotnych w społeczeństwie - gdy lekarze zaczęli wydawać oświadczenia, że lista jest fałszywa, wiele osób zaczęło bardziej w nią wierzyć uznając, że gdyby coś nie było na rzeczy, nikt by się tym tak bardzo nie przejmował. Podobne listy można spotkać w polskim internecie, niejednokrotnie poszerzone na wszystkie 1200 dodatków z listy E. Można się tam zresztą spotkać z zabawną niekonsekwencją - za rakotwórczy uznany jest tam kwas cytrynowy, ale jego sole już nie. Nawiasem mówiąc tak wychwalany kwas askorbinowy, znajduje się na tej liście pod nazwą E 300...
-------
[1],[2],[3] http://astromaria.wordpress.com/2009/09/23/kolejna-podstepna-trucizna/
[4] http://www.inchem.org/documents/sids/sids/77929.pdf
[5] Yong‐Hua Yanga & Hong‐Yan Zhanga Effect of citric acid on aluminum toxicity in the growth of mungbean seedlings, Journal of Plant Nutrition Volume 21, Issue 5, 1998
[6] Kang DE , Sur RL , Haleblian GE , Fitzsimons NJ , Borawski KM , Preminger GM .
Long-term lemonade based dietary manipulation in patients with hypocitraturic nephrolithiasis. J Urol. 2007 Apr;177(4):1358-62; discussion 1362; quiz 1591
[7] http://cudownediety.blogspot.com/2012/03/kuracja-cytrynowa-m-tombaka.html
poniedziałek, 13 lutego 2012
Ten straszny benzoesan!

W trakcie przygotowywania dłuższej notki o pewnej ciekawej reakcji zachodzącej w niektórych napojach musiałem opowiedzieć o jednym z jej substratów - kwasie benzoesowym. Jednak, jak już zdążyliście zapewne zauważyć, moje niewinne uwagi wstępne częstokroć rozwlekają się w formę dłuższych chemiko-historycznych dygresji, wprawdzie tworzących z właściwym tematem intrygującą opowieść objaśniającą wiele rzeczy, ale przecież gubiącą właściwy wątek. Tak też stało się i tym razem. Gdy objętość tekstu o benzoesanach przekroczyła trzy akapity zorientowałem się, że albo stworzę długaśną notkę nie wiadomo o czym, albo tak dobrze się zapowiadający "wstęp" przerzucę do oddzielnej notki, do której potem będę we właściwym wpisie linkował i odnosił się. A temat jest przecież ciekawy, i ma pewne powiązania z tym co stanowi o charakterze bloga. Ale najpierw o wonnościach i alchemikach:
Kwas benzoesowy to pospolity związek, występujący naturalnie w wielu roślinach, będący najprostszym aromatycznym kwasem
 karboksylowym (choć przychodzi mi jeszcze do głowy kwas furanokarboksylowy), w którym do pierścienia sześcioczłonowego doczepiona jest grupa karboksylowa. Może być traktowany jako pochodna toluenu z którego powstaje w wyniku utleniania - i tak też może być otrzymywany. Inna metoda to reakcja Canizarro, w której benzaldehyd potraktowany zasadą zamienia się w alkohol benzylowy i kwas benzoesowy - a zatem jedna część substratu jest redukowana a druga utleniana. Benzaldehyd otrzymuje się hydrolizując dichlorotoluen, po czym oddziela się go i poddaje reakcji, dzięki czemu unika się zanieczyszczenia chloropochodnymi.
karboksylowym (choć przychodzi mi jeszcze do głowy kwas furanokarboksylowy), w którym do pierścienia sześcioczłonowego doczepiona jest grupa karboksylowa. Może być traktowany jako pochodna toluenu z którego powstaje w wyniku utleniania - i tak też może być otrzymywany. Inna metoda to reakcja Canizarro, w której benzaldehyd potraktowany zasadą zamienia się w alkohol benzylowy i kwas benzoesowy - a zatem jedna część substratu jest redukowana a druga utleniana. Benzaldehyd otrzymuje się hydrolizując dichlorotoluen, po czym oddziela się go i poddaje reakcji, dzięki czemu unika się zanieczyszczenia chloropochodnymi.O wonnościach i alchemikach:
Związek ma dosyć ciekawą historię, której nie omieszkam tu zreferować. Od wieków w świątyniach i miejscach zgromadzeń palono kadzidła i wonności. W Indiach po dziś dzień pali się patyczki z trocin aromatycznego drzewa sandałowego, nazywane trociczkami - których odległym odpowiednikiem są nasze kadzidełka. Inne aromatyczne rośliny dostarczały podobnych materiałów - z żywicy olibanowej kadzidłowca powstawało prawdziwe kadzidło, z żywicy krzewu balsamowca powstawała Mirra. Wszystkie te materiały były bardzo cenne, stąd zwyczaj dawania ich w darze władcom, utrwalony w nowotestamentowej opowieści o królach czy mędrcach przybyłych do Betlejem. Ich spalanie w świątyniach miało zatem formę cennej ofiary bóstwom, było nawet określone ile kadzidła trzeba spalić przy konkretnych obrządkach. Zastanawiające, że w takiej formie - a więc właśnie ofiary dla Boga, przedostało się kadzidło do Chrześcijaństwa, choć dziś o takiej celowości obrządku kadzenia się wprost nie mówi*
Z celów bardziej praktycznych, wonności oczyszczały atmosferę a ta, w ciasnych budynkach, napełnionych tłumem przybyłych pątników mogła być w dawnych czasach bardzo ciężka. Jednym z tych kadzidlanych materiałów był Styraks, używany do dziś w kościołach obrządku wschodniego.
Arabowie nazywali go "lubān jāwī" (لبان خاوي ) czyli Kadzidło z Jawy - stamtąd bowiem po raz pierwszy go przywieziono. Nazwa w czasach mauretańskich trafiła do Hiszpanów, którzy przekazali ją w zmienionej formie jako Benjawi, z nimi handlowali Włosi, którzy usłyszeli nazwę jako benjuì lub bensui co ostatecznie stało się łacińskim benzoë - stąd dawna nazwa żywicy benzoinowej. Wcześniejsza hiszpańska forma musiała się jednak jeszcze gdzieś zachować, skoro w zupełnie zniekształconej postaci funkcjonuje w języku angielskim jako guma Benjamina[1]
W XVI wieku próbowano otrzymać ze styraksu olejki eteryczne, lecz podczas suchej destylacji otrzymywano jedynie biały proszek, o lekkich właściwościach kwasowych, nazwany kwasem benzoesowym - co ciekawe, jednym z pierwszych alchemików którzy opisali ten proces, był Nostre Dame czyli Nostradamus. W późniejszym czasie znaleziono ten związek jeszcze w migdałach, jako jeden z produktów rozkładu glikozydów cyjanogennych - amigdaliny, zaś pod koniec XIX wieku odkryto, że ma właściwości przeciwgrzybicze i zaczęto używać go do konserwacji owoców.
Wcześniej używano tu chemicznego krewniaka - kwasu salicylowego. Zakodowany w głowach obraz domowych przetworów, jako wekowanych słoików obwiniętych u góry papierem, wiąże się ze praktyką zakrywania słoików, przed zamknięciem wieczka, arkuszem papieru salicylowego nasączonego tym związkiem, zaś jeszcze przed wojną domowe przepisy obejmowały też dodawanie do dżemów "proszku salicylowego", który jako konserwant zabezpieczał przed zapleśnieniem. Jeszcze Stobiński w latach 70. w swej wspaniałej "Chemii i życiu" podaje takie przedwojenne przepisy, już jednak zastrzegając, że dodatek taki może źle odbić się na zdrowiu - jak wspominałem w notce o aspirynie, kwas salicylowy powoduje krwawienia z przewodu pokarmowego i zaburzenia żołądkowe.
Kwas benzoesowy okazał się więc zamiennikiem, o tyle bezpiecznym, że nie wywołującym takich skutków. I rzeczywiście, używa się go dziś, w formie soli, jako konserwantu żywności. Ma właściwości grzybobójcze i bakteriobójcze, a niektóre pochodne są używane jako fungicydy lub leki w grzybicach skóry. Sam kwas benzoesowy, rzadziej używany w stanie czystym, to E 210, sól sodowa to E 211, potasowa E212 a wapniowa E213.
Opisany już Styraks zawiera do 20% kwasu benzoesowego i co najmniej drugie tyle połączeń estrowych o intensywnym zapachu. Uzasadniałoby to skądinąd użyteczność styraksu w kadzidłach - kwas łatwo sublimował i w postaci stałych cząstek osiadał na podłodze, ścianach i pątnikach, zapobiegając rozprzestrzenianiu się w takiej ciżbie chorób bakteryjnych. Inne kadzidła jak mirra czy drzewo sandałowe, też mają takie właściwości, tym samym zalecenia pisarzy starożytnych, aby używać styraksu na rany w formie tynktur czy nasączonych płatków tkaniny, wydają się bardzo trafne.
Zatem benzoesany są obecne w żywności od stu lat. Jednak ostatnio coraz więcej słyszy się o wątpliwościach co do ich używania. Po słynnej reklamie wody smakowej, gdzie aktorka po przeczytaniu składu na etykiecie produktu konkretnej firmy, stwierdziła "wkrótce będziemy świecić" (po czym polecała produkt jakoby pozbawiony żadnych dodatków) benzoesan sodu stał się wręcz symbolem "chemii" w żywności a tym samym dostał się na języki internautów:
Gwiazdami w konserwowaniu żywności są dwa związki: benzoesan sodu i sorbinian potasu. Ten pierwszy, mający oznaczenie E 211, wzmacnia naturalny smak pożywienia, a zarazem niszczy drożdże, pleśnie i wirusy. Chętnie dodaje się go do napoi gazowanych, majonezu, marynat, konserw owocowych i warzywnych. Niestety, ma poważne wady. Jest kancerogenny, a także ma szkodliwy wpływ na procesy zachodzące w naszym mózgu,
Na początku lat 90 ograniczono w Polsce zastosowanie benzoesanu. Do publicznej wiadomości podano, że to z powodu jego znaczenia dla procesów przemian aminokwasów, zachodzących w mózgu (nie podano konkretnie, jakie jest to znaczenie).
Na stronie internetowej jednej z większych firm spożywczych możemy znaleźć informację, że benzoesany spożywane w nadmiarze mogą powodować uczulenia u astmatyków i alergików, a u osób wrażliwych na aspirynę zaburzenia w funkcjonowaniu przewodu pokarmowego (co to znaczy "w nadmiarze", nie podano).[2]
Lista szkodliwych konserwantów
E 210 rakotwórczy (benzoesan, syntetyczny, dodatek do napoi gazowanych, majonezów, marynat, konserw owocowych i warzwynnych, sałatek)
E 211 rakotwórczy (benzoesan sodu, syntetyczny)
E 212 rakotwórczy (benzoesan potasu, syntetyczny)
E 213 rakotwórczy (benzoesan wapnia, syntetyczny)
E 214 rakotwórczy (benzoesan etylu, p-hydroksybenzoesan etylu i pochodne, [3]
Peter Peiper, biolog molekularny z Sheffield University, twierdzi, że benzoesan sodu (E211) jest szkodliwy dla kodu genetycznego. Ten związek chemiczny jest w stanie poważnie uszkodzić mitochondria – mówi Piper. To z kolei powoduje tak wielką degenerację komórek, że z czasem może doprowadzić do choroby Parkinsona czy marskości wątroby. Piper ostrzega, że typ uszkodzenia powodowany przez benzoesan sodu jest powiązany z wieloma chorobami neurodegeneracyjnymi, które pojawiają się w późniejszym wieku. Co więcej, benzoesan sodu w połączeniu z witaminą C tworzy benzen, związek rakotwórczy.[4]Jeszcze nie tak źle w porównaniu z innymi dodatkami. Znam takie listy E gdzie szkodliwość przypisano wszystkim 1200 substancjom, włącznie z tymi które występują naturalnie w żywności, w tym kwaskowi cytrynowemu (E 330) witaminie C (E 300), pektynom owocowym (E 440) czy azotowi (E 941).
Na początek może rozprawię się z informacją o zabijaniu bakterii jelitowych - benzoesan owszem, jest bakteriobójczy, ale w środowisku kwaśnym (pH w zakresie 2-5). Niszczy bakterie w ten sposób, że jego forma kwasowa jest wchłaniana do komórki i zwiększając kwasowość wewnątrz hamuje metabolizm komórek. Słabo radzi sobie natomiast z bakteriami nawykłymi do kwaśnego środowiska, a więc z bakteriami fermentacji octowej, a prawie w ogóle nie rusza bakterii mlekowych, uważanych powszechnie za korzystne. Po przejściu przez żołądek trafia do jelit, gdzie dzięki obecności żółci panują warunki zasadowe. A w tych kwas benzoesowy traci swoje właściwości.
A jak jest z tymi alergiami? Jego struktura chemiczna jest zbliżona do kwasu salicylowego, dlatego u osób nadwrażliwych na salicylany wywołuje objawy podobne do astmy aspirynowej, jedynie trwające krócej ze względu na szybszy metabolizm. Z tego samego powodu może wywoływać alergie u osób wrażliwych, objawiające się wysypkami i podrażnieniami, choć w szerokich badaniach objawy pojawiały się zaledwie u 0,5-0,8% ludzi.
Co do rakotwórczości, nie wiem skąd autorzy takich stron biorą informację, ale gdy tylko grzebię po różnych pracach i artykułach, to za każdym razem związek okazywał się nierakotwórczy i mało szkodliwy. Weźmy choćby takie badania: sześciu mężczyzn zażywało w diecie 0,2-0,4 g kwasu benzoesowego przez dwa miesiące - nie stwierdzono pogorszonego samopoczucia, zmian obrazu krwi, czy składu moczu; albo studenci zażywali związek wedle planu, że najpierw przez pięć dni brali 1 g, potem część przez następne 5 dni brała 1,5 g, potem 2 g i na koniec trzech studentów brało 2,5 g, łącznie przez dwadzieścia dni przyjąwszy dawkę 35 g - stwierdzono takie objawy jak nudności, podrażnienia żołądka czy bóle głowy, objawy zanikły po skończeniu badania.[5] Związek jest też niekiedy używany w leczeniu osób z wrodzonymi zaburzeniami cyklu mocznikowego, aby wraz ze sprzęganą z nim glicyną usuwać nadmiar azotu alternatywną drogą. I tu podawanie dawek rzędu 200-500 mg przez kilka lat nie wywoływało negatywnych skutków. Obecnie ustalona maksymalna dopuszczalna dawka 5 mg/kg masy ciała na dobę została oparta na badaniach nadwrażliwości u alergików, uznając że poniżej tej dawki nie wystąpią u nich żadne objawy.
Wrażliwość zwierząt jest zróżnicowana - dawka toksyczna dla kotów to tylko 450 mg/kg kota, u gryzoni LD50 to prawie 2g/kg szczura. Nie stwierdzono niekorzystnych skutków podawania 500 mg/kg czterem kolejnym pokoleniom szczurów. W innych badaniach nie wykazano działania rakotwórczego w pięciu pokoleniach szczurów i myszy. U ciężarnych szczurzyc uszkodzenia płodu następowały dopiero przy zastosowaniu dawki toksycznej dla matki, w dawkach niższych uszkodzeń nie zanotowano.
Nie stwierdzono aby związek kumulował się w organizmach ani w glebie.[6]
Piotr Pieprz
Najciekawsza kwestia wiąże się z cytowanymi tu wnioskami biologa Petera Pipera, którzy przestrzegał przed piciem napojów, twierdząc że kwas benzoesowy uszkadza mitochondria, w związku z czym uszkadza tkanki, w związku z czym wywołuje Parkinsona i marskość wątroby.
W polskim internecie natykam się tylko na zeszłoroczne kopie wzajemne, w internecie anglojęzycznym znajduję dosłowne kopie aż do 2007 roku, nigdzie jednak nie znalazłem odniesienia do badań jakie przeprowadzał Piper. Nie mogłem znaleźć nic na ten temat w takich miejscach jak PubMed i innych w związku z czym zacząłem podejrzewać, że ktoś taki może nie istnieć - Peter Piper, czyli Piotr Pieprz to bohater starego angielskiego wierszyka - łamacza języka.** Potem oczywiście okazało się, że jest ktoś taki jak prof Peter W. Piper, czyli że wszyscy źle cytowali.
Wydaje się że źródłem jest artykuł z sobotniego dodatku do The Independent "Some soft drinks may seriously harm your health" w którym pan profesor opiera się na wynikach swoich badań z 1999 roku. Oryginalnego artykułu nie mogę znaleźć na stronach gazety, a po kliknięciu na odpowiednie linki wyskakuje mi, że takiej strony nie ma. Mamy zatem ustną opinię opartą na jakiś nieznanych badaniach własnych. Wreszcie okrężną drogą znalazłem pierwotny artykuł.
Co też takiego badał pan profesor? Drożdże.

Drożdże w kroplach.
Powiększenie ok. 400 razy.
Pan Pieprz potraktował drożdże na szalce Petriego roztworem benzoesanu sodu i sprawdzał jak sobie radzą. Dobrze wiadomo, że związek ten jest grzybobójczy, dlatego nie powinno być niezwykłe, że drożdże rozwijały się źle. W dodatku były to specjalne drożdże-mutanty, nie wytwarzające enzymu dysmutazy ponadtlenkowej, która ma za zadanie usuwać z komórki wolne rodniki, dlatego użyto ich jako organizmu modelowego, mającego sprawdzić wpływ związku na wytwarzanie rodników. No i stwierdzono że kwasy organiczne, w tym benzoesowy, sorbowy i propionowy, używane jako konserwanty, uszkadzają mitochondria zmutowanych drożdży z powodu wytwarzania wolnych rodników. Autor pracy wyrażał w związku z tym obawy o możliwy wpływ tych substancji na stres oksydacyjny komórek nabłonka przewodu pokarmowego. Tyle. [6]
Nie wiem jak natomiast odnieść te wyniki do zdrowia człowieka. Ludzkie komórki wytwarzają dysmutazę, więc bronią się przed rodnikami. Skoro tak, to ich mitochondria są chronione. Zatem kwas benzoesowy może dodać od siebie nieco więcej rodników, ale nie musi to przesądzać o uszkodzeniu komórek. Zresztą najwięcej enzymu zawierają komórki wątroby o którą tak się pan Pieprz obawiał. Co do Parkinsona, to aby wywołać jakieś zmiany w mózgu, kwas benzoesowy musiałby być wchłonięty, rozprowadzony we krwi i jeszcze przejść przez barierę krew-mózg, niestety jednak jak wiadomo, po wchłonięciu z przewodu pokarmowego w całości trafia do wątroby, gdzie traktowany jest glicyną i jako pochodna hipurowa wydalany wraz z moczem. Jest nawet używany do badań funkcji wątroby.
Zatem wnioski przedstawione w artykule prasowym były w najlepszym razie nadinterpretacją
Kolorowe napoje
Innym zarzutem stawianym temu związkowi, mającym trochę lepsze moim zdaniem oparcie w faktach, jest możliwość wzmagania nadpobudliwości u dzieci. Takie badania przeprowadzono na zlecenie Brytyjskiej Agencji Standardów Żywności (FSA) i dotyczyły wpływu mieszanek dodatków na stan dzieci nadaktywnych. Popularne media nie zauważyły jednak niuansów pracy i napisały, że dodatki w kolorowych napojach ową nadpobudliwość wywołują. Tymczasem badanie dotyczyło wpływu mieszanek barwników i konserwantów na aktywność dzieci które już są nadaktywne. Badanie polegało na podaniu dzieciom ze stwierdzonym ADHD roztworów czterech barwników i benzoesanu sodu, a następnie obserwacji czy ich zachowanie się zmieniło. Dla porównania części dzieci podano słodzoną wodę. U części dzieci stwierdzono wzrost aktywności, jednak wyniki były nie miarodajne - zależności nie pojawiały się we wszystkich grupach wiekowych, nie u wszystkich dzieci z takim samym natężeniem, u niektórych powtórne dawki nie wywoływały efektu. Uznano zatem, że choć nie jest to pewny dowód, to coś na rzeczy jest.[8] Dlatego też w 2008 ogólnoeuropejska FSA wezwała producentów aby dobrowolnie wycofali podejrzane barwniki z produktów spożywanych przez dzieci - gum, cukierków i napojów[9].
Podsumowując:
Wszystkie panikarskie stwierdzenia, że benzoesany są rakotwórcze, okropnie niebezpieczne, że dostaniemy po nich impotencji, łysienia i skrętu kiszek są bezpodstawne. Doniesienia o genotoksyczności wydają się nadinterpretacją. Jak na razie wszystko wskazuje, że benzoesan sodu należy do najbezpieczniejszych konserwantów, zabezpieczających żywność przed rozwojem bakterii a zwłaszcza wytwarzających rakotwórcze mykotoksyny pleśni.
Jeśli wolicie go unikać, bardzo proszę. Nigdy nie sądziłem aby takie przekąski jak cukierki czy gazowane napoje są zdrowe i mogą stanowić znaczący składnik diety. Ale wybierajcie z rozmysłu a nie z przestrachu. jeśli zaś przerzucicie się na zdrową, ekologiczną, naturalną żywność, to pamiętajcie że od benzoesanów i tak nie uciekniecie, występują bowiem naturalnie w całkiem pokaźnej grupie produktów:

Naturalne benzoesany: Styraks, żurawina i cynamon
Najwyższe stężenia naturalnych benzoesanów występują w owocach żurawiny, aż do 1300mg/100 g suszonych owoców. Z tego powodu jej jagódki nie psują się i zwierzęta wygrzebują je spod śniegu aż do wiosny. Między innymi dzięki nim żurawina ma właściwości zapobiegające zakażeniom pęcherza.
Niewiele mniej mają ich inne owoce leśne, a więc czarne borówki, czerwone jagody, jeżyny, poziomki, a maliny zawierają je pomieszane z salicylanami, co tłumaczyłoby ich wykorzystanie przy przeziębieniach. Całkiem sporo benzoesanów, głównie w formie estrów, zawiera anyżek i fenkuł, oraz ich olejki. Z innych przypraw mają ich całkiem sporo przyprawy korzenne w tym cynamon. Ponadto pojawiają się w serach i grzybach jako produkty fermentacji. Znaczyłoby to, że nasi przodkowie, jedzący wyłącznie naturalne nieprzetworzone jedzenie też często stykali się z tym związkiem, więc dla ludzkości to nie pierwszyzna.
A jak to jest z benzoesanem, witaminą C i benzenem? No cóż, o tym już miałem opowiedzieć, ale zacząłem zbytnio rozwlekle. Jak to z tą reakcją jest, a jest ciekawie, opowiem, ale w następnym wpisie.
-------
*żeby nie zaśmiecać wątku jeszcze bardziej dodam tu na końcu, że ciekawy ślad wonności, jako zastępczej, bo nie krwawej ofiary, znajdujemy w opowieści o Marcie. Gdy do domu Łazarza przybył Jezus, gospodarze oczywiście ugościli go chętnie, zaś jedna z sióstr Łazarza, skropiła gościowi stopy cennym olejkiem i otarła włosami. Opowieść była potem różnie interpretowana, ale ogólny sens jest taki, żeby dawać Panu co się ma najcenniejszego. Zapewne w późniejszych wiekach powoływano się na tą opowieść, aby uzasadnić potrzebność drogich wotów i złota w świątyniach.
**Peter Piper picked a peck of pickled peppers;
A peck of pickled peppers Peter Piper picked;
If Peter Piper picked a peck of pickled peppers,
Where's the peck of pickled peppers Peter Piper picked?!
[1] http://en.wikipedia.org/wiki/Benzoic_acid
[2] http://www.klinika-zdrowia.com/prasa.php?o=czytaj&p_id=10
[3] http://merlin-zdrowie.pl/?id=drobnoustroje
[4] http://www.roik.pl/benzoesan-sodu-e211-szkodliwy-dla-kodu-genetycznego/
[5] http://toxnet.nlm.nih.gov/cgi-bin/sis/search/a?dbs+hsdb:@term+@DOCNO+704
[6] http://www.inchem.org/documents/cicads/cicads/cicad26.htm - tu całościowy przegląd badań
[7] Piper, P. (1999). Yeast superoxide dismutase mutants reveal a pro-oxidant action of weak organic acid food preservatives Free Radical Biology and Medicine, 27 (11-12), 1219-1227 DOI: 10.1016/S0891-5849(99)00147-1
[8] http://www.myomancy.com/2007/09/food-colorings-and-hyperactivity/
[9] http://news.bbc.co.uk/2/hi/health/7340426.stm
Subskrybuj:
Posty (Atom)