Misja Rosetta badająca kometę 67/P Churymov-Gerasimenko budzi dziś mniejsze zainteresowanie, zwłaszcza od czasu nieszczęśliwie przedwczesnego końca lądownika, niemniej instrumenty sondy wciąż wysyłają ciekawe dane. Najnowsza publikacja Nature donosi o wykryciu w gazach wytryskujących z powierzchni jądra kometarnego molekularnego tlenu.
Jednym z instrumentów badawczych sondy jest spektrometr masowy ROSINA-DFMS. Przyrząd ten jonizuje gazy i wykrywa masy składających się nań cząsteczek, wykorzystując skłonność jonów do ruchu w polu elektrycznym z prędkością zależną od stosunku masy do ładunku. Dzięki temu możliwa jest szybka identyfikacja składu.
Dzięki niemu wiadomo było, że większość składu gazów emitowanych przez jądro kometarne (do 95%) stanowiła para wodna oraz tlenek i dwutlenek węgla. Bardziej interesujące okazały się składniki stanowiące resztę. Głównym okazał się być cząsteczkowy tlen, po nim elementarna siarka i metanol, ponadto ślady tlenków azotu i hydrazyny.
Skąd jednak tlen na komecie?
Jego zawartość porównano ze stężeniem dwutlenku węgla, tlenku i pary wodnej, wykazując że tylko w tym trzecim przypadku zachodzi wyraźna korelacja stężeń. Jeśli stężenia tlenu są powiązane ze stężeniami wody, to widocznie gazy te uwalniane są razem. Najprawdopodobniej promieniowanie ultrafioletowe wywołuje radiolizę lodu wodnego na powierzchni komety, powodując powstanie tlenu, który miesza się z lodem i wraz z nim sublimuje. Zachodzenie takiej reakcji potwierdzono zresztą eksperymentalnie. [1]
Fraktalne trójkąty
Fraktale to struktury samopodobne. Matematycznie ujmując, strukturę opisuje pewien prosty algorytm, którego nieskończone iteracje tworzą coraz mniejsze elementy, zachowujące podobieństwo do całości. Ta prostota sprawiająca, że rozległy i wydawałoby się skomplikowany wzór da się wywieść z kilku powtarzanych wciąż reguł sprawia, że struktury fraktalne bardzo często pojawiają się w przyrodzie, jako podstawa dla na przykład organizacji kolonii, układu żyłkowania liści, rozkładu pierzastych listków paproci czy form krystalicznych.
Jednym z pierwszych opisanych matematycznie fraktali, jest trójkąt Sierpińskiego. Ten polski matematyk zaproponował w 1915 roku figurę, otrzymaną wedle następującego algorytmu:
- Weź trójkąt równoboczny i łącząc środki boków podziel go na cztery mniejsze trójkąty
- Usuń trójkąt w środku
- Podziel w taki sam sposób trójkąty które pozostały
- Usuń trójkąciki po środku
- Powtórz operację w nieskończoność.
Wydawałoby się że w takiej sytuacji nic na z tego trójkąta powinno nie pozostać, w rzeczywistości jednak, ponieważ operujemy tutaj matematycznie na figurach teoretycznych, po nieskończonych podziałach i usuwaniach trójkątów otrzymamy zbiór punktów matematycznych o charakterystycznym, stałym układzie, który powtarza się w kolejnych powiększeniach w dowolnym miejscu tego trójkąta. Pole takiej figury jest zerowe.
Później wymyślono jeszcze inne podobne figury, jak dywan Sierpińskiego oparty o kwadraty, czy też bardziej dziś znane drzewkowate fraktale używane do tworzenia pięknych grafik komputerowych.
Ale co to ma wspólnego z chemią? Otóż chemicy od dawna zastanawiali się nad produkcją materiałów o strukturze fraktalnej. Jednym z rozwiązań są dendrymery, czyli cząsteczki o wielu rozgałęzieniach, które rozgałęziają się na mniejsze rozgałęzienia a te na jeszcze mniejsze i tak dalej dopóki tylko atomy gałązek jeszcze się w kolejnej warstwie mieszczą. Cząsteczki takie mają formę kulek, których modele przypominają nieco skonfundowanego jeża. Ta oparta jest o etylenodiaminę i amid kwasu propanowego:
Dendrymery bada się obecnie intensywnie pod kątem użycia jako nośniki leków, zewnętrzna warstwa gałązek tworzy bowiem powłoczkę z małymi porami, lecz wewnątrz pojawiają się znaczne, puste przestrzenie w których umieścić można pewną ilość potrzebnej substancji, jaką należy przetransportować w organizmie w pewne określone miejsca.
Tym ciekawsze są próby stworzenia płaskiej cząsteczki o strukturze Trójkąta Sierpińskiego.
Pierwszym takim doniesieniem była obserwacja struktur w pewnym stopniu podobnych do tego fraktala w agregatach DNA na odpowiednim podłożu. Fragmenty DNA ukształtowane w formie molekularnych płytek łączyły się końcami tworząc wzór, który badano mikroskopem sił atomowych.[2]
W zeszłym roku dwaj badacze z UMCS przedstawili symulacje, pokazujące że struktury Trójkąta Sierpińskiego powinny powstawać w warstwach zawierających sztywne cząsteczki organiczne zgięte pod odpowiednim kątem i łączące się na obu końcach za pośrednictwem jonów metalu, jako wynik spontanicznej samoorganizacji.[3]
Pomysł ten okazał się chyba bardzo obiecujący, skoro wyraźnie opierają się na nim najnowsze doniesienia. Najpierw podano informację o tym, że kompleksy terpirydyny z jonami miedzi tworzą struktury stanowiące fragment trójkąta Sierpińskiego.[4] W marcu pojawiła się praca chińskich chemików opisujących tworzenie się rozległych płatów fraktalnego wzoru w wyniku osadzania na powierzchni srebra dwóch podstawowych "cegiełek" - pochodnej terfenylu, z trzema pierścieniami benzenowymi połączonymi wiązaniem w zagiętą cząsteczkę i dwoma atomami bromu na końcach; oraz pochodnej kwaterfenylu zawierającej jeden pierścień benzenu więcej. Cząsteczki te łączyły się ze sobą przez oddziaływania między bromem a wodorem.[5]
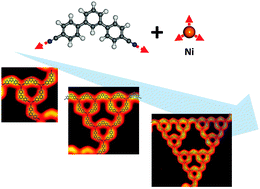
Najnowsza praca opisuje płaty kompleksów dwunitrylu terfenylu z niklem na powierzchni srebra, w których pojawiają się płaty wzoru Trójkąta Sierpińskiego. [6]
Barwnik z ery jurajskiej
Skamieniałości dawnych zwierząt i roślin w większości wyglądają jak specyficznie ukształtowana skała, są szare, białe, niekiedy opalizują jak perła. Dlatego zachowanie się pewnych barwników sprzed milionów lat stanowi ciekawy przypadek. Tak jest ze skamieniałościami wymarłych jurajskich alg Solenopora o wapiennych skorupkach, które tworzyły gąbczaste kolonie, z czasem kamieniejące, z przerastającymi rocznymi warstwami. W przypadku niektórych okazów daje się zauważyć wyraźne różowe zabarwienie, będące najwyraźniej pozostałościami pierwotnego pigmentu. W niedawno opublikowanej pracy zbadano właściwości tego barwnika, stwierdzając że to bardzo nietypowa substancja.
Barwnik otrzymany ze skamielin Solenopora jurassica sprzed około 150 milionów lat, składa się z dwóch fragmentów węglowodorowych, stanowiących najwyraźniej nie znaną pochodną antybiotyku klostrubiny A (clostrubin A) i połączonych przez atom boru ugrupowaniem spiroboranowym. Związki organiczne zawierające bor są w naturze ogółem dosyć rzadkie.
Klostrubina jest antybiotykiem wykazującym aktywność przeciwko wielu szczepom odpornych drobnoustrojów i dlatego wzbudza duże nadzieje. Jest substancją poznaną całkiem niedawno, wyizolowaną w zeszłym roku z bakterii z rodzaju Clostridium. Duże podobieństwo struktur nowego antybiotyku i cząsteczki skamieniałego barwnika, nazwanego borolitochromem (czyli dosłownie borowym barwnikiem kamieni) jest o tyle ciekawe, że dotyczy różnych grup organizmów. Najwyraźniej geny odpowiedzialne za syntezę od dawna krążą w ekosystemie, gdzieniegdzie ujawniając się wyraźnie.
[7]
 |
| Borolitochrom i skała z której go otrzymano. |
Ile atomów tworzy metal?
Wraz z przyjęciem i potwierdzeniem atomowej teorii budowy materii, chemicy i fizycy o bardziej filozoficznym zacięciu zaczęli zastanawiać się nad w sumie dość oczywistym pytaniem - ile potrzeba atomów bądź cząsteczek, aby z materii utworzyć materiał? Pojedynczy atom węgla ma inne właściwości niż choćby najmniejszy diament, trudno jest jednak wskazać moment, gdy następuje to przejście. Jest to swoisty odpowiednik "paradoksu łysego" - dwa stany skrajne, to jest łysina i pełne owłosienie, są od siebie bardzo wyraźnie różne; zarazem jednak jeśli osobie o pełnym owłosieniu zaczną pojedynczo wypadać włosy, trudno będzie nam wyznaczyć dokładną granicę od kiedy można już mówić o łysinie a kiedy jeszcze jest to tylko przerzedzenie włosów.
Ostatnie badania klastrów atomów metali pokazują jednak, że granicę naszej niepewności można w dużym stopniu zawęzić.
Metale to substancje stałe charakteryzujące się obecnością swobodnych elektronów poruszających się po sieci krystalicznej i tworzących wspólną, dużą chmurę elektronową. Właśnie dlatego metale dobrze przewodzą ciepło i elektryczność oraz odbijają światło ze srebrzystym, metalicznym połyskiem. Odpowiednio duże skupiska atomów metali też będą tworzyły swoją chmurę elektronową ale już pozostałe właściwości metaliczne niekoniecznie mogą być realizowane. Bardzo małe klastry zachowują się jak cząsteczki jakiegoś związku, często wykazując dość nieoczekiwane właściwości, przykładowo klastry 13 atomów glinu zachowują się jakby były atomem halogenku, mogąc oddawać elektrony i tworzyć aniony.
Fińscy chemicy z Uniwersytetu Jyväskylä badali takie właśnie graniczne klastry atomów złota, sprawdzając w jaki sposób reagują ze światłem. Klastry małe, mniejsze niż 102 atomy, zachowywały się jak cząsteczki. Pod wpływem fotonów przybierały pewne stany energetyczne obejmujące cały klaster, a wypromieniowanie i rozproszenie energii następowało stosunkowo (jak na atomową skalę) wolno. Grupy powyżej 144 atomów zachowywały się tak jak makroskopowe kawałki metalu, to jest szybko rozpraszały energię padającego światła, odbijały je zgodnie z prawem odbicia od lustra i nie przyjmowały ogólnoklastrowych stanów energetycznych.
Różnica była dość drastyczna - klastry większe o 42 atomy rozpraszały energię fotonów 100 razy szybciej. Natomiast klastry o wielkościach pośrednich wykazywały pośrednie własności, szybko zmieniające się z dodawaniem kolejnych atomów.
Tym samym w pewnym stopniu możliwe staje się wyznaczenie granicy między światem praw kwantowych a światem zjawisk fizyki klasycznej.[8]
-------------------
Źródła:
[1] A Bieler et al, Nature, 2015, DOI: 10.1038/nature15707
[2] Paul W K Rothemund, Nick Papadakis, Erik Winfree; Algorithmic self-assembly of DNA Sierpinski triangles. PLoS Biol 2004 Dec 7;2(12):e424. Epub 2004 Dec 7. [Open Acces]
[3] Simulation of the self-assembly of simple molecular bricks into Sierpiński triangle, Chem. Commun., 2014,50, 6843-6845
[4] Rajarshi S. et al.; One-step multicomponent self-assembly of a first-generation Sierpiński triangle: from fractal design to chemical reality. Angew Chem Int Ed Engl 2014 Nov 11;53(45):12182-5.
[5] Shang J. et al.; Assembling molecular Sierpiński triangle fractals, Nature Chemistry 7, 389–393
On-surface construction of a metal–organic Sierpiński triangle, Chem. Commun., 2015,51, 14164-14166
[7] Klaus Wolkenstein et al. Structure and Absolute Configuration of Jurassic Polyketide-Derived Spiroborate Pigments Obtained from Microgram Quantities, J. Am. Chem. Soc., 2015, 137 (42), pp 13460–13463 (2015).[Open Access]
[8] Mustalhi S. et al.; Molecule-like Photodynamics of Au102(pMBA)44 Nanocluster, ACS Nano, 2015, 9 (3), pp 2328–2335