Często w laboratoriach przez dłuższy czas używa się tych samych, przymocowanych na stałe, chłodnic szklanych, na przykład w zestawach do suszenia rozpuszczalników lub w wyparkach. Woda w nich nie zawsze jest spuszczana po użyciu, toteż wewnątrz, w wilgotnych i dobrze doświetlonych warunkach, chętnie rosną zielonkawe glony:
Wedle zasłyszanej opinii chemicy dzielą się na tych, który co jakiś czas rozbierają chłodnicę i czyszczą glony, i tych którym to nie przeszkadza, na zasadzie "jak będzie za duże to się spłucze".
Zawsze to jakaś roślinka...
informacje
wtorek, 20 maja 2014
sobota, 17 maja 2014
Kiedyś w laboratorium (39.)
W trakcie sprawdzania reaktywności jednego z ligandów, okazało się że daje on z miedzią dosyć trwałe połączenie - na tyle, że wytrącało się z izopropanolu w postaci ciemnobrązowego proszku, możliwego do oddzielenia. Podjąłem się próby wyizolowania kompleksu, i udało mi się odsączyć małą porcję, wyglądem przypominającą kawę rozpuszczalną:
Proszek był bezpostaciowy. Ponieważ połączenie wydawało się dosyć trwałe, postanowiłem je przekrystalizować - otrzymanie kryształów i zbadanie ich rentgenowsko mogłoby potwierdzać teorie na temat struktury kompleksu powstającego podczas reakcji, co było tym bardziej ciekawe, że dla tego typu ligandów jeszcze się to nie udało.
Rozpuściłem więc kompleks w chlorku metylenu, otrzymując żółtobrązowy roztwór:
Po czym wstawiłem całą fiolkę do naczynia z oktanolem. Ten mało lotny alkohol alifatyczny nasycał sobą powietrze w naczyniu, po wstawieniu fiolki część oktanolu z par rozpuszczała się w fiolce, zmniejszając rozpuszczalność związku. Równocześnie część chlorku odparowywała i rozpuszczała się w oktanolu.
Ta wyrafinowana technika miała powoli zatężać roztwór i sprzyjać powstaniu kryształów.
Niestety nie udało się - chlorek po kilku dniach odparował do końca a kompleks zbił się w bezpostaciowe kuleczki. Bywa.
Natomiast pisanie pracy idzie mi jak przez bagna.
Proszek był bezpostaciowy. Ponieważ połączenie wydawało się dosyć trwałe, postanowiłem je przekrystalizować - otrzymanie kryształów i zbadanie ich rentgenowsko mogłoby potwierdzać teorie na temat struktury kompleksu powstającego podczas reakcji, co było tym bardziej ciekawe, że dla tego typu ligandów jeszcze się to nie udało.
Rozpuściłem więc kompleks w chlorku metylenu, otrzymując żółtobrązowy roztwór:
Po czym wstawiłem całą fiolkę do naczynia z oktanolem. Ten mało lotny alkohol alifatyczny nasycał sobą powietrze w naczyniu, po wstawieniu fiolki część oktanolu z par rozpuszczała się w fiolce, zmniejszając rozpuszczalność związku. Równocześnie część chlorku odparowywała i rozpuszczała się w oktanolu.
Ta wyrafinowana technika miała powoli zatężać roztwór i sprzyjać powstaniu kryształów.
Niestety nie udało się - chlorek po kilku dniach odparował do końca a kompleks zbił się w bezpostaciowe kuleczki. Bywa.
Natomiast pisanie pracy idzie mi jak przez bagna.
poniedziałek, 12 maja 2014
Pisząc...
Pisząc sobie właśnie pracę magisterską musiałem pogrzebać w bibliotece:
W sumie najwięcej czasu zajmuje mi robienie rysunków reakcji i wpisywanie danych do tabel, jakoś tak trudno mi się przybrać. Jeśli chodzi o literaturę, irytuje mnie że nie każda praca jest dostępna - uniwersytet ma Tetrahedron Lett. do 1991 roku. Ma też wykupiony dostęp do wersji elektronicznej, ale w formie dokumentów tekstowych prace są dostępne od 1995 roku. W niedostępnym przedziale znajduje się kilka prac w sam raz mi pasujących. Chyba się przejadę do Warszawy i poszukam w PANie.
A. Jeszcze mam poster do zrobienia.
środa, 7 maja 2014
Chemiczne ogrody
Każdy pewnie kiedyś słyszał o tym doświadczeniu - do odpowiedniego roztworu wrzuca się małe kryształki, i po chwili zaczynają z nich wyrastać łodyżki i gałązki, podobne do fantastycznych wodorostów albo kwiatów. Mieliśmy coś takiego w małej skali na drugim roku:
Pytanie zatem - jak to powstaje i jak można coś takiego samemu zrobić?
Sama procedura sporządzania jest bardzo prosta - naczynie napełnia się roztworem krzemianu sodu, po czym wrzuca do niego kryształki soli metali przejściowych. Wokół kryształka powstaje mała banieczka, która uwypukla się aż z jej szczytu wysnuwać się zaczyna cienka wić, czasem rozgałęziająca się. Stopniowo wzrasta aż dotrze do powierzchni gdzie czasem jeszcze jest zdolna wyprodukować pływające zgrubienie. Gdy "roślinki" przestają rosnąć, naczynie można zamknąć i postawić w widocznym miejscu.
Krzemian sodu to inaczej szkło wodne, możliwe do dostania jako środek konserwujący do kamienia i betonu, natomiast sole metali przejściowych powinny być możliwe do kupienia w sklepach z odczynnikami. Samo wykonanie we własnym zakresie nie jest więc tak skomplikowane.
Szkło wodne, to roztwór krzemianów sodu i potasu, które można otrzymać stapiając krzemionkę z wodorotlenkami tych pierwiastków. Powstałe krzemiany tworzą gęsty, dosyć lepki roztwór o lekko opalizującym wyglądzie. Prawdopodobnie roztwór nie zawiera swobodnych anionów krzemianowych, lecz różnej wielkości połączenia liniowe i rozgałęzione aż do rozmiaru cząstek koloidalnych. Jest to i tak dobrze, bo z większością metali kwas krzemowy daje sole nierozpuszczalne.
Dodawane przez nas sole zwierają właśnie te metale, dające nierozpuszczalne krzemiany, dlatego gdy wrzucimy do roztworu kryształek, powstanie na nim natychmiast nierozpuszczalna warstewka krzemianu i reakcja ustanie. Warstewka ta nie przepuszcza krzemianów, więc reakcja nie może postępować dalej.
Zarazem jednak jest to warstewka na tyle cienka, iż przepuszcza wodę, stanowi więc błonę półprzepuszczalną. Gdy woda zacznie przenikać pod błonkę, rozpuści kryształek soli wewnątrz, tworząc bardzo stężony roztwór.
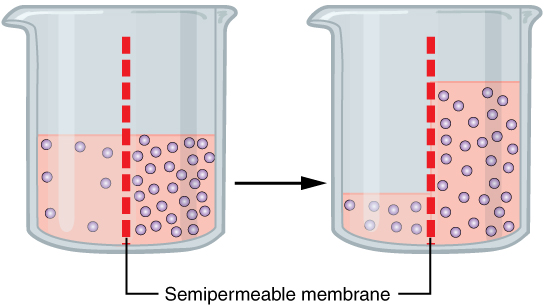
Prawa osmotyki mówią, że jeśli dwa roztwory o tym samym rozpuszczalniku ale różnych stężeniach przedzielimy membraną, przepuszczającą rozpuszczalnik, to zacznie on przenikać z roztworu mniej stężonego do bardziej. Ma to źródło w prostych prawach - od strony roztworu bardziej rozcieńczonego w membranę uderza w tym samym czasie więcej cząsteczek wody niż od strony bardziej zatężonego, można więc mówić o wyższym ciśnieniu cząstkowym; jeśli zaś część uderzających w błonkę cząsteczek może przez nią przeniknąć, to będzie następował przepływ rozpuszczalnika. W momencie gdy ciśnienia cząstkowe po obu stronach się wyrównają, bo roztwór bardziej rozcieńczony się zatężył a bardziej stężony rozcieńczył, przepływ ustaje.
Przepływ ten może, w sytuacji gdy błonka otacza pewną zamkniętą przestrzeń, doprowadzać do znacznego wzrostu ciśnienia, lub zmienić poziom roztworu, co też następuje w naszym przypadku - błonka wokół kryształu napina się, rozpierana rosnącą objętością roztworu, aż pęka. Gdy tylko błonka pęknie w jakimś punkcie, wokół wylewającej się porcji roztworu soli powstaje na nowo cienka błonka krzemianów. Przez błonkę do środka wnika woda, rozpuszcza się nowa porcja soli a ciśnienie rośnie do kolejnego pęknięcia.
Wzrost roślinek jest więc wynikiem ciągłego rozrywania wciąż powstającej błonki, i trwa do momentu aż rozpuści się cała sól z wrzuconego kryształka, a stężenia między środkiem a zewnętrzem się wyrównają.
Jeśli chodzi o kształt, to jest determinowany przez dwie siły - ciśnienie hydrostatyczne i siłę wyporu. Wielkość ciśnienia hydrostatycznego zależy od wielkości słupa roztworu nad danym punktem. O góry rosnącej błonki słup ten, a więc i ciśnienie, są nieco niższe niż przy dnie, dlatego tam najłatwiej jest ciśnieniu wewnątrz rozerwać błonkę i gałązka rośnie do góry. Dodatkowo roztwory soli w pęcherzyku są zwykle nieco lżejsze niż szkło wodne i dlatego powstająca gałązka zachowuje pion. Jakieś znaczenie mają też pęcherzyki powietrza przyczepiające się do błonki.
Kolor powstającej roślinki zależy od dodanej soli. Chlorek wapnia i siarczan glinu dadzą pędy białe, siarczan miedzi niebieskie, chlorki chromu III, niklu II i żelaza II dadzą rośliny zielone o różnych odcieniach, chlorek kobaltu da roślinę fioletowo-różową. Kształt pędu bardziej zależy od wielkości i kształtu pierwotnej grudni niż od rodzaju soli. Swój wpływ ma też stężenie szkła wodnego, od którego zależy grubość pędów.
Zastanawia mnie czy efekt taki dałyby kryształy kwasu cytrynowego, który powinien pokrywać się błonką uwodnionej krzemionki.
Doświadczenie to znane jest od dawna, i znane są liczne jego warianty. do najciekawszych należy chyba eksperyment na międzynarodowej stacji kosmicznej, gdzie chciano sprawdzić, czy w stanie nieważkości roślinki przybiorą jakieś ciekawe kształty - okazało się że brak kierowania przez ciśnienie hydrostatyczne, powoduje powstawanie nieregularnych odgałęzień skierowanych w różne strony.
Kolor powstającej roślinki zależy od dodanej soli. Chlorek wapnia i siarczan glinu dadzą pędy białe, siarczan miedzi niebieskie, chlorki chromu III, niklu II i żelaza II dadzą rośliny zielone o różnych odcieniach, chlorek kobaltu da roślinę fioletowo-różową. Kształt pędu bardziej zależy od wielkości i kształtu pierwotnej grudni niż od rodzaju soli. Swój wpływ ma też stężenie szkła wodnego, od którego zależy grubość pędów.
Zastanawia mnie czy efekt taki dałyby kryształy kwasu cytrynowego, który powinien pokrywać się błonką uwodnionej krzemionki.
Doświadczenie to znane jest od dawna, i znane są liczne jego warianty. do najciekawszych należy chyba eksperyment na międzynarodowej stacji kosmicznej, gdzie chciano sprawdzić, czy w stanie nieważkości roślinki przybiorą jakieś ciekawe kształty - okazało się że brak kierowania przez ciśnienie hydrostatyczne, powoduje powstawanie nieregularnych odgałęzień skierowanych w różne strony.
Subskrybuj:
Posty (Atom)