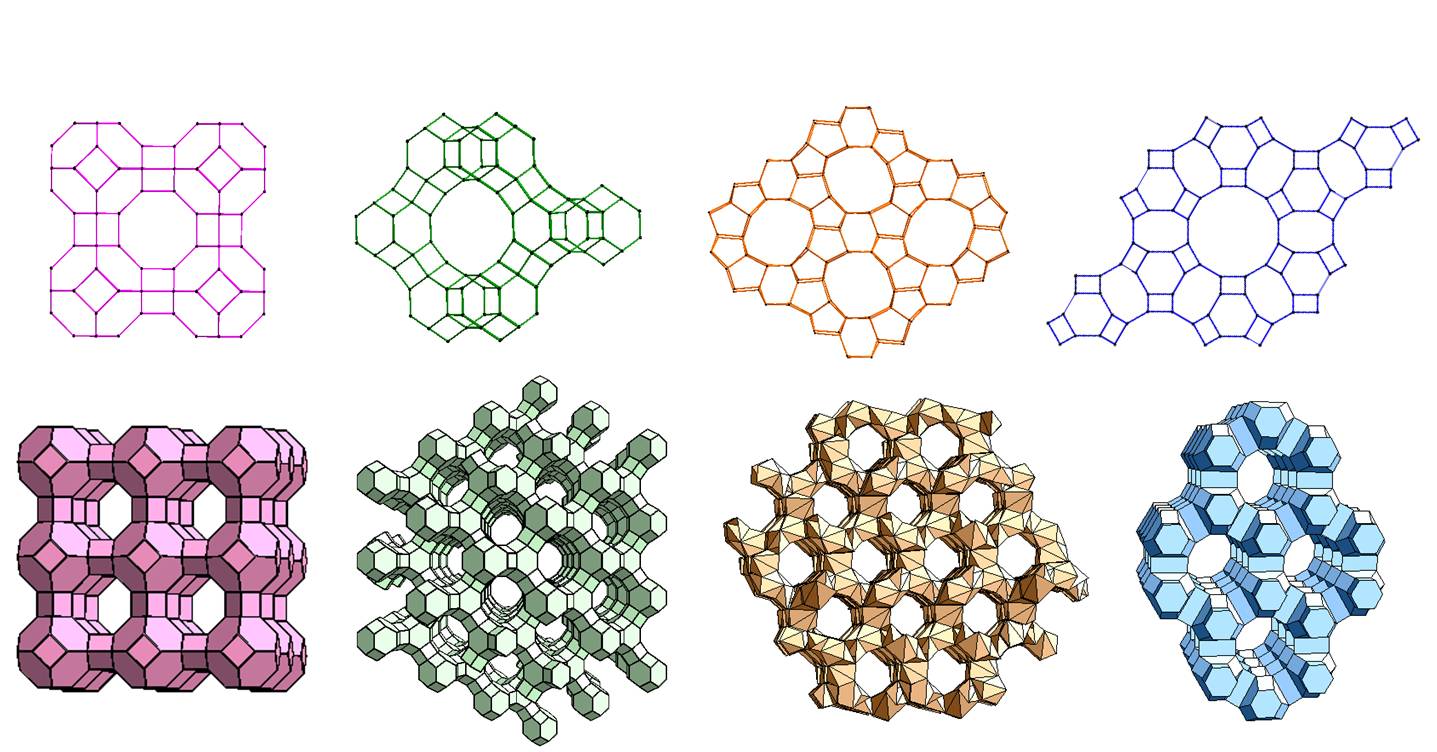
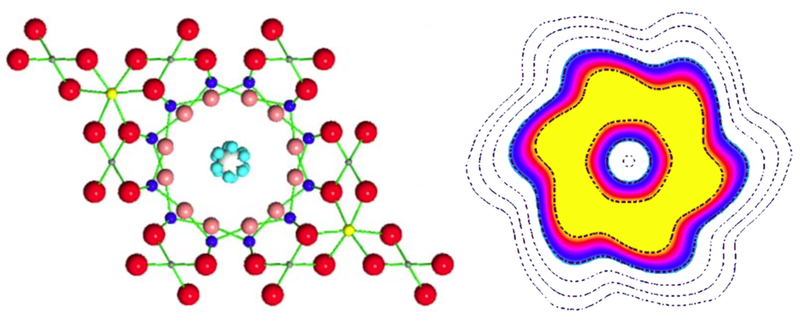
Na pomysł tego wpisu naprowadziły mnie pastylki na kaszel. Gdy przeglądałem dostępne w aptece znalazłem też takie, które chwaliły się że nie zawierają cukru. Zajrzałem więc na skład gdzie jako główny środek słodzący wymieniono ksylitol. To, samo w sobie, nie było jeszcze zaskakujące, jednak producent uznał za potrzebne uspokojenie klienta, tak aby nie zaniepokoił się tą trudną nazwą i w nawiasie wyjaśnił "ekstrakt z kory brzozy". I w tym problem, że składnik ten jest akurat takim ekstraktem, jak wódka sokiem...
Zacznijmy może od najbardziej podstawowej rzeczy - ksylitol nie jest cukrem. Więc pisanie wszędzie, we wszystkich reklamach, że to "cukier brzozowy" jest błędem. Na właściwy trop powinna naprowadzać nas już nazwa - końcówka -ol jest właściwa dla alkoholi, i faktycznie, ksylitol należy do grupy alkoholi cukrowych.
Typowy cukier to cząsteczka nasycona będąca łańcuchem węglowodorowym w którym każdy (lub prawie dla cukrów deoksy) węgiel jest przyłączony z grupą -OH, stąd wzór ogólny Cx(H2O)y i nazwa węglowodany, wydaje się bowiem sądząc po tym wzorze, jakby składały się z węgla i wody. Tym co odróżnia je od alkoholi wielohydroksylowych jest obecność grupy aldehydowej lub ketonowej, a więc z podwójnym wiązaniem węgiel-tlen C=O. Grupa ta wpływa na ich reaktywność oraz umożliwia im występowanie w formie pierścieniowej po utworzeniu hemiacetalu.
Jeśli teraz zredukujemy cukier tak, aby także tą grupę aldehydową lub ketonową zamienić w kolejną grupę -OH otrzymamy alkohol polihydroksylowy. Ze zredukowania glukozy powstaje sorbitol, także znany jako środek słodzący, ze zredukowanej mannozy mannitol. Możliwe jest też selektywne redukowanie wielocukrów. Ogółem różnym alkoholom cukrowym poświęcę jakiś osobny wpis, ale teraz zajmę się tym jednym. Natomiast ksylitol to produkt zredukowania ksylozy.
Ksyloza to cukier prosty zawierający pięć atomów węgla; glukoza i fruktoza zawierają ich sześć. W przyrodzie rzadko występuje swobodnie, najczęściej jest składnikiem hemiceluloz, będących budulcem ścian komórkowych roślin. Wiele połączonych cząsteczek ksylozy, czasem też arabinozy, tworzy łańcuchy nie tak długie i silnie połączone jak celuloza, stanowiące raczej spoiwo. Głównym wyróżnikiem jest łatwa rozpuszczalność w rozcieńczonych zasadach, dzięki czemu można je oddzielić od celulozy.
Hemicelulozy są w świecie roślinnym wszechobecne, spotykamy je w tkankach, szczególnie dużo w tych łykowatych i drewniejących. Są też obecne w drewnie zwłaszcza młodych drzew, przy czym im ich więcej tym bardziej jest miękkie i skłonne do pęcznienia, najwięcej bo do 30% zawiera ich drewno brzozy i buka. Aby otrzymać z tkanek ksylozę, najpierw trzeba oddzielić od nich hemicelulozy.
Rozdrobione tkanki roślinne traktuje się rozcieńczonymi zasadami, w których dobrze się rozpuszczają. Następnie zakwasza i poddaje hydrolizie bądź w warunkach silnie kwaśnych, bądź enzymatycznej. Po oczyszczeniu i wykrystalizowaniu otrzymujemy ksylozę. W czasie wojny Finowie pozbawieni dobrych źródeł cukru stosowali jako zamiennik właśnie ksylozę, która wprawdzie nie jest tak bardzo słodka jak cukier stołowy, ale w kraju gdzie burak cukrowy nie urośnie było to zawsze coś.
W Europie zwykle produkuje się ksylozę z drewna, mamy bowiem dość dobre źródła, natomiast na świecie są to łykowate części roślin, zwłaszcza łodygi kukurydzy, ale także wytłoki trzciny cukrowej, słoma z owsa lub ryżu a nawet łuski nasion bawełny. Często ksyloza jest spotykana pod nazwą cukru drzewnego, ale niekoniecznie brzozowego.
 |
| Ksyloza |
No dobra. Mamy już ksylozę. Co zrobić aby otrzymać z niej ksylitol? A no zredukować.
W przemyśle stosuje się głównie uwodornianie na katalizatorze niklowym [1] Robi się też próby z redukcją mikrobiologiczną przy pomocy pewnych gatunków drożdży lub pleśni, ale te nie mają takiego znaczenia.
U niektórych zwierząt wykazuje wręcz przeciwne działanie - podany psom wywołuje na tyle silne wydzielenie insuliny, że może im grozić śmierć z powodu hipoglikemii; wystarczy już dawka rzędu 100 mg/kg psa. Było to dawniej przyczyną problemów z wprowadzeniem na rynek, ale dopiero potem badania pokazały że u ludzi ma zupełnie odmienny metabolizm i nie jest dla nich szkodliwy.
Jest dość wolno wchłaniany z jelita i większość jest przetwarzana przez bakterie jelitowe do krótkołańcuchowych kwasów tłuszczowych. W takiej formie metabolity ksylitolu mogą być wchłaniane i zużywane, w związku z czym wbrew temu co piszą niektóre strony nie jest to związek "bez kalorii"; wartość energetyczna to około 70% kaloryczności glukozy. Słabe wchłanianie w jelitach ma też swoje złe strony, może bowiem w zbyt dużych ilościach wywołać biegunkę osmotyczną, związaną z wydalaniem wody do treści jelit dla wyrównania stężenia, jednak organizm stopniowo adaptuje się do wchłaniania dzięki czemu po pewnym czasie można spożyć nawet kilkadziesiąt gramów bez złych skutków. Ponadto bakterie jelitowe mogą przetwarzać go nazbyt ochoczo doprowadzając do wzdęć.
Jak wykazują badania ze względu na to że nie jest metabolizowany przez bakterie w jamie ustnej nie przyczynia się do rozwoju próchnicy a nawet w pewnym stopniu ją hamuje wpływając na mineralizację szkliwa.
Czym więc nie jest ksylitol? Na pewno nie jest "ekstraktem z kory brzozy" - w tym przypadku producent pojechał po bandzie. Problematyczne są też reklamy opisujące, że jest otrzymywany z brzozy bez uściślenia w jaki sposób. W efekcie wielu ludzi wyobraża sobie, że występuje w drewnie, liściach lub soku i stamtąd jest po prostu wymywany, parę razy widziałem domysły, że krystalizuje się go z soku brzozowego w związku z czym sok taki propaguje się przypisując mu jego właściwości, a nawet domysły, że to po prostu wysuszony sok z brzozy (w rzeczywistości sok brzozy zawiera głownie sacharozę i glukozę[2]). W dodatku producenci skrzętnie omijają w reklamach inne źródła, jak wspomniane łodygi kukurydzy czy słoma owsiana, bo brzoza budzi lepsze skojarzenia, brzmi bardziej dziko i naturalnie.
Inny problem to reklamy opisujące że ksylitol jest składnikiem "występującym w naturze" czy wręcz "naturalnym" - faktycznie, występuje w naturze, szczególnie dużo (ok. 1%) jest go w owocach jagodowych i niektórych warzywach, ale nie stamtąd się go otrzymuje. A akurat ten sprzedawany z sklepach jest otrzymywany z drewna które go nie zawiera po dwuetapowym procesie, więc w najlepszym razie jest produktem półsyntetycznym. Niestety kult naturalności i przekonanie że wszystko co sztuczne musi być złe powodują, że dla większych zysków producenci starają się mniej lub bardziej oszukać klientów.
Jako ciekawostkę dodam na koniec, że po znitrowaniu można z ksylitolu zrobić całkiem niezły materiał wybuchowy. To tak a'propos argumentacji "to musi być złe bo ma złe zastosowania".
-------------
Źródła:
* https://en.wikipedia.org/wiki/Xylitol
* https://www.dcnutrition.com/miscellaneous/Detail.CFM?RecordNumber=695
* http://www.danisco.com/fileadmin/user_upload/danisco/documents/products/2e_XIVIA_White_Paper.pdf
[1] http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0104-66322003000300006
[2] http://luczaj.com/publikacje/2014%20Luczaj%20Bilek%20Stawarczyk.pdf
Polecam obszerny artykuł na temat ksylitolu, nie znalazłem go gdy szukałem informacji do swojego a dużo uzupełnia:
http://pinkcake.blox.pl/2015/02/Ksylitol-bialy-oczyszczony-nienaturalny.html