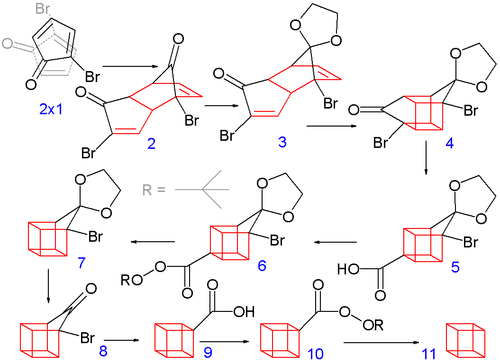
Przebarwianie się grzybów pod wpływem uszkodzenia czy rozkrojenia, jest zjawiskiem częstym. Zazwyczaj spotykamy się z nim u Podgrzybków i Borowików oraz innych gatunków rodzaju Boletus, obserwuje się też przebarwianie się białego soku Mleczajów. Dlatego może nas zastanowić skąd się to bierze i czy można w ten sposób odróżnić grzyb jadalny od trującego?
No, niestety zarówno pierwsza jak i druga sprawa, nie są takie proste...
To co pospolicie nazywamy grzybem, stanowi jedynie naziemną, wypuszczaną co pewien czas część grzybicznego osobnika, kryjącego się w ziemi lub drewnie w postaci pleśniowatych strzępków. Owocnik ten, spleciony z twardej tkanki, ma za zadanie rozsiewać zarodniki tworzące się zwykle pod "okapem" kapelusza i uwalniane do powietrza, aby wraz z wiatrem dotrzeć na znaczne odległości. Inne grzyby pomagają sobie wstrzykując zawiesinę zarodników do powietrza, jak choćby pospolite purchawki. Jeszcze inne wykorzystują owady, przyciągane nie miłą wonią padliny i odchodów.
Owocniki te jednakowoż nie po to są produkowane przez grzybnię, aby je jakieś dwunożne zwierzę wycięło kozikiem i zeżarło, toteż grzyby utrudniają mykożercom zadanie bądź maskując się powierzchnią kapelusza podobną do zbrązowiałych liści, bądź wytwarzając rozmaite substancje zniechęcające czy trujące.
Jednym ze sposobów zniechęcenia zwierzęcia jest brunatnienie w miejscach uszkodzonych - pociemniały owocnik wygląda mniej atrakcyjnie - stąd też wiele gatunków grzybów wykazuje tego typu zmiany barwy. Interesujące jest przy tym co właściwie zmienia barwę i w jaki sposób.
Uszkodzenie tkanki grzyba powoduje uwolnienie z wnętrza komórek enzymów degradacyjnych, wśród nich także oksydazę fenolową. Zgodnie z nazwą wywołuje ona utlenienie związków fenolowych. Powstające chinony mają zwykle ciemniejszy kolor. Ponadto połączenie chinonów z pierwotnymi polifenolami tworzy kompleksy z przeniesieniem ładunku, mające bardzo żywe kolory. Wszystkie te efekty wywołują zmianę barwy na niebieską, granatową czy wręcz czarną, ale czasem też czerwoną lub fioletową. Wszystko zależy od tego jakie polifenole są zawarte w danym grzybie.
Podobną przyczynę ma przy okazji brązowienie ziemniaków.
Rekcja zachodzi dosyć szybko:
Borowikowe
Rodzina borowikowatych jest bardzo obszerna i obfituje w grzyby smaczne i jadalne. Należą tu borowiki jak i podgrzybki (w nowszej klasyfikacji uznaje się że podgrzybki należą do tego samego rodzaju co borowik i nie stanowią osobnej grupy), ale też koźlarze, maślaczki, złotaki i bardzo nie lubiane goryczaki. Są to grzyby o rurkowatym spodzie kapelusza, podobnym do powierzchni gąbki.
Głównym czynnikiem barwiącym jest w nich brunatna atromentyna i , kwas wariegatowy (variegatic acid) będący pomarańczowym pigmentem, czy powstające z utlenienia atromentyny kwas pulwinowy i kwas wulpinowy (pulvinic acid i vulpinic acid - nazwy są przy okazji anagramami), oraz ich pochodne jak lakton pulwinon, odpowiedzialny za kolor kapelusza maślaka żółtego.
Po uszkodzeniu tkanek, ulegają one dalszemu utlenieniu, przykładowo z podobnych kwasu wariegatowego i kserokomowego (a może borowikowego?) przez utlenianie enzymatyczne powstają niebieskie chinony, a bez enzymu z tego pierwszego powstaje czerwona wariegatorubina[1] :
Do borowików bardzo podobny jest też Piaskowiec, przy czym dla mnie interesujący jest jadalny piaskowiec modrzak, po przekrojeniu zabarwiający się na dość wyraźny niebieski kolor
Wymienione polifenole oprócz wpływu na kolor grzyba, miewają też ciekawy wpływ biologiczny - wspomniany pulwinon i jego pochodne mają działanie cytostatyczne, mogą stanowić nowe antybiotyki, ale też leki przeciwgólowe i przeciwzapalne, kwas wariegatowy to silny przeciwutleniacz.
Mleczaje
Mleczaje to rodzaj grzybów należących do rodziny gołąbkowatych. Ich charakterystyczną cechą jest mleczko wypływające z uszkodzonych miejsc, czasem zabarwione i dodatkowo zmieniające kolor podobnie jak miąższ. Przykładowo ceniony mleczaj rydz ma pomarańczowe mleczko nie zmieniające koloru i zieleniejący miąższ, lekko trujący mleczaj złocisty ma biały miąższ i mleczko, które po kilku sekundach robi się żółte.
Ich głównymi związkami barwnymi są seskwiterpenoidy zawierające cząsteczkę azulenu, ciekawego węglowodoru aromatycznego, będącego połączeniem pierścienia pentenu i heptatrienu. Cząsteczka ta nadaje im żywe barwy. Przykładowo w mleczaju czerwieniejącym, sączącym po przekrojeniu krwiste mleczko, głównym barwnikiem jest czerwona laktarowiolina (lactaroviolin) będąca aldehydem
Mleczaj świerkowy ma mleczko początkowo pomarańczowe, jednak w ciągu pół godziny staje się ciemnoczerwone by na koniec przy wysychaniu stać się zielonkawe.
Co ciekawe mleczko tego grzyba zawiera zielonkawy laktarofulwen i niebieski laktarazulenen, tych jednak początkowo nie widać. Zmiany koloru są związane z enzymatyczną przemianą nietrwałych estrów pomarańczowego dihydroazulen-1-olu, o dużej intensywności barwy, z których uwalniany jest wolny azulenol o słabszym, żółtym kolorze. Ten ulega dalszemu utlenieniu, enzymatycznemu lub nie, do pochodnych jak fioletowa laktarowiolina, żółtawy delicial czy niebieski deterrol. Mieszanka tych pochodnych, z przewagą laktarowioliny tworzy bordowy kolor. Z czasem nie żółty delicial i azulenol polimeryzują do utworzenia zielonych produktów, które wraz z cały czas obecnym niebieskim laktarazulenem dają w efekcie brudnozielony kolor wysychającego mleczka.[3]
W zasadzie tymi reakcjami można tłumaczyć wszystkie zmiany barwy. Jeśli mleczaje nie zawierają estrów azulenolu, to ich mleczko jest białe i nie zmienia koloru, jak to ma miejsce u mleczaja modrzewiowego. Jeśli je zawierają bez innych azulenów i zawierają enzym je rozbijający, to białe mleczko żółcieje, jak u mleczaja złotawego. Jeśli zawierają inne azuleny, to mleczko jest pomarańczowe i z czasem może zielenieć, jak u mleczaja rydza. Jeśli zawierają estry azulenolu i enzym je rozbijający oraz drugi enzym utleniający, to pomarańczowy sok z czasem czerwienieje, jak u mleczaja jodłowego. A jeśli zawierają estry, enzym hydrolizujący i enzym utleniający o małej aktywności, to mleczko żółcieje, czerwienieje i zielenieje.
Mam wrażenie że przydałoby się zrobić z tego tabelkę kolorów.
Omówione seskwiterpenoidy oprócz koloru, nadają też grzybom smak, często palący. Są dla grzyba obroną przed nadgryzającymi owadami, zalewanymi lepkim mleczkiem, choć często nie przeszkadza to ich larwom. Ponieważ mają budowę podobną do hormonów roślinnych, mogą być użyte do przyspieszenia kiełkowania lub do ukorzeniania roślin. Niektóre mogą przydać się jako antybiotyki, inne są testowane jako potencjalne środki przeciwnowotworowe
Próby barwne
Fakt występowania w grzybach różnych substancji barwnych, stał się podstawą dla prób chemicznych, opierających się na traktowaniu kawałków grzybów różnymi odczynnikami. Ma to znaczenie właściwie raczej dla specjalistów, pozwalając odróżniać podobne gatunki, nie ma natomiast zbyt wielkiego dla przeciętnych grzybiarzy.
Najczęściej stosowanym odczynnikiem jest roztwór wodorotlenku potasu. Ma on za zadanie wywołać zmianę barwy polifenoli o właściwościach wskaźników kwasowości i jest używany głównie do podgrzybków, w mniejszym stopniu do pieczarek. W podobnym celu stosuje się wodny roztwór amoniaku. często stosowany jest też roztwór siarczanu żelaza II tworzący z polifenolami mocno zabarwione kompleksy.
Testy te pozwalają na odróżnienie zbliżonych do siebie gatunków, ale nie mają znaczenia dla zwykłego grzybiarza. Mleczaj chrząstka czy mleczaj piekący to tak czy siak niejadalny grzyb, nawet jeden inaczej reaguje z odczynnikiem.
Pewną wartość w wątpliwych przypadkach może mieć natomiast test Meixnera wykrywający toksyny muchomora, na przykład sromotnikowego. Wykonuje się go stosunkowo prosto, jeśli oczywiście ma się pod ręką odczynnik. Kawałek grzyba kładzie się na papierze gazetowym, tak aby papier nasączył się sokiem z miąższu. Potem na ten kawałek daje się kroplę mocnego kwasu solnego i lekko ogrzewa, na przykład suszarką do włosów. W razie obecności trucizny po kilku minutach papier zabarwia się na zielonkawo-niebiesko.
Zasada działania jest ciekawa - papier na którym drukuje się gazety (ten nielakierowany) jest robiony z pulpy z której nie oddzielono ligniny. Taki papier lepiej przyjmuje tusz, ale też szybciej żółknie i kruszy się. Lignina składa się z mieszaniny cząsteczek aromatycznych i fenolowych. Pod wpływem mocnego kwasu solnego, reaguje z toksyną tworząc konglomeraty o kolorze niebieskawym. Testu nie można robić na słońcu. Wykrywa podobne do siebie amatoksyny, związki łączące pierścień peptydu z aminą z grupą indolową:
Występują w grzybach z rodzajów muchomor, czy hełmówka, oraz niektórych czubajeczkach, wywołując po spożyciu ciężkie uszkodzenie wątroby. Grupa indolowa ulega podczas testu podstawieniu przez polifenole ligniny, tworząc związki o silniejszym kolorze.[4]
Test mógłby przydać się chociażby smakoszom, chcącym spróbować jadalnych gatunków muchomora, na przykład bardzo cenionego muchomora cesarskiego czy smacznego muchomora żółtego.
Test ten może dawać fałszywe wyniki w przypadku kilku grzybów niejadalnych, a także w przypadku grzybów zawierających psylocybinę, z ugrupowaniem indolowym w cząsteczce. Powoduje to, że miłośnicy podobnych używek próbują stosować ten test do rozpoznawania grzybów halucynogennych. Ponieważ jednak większość grzybów dających tą reakcję, to grzyby trujące, zwłaszcza hełmówki wyglądające identycznie jak niektóre łysiczki, w Ameryce notuje się rocznie po kilka zgonów z powodu pomyłki tą drogą.
W ogóle niebieszczenie grzybów jest przez wielu uważane za oznakę halucynogenności. Może to wynikać stąd że jeden z najpopularniejszych takich grzybów ma niebieski kolor. Mit ten jest tak powszechny i silny w wielu krajach, że szukając czegoś na temat "bluing mushrooms" nie mogłem znaleźć nic innego jak tylko setki stron o grzybkach rekreacyjnych. Nawet gdy dopisywałem nazwę konkretnego, jadalnego grzyba to i tak wyskakiwały mi fora używkowe, na których nastolatki rozprawiały o tym, czy jeśli podgrzybek sinieje to czy wywołuje halucynacje "jak wszystkie niebieskie grzyby".
Farbowanie grzybem?
W poszukiwaniu informacji natknąłem się na ciekawy wątek. Jednym z rodzajów hobbystycznego rękodzieła jest samodzielne farbowanie tkanin. Znani są zapaleńcy stosowania urzetu, są zapaleńcy testowania na bawełnie wywaru z kory olchy, liści brzozy czy marzanki, natomiast mało znani są eksperymentatorzy próbujący farbować tkaniny grzybami i porostami.[5] A wygląda na to że potrafią osiągać na prawdę ciekawe efekty kolorystyczne:
Test na trującego grzyba?
Niestety w naszym kraju jest tak, że więcej osób grzyby zbiera niż się na nich zna. I gdy potem w domu pojawią się wątpliwości, ludzie próbują rozpoznać grzyba na podstawie zasłyszanych mitów, co czasem kończy się tragicznie. Mity tego rodzaju mają jedną wspólną cechę - opierają się na przekonaniu że wszystkie grzyby trujące mają jakąś wspólną cechę, którą można poznać wizualnie lub w inny sposób przed zjedzeniem. Tak powstają zasady w rodzaju "wszystkie trujące grzyby mają X". Tylko że grzyb od grzyba się różni.
Do najpopularniejszych należy przekonanie, że grzyba trującego nie zjadają ślimaki. Akurat to nie jest prawda, niektóre trujące grzyby zjadają nawet chętniej niż jadalne. Ślimak ma inny metabolizm i na niego pewne trucizny mogą nie działać.
Inny mit to przekonanie, że od wszystkich trujących grzybów czernieje srebro. Bierze się zapewne z podobnego mitu na temat trucizn roślinnych, mogącego mieć pewne uzasadnienie w przypadku trucizn zawierających w składzie siarkę. Grzyby niestety są w siarkę raczej ubogie a ich substancje toksyczne ze srebrem nie reagują.
Nie lepiej jest z próbowaniem na smak - na pewno można tak rozpoznać goryczaka żółciowego, który zresztą nie jest trujący tylko okropnie smakuje, ale wiele grzybów trujących nie ma niemiłego, czy palącego smaku. Sromotnik jest podobno nawet słodkawy i ma przyjemny aromat. Czubajeczka czerwonobrązowawa ma owocowy aromat i niewyczuwalny smak.
Zasadniczo najlepiej jest zbierać grzyby które się zna i nie eksperymentować.
-------
* http://www.grzyby.pl/slownik-odczynniki.htm
* http://www.mushroomexpert.com/macrochemicals.html
* Jan VELÍŠEK, Karel CEJPEK, Pigments of Higher Fungi: A Review, Czech J. Food Sci.
Vol. 29, 2011, No. 2: 87–102
* http://mycopigments.com/
[1] Bluing Components and Other Pigments Boletes, Stephen F. Nelson
[2] Helmut Besl, Andreas Bresinsky, Wolfgang Steglich, Klaus Zipfel, Pilzpigmente, XVII. Über Gyrocyanin, das blauende Prinzip des Kornblumenröhrlings (Gyroporus cyanescens), und eine oxidative Ringverengung des Atromentins, Chemische Berichte Volume 106, Issue 10, pages 3223–3229, Oktober 1973
[3] http://de.wikipedia.org/wiki/Fichten-Reizker
[4] http://www.mykoweb.com/TFWNA/P-17.html
[5] http://mushroom-collecting.com/mushroomdyeing.html
[3] http://de.wikipedia.org/wiki/Fichten-Reizker
[4] http://www.mykoweb.com/TFWNA/P-17.html
[5] http://mushroom-collecting.com/mushroomdyeing.html