Ostatnie w tym roku chemiczne newsy, które uznałem za na tyle ciekawe, że warte krótkiego omówienia.
Wyniki programu AI do przewidywania zachowania białek niezbyt wiarygodne
Problem złożenia białek i oddziaływania cząsteczek z tak utworzoną strukturą, to ważny temat w badaniach podstawowych. Białka są niciami aminokwasów, które nie pływają jako proste nitki, lecz wskutek wewnętrznych oddziaływań skręcają się w różnego typu sprężynki, kłębki i pętelki. Na podstawie znanych podobieństw można przewidywać w pewnym stopniu, że w strukturze białka będzie zawarty pewien znany motyw, ale przewidzenie najbardziej prawdopodobnego kształtu w organizmie to trafienie w jedną z bardzo wielu fizycznie możliwych kombinacji.
Białko skręcone w odpowiedni kształt w organizmie pełni swoją funkcję, czy to enzymu, czy to receptora, czy to elementu strukturalnego. Mutacje powodują zmianę tego kształtu i wpływają na skuteczność działania, z kolei leki łączą się z tymi skręconymi białkami w sposób zależny od dopasowania struktur. Metody obliczeniowe przewidujące jak prawdopodobnie pofałduje się białko o znanej sekwencji zajmują dużo czasu obliczeniowego i wymagają skomplikowanych algorytmów uruchamianych na rdzeniach o dużej mocy obliczeniowej.
Dlatego narzędzia takie jak Alpha Fold, obiecujące, że ich AI nauczyło się na podstawie setek tysięcy przykładów jak działają białka i teraz odgaduje prawidłowy kształt dużo szybciej, zostały bardzo ciepło przyjęte. Rok temu twórcy programu otrzymali Nagrodę Nobla.
Teraz jednak pojawiła się publikacja zawierająca więcej wątpliwości. Czego tak naprawdę nauczyła się AI na wielu przykładach z bazy i czy rzeczywiście rozumie o co chodzi w fizyce oddziaływań?
Nowe wersje tych programów obiecują uproszczenie ważnego problemu dokowania ligandów, czyli sposobu i siły wiązania drobnych cząsteczek z białkiem. Jakie to ma znaczenie? - Oddziaływanie białka z substancją to podstawa do wyszukiwania leków, bo lek powinien ostatecznie zadziałać na jakiś enzym czy receptor i wywołać skutek. Bardzo dokładne modelowania tego typu wymagają obliczeń na superkomputerach. Obecnie na najważniejszych klastrach obliczeniowych biochemicy liczący struktury i dynamikę długich białek walczą o czas obliczeniowy z fizykami symulującymi supergromady galaktyk. Programy takie jak Alpha Fold czy Rosetta Fold miały robić to samo prościej w oparciu o podobieństwa strukturalne i ogólną logikę i albo dawać mniej precyzyjne ale wystarczające do szybkiego przeglądu dane, albo przygotować dane wstępne do symulacji, co skraca czas obliczeniowy.
Profesor Marcus Lill z University of Basel zajmuje się podobną tematyką i skuteczne narzędzie tego rodzaju byłoby bardzo pomocne, jednak gdy przeglądał udostępnione przez producenta informacje o skuteczności przewidywania struktur zaczął nabierać wątpliwości. Obliczenia miały dawać podejrzanie wysokie statystyki odtworzenia znanych już struktur, jak na program opierający się na ilości przykładów do nauki dużo mniejszej niż wcześniejsze bazy struktur białek generalnie. Można było oczekiwać, że dokładność modelowania będzie mniejsza.
Aby przetestować fizykę modelów zadał im do rozwiązania problem dokowania ligandów do białka dzikiego, białka zmodyfikowanego tak aby miejsce wiążące działało słabiej i białka zmienionego tak bardzo ze miejsce wiążące przestało być wiążące. Ogólny kształt białka był podobny ale kluczowy rejon, z którym lek tworzył powiązanie miał na przykład aminokwasy zastąpione odpowiednikami o przeciwnej jonizacji. Mimo to program tworzył bardzo podobne rozwiązania, nie zauważając, że w zmodyfikowanej wersji białka coś jest nie halo. Podobnie modyfikacja cząsteczki ligandu nie wiele zmieniały - cząsteczka o podobnym kształcie ale nie zawierająca grup wiążących nadal dokowała się do białka tak jak prawdziwy ligand. Programowi nie przeszkadzały oczywiste konflikty geometryczne, np. umieszczał cząsteczkę w miejscu białka, gdzie w dzikiej wersji była kieszeń o odpowiedniej wielkości, a w zmienionej wersji tej kieszeni właściwie nie było.
Wniosek był więc taki, że programy nauczyły się ogólnych zasad geometrycznego ułożenia ligandów obok białek, tak na prawdę nie rozumiejąc o co chodzi w fizyce i chemii oddziaływań i dlatego nie zauważają, ze ich rozwiązania są niemożliwe fizycznie.
https://phys.org/news/2025-10-ai-drug-physics-1.html
Kwas ortowęglowy jednak istnieje
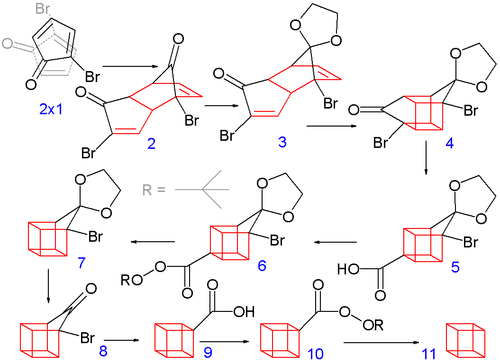
Kwas ortowęglowy to ostatni kawałek w układance możliwych przemian utlenionych związków węgla, a jego istnienie było przewidywane od tak dawna, że chemicy odetchnęli z ulgą, gdy w końcu udało się potwierdzić jego istnienie. Można przedstawić pewien ciąg coraz bardziej utlenionych pochodnych metanu - metanol z jedną grupą OH, metanodiol, nazywany też hydratem formaldehydu, z dwiema grupami OH. Znane są pochodne estrowe kwasu ortomrówkowego z trzema grupami OH i kwasu ortowęglowego z czterema - jednak wolne kwasy tych estrów nie były przez długi czas możliwe do wykrycia i zastanawiano się, czy takie połączenie będzie w ogóle możliwe.
Wolny kwas ortomrówkowy wyizolowano w roku 2024 przez napromieniowanie zamrożonej mieszaniny metanolu i tlenu i odparowanie produktów, dlatego kwas ortowęglowy wydawał się w zasięgu. Teoretycznie powinien powstawać w wyniku hydratacji kwasu węglowego, ten zaś daje się izolować w stanie czystym. Jednak kwas węglowy w kontakcie z wodą preferencyjnie ulega rozpadowi na wodorowęglan, a także kwas ortowęglowy powinien być wrażliwy na reakcje z wodą i na reakcje sam ze sobą. W utworzeniu związku przeszkadza też napięcie steryczne wprowadzane przez osiem niewiążących par elektronowych wszystkich tlenów, które silnie się odpychają, mając tendencję do odchodzenia jako rodniki hydroksylowe, dlatego pojawiały się wątpliwości czy związek z czterema wiązaniami węgiel-hydroksyl istnieje, czy może stanowi kompleks rodników.
Grupa badawcza z USA i Chin wykonała jednak symulacje, z których wynikało, że w niskich temperaturach w fazie gazowej cząsteczka ortowęglanu powinna posiadać barierę energetyczną umożliwiającą utrzymanie się cząsteczki. Warunki musiały stanowić w zasadzie wysoką próżnię aby ograniczyć kontakt z czymkolwiek z czym kwas mógłby wejść w reakcje. Obliczono teoretyczne energie jonizacji, które okazały się różne od energii jonizacji kwasu węglowego i ortomrówkowego, i wiedząc to wszystko zaprojektowano eksperyment.
Mieszanina lodu wodnego i stałego dwutlenku węgla została umieszczona w wysokiej próżni i naświetlana elektronami. Wybite z powierzchni cząsteczki tworzyły parę, którą naświetlano światłem o częstotliwościach odpowiadających wyliczonym energiom jonizacji. Spektroskopia czasu przelotu pokazała pojawienie się jonów, które nie pojawiały się bez zastosowania tego światła, zatem powstały wskutek fotojonizacji cząstek w fazie gazowej. Użycie znakowanego węglem C-13 dwutlenku i deuterowanego lodu pokazało, że masy rejestrowanych jonów zmieniły się zgodnie z przewidywaniami ilości węgla i wodoru. Ostatecznie potwierdziło to, że jonizującą się cząsteczką w fazie gazowej musiał był kwas C(OH)4, a zatem cząsteczka taka tworzy się.
Kwas ortowęglowy był przewidywany jako istotny związek pośredni w chemii węgla, tlenu i wodoru w kosmosie, a jego istnienie jako etapu pośredniego umożliwia zajście pewnych reakcji prowadzących do skomplikowanych związków organicznych - w tym tych stanowiących cegiełki budulcowe potencjalnego życia. Wykrycie jaka jest energia rozpadu, ile energii jest potrzebne do jego utworzenia i jaki jest czas półtrwania, pozwala doprecyzować obliczenia ilościowe zagęszczenia dalszych produktów reakcji w mgławicach.
https://pubs.acs.org/doi/10.1021/jacs.4c02637
https://pmc.ncbi.nlm.nih.gov/articles/PMC12260057/
Największa cząsteczka aromatyczna wykryta w kosmosie
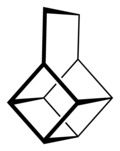
Koronen to wielopierścieniowy węglowodór aromatyczny (WWA) o szczególnej, regularnej budowie. W zasadzie jest to struktura utworzona przez sześciokątny pierścień benzenowy otoczony sześcioma takimi pierścieniami. Ze względu na symetrię i silnie wyrażone właściwości aromatyczne, jest jednym z częstych produktów reakcji zwęglania, częściowego spalania czy kondensacji par węgla w próżni.
 |
| Koronen |
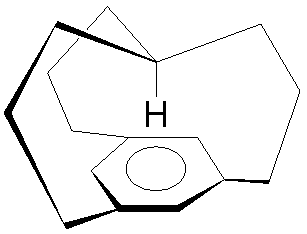
Ponieważ podejrzewa się, że WWA stanowią znaczną część wolnego węgla we wszechświecie, poszukiwane są cząsteczki dające na tyle charakterystyczne sygnały, żeby można było je wykryć i na tej podstawie oszacować ile węgla ogółem jest w danym miejscu kosmosu. W nowym doniesieniu badaczy z Green Bank Observatory informują oni, że wytypowali jako możliwą taką cząsteczkę 1-koronenonitryl, to jest koronen z jedną grupą cyjankową. Jony lub rodniki CN stanowią częsty składnik obłoków molekularnych zawierających wegiel i azot i mogą podstawiać inne cząsteczki. Powstałe tak nitryle powinny wykazywać charakterystyczne sygnały w widmie światła przechodzącego przez obłok, inne niż sygnały związków wyjściowych.
Aby to zweryfikować chemicy zsyntezowali nie opisany wcześniej związek i poddali go warunkom podobnym do próżni kosmicznej aby zbadać jak oddziałuje ze światłem. Następnie poszukali wykrytych cech widma w świetle nadbiegającym z obłoku. Twierdzą , że dzięki trafianiu tych sygnałów w mało zaszumione rejony częstotliwości światła, mogą potwierdzić wykrycie związku ze stopniem pewności 17 sigma, czyli naprawdę bardzo dużym. Czy twierdzenie to wytrzyma próbę krytyki zobaczymy później, niedawne doniesienie o wykryciu "sygnatury życia" w atmosferze obcej planety jest podważane właśnie ze względu na statystyki prawdopodobieństwa identyfikacji.
https://greenbankobservatory.org/front-page-news/cosmic-chemistry-breakthrough-largest-aromatic-molecule-found-in-deep-space/
Używanie śrutu ołowiowego zostawia mikrocząstki w dziczyźnie
Mimo stopniowej akcji wycofywania ołowiu z pocisków używanych przez myśliwych, nadal nie wszyscy się przestawili, a pozyskane w ten sposób mięso pojawia się na rynku. Ryzyko zdrowotne połknięcia śrucin jest znane od dawna i notowano zatrucia ołowiem od połknięcia nawet jednej w swojskiej dziczyźnie. Aby zmniejszyć to ryzyko przepatruje się tuszę i wycina kawałki z uszkodzeniami, niektóre zakłady przetwórstwa prześwietlają mięso. Może to być jednak za mało dokładne. Jak pokazały wcześniejsze analizy z użyciem żelatyny balistycznej, mimo stosunkowo małej twardości kulka ołowiana wbijająca się w materiał tworzy rozpryski, które mogą rozchodzić się także na boki. Nowa analiza z użyciem promieniowania synchrotronowego, umożliwiająca zbadanie mięsa z ultra wysoką rozdzielczością pokazuje jednak, że cząstki ołowiu mogą być tak drobne, że możliwe do przeoczenia standardowym sprzętem.
W fragmencie piersi jelenia postrzelonego kulą ołowianą, przy pomocy medycznego rentgenu możliwe było znalezienie kilkunastu fragmentów. Synchrotron ukazał w mięsie 1800 fragmentów, z czego 1600 o średnicy poniżej 150 mikrometrów. W piersi pardwy pobranej z polowania, sześć śrucin przeszło przez mięsień na wylot a rentgen medyczny nie pokazał odłamków. Synchrotron pokazał 160 rozsianych wokół kanałów postrzałowych odłamków oddalonych o pół centymetra od postrzału.
https://www.nature.com/articles/s41598-025-20285-2
Prawdziwy kolor błękitnego gazu
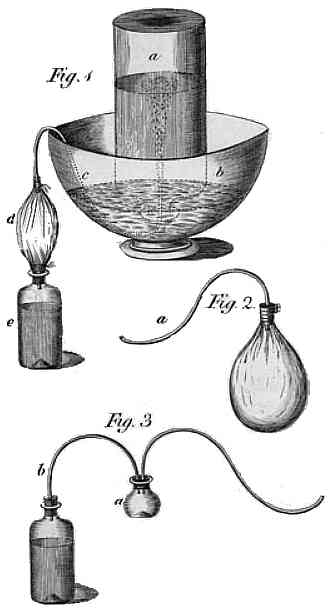
Większość znanych gazów jest bezbarwna lub lekko żółtawa a odcień staje się zauważalny w grubej warstwie lub po skropleniu. Gazów mających wyraźny kolor jest nie tak wiele - żóltozielony chlor, brązowy brom, pomarańczowy tlenek azotu, fioletowe pary jodu. Jednym z tych wyjątków jest też bardzo reaktywny i rzadko do czegoś wykorzystywany trifluoronitrozometan, gdzie niebieski kolor nadaje mu grupa nitrozowa. Trzy fluory przy węglu skutkują niskimi oddziaływaniami międzycząsteczkowymi, dzięki czemu związek o niskiej masie cząsteczkowej wrze w warunkach kriogenicznych (wyjściowy nitrozometan i analog trichlorowy są w warunkach normalnych cieczą).
Anglojęzyczna Wikipedia obrazowała kolor gazu zdjęciem kolby w uderzająco granatowym kolorze. Jednak chemik i youtuber z kanału Advanced Thinkering szukający informacji o tym gazie, podczas sprawdzania danych zdjęcia na wiki odkrył z rozczarowaniem, że zdjęcie to tak na prawde wizualizacja, otrzymana przez zmianę koloru na zdjęciu kolby z chlorem. Nie znalazł też w żadnej publikacji innego zdjęcia tego gazu, co oznaczało, że poza pamięcią nielicznych badaczy nikt nie może powiedzieć jaki właściwie ma on kolor.
Dlatego postanowił go zsyntezować a otrzymaną próbkę sfootografować i udostępnić na Wikipedii na wolnej licencji. Polecam filmy na ten temat, bo jest tam pokazany kawałek niezłej pracy laboratoryjnej.
I nowszy:













-side-3D-balls.png)
