Któregoś razu, chyba na praktykach, bawiłem się Spekolem.
Jest to stary acz poczciwy sprzęt do spektrofotometrii, badający absorbancję (odwrotność przepuszczalności) światła o zadanej częstotliwości fali. Otrzymanie wiązki o odpowiedniej fali odbywa się dosyć prosto - źródło światła wewnątrz wytwarza światło białe, rozszczepiane siatką dyfrakcyjną na pełne widmo. Przy pomocy pokrętła obracamy siatkę powodując, że do wąskiej szczeliny na którą nasadzony jest układ w który wkładamy próbki wpada światło jednej określonej barwy, a więc o konkretnej długości fali. Taki układ ma oczywiście pewne ograniczenia, ale sam sprzęt mimo wszystko działa dosyć dobrze i nadal można spotkać się w nim w wielu laboratoriach.
Po zdjęciu przykręconej części na próbki odsłania się wspomniana szczelina. I otóż korzystając kiedyś z okazji zrobiłem kilka zdjęć pokazujących światło o konkretnych długościach fali:
Zdjęcia nie zupełnie oddają rzeczywiste odcienie, z powodu ograniczeń matrycy. Przy końcu skali za fioletem dało się jeszcze zauważyć słaby fioletowy odcień, zauważalny gołym okiem ale już nie przez okulary.
informacje
niedziela, 29 września 2013
niedziela, 22 września 2013
Cebulowe łzy
O tym dlaczego czosnek śmierdzi a cebula skłania nas do płaczu.
Cebula jadalna to gatunek wieloletniej rośliny, należący formalnie do rodzaju czosnek w ramach szerszej rodziny amarylkowatych, wobec czego jej krewniakiem jest też narcyz. Stanowi składnik ludzkiej diety od kilku tysięcy lat - cebulowe łuski i ślady zwęglonych w ognisku cebulek znane są aż z 5 tysiąclecia przed naszą erą. Były też powszechnie spożywane w starożytnym Egipcie, o czym często wspominają zachowane inskrypcje, stanowiąc obok chleba i piwo podstawę diety klas niższych. Była czczona prawdopodobnie jako jeden z symboli odrodzenia, na co wskazują jej znaleziska w grobowcach i obecność na malowidłach grobowych. Ślady cebulowych łusek znaleziono w oczodołach mumii Ramzesa IV.
W kontekście Egiptu wspomina o niej także Biblia: w Księdze Liczb w rozdziale 11 Izraelici wędrujący przez pustynię zaczynają narzekać na brak dobrego jedzenia, wspominając że w Egipcie mieli pod dostatkiem ryb, ogórków, melonów, cebuli, czosnku i porów, co wskazywałoby na całkiem przyzwoitą dietę jak na przymusowych robotników.
Warzywa te znane były też w starożytnej Grecji i Rzymie. W języku łacińskim zwano ją cepa lub zdrobniale cepula, co wpłynęło zarówno na nazwę polską jak i niemiecką (Zwiebel od staroniemieckiego Zwibolle). Cebula uważana była za środek wzmacniający, stąd też zjadali ją gladiatorzy dbający o formę, czosnek miał chronić przed chorobami i złymi duchami, przy czym zwykle był dla tych zastosowań nie jedzony tylko noszony jak amulet; z kolei por był uważany za afrodyzjak. Cesarz Neron zajadał się porem w ogromnych ilościach, uważając go za środek poprawiający jakość głosu, stąd też popularny przydomek "porrophagos" - porożerca.
Czosnek zdobył sobie dużą popularność wśród ludów semickich, najbardziej znani byli z tego Żydzi, regularnie jedzący czosnek w szabat. W późniejszych czasach doprowadziło to do wykształcenia stereotypu Żyda-śmierdziela* Co ciekawe dokładnie przeciwny stosunek mieli do niego Arabowie - w kilku miejscach Koranu wspomniane jest, że osoby jedzące czosnek nie powinny zbliżać się do meczetu lub grup modlących się, i czekać w domu aż przestaną pachnieć. Ostatecznie jednak w Islamie nie jest to warzywo zakazane.
Wszystkie rośliny z tego rodzaju charakteryzuje silny, ostry zapach i smak, spowodowany obecnością wtkankach aktywnego związku siarkoorganicznego Alliiny ulegającego dalszym przemianom podczas krojenia. A przemiany te są nieco bardziej skomplikowane, niż to się nam dotychczas wydawało.
Alliina formalnie rzecz biorąc jest pochodną aminokwasu Cysteiny, w której końcowa siarka została utleniona do sulfotlenku i zalkilowana grupą allilową:
W sulfotlenkach siarka jest na czwartym stopniu utlenienia i formalnie tworzy z tlenem wiązanie podwójne będąc analogiem ketonów, jest ono jednak tak silnie spolaryzowane, że często używa się zapisu jonowego z ładunkiem dodatnim na siarce i ujemnym na tlenie. Przy takiej strukturze jedna z par elektronowych zostaje wolna a jej odpychanie nadaje pozostałym wiązaniom formę piramidy trygonalnej. W efekcie pojawia się asymetria umożliwiająca powstanie dwóch form chiralnych, tak jak to jest w przypadku tetraedrycznym węglem. Alliina ma w związku z tym dwa centra stereogeniczne - na siarce (S) i na węglu (R) w części pochodzącej od aminokwasu.
W chwili wyodrębnienia był to pierwszy znany naturalny związek z takim układem centrów. W Cebuli ponadto występuje izoalliina, z podwójnym wiązaniem przesuniętym o jedno miejsce. Oba związki są bezwonne. Gdy zaczynami kroić, żuć czy rozgniatać cebulki, sytuacja ulega zmianie - ze zniszczonych komórek uwolnione zostają enzymy, głównie allinaza.
Od tego momentu zaczyna się kaskada reakcji: alliinaza hydrolizuje alliinę, dzieląc wiązanie między siarką a węglem części aminokwasowej. Z części siarkowej powstaje kwas 2-propenosulfonowy, a z aminokwasowej dehydroalaniny. Ta ostatnia spontanicznie rozkłada się do amoniaku i kwasu pirogronowego.
Kwas sulfonowy jest cząsteczką nietrwałą, stąd też bardo chętnie reaguje sam ze sobą. Dwie cząsteczki kondensują, tworząc allicynę, będącą głównym składnikiem zapachowym czosnku.
Cebula zawiera zarówno alliinę jak i izoalliinę, z których po reakcji z alliinazą powstaje kwas 2-propenosulfonowy i 1-propenosulfonowy, z ich kondensacji powstaje allicyna, choć raczej w ilościach śladowych, i związki polisiarkowe. A skąd łzy?
Jak dawniej sądzono, przyczyną są kwasy sulfonowe uwalniane do powietrza przed kondensacją, które rozpuszczając się w łzach zakwaszały je wywołując łzawienie. Jednak w 2002 roku odkryto inny mechanizm[1]. Powstający specyficznie w cebuli kwas 1-propenosulfonowy zostaje przekształcony przez kolejny enzym, nazwany syntazą czynnika łzawiącego, czyli w skrócie LFS. Powoduje on przesunięcie jednego wodoru i wiązania podwójnego, tworząc związek z wiązaniem podwójnym między siarką a węglem - propanotial-S-tlenek. Formalnie nadal jest on S-tlenkiem ale bez właściwości kwasowych. Możliwe są dwa położenia tlenu, stąd dwa izomery syn i anti, z przewagą tej pierwszej.
Związek ten jest bardzo łatwo lotny i szybko przedostaje się do powietrza, rozpuszcza w łzach i tutaj podrażnia oko, ale nie poprzez zakwaszanie lecz działanie na receptory bólu. Jest zatem silnym lakrymatorem, którego wydzielanie przez roślinę jest strategią mającą odstraszyć roślinożercę. Właśnie za to odkrycie, ostatecznie tłumaczące sprawę, przyznano tegorocznego Ig-Nobla choć samo w sobie nie jest specjalnie zabawne.
Tak rozpoczęty łańcuch reakcji nie kończy się. Łzawiący S-tlenek jest cząsteczką aktywną, chętnie więc, zwłaszcza podczas smażenia i gotowania, łączy się sam ze sobą tworząc dipropylodisulfid z mostkiem siarczkowym. Formalnie rzecz biorąc jest to uwodorniona allicyna. Wyjściowy związek ulega też hydrolizie do aldehydu propionowego o ostrym ale raczej owocowym zapachu, ale też kondensacji do związków wielosiarczkowych, nawet cyklicznych, o zapachach ostrych i nieprzyjemnych.
W przypadku czosnku końcowa allicyna jest głównym związkiem o specyficznym zapachu, ale nie jedynym. W wyniku jej rozkładu czy to w organizmie czy podczas gotowania, poprzez redukcję S-tlenek zamienia się w beztlenowy dwusiarczek dwuallilu (DADS), o zapachu jeszcze bardziej nieprzyjemnym. Jest to związek łatwo lotny. Powstając w organizmie podczas trawienia przedostaje się do krwioobiegu, stamtąd w płucach a wreszcie w naszym oddechu wpływając na zapach z ust. Inną pochodną jest dwusiarczek alliowo propylowy, decydujący z kolei o ostrym smaku cebuli. Oba związki są łatwo lotne i odparowują podczas gotowania, stąd słodkawy smak przyrządzonego warzywa. Są też alergenami, stąd możliwość uczulenia na czosnek.
Możliwe są też pochodne z większą ilością atomów siarki. Gdy czosnek jest macerowany w tłuszczu, czynnik łzawiący łączy się z allicyną tworząc ajoen. Tak więc z jednej czy dwóch cząsteczek może powstać kilkadziesiąt podobnych związków, w tym kilka o działaniu łzawiącym. Ponieważ czosnek nie zawiera enzymu LFS przy jego krojeniu już tak nie płaczemy.
A co zrobić, aby nie płakać przy cebuli? Zbyt dobrych rad nie ma, enzymy przestają działać przy podgrzaniu do 60 stopni, więc być może blanszowanie w wodzie o temperaturze 70-80 stopni i ochłodzenie, powinno spowodować że krojona cebula nie będzie tak działać, zachowując smak. Allinaza praktycznie nie działa w niskich temperaturach, więc można też kroić cebulki ochłodzone wcześniej na górnej półce lodówki do kilku stopni albo krótko w zamrażalniku prawie do zera - taka cebula zacznie działać dopiero po ogrzaniu w sałatce. Oba enzymy przestają też być aktywne przy zakwaszeniu, więc można spróbować zakwaszać cytryną, ale nie do każdych zastosowań się to przyda.
Swój sposób przeprowadzili biotechnolodzy, za pomocą różnych technik hybrydyzacji wyciszając gen produkujący LFS i tworząc "niepłaczliwą" odmianę.[2]
Wszystkie opisane związki mają różnorodne działanie na organizm. Często są bakteriobójcze, mogą obniżać poziom cholesterolu albo zmniejszać krzepliwość; są przeciwutleniaczami, związkami przeciwzapalnymi czy pobudzającymi odpowiedź immunologiczną. Oczywiście roślina nie po to je wytwarza. Ich ostry zapach i drażniące działanie ma odstraszać, zniechęcać roślinożercę do zjadania cebulek. Tego jednak, że znajdzie się zwierzę, które będzie je zjadało właśnie dla tego smaku i zapach, matka natura nie przewidziała.
--------
* Stereotyp ten wykazuje duże podobieństwo do różnych rasistowskich mitów. Jednym z elementów dehumanizacji nienawidzonej grupy, jest zawsze twierdzenie, że jej członkowie są brudni i śmierdzą. Jeszcze na początku XX wieku powszechne było w Ameryce przekonanie, że murzyna można poznać po smrodzie. Identycznie postrzegano w Chinach pierwszych europejczyków. "Zapach Żyda" był też w dawnej Europie uważany za cechę wrodzoną, wywołaną grzechem przodków, którzy nie uznali Jezusa. W jednej z wersji mitu o morderstwach rytualnych, spożywanie macy z krwią miało likwidować ten wrodzony odór. A wszystko przez czosnek...
[1] Imai S, Akita K, Tomotake M, Sawada H (2006. a) Identification of two novel pigment precursors and a reddish-purple pigment involved in the blue-green discoloration of onion and garlic. J Agric Food Chem 54 843–847.
[2] Colin C. Eady, Takahiro Kamoi, [...], and Shinsuke Imai, Silencing Onion Lachrymatory Factor Synthase Causes a Significant Change in the Sulfur Secondary Metabolite Profile, Plant. Physiol. August 2008 147(4) 2096-2106
*http://en.wikipedia.org/wiki/Garlic
*http://en.wikipedia.org/wiki/Onion
*http://pl.wikipedia.org/wiki/Alliina
*http://de.wikipedia.org/wiki/Alliin
*http://en.wikipedia.org/wiki/Alliin
*http://en.wikipedia.org/wiki/Allicin
*http://en.wikipedia.org/wiki/Alliinase
* http://en.wikipedia.org/wiki/Syn-propanethial-S-oxide
*http://en.wikipedia.org/wiki/Diallyl_disulfide
*http://antaryamin.wordpress.com/2012/07/08/what-islam-says-about-eating-onion-and-garlic/
*http://www.touregypt.net/featurestories/neferherenptaht.htm
*http://onions-usa.org/all-about-onions/history-of-onions
Cebula jadalna to gatunek wieloletniej rośliny, należący formalnie do rodzaju czosnek w ramach szerszej rodziny amarylkowatych, wobec czego jej krewniakiem jest też narcyz. Stanowi składnik ludzkiej diety od kilku tysięcy lat - cebulowe łuski i ślady zwęglonych w ognisku cebulek znane są aż z 5 tysiąclecia przed naszą erą. Były też powszechnie spożywane w starożytnym Egipcie, o czym często wspominają zachowane inskrypcje, stanowiąc obok chleba i piwo podstawę diety klas niższych. Była czczona prawdopodobnie jako jeden z symboli odrodzenia, na co wskazują jej znaleziska w grobowcach i obecność na malowidłach grobowych. Ślady cebulowych łusek znaleziono w oczodołach mumii Ramzesa IV.
W kontekście Egiptu wspomina o niej także Biblia: w Księdze Liczb w rozdziale 11 Izraelici wędrujący przez pustynię zaczynają narzekać na brak dobrego jedzenia, wspominając że w Egipcie mieli pod dostatkiem ryb, ogórków, melonów, cebuli, czosnku i porów, co wskazywałoby na całkiem przyzwoitą dietę jak na przymusowych robotników.
Uprawa cebuli na rysunkach z "ptasiego grobowca" z nekropolii w Sakkarze
Czosnek zdobył sobie dużą popularność wśród ludów semickich, najbardziej znani byli z tego Żydzi, regularnie jedzący czosnek w szabat. W późniejszych czasach doprowadziło to do wykształcenia stereotypu Żyda-śmierdziela* Co ciekawe dokładnie przeciwny stosunek mieli do niego Arabowie - w kilku miejscach Koranu wspomniane jest, że osoby jedzące czosnek nie powinny zbliżać się do meczetu lub grup modlących się, i czekać w domu aż przestaną pachnieć. Ostatecznie jednak w Islamie nie jest to warzywo zakazane.
Wszystkie rośliny z tego rodzaju charakteryzuje silny, ostry zapach i smak, spowodowany obecnością wtkankach aktywnego związku siarkoorganicznego Alliiny ulegającego dalszym przemianom podczas krojenia. A przemiany te są nieco bardziej skomplikowane, niż to się nam dotychczas wydawało.
Alliina formalnie rzecz biorąc jest pochodną aminokwasu Cysteiny, w której końcowa siarka została utleniona do sulfotlenku i zalkilowana grupą allilową:
W sulfotlenkach siarka jest na czwartym stopniu utlenienia i formalnie tworzy z tlenem wiązanie podwójne będąc analogiem ketonów, jest ono jednak tak silnie spolaryzowane, że często używa się zapisu jonowego z ładunkiem dodatnim na siarce i ujemnym na tlenie. Przy takiej strukturze jedna z par elektronowych zostaje wolna a jej odpychanie nadaje pozostałym wiązaniom formę piramidy trygonalnej. W efekcie pojawia się asymetria umożliwiająca powstanie dwóch form chiralnych, tak jak to jest w przypadku tetraedrycznym węglem. Alliina ma w związku z tym dwa centra stereogeniczne - na siarce (S) i na węglu (R) w części pochodzącej od aminokwasu.
W chwili wyodrębnienia był to pierwszy znany naturalny związek z takim układem centrów. W Cebuli ponadto występuje izoalliina, z podwójnym wiązaniem przesuniętym o jedno miejsce. Oba związki są bezwonne. Gdy zaczynami kroić, żuć czy rozgniatać cebulki, sytuacja ulega zmianie - ze zniszczonych komórek uwolnione zostają enzymy, głównie allinaza.
Od tego momentu zaczyna się kaskada reakcji: alliinaza hydrolizuje alliinę, dzieląc wiązanie między siarką a węglem części aminokwasowej. Z części siarkowej powstaje kwas 2-propenosulfonowy, a z aminokwasowej dehydroalaniny. Ta ostatnia spontanicznie rozkłada się do amoniaku i kwasu pirogronowego.
Kwas sulfonowy jest cząsteczką nietrwałą, stąd też bardo chętnie reaguje sam ze sobą. Dwie cząsteczki kondensują, tworząc allicynę, będącą głównym składnikiem zapachowym czosnku.
Cebula zawiera zarówno alliinę jak i izoalliinę, z których po reakcji z alliinazą powstaje kwas 2-propenosulfonowy i 1-propenosulfonowy, z ich kondensacji powstaje allicyna, choć raczej w ilościach śladowych, i związki polisiarkowe. A skąd łzy?
Jak dawniej sądzono, przyczyną są kwasy sulfonowe uwalniane do powietrza przed kondensacją, które rozpuszczając się w łzach zakwaszały je wywołując łzawienie. Jednak w 2002 roku odkryto inny mechanizm[1]. Powstający specyficznie w cebuli kwas 1-propenosulfonowy zostaje przekształcony przez kolejny enzym, nazwany syntazą czynnika łzawiącego, czyli w skrócie LFS. Powoduje on przesunięcie jednego wodoru i wiązania podwójnego, tworząc związek z wiązaniem podwójnym między siarką a węglem - propanotial-S-tlenek. Formalnie nadal jest on S-tlenkiem ale bez właściwości kwasowych. Możliwe są dwa położenia tlenu, stąd dwa izomery syn i anti, z przewagą tej pierwszej.
Związek ten jest bardzo łatwo lotny i szybko przedostaje się do powietrza, rozpuszcza w łzach i tutaj podrażnia oko, ale nie poprzez zakwaszanie lecz działanie na receptory bólu. Jest zatem silnym lakrymatorem, którego wydzielanie przez roślinę jest strategią mającą odstraszyć roślinożercę. Właśnie za to odkrycie, ostatecznie tłumaczące sprawę, przyznano tegorocznego Ig-Nobla choć samo w sobie nie jest specjalnie zabawne.
Tak rozpoczęty łańcuch reakcji nie kończy się. Łzawiący S-tlenek jest cząsteczką aktywną, chętnie więc, zwłaszcza podczas smażenia i gotowania, łączy się sam ze sobą tworząc dipropylodisulfid z mostkiem siarczkowym. Formalnie rzecz biorąc jest to uwodorniona allicyna. Wyjściowy związek ulega też hydrolizie do aldehydu propionowego o ostrym ale raczej owocowym zapachu, ale też kondensacji do związków wielosiarczkowych, nawet cyklicznych, o zapachach ostrych i nieprzyjemnych.
W przypadku czosnku końcowa allicyna jest głównym związkiem o specyficznym zapachu, ale nie jedynym. W wyniku jej rozkładu czy to w organizmie czy podczas gotowania, poprzez redukcję S-tlenek zamienia się w beztlenowy dwusiarczek dwuallilu (DADS), o zapachu jeszcze bardziej nieprzyjemnym. Jest to związek łatwo lotny. Powstając w organizmie podczas trawienia przedostaje się do krwioobiegu, stamtąd w płucach a wreszcie w naszym oddechu wpływając na zapach z ust. Inną pochodną jest dwusiarczek alliowo propylowy, decydujący z kolei o ostrym smaku cebuli. Oba związki są łatwo lotne i odparowują podczas gotowania, stąd słodkawy smak przyrządzonego warzywa. Są też alergenami, stąd możliwość uczulenia na czosnek.
Możliwe są też pochodne z większą ilością atomów siarki. Gdy czosnek jest macerowany w tłuszczu, czynnik łzawiący łączy się z allicyną tworząc ajoen. Tak więc z jednej czy dwóch cząsteczek może powstać kilkadziesiąt podobnych związków, w tym kilka o działaniu łzawiącym. Ponieważ czosnek nie zawiera enzymu LFS przy jego krojeniu już tak nie płaczemy.
A co zrobić, aby nie płakać przy cebuli? Zbyt dobrych rad nie ma, enzymy przestają działać przy podgrzaniu do 60 stopni, więc być może blanszowanie w wodzie o temperaturze 70-80 stopni i ochłodzenie, powinno spowodować że krojona cebula nie będzie tak działać, zachowując smak. Allinaza praktycznie nie działa w niskich temperaturach, więc można też kroić cebulki ochłodzone wcześniej na górnej półce lodówki do kilku stopni albo krótko w zamrażalniku prawie do zera - taka cebula zacznie działać dopiero po ogrzaniu w sałatce. Oba enzymy przestają też być aktywne przy zakwaszeniu, więc można spróbować zakwaszać cytryną, ale nie do każdych zastosowań się to przyda.
Swój sposób przeprowadzili biotechnolodzy, za pomocą różnych technik hybrydyzacji wyciszając gen produkujący LFS i tworząc "niepłaczliwą" odmianę.[2]
Wszystkie opisane związki mają różnorodne działanie na organizm. Często są bakteriobójcze, mogą obniżać poziom cholesterolu albo zmniejszać krzepliwość; są przeciwutleniaczami, związkami przeciwzapalnymi czy pobudzającymi odpowiedź immunologiczną. Oczywiście roślina nie po to je wytwarza. Ich ostry zapach i drażniące działanie ma odstraszać, zniechęcać roślinożercę do zjadania cebulek. Tego jednak, że znajdzie się zwierzę, które będzie je zjadało właśnie dla tego smaku i zapach, matka natura nie przewidziała.
--------
* Stereotyp ten wykazuje duże podobieństwo do różnych rasistowskich mitów. Jednym z elementów dehumanizacji nienawidzonej grupy, jest zawsze twierdzenie, że jej członkowie są brudni i śmierdzą. Jeszcze na początku XX wieku powszechne było w Ameryce przekonanie, że murzyna można poznać po smrodzie. Identycznie postrzegano w Chinach pierwszych europejczyków. "Zapach Żyda" był też w dawnej Europie uważany za cechę wrodzoną, wywołaną grzechem przodków, którzy nie uznali Jezusa. W jednej z wersji mitu o morderstwach rytualnych, spożywanie macy z krwią miało likwidować ten wrodzony odór. A wszystko przez czosnek...
[1] Imai S, Akita K, Tomotake M, Sawada H (2006. a) Identification of two novel pigment precursors and a reddish-purple pigment involved in the blue-green discoloration of onion and garlic. J Agric Food Chem 54 843–847.
[2] Colin C. Eady, Takahiro Kamoi, [...], and Shinsuke Imai, Silencing Onion Lachrymatory Factor Synthase Causes a Significant Change in the Sulfur Secondary Metabolite Profile, Plant. Physiol. August 2008 147(4) 2096-2106
*http://en.wikipedia.org/wiki/Garlic
*http://en.wikipedia.org/wiki/Onion
*http://pl.wikipedia.org/wiki/Alliina
*http://de.wikipedia.org/wiki/Alliin
*http://en.wikipedia.org/wiki/Alliin
*http://en.wikipedia.org/wiki/Allicin
*http://en.wikipedia.org/wiki/Alliinase
* http://en.wikipedia.org/wiki/Syn-propanethial-S-oxide
*http://en.wikipedia.org/wiki/Diallyl_disulfide
*http://antaryamin.wordpress.com/2012/07/08/what-islam-says-about-eating-onion-and-garlic/
*http://www.touregypt.net/featurestories/neferherenptaht.htm
*http://onions-usa.org/all-about-onions/history-of-onions
środa, 11 września 2013
Kiedyś w laboratorium (32.)
Na zajęciach z chemii fizycznej jednym z ćwiczeń było badanie stałej kwasowej wskaźnika pH czerwieni fenolowej. Do roztworu bufora z dodatkiem wskaźnika, dodawaliśmy po 0,2 ml wodorotlenku sodu. Po każdym dodatku i rozmieszaniu mieszadełkiem sprawdzaliśmy absorbancję roztworu w spektrofotometrze. Oczywiście nie mogłem się powstrzymać przed zrobieniem zdjęć ukazujących powolną zmianę barw - ostatni odcień podobał mi się najbardziej.
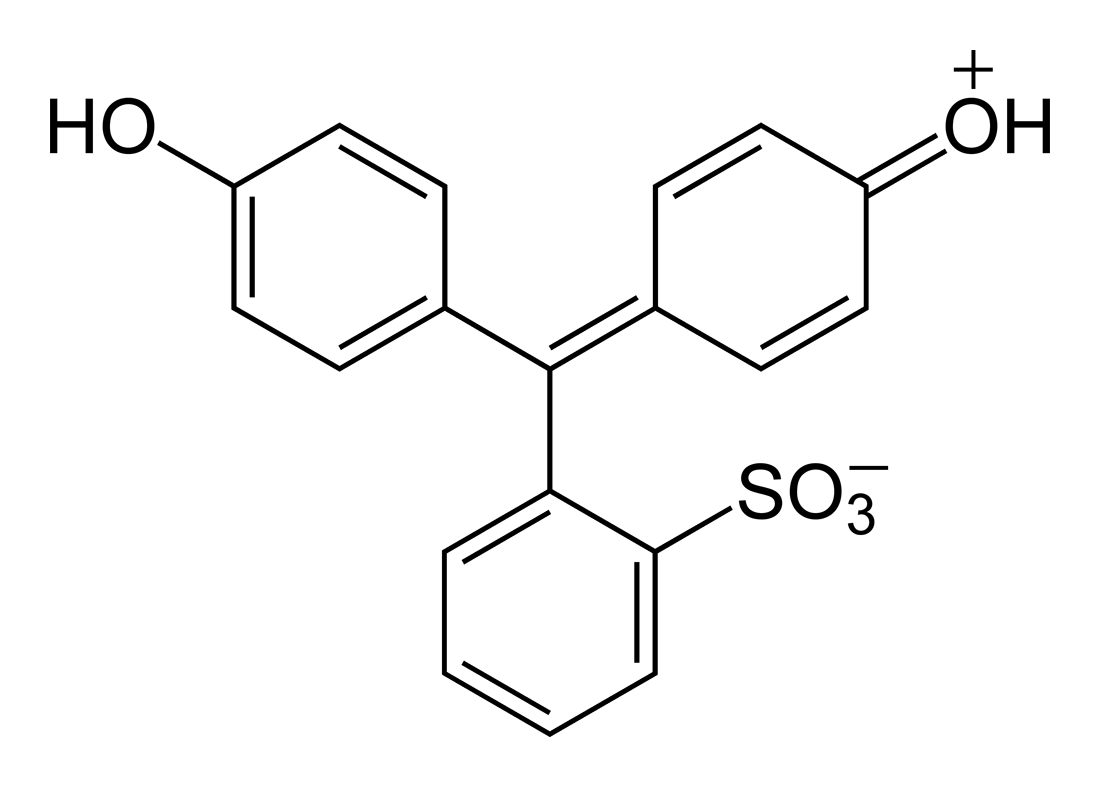
Czerwień fenolowa to wskaźnik zmieniający barwę od żółtej w roztworach obojętnych, do różowo-purpurowej w zasadowych. Jej cząsteczka jest bardzo podobna do zasadowej formy fenoloftaleiny - ten sam układ trifenylowy z dwoma pierścieniami z grupą hydroksylową i jednym z sulfonową.
W warunkach zasadowych następuje odszczepienie obu protonów z grup hydroksylowych i zmiana struktury elektronowej, co skutkuje zmianą barwy. Barwnik dawniej był używany w testach medycznych (tzw. PSP test) do sprawdzania czynności nerek. Po wstrzyknięciu do krwi lub bezpośrednio do tętnicy nerkowej, czerwień fenolowa była wydalana z moczem, co w normalnej sytuacji następowało szybko i w całości. Kolorymetryczne oznaczenie stężenia pozwalało stwierdzić, czy nerki wydalają we właściwy sposób. Obecnie test wyszedł już chyba z użytku.
Odczyn przy którym następuje zmiana barwy, jest zbliżony do normalnego odczynu płynów komórkowych i krwi, stąd dodatek czerwieni fenolowej do hodowli tkankowych pozwala szybko ocenić czy nie dochodzi do zakwaszenia, zwykle z powodu zakażenia bakteryjnego.
Przy okazji zrobiłem też krótki film:
Czerwień fenolowa to wskaźnik zmieniający barwę od żółtej w roztworach obojętnych, do różowo-purpurowej w zasadowych. Jej cząsteczka jest bardzo podobna do zasadowej formy fenoloftaleiny - ten sam układ trifenylowy z dwoma pierścieniami z grupą hydroksylową i jednym z sulfonową.
W warunkach zasadowych następuje odszczepienie obu protonów z grup hydroksylowych i zmiana struktury elektronowej, co skutkuje zmianą barwy. Barwnik dawniej był używany w testach medycznych (tzw. PSP test) do sprawdzania czynności nerek. Po wstrzyknięciu do krwi lub bezpośrednio do tętnicy nerkowej, czerwień fenolowa była wydalana z moczem, co w normalnej sytuacji następowało szybko i w całości. Kolorymetryczne oznaczenie stężenia pozwalało stwierdzić, czy nerki wydalają we właściwy sposób. Obecnie test wyszedł już chyba z użytku.
Odczyn przy którym następuje zmiana barwy, jest zbliżony do normalnego odczynu płynów komórkowych i krwi, stąd dodatek czerwieni fenolowej do hodowli tkankowych pozwala szybko ocenić czy nie dochodzi do zakwaszenia, zwykle z powodu zakażenia bakteryjnego.
Przy okazji zrobiłem też krótki film:
środa, 4 września 2013
Skąd ten zapach?
Każdego kto co nieco liznął na temat mechanizmów odczuwania zapachu, musiało zastanowić jak to się dzieje, że wyraźny i charakterystyczny zapach mają substancje zdecydowanie nielotne, jak żelazo, miedź czy kawałek wapienia.
Zapach żelaza
W znanej powieści "Pachnidło" jedną z pierwszych prób uzyskania nietypowych zapachów otoczenia, jest uzyskanie ekstraktu o zapachu miedzianej gałki u drzwi. Gałka była moczona w chłodnym tłuszczu, z którego po zagęszczaniu uzyskał bohater substancję pachnącą właśnie tak jak metal. Nie jest to ze strony autora taka zupełna fantazja, bo metalowe przedmioty z jakimi się często spotykamy, rzeczywiście mają swój specyficzny, metaliczny zapach, porównywany niekiedy do zapachu zaschniętej krwi. Co takiego jednak pachnie, skoro metal i jego tlenki są nielotne?
Jak można zauważyć, woni takiej nabiera metal używany, często dotykany, nie będzie go miał natomiast dobrze oczyszczony. Zapach ten jest w istocie bardziej związany z nasza skórą. Skóra jest w naturalny sposób natłuszczona za sprawą pracy odpowiednich gruczołów łojowych. Łój jest mieszaniną zawierającą między innymi krótkołańcuchowe nienasycone kwasy tłuszczowe. Kwasy te mają to do siebie, że pod wpływem powietrza i światła łatwo utleniają się do nadtlenków, te z kolei pod wpływem jonów metali na niższych stopniach utlenienia, chętnie redukują się, tworząc rozmaite ketony i alkohole. Wśród nich 1-okten-3-on, związek o silnym, łatwo wyczuwalnym zapachu, choć pewne znaczenie mają też inne ketony. Na powierzchni metalu zawsze obecna jest pewna ilość wolnych jonów, zwłaszcza gdy jest pokryty warstewką zabrudzeń; jony reagują z nadtlenkami i metal zaczyna pachnieć. Aby uzyskać podobny efekt, wystarczy nasmarować dłonie niewielką ilością roztworu żelaza II. Dostarczycielem jonów może być też zaschnięta krew, w czym też naukowcy widzą wytłumaczenie dużego wyczulenia naszych nosów na takie związki.
W przypadku stali i żeliwa, pewne znaczenie mają też zanieczyszczenia metalu. Stal zawiera węgiel oraz domieszki fosforu. W obecności wilgoci cząstki węgla stają się półogniwami z pewnym ładunkiem elektrycznym, na których fosfor może utleniać się do fosforowodoru i organicznych fosfin o nieprzyjemnym zapachu, stąd dodatkowa nuta.[1] Zapach ma też duże znaczenie dla wyczuwania metalicznego smaku - w badaniach z ochotnikami, metaliczny smak wyczuwalny dla soli żelaza znikał po zatkaniu nosa, dla miedzi wyniki były niejednoznaczne.[2] Pewne znaczenie dla smaku metalu ma też powstawanie słabych prądów gdy jeden metal, na przykład kawałek folii aluminiowej, zetknie się z amalgamatową plombą.
Swój własny, nieprzyjemny zapach ma natomiast osm, a to z powodu powstawania na powierzchni lotnego czterotlenku.
Zapach kredy...
Zapach mokrej kredy, bądź świeżego wapienia, jest bardzo charakterystyczny. I smaczny. Trudno dokładnie określić dlaczego, ale często miałoby się ochotę zjeść taki kamień. Jedni opisują go jako "mineralny" inni jako "roślinny" ale spotkałem się też ze stwierdzeniami, że naturalny wapień pachnie jabłkiem i pieczonym chlebem. Moje skojarzenia są raczej synestetyczne, bo kojarzy mi się z wyglądem zmąconej wody, chociaż niedawno jednak stwierdziłem że kreda z kopalni w Mielniku ma miękki zapach mąki.
Niekiedy mówi się, że ochota na zjedzenie kredy, to skutek niedoboru wapnia. Gdyby ta zasada odnosiła się też do innych substancji, musiałbym stwierdzić w swym organizmie przewlekły niedobór czekolady...
Ale właściwie czym pachnie kreda? Kwesta ta nie została chyba zbyt dokładnie zbadana, skoro żadnego "oficjalnego" wyjaśnienia nie znalazłem. Najczęstsze przypuszczenie odnosi się do tego, że zapach ma kreda bądź pyląca się bądź wilgotna. Prawdopodobnie podczas wysychania tworzą się drobne cząstki, które dostając się do nosa wywołują odczuwane wrażenie.
Dlaczego jednak te drobne cząstki miałyby wywoływać takie nietypowe wrażenia? Sama alkalizacja czy obecność węglanów nie wystarczy, skoro soda oczyszczona nie ma takiej woni, zapewne więc znaczenie ma tutaj wapń. Pierwiastek ten jest ważny dla utrzymania równowagi elektrycznej komórek nerwowych, w tym komórek węchowych. W normalnym przypadku poburzenie receptorów na powierzchni komórki węchowej, powoduje napływ do jej wnętrza jonów wapnia i odpływ jonów chlorkowych; powstająca zmiana potencjału tworzy sygnał przekazywany przez nerw. Mogę zatem domniemywać że dostarczenie wapnia bez jonów chlorkowych na powierzchnię z komórkami węchowymi w jakiś sposób zmienia bądź inicjuje ten proces, przez co mózg odczuwa jakby mieszankę wszystkich zapachów. Myślę że byłby to ciekawy temat badań dla jakiegoś biochemika.
... i innych minerałów
Własny, specyficzny zapach posiadać mogą też inne minerały. Siarka rodzima ma charakterystyczny zapach, szczególnie silny przy pocieraniu, biorący się po trosze z oparów siarki jak i z jej tlenków. Podobnie pachnieć mogą minerały siarczkowe jak piryt, co też jest związane z powolnym utlenianiem, w jakimś stopniu może też z powodu wydzielania siarkowodoru. Minerały arsenu, jak arsenopiryt, mają dla odmiany czosnkowy zapach powstający przy rozdrabnianiu i kruszeniu - chętnie wówczas iskrzą - wywołany arsenowodorem i siarczkiem arsenu. Łupki bitumiczne i pewne odmiany wapieni zawierających domieszki substancji organicznych, przy rozłupywaniu dają niemiły zapach siarkowodoru, skąd też doczekały się nazwy śmierdząca kreda (Stinkstone).
Wśród minerałów szczególnym przypadkiem jest Anozonit - minerał fluoru. Zapach jaki wydziela jest ostry i niezupełnie przyjemny; bywa porównywany do zapachu ozonu albo przepalonej elektroniki. Wiadomo że jest to fluoryt, który utworzył się w pobliżu promieniotwórczych skał, których oddziaływanie zaburzyło jego sieć krystaliczną. Przez długi czas sądzono, że zapach jest wynikiem wybijania przez promieniowanie fluoru, który natychmiast reagował z powietrzem w porach minerału, tworząc ostro pachnący fluorek tlenu i ślady ozonu - niedawno jednak odkryto, że przyczyna jest jeszcze bardziej interesująca.
Fluor jest pierwiastkiem tak ogromnie reaktywnym, że Moissan chcąc go po raz pierwszy wyodrębnić, musiał użyć aparatury wykonanej z platyny, bo ze szkłem reagował bardzo szybko. W mieszaninie z powietrzem bardzo chętnie przechodzi w fluorki tlenu i azotu, reaguje z wodą. Dla wszystkich jest więc oczywiste, że nie występuje w naturze w stanie rodzimym. Albo może inaczej - dotychczas dla wszystkich był to fakt najzupełniej oczywisty. Jednak badania jakim poddał anozonit Florian Kraus, powinny zmienić tą opinię.
Postanowił on sprawdzić dawne teorie przyczyn zapachu tego minerału, ale w sposób nie niszczący - rozkruszenie wystawia wnętrze na działanie wilgoci. Dlatego też zbadał kilka kryształków za pomocą spektrometrii magnetycznego rezonansu jądrowego NMR. Ponieważ jądra atomów fluoru posiadają spin i moment magnetyczny, ich sygnały mogą być obserwowane w ten sposób. Wyniki badania pokazały jednoznacznie, że obserwowany sygnał pochodzi od wolnego, cząsteczkowego fluoru, zamkniętego w mikroporach minerału[3]
To zatem co czuć od kryształków, to mieszanka zapachów fluoru, fluorku tlenu i ozonu. Ciekawe swoją drogą co by przyniosło zbadanie pewnej odmiany halitu, która a sprawą bliskości promieniotwórczych minerałów przybrała fioletowawy kolor - efekt taki może dawać stały koloid sodu.
Zapach karbidu
Każdy kto zetknął się z karbidem pewnie zauważył też niemiły zapach tej substancji. Nie każdy jednak zastanowił się, że bezwonny jest zarówno powstający w reakcji acetylen jak i wodorotlenek wapnia.
-------

* http://www.mindat.org/forum.php?read,6,284681,284731
[1] Glindemann D, Dietrich A, Staerk HJ, & Kuschk P (2006). The two odors of iron when touched or pickled: (skin) carbonyl compounds and organophosphines. Angewandte Chemie (International ed. in English), 45 (42), 7006-9 PMID: 17009284
[2] Harry T. Lawless, Serena Schlake, John Smythe, Juyun Lim, Heidi Yang, Kathryn Chapman and Bryson Bolton (2004). Metallic Taste and Retronasal Smell Chem. Senses, 29 (1) DOI: 10.1093/chemse/bjh003
[3] http://www.nature.com/news/stinky-rocks-hide-earth-s-only-haven-for-natural-fluorine-1.10992
Zapach żelaza
W znanej powieści "Pachnidło" jedną z pierwszych prób uzyskania nietypowych zapachów otoczenia, jest uzyskanie ekstraktu o zapachu miedzianej gałki u drzwi. Gałka była moczona w chłodnym tłuszczu, z którego po zagęszczaniu uzyskał bohater substancję pachnącą właśnie tak jak metal. Nie jest to ze strony autora taka zupełna fantazja, bo metalowe przedmioty z jakimi się często spotykamy, rzeczywiście mają swój specyficzny, metaliczny zapach, porównywany niekiedy do zapachu zaschniętej krwi. Co takiego jednak pachnie, skoro metal i jego tlenki są nielotne?
Jak można zauważyć, woni takiej nabiera metal używany, często dotykany, nie będzie go miał natomiast dobrze oczyszczony. Zapach ten jest w istocie bardziej związany z nasza skórą. Skóra jest w naturalny sposób natłuszczona za sprawą pracy odpowiednich gruczołów łojowych. Łój jest mieszaniną zawierającą między innymi krótkołańcuchowe nienasycone kwasy tłuszczowe. Kwasy te mają to do siebie, że pod wpływem powietrza i światła łatwo utleniają się do nadtlenków, te z kolei pod wpływem jonów metali na niższych stopniach utlenienia, chętnie redukują się, tworząc rozmaite ketony i alkohole. Wśród nich 1-okten-3-on, związek o silnym, łatwo wyczuwalnym zapachu, choć pewne znaczenie mają też inne ketony. Na powierzchni metalu zawsze obecna jest pewna ilość wolnych jonów, zwłaszcza gdy jest pokryty warstewką zabrudzeń; jony reagują z nadtlenkami i metal zaczyna pachnieć. Aby uzyskać podobny efekt, wystarczy nasmarować dłonie niewielką ilością roztworu żelaza II. Dostarczycielem jonów może być też zaschnięta krew, w czym też naukowcy widzą wytłumaczenie dużego wyczulenia naszych nosów na takie związki.
W przypadku stali i żeliwa, pewne znaczenie mają też zanieczyszczenia metalu. Stal zawiera węgiel oraz domieszki fosforu. W obecności wilgoci cząstki węgla stają się półogniwami z pewnym ładunkiem elektrycznym, na których fosfor może utleniać się do fosforowodoru i organicznych fosfin o nieprzyjemnym zapachu, stąd dodatkowa nuta.[1] Zapach ma też duże znaczenie dla wyczuwania metalicznego smaku - w badaniach z ochotnikami, metaliczny smak wyczuwalny dla soli żelaza znikał po zatkaniu nosa, dla miedzi wyniki były niejednoznaczne.[2] Pewne znaczenie dla smaku metalu ma też powstawanie słabych prądów gdy jeden metal, na przykład kawałek folii aluminiowej, zetknie się z amalgamatową plombą.
Swój własny, nieprzyjemny zapach ma natomiast osm, a to z powodu powstawania na powierzchni lotnego czterotlenku.
Zapach kredy...
Zapach mokrej kredy, bądź świeżego wapienia, jest bardzo charakterystyczny. I smaczny. Trudno dokładnie określić dlaczego, ale często miałoby się ochotę zjeść taki kamień. Jedni opisują go jako "mineralny" inni jako "roślinny" ale spotkałem się też ze stwierdzeniami, że naturalny wapień pachnie jabłkiem i pieczonym chlebem. Moje skojarzenia są raczej synestetyczne, bo kojarzy mi się z wyglądem zmąconej wody, chociaż niedawno jednak stwierdziłem że kreda z kopalni w Mielniku ma miękki zapach mąki.
Niekiedy mówi się, że ochota na zjedzenie kredy, to skutek niedoboru wapnia. Gdyby ta zasada odnosiła się też do innych substancji, musiałbym stwierdzić w swym organizmie przewlekły niedobór czekolady...
Ale właściwie czym pachnie kreda? Kwesta ta nie została chyba zbyt dokładnie zbadana, skoro żadnego "oficjalnego" wyjaśnienia nie znalazłem. Najczęstsze przypuszczenie odnosi się do tego, że zapach ma kreda bądź pyląca się bądź wilgotna. Prawdopodobnie podczas wysychania tworzą się drobne cząstki, które dostając się do nosa wywołują odczuwane wrażenie.
Dlaczego jednak te drobne cząstki miałyby wywoływać takie nietypowe wrażenia? Sama alkalizacja czy obecność węglanów nie wystarczy, skoro soda oczyszczona nie ma takiej woni, zapewne więc znaczenie ma tutaj wapń. Pierwiastek ten jest ważny dla utrzymania równowagi elektrycznej komórek nerwowych, w tym komórek węchowych. W normalnym przypadku poburzenie receptorów na powierzchni komórki węchowej, powoduje napływ do jej wnętrza jonów wapnia i odpływ jonów chlorkowych; powstająca zmiana potencjału tworzy sygnał przekazywany przez nerw. Mogę zatem domniemywać że dostarczenie wapnia bez jonów chlorkowych na powierzchnię z komórkami węchowymi w jakiś sposób zmienia bądź inicjuje ten proces, przez co mózg odczuwa jakby mieszankę wszystkich zapachów. Myślę że byłby to ciekawy temat badań dla jakiegoś biochemika.
... i innych minerałów
Własny, specyficzny zapach posiadać mogą też inne minerały. Siarka rodzima ma charakterystyczny zapach, szczególnie silny przy pocieraniu, biorący się po trosze z oparów siarki jak i z jej tlenków. Podobnie pachnieć mogą minerały siarczkowe jak piryt, co też jest związane z powolnym utlenianiem, w jakimś stopniu może też z powodu wydzielania siarkowodoru. Minerały arsenu, jak arsenopiryt, mają dla odmiany czosnkowy zapach powstający przy rozdrabnianiu i kruszeniu - chętnie wówczas iskrzą - wywołany arsenowodorem i siarczkiem arsenu. Łupki bitumiczne i pewne odmiany wapieni zawierających domieszki substancji organicznych, przy rozłupywaniu dają niemiły zapach siarkowodoru, skąd też doczekały się nazwy śmierdząca kreda (Stinkstone).
Wśród minerałów szczególnym przypadkiem jest Anozonit - minerał fluoru. Zapach jaki wydziela jest ostry i niezupełnie przyjemny; bywa porównywany do zapachu ozonu albo przepalonej elektroniki. Wiadomo że jest to fluoryt, który utworzył się w pobliżu promieniotwórczych skał, których oddziaływanie zaburzyło jego sieć krystaliczną. Przez długi czas sądzono, że zapach jest wynikiem wybijania przez promieniowanie fluoru, który natychmiast reagował z powietrzem w porach minerału, tworząc ostro pachnący fluorek tlenu i ślady ozonu - niedawno jednak odkryto, że przyczyna jest jeszcze bardziej interesująca.
Fluor jest pierwiastkiem tak ogromnie reaktywnym, że Moissan chcąc go po raz pierwszy wyodrębnić, musiał użyć aparatury wykonanej z platyny, bo ze szkłem reagował bardzo szybko. W mieszaninie z powietrzem bardzo chętnie przechodzi w fluorki tlenu i azotu, reaguje z wodą. Dla wszystkich jest więc oczywiste, że nie występuje w naturze w stanie rodzimym. Albo może inaczej - dotychczas dla wszystkich był to fakt najzupełniej oczywisty. Jednak badania jakim poddał anozonit Florian Kraus, powinny zmienić tą opinię.
Postanowił on sprawdzić dawne teorie przyczyn zapachu tego minerału, ale w sposób nie niszczący - rozkruszenie wystawia wnętrze na działanie wilgoci. Dlatego też zbadał kilka kryształków za pomocą spektrometrii magnetycznego rezonansu jądrowego NMR. Ponieważ jądra atomów fluoru posiadają spin i moment magnetyczny, ich sygnały mogą być obserwowane w ten sposób. Wyniki badania pokazały jednoznacznie, że obserwowany sygnał pochodzi od wolnego, cząsteczkowego fluoru, zamkniętego w mikroporach minerału[3]
To zatem co czuć od kryształków, to mieszanka zapachów fluoru, fluorku tlenu i ozonu. Ciekawe swoją drogą co by przyniosło zbadanie pewnej odmiany halitu, która a sprawą bliskości promieniotwórczych minerałów przybrała fioletowawy kolor - efekt taki może dawać stały koloid sodu.
Zapach karbidu
Każdy kto zetknął się z karbidem pewnie zauważył też niemiły zapach tej substancji. Nie każdy jednak zastanowił się, że bezwonny jest zarówno powstający w reakcji acetylen jak i wodorotlenek wapnia.
CaC2 + 2H2O → Ca(OH)2 + C2H2
W tym przypadku sprawa jest łatwa do wyjaśnienia - karbid wytwarza się prażąc wapień z węglem. Wapień naturalny zawiera domieszki innych niż węglan soli wapnia, a więc siarczanu i fosforanu, które po zredukowaniu zamieniają się w siarczek i fosforek wapnia. Te podczas reakcji z wodą wydzielają siarkowodór i związki fosforowodorowe (głównie difosfina, sam fosforowodór jest bezwonny), pierwszy o zapachu zgniłych jaj a drugie o zapachu zepsutego czosnku.-------
* http://www.mindat.org/forum.php?read,6,284681,284731
[1] Glindemann D, Dietrich A, Staerk HJ, & Kuschk P (2006). The two odors of iron when touched or pickled: (skin) carbonyl compounds and organophosphines. Angewandte Chemie (International ed. in English), 45 (42), 7006-9 PMID: 17009284
[2] Harry T. Lawless, Serena Schlake, John Smythe, Juyun Lim, Heidi Yang, Kathryn Chapman and Bryson Bolton (2004). Metallic Taste and Retronasal Smell Chem. Senses, 29 (1) DOI: 10.1093/chemse/bjh003
[3] http://www.nature.com/news/stinky-rocks-hide-earth-s-only-haven-for-natural-fluorine-1.10992
Subskrybuj:
Komentarze (Atom)