Jednym z prostych pomiarów fizykochemicznych, które być może były omawiane w szkołach, jest pomiar skręcalności optycznej substancji. Podobny wykonuję też i ja na pracowni, ale sprzętem nieco dokładniejszym. Tylko po co to wszystko?
U początków wielkiej naukowej debaty o prawdziwej naturze światła zwrócono uwagę na zjawisko polaryzacji. Przezroczyste kryształy szpatu islandzkiego podwajały obraz jaki przez nie obserwowano, a wpuszczony w nie promień światła rozdzielał się na dwa - normalny, biegnący zgodnie z wartością załamania, i nadzwyczajny o silniejszym załamaniu.
Jeszcze zaś dziwaczniej zachowywały się dwa takie kryształy położone na sobie - w pewnej wzajemnej orientacji pozostawały przezroczyste, po obróceniu o 90 stopni wygaszały obraz. Zjawisko to nazwano polaryzacją i niespecjalnie się nim potem przejmowano, gdy tymczasem trwał spór między fizykami - czy światło to promień czy może wiązka przenikliwych cząstek? Istniało wiele zjawisk które udawało się łatwo wytłumaczyć modelem cząstkowym i on w zasadzie był powszechnie przyjmowany aż do 1801, gdy Thomas Young zaproponował doświadczenie z dwoma szczelinami.
Weźmy źródło światła i ujednolićmy je przepuszczając przez mały otwór. Teraz przepuśćmy nasze spójne światło przez dwa małe otworki, wielkości nakłuć końcem igły, położone blisko siebie. Zgodnie z teorią cząstkowa, powinniśmy zobaczyć dwie jasne plamki. Zamiast tego obserwowano jasną plamę pośrodku i rząd rozchodzących się po bokach mniejszych, kolorowych plamek oddzielonych plamami cienia. W sposób cząstkowy wyjaśnić się tego nie dało. Chyba że światło jest jednak falą:
Dwie szczeliny tworzą dwa źródła rozchodzących się fal, które nakładają się na siebie raz wzmacniając raz wygaszając. Young zainspirował się tu obserwacją fal na powierzchni wody, przy czym z występowania tego zjawiska wynikało, że jeśli już światło faluje, to poprzecznie do kierunku ruchu.
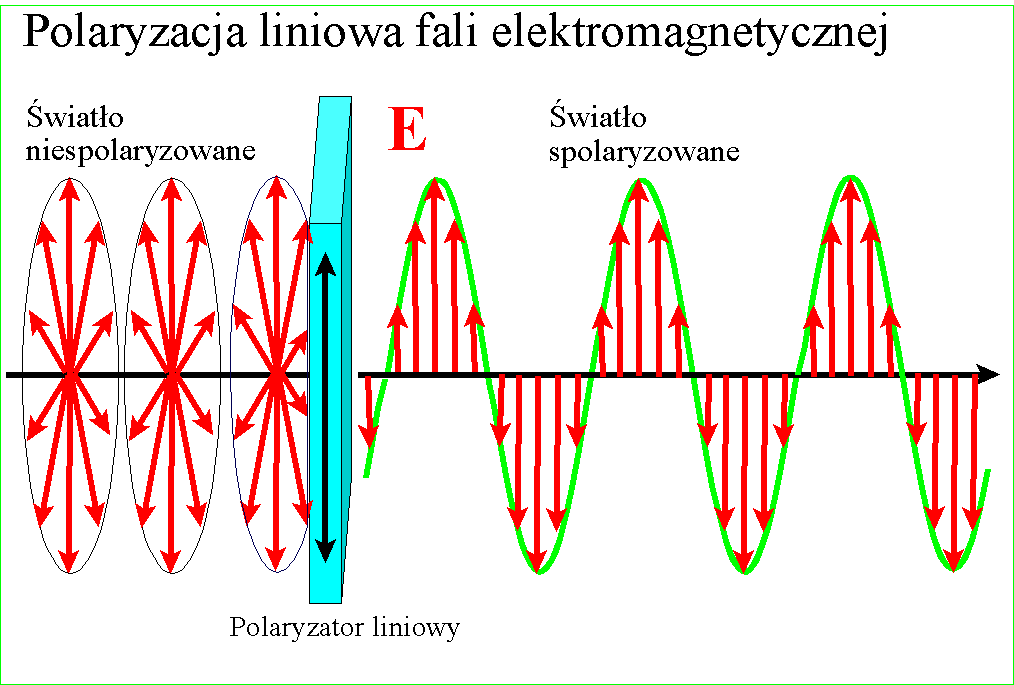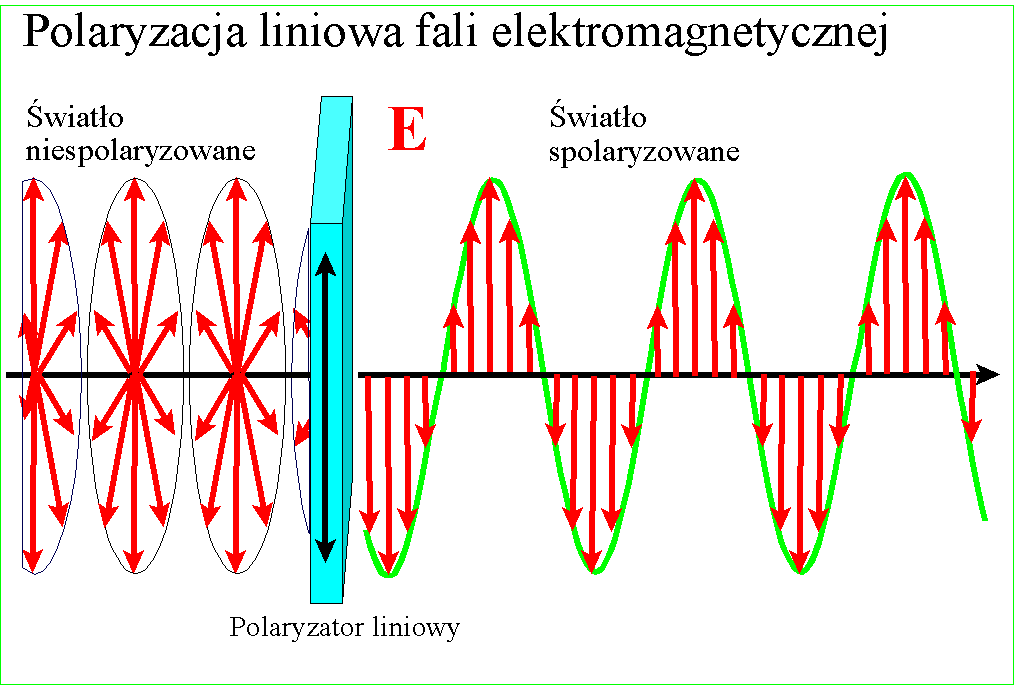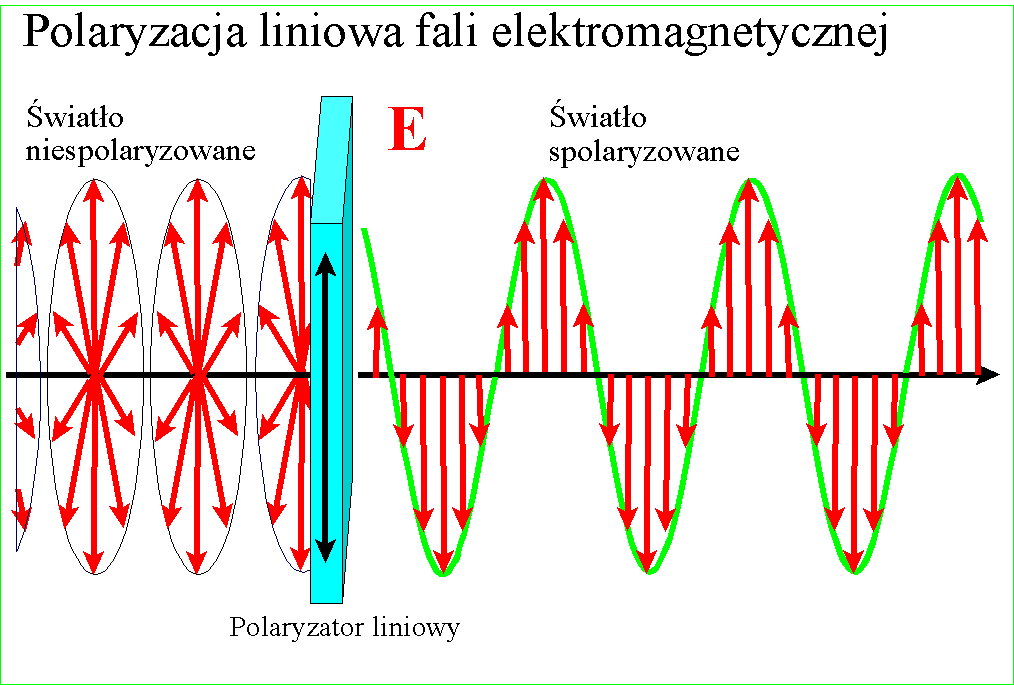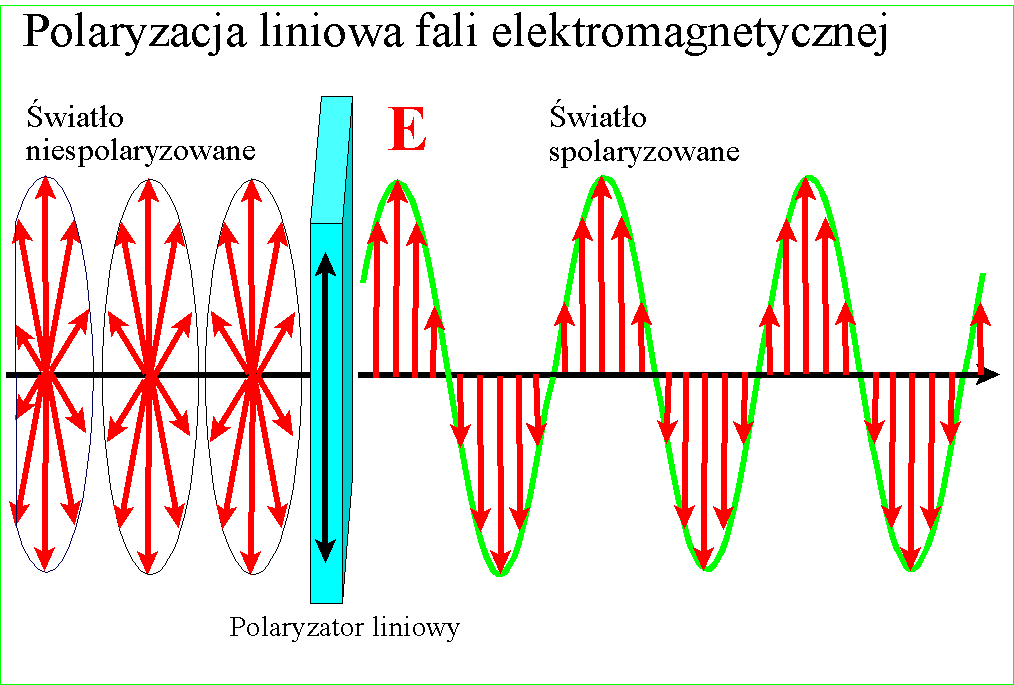
Późniejsza teoria powiązała światło z zaburzeniami w rozprzestrzeniającym się polu elektrycznym i magnetycznym. Pole magnetyczne które zmienia natężenie i kierunek powoduje wygenerowane pola elektrycznego, ale także o zmiennym kierunku. Zmienne pole elektryczne z kolei generuje zmienne pole magnetyczne. Te dwa wzajemnie się indukujące pola łączą się ze sobą tworząc promieniowanie elektro-magnetyczne. Wektor pola magnetycznego jest prostopadły do wektora pola elektrycznego a obydwa do kierunku rozchodzenia się promieni.:
Późniejsza teoria kwantowa zmodyfikowała ten model, wprowadzając podwójną falowo-cząstkowa naturę światła.
W każdym razie gdy Young udowodnił falową naturę światła, znane wcześniej zjawisko polaryzacji stało się zrozumiałe - po postu wektory pól zajmują w przestrzeni jakieś płaszczyzny względem kierunku rozchodzenia, ale w świetle zwykłym są one przemieszane. Gdy światło zostanie spolaryzowane, kierunki te porządkują się :
i wszystkie wektory spolaryzowanego światła leżą w jednej płaszczyźnie. Wyjaśnienie dwójłomności szpatu islandzkiego, powodującej podwojenie obrazu jest w tym kontekście ciekawe - prędkość światła w takim krysztale zależy od kierunku polaryzacji pól składowych. Różnica prędkości światła między kryształem a powietrzem jest przyczyną załamania światła, zatem zależnie od polaryzacji światło będzie się załamywało pod różnym kątem
Gdy wpuścimy do kryształu promień, zostanie on rozdzielony na dwa o połowę słabsze - jeden, normalny, będzie miał jedną polaryzację, a drugi, nadzwyczajny, polaryzację obróconą pod kątem prostym do polaryzacji tamtego. Każdy z promieni ma nieco inny kąt załamania dlatego oddzielają się od siebie:
Niedługo potem Malus odkrył że światło częściowo polaryzuje się przy odbiciu, zaś William Nicol wpadł na pomysł, jak za pomocą dwójłomnego kryształu uzyskać pojedynczą wiązkę spolaryzowanego światła. Wziął on rombowy kryształ szpatu islandzkiego i przeciął na ukos, otrzymując dwa pryzmaty. Połączył je ze sobą cienką warstwą przezroczystego kleju. Wiadomo było wówczas, że promień biegnący wewnątrz przezroczystego materiału może zostać całkowicie odbity, jeśli padnie na jego ścianę pod odpowiednim kątem - z tego prawa korzystają światłowody - połączenie tego z dwójłomnością pozwoliło na oddzielenie powstających dwóch promieni.
Cięcie między dwoma pryzmatami zostało poprowadzone pod takim kątem, że niewiele brakuje aby promień biegnący przez kryształ odbił się całkowicie. Wpuszczamy w kryształ promień zwykłego światła - promień rozdziela się na dwa załamane pod różnym kątem. Mniej załamany normalny biegnie dalej, silniej załamany promień nadzwyczajny odbija się całkowicie i wypada bokiem. Przechodząca wiązka zostaje spolaryzowana.
Dzięki temu urządzeniu można było badać właściwości światła spolaryzowanego, na przykład zabarwianie się minerałów i tworzyw sztucznych wykazujących choć niewielką dwójłomność.
Tym jednak co najbardziej mnie interesuje, jest odkrycie, że po przejściu przez pewne substancje, polaryzacja światła może się zmienić. Aby wygasić całkowicie liniowo spolaryzowane światło, należy umieścić na jego drodze filtr bądź drugi układ pryzmatów, ale obrócony o 90 stopni. Jednak jeśli między nie wsuniemy próbkę jakiejś substancji, jak na przykład roztwór cukru, okaże się że światło już nie jest całkowicie pochłaniane, i aby znów uzyskać ten efekt trzeba obrócić układ o jeszcze pewien kąt.
Zdolność do zmiany płaszczyzny polaryzacji światła to skręcalność optyczna, a substancje które tak robią nazywany czynnymi optycznie. Czynność ta jest związana z budową cząsteczki o asymetrii polaryzacji a co za tym idzie, asymetrią budowy. W związkach organicznych możliwa jest sytuacja, że cząsteczka może posiadać dwie formy przestrzenne, podobne do siebie jak lustrzane odbicia. Są to cząsteczki chiralne. Szersze wytłumaczenie jak to zachodzi i jakie ma znaczenie, już omawiałem w pewnym artykule.
Gdy światło spolaryzowane przejdzie przez roztwór substancji czynnej optycznie, płaszczyzna w której sytuują się wektory fali elektromagnetycznej, przekręci się o pewien kąt. Ilościowa zdolność do skręcania płaszczyzny to skręcalność, zależna od grubości roztworu, rozpuszczalnika, długości fali świetlnej i stężenia.
Własności te znalazły bardzo szerokie zastosowanie do szybkiego mierzenia zawartości cukru w sokach roślinnych. I takie też ćwiczenie wykonywałem kiedyś na pracowni jeszcze w technikum.
Wzięliśmy jabłko, z którego odważyliśmy określoną ilość miąższu, a ten po rozgnieceniu zalaliśmy odmierzoną ilością wody i zagotowaliśmy:
Po odsączeniu wyciągu wlaliśmy go do polarymetru widocznym na pierwszej fotografii - to bardzo proste urządzenie. Lampa sodowa daje intensywne światło o określonej długości fali, wpadające do urządzenia przez wstępny filtr polaryzacyjny. Następnie przechodzi przez szklaną rurkę w tubie przyrządu gdzie wlany został nasz sok. Na jego drodze staje następnie prostokąt drugiego filtru polaryzacyjnego, o polaryzacji takiej samej jak pierwszy. Gdy w urządzeniu była nieaktywna woda, w okularze widać było jednolity krążek światła:
Jednak zawierający czynne optycznie cukry sok jabłkowy skręcał płaszczyznę światła spolaryzowanego przez pierwszy filtr. Takie światło było więc częściowo zatrzymywane przez drugi filtr i na tle jasnego krążka pojawiał się ciemniejszy prostokąt:
Teraz należało przekręcić małą tarczę przy okularze tak, aby obrócić drugi filtr zgodnie z polaryzacją o pewien kąt. Ten kąt to właśnie skręcalność roztworu. Z boku obiektywu przez małą lupę można było obserwować skalę podającą z jednej strony kąt skręcenia a z drugiej stężenie cukru w roztworze.
Podobne pomiary wykonuję czasem na pracowni. Zasadniczy temat pracy magisterskiej polega na wytworzeniu ligandów do asymetrycznej reakcji Henry'ego. W takiej reakcji powinienem otrzymać mieszaninę chiralnych beta nitroalkoholi z przewagą jednej, pożądanej formy
Ale jak poznać z jak dużą przewagą? Każda forma skręca płaszczyznę polaryzacji światła o taką samą wartość ale w przeciwne strony. Mieszanina 1:1 jest wobec tego nie czynna, zaś każda przewaga którejś z form objawia się jakąś skręcalnością wypadkową. Mając porównanie z danymi literaturowymi, gdzie obie formy oddzielono i ustalono konfigurację, i gdzie podana została skręcalność mieszaniny o ustalonym stosunku, mogę przez własny pomiar w identycznych warunkach określić skład swojej otrzymanej mieszaniny wyrażony w jednostce nadmiaru enancjomerycznego - czyli procentowej nadwyżki jednej z form nad drugą.
Jak na razie najlepszy wynik jednej reakcji to nadmiar 88% ee, ale czekam na więcej.
ps. to mój 150 opublikowany wpis.
informacje
czwartek, 13 lutego 2014
piątek, 24 stycznia 2014
Ostatnio w laboratorium (37.)
W postępach syntetycznych dotarłem już do trzeciego z pięciu zaplanowanych ligandów, zawierającego grupę izopropylową przy pierścieniu oksazolinowym. Problemy z oczyszczeniem powodowały jednak, że otrzymałem niespełna 20 mg związku, więc będę musiał chyba powtórzyć reakcję. Oprócz widma NMR mogłem z tak małą ilością zbadać jeszcze temperaturę topnienia. Przy okazji sfotografowałem drobne kryształki związku:
Topiły się w 159 stopniach. A oto wysumulowany kształt cząsteczki:
Topiły się w 159 stopniach. A oto wysumulowany kształt cząsteczki:
niedziela, 19 stycznia 2014
Środki osuszające
Zimą, zamknięci w uszczelnionych przed chłodem mieszkaniach, susząc pranie na rozgrzanych kaloryferach doświadczamy niekiedy warunków iście tropikalnych, gdy nasycona wilgocią atmosfera nie pozwala schładzać się ciału. Wtedy też widzimy wilgoć spływającą z chłodnych okien i marszczące się papierowe gazety. I być może przypominamy sobie wówczas reklamy osuszaczy powietrza, które w jakiś magiczny sposób mają wyssać z powietrza wilgoć.
W jaki sposób? W sposób fizyko-chemiczny...
Skłonność substancji do wchłaniania wody obecnej w powietrzu nazywamy higroskopijnością. Aby proces taki mógł zachodzić, między wodą a materiałem wchłaniającym powinny zachodzić odpowiednio silne oddziaływania. Bardzo hydrofobowy polietylen w zasadzie nie wchłania wilgoci, zaś hydrofilowa celuloza czyni to chętnie. Sam proces chłonięcia wody odbywa się na dwa sposoby - przez osadzanie wody na powierzchni, czyli adsorpcję, albo poprzez wchłanianie do wewnątrz struktury materiału.
Głównym oddziaływaniem mającym wpływ na zdolność osuszająca materiału, są wiązania wodorowe, rozpięte między atomem posiadającego wolne pary elektronowe niemetalu w jednej cząsteczce a wodorem w drugiej. Są to dosyć luźne połączenia, raczej przyciąganie elektrostatyczne niż prawdziwe wiązania, jednak występują często i licznie, wpływając na kształt dużych cząsteczek i właściwości fizyczne substancji. Przykładem może być woda w której każda cząsteczka może tworzyć takie wiązania z trzema innymi. Co prawda ruchy termiczne już w temperaturze pokojowej na tyle silnie miotają cząstkami, że wiązania co chwila rozrywają się i tworzą na nowo, ale sumą ich efemerycznego istnienia jest istotne zwiększenie temperatury wrzenia i krzepnięcia - bez nich tlenek wodoru byłby gazem o temperaturze skraplania poniżej -50 stopni.
Jeśli stały materiał zawiera na swej powierzchni grupy z silnie elektroujemnym niemetalem o wolnych parach elektronowych, to cząsteczka wody z powietrza może zostać z nim związana. Takimi materiałami będzie na przykład celuloza lub cukier, mające w strukturze wiele grup hydroksylowych. Między tlenem takiej grupy a wodorem cząsteczki wody powstaje wiązanie. Możliwe jest też wiązanie między wodorem grupy hydroksylowej a tlenem cząsteczki wody. W podobny sposób wodę chłoną białka, gdzie mamy pod dostatkiem atomów elektroujemnych (azot, tlen).
W przypadku naturalnych włókien, ilość pochłoniętej wilgoci wpływa na ich długość - włókno nawodnione rozciąga się a wysuszone kurczy. Praktycznie wykorzystano tą własność w "domkach pogodowych" gdzie włos lub nić bawełniana owinięty wokół osi, rozciągając się lub skracając przy różnej wilgotności powietrza powoduje, że raz z domku wysuwa się figurka kobiety a raz mężczyzny z parasolem.
Nieco inny jest mechanizm wchłaniania wody przez sole nieorganiczne i materiały ceramiczne. Sól taka składa się z anionów reszty kwasowej i kationów metalu. Każdy jon wytwarza wokół siebie niewielkie pole elektryczne, do którego przyciągane są cząsteczki wody o właściwościach dipola. Zależnie od wielkości i tego na ile jest osłonięty przez inne atomy, jon przyciągnie w ten sposób od jednej do sześciu cząsteczek wody. W taki sposób zwykle rozpoczyna się rozpuszczanie soli w wodzie, tu jednak powstaje jedynie jednocząsteczkowa warstwa na samej powierzchni
Ten powierzchniowy sposób nie ma zwykle wpływu na strukturę materiału, chyba że cząsteczki wody utworzą z jonami dużo trwalszą strukturę - hydrat.
W hydracie cząsteczki wody stają się części sieci krystalicznej. Kationy metali chętnie bowiem tworzą z wodą akwakompleksy, a więc związki z przeniesieniem elektronów tlenu na puste powłoki metalu. Powstający wówczas jon kompleksowy może być bardzo trwały. Aniony z kolei mogą wiązać wodę bądź elektrostatycznie, bądź przez wiązania wodorowe jeśli są resztami kwasów tlenowych.
Hydratacja soli często zmienia jej właściwości - bezwodny siarczan miedzi jest sypkim, białym proszkiem; po nawodnieniu staje się intensywnie niebieski za sprawą powstającego jonu kompleksowego Cu[(H2O)4]2+ , piątą cząsteczkę wody wiąże reszta siarczanowa poprzez wiązanie wodorowe, stąd pełny wzór hydratu CuSO4 X 5 H2O.
Wyjątkowo dużo wody może związać krystalicznie siarczan sodu, nazywany solą glauberską. Uwodnione kryształy zwierają 10 cząsteczek wody na jeden ekwiwalent związku, co stanowi więcej niż 50% masy. Sześć cząsteczek wiąże w mało trwałym kompleksie kation sodowy, dwie wiąże reszta siarczanowa zaś dwie kolejne zawierają się w pustych przestrzeniach sieci. Podobny związek w formie przezroczystych kryształów daje węglan sodu. Bezwodny chlorek kobaltu jest intensywnie niebieski (zabarwia się nim emalię), uwodniony staje się różowy.
Małe i silnie naładowane jony na powierzchni kryształu nie tylko przyciągają kilka cząsteczek wody, ale też często ich oddziaływanie jest nadal wystarczające aby do tej warstewki dołączać kolejne, przez co materiał pokrywa się warstwą wody w której może zachodzić rozpuszczanie. Takim jonem jest jon wodorotlenkowy, w efekcie rozpuszczalne wodorotlenki jak sodu czy potasu, pozostawione na powietrzu rozpływają się w gęsty roztwór.
Wreszcie w przypadku materiałów porowatych pewną rolę pełni też kondensacja kapilarna
Osuszacze
Jak wobec powyższego działają komercyjne osuszacze powietrza?
Część urządzeń opiera się na wykraplaniu wilgoci na elemencie chłodzącym, są to urządzenia potrzebujące prądu, ja jednak zajmę się tymi bezprądowymi, opartymi na higroskopii.
Typ jaki najczęściej spotykam to prosty pojemnik z podziurkowanym wieczkiem, do którego wsypuje się granulki, te po pewnym czasie rozpływają się zaś ilość roztworu zwiększa się do pewnego poziomu. Takie osuszacze bazują na pochłanianiu wody przez sole nieorganiczne, najczęściej przez suchy chlorek wapnia.
Związek ten chłonie wodę zamieniając się w hydrat, wiążąc w formie krystalicznej do sześciu cząsteczek wody na jeden równoważnik związku. Hydrat ten jest jednak nadal higroskopijny, chłonąc wodę na powierzchni ziaren tak silnie, że zaczyna rozpływać się "we własnym sosie" tworząc roztwór.
Gdy grudki się rozpłyną, w pojemniku tworzy się syropowata ciecz, zaś w pochłanianiu wilgoci przeważać zaczyna inne niż wyżej opisane zjawisko fizyczne - mianowicie równowaga między parą nasyconą a roztworem. Gdy umieścimy w pojemniku lotną ciecz, zacznie ona parować aż do momentu gdy gazowa część zbiornika osiągnie stan nasycenia. W takim stanie para pozostaje w równowadze z cieczą, co oznacza, że tyle samo cieczy paruje co pozostaje wchłonięte przez roztwór. Jeśli nasz pojemnik nie będzie szczelny, para będzie uciekała i nie osiągnie nasycenia, zaś lotna ciecz powolutku wyschnie.
Zamknięte mieszkanie może być potraktowane jak taki pojemnik, w którym znajdują się źródła pary wodnej. Jej stężenie w powietrzu zmienia się, czasem wzrastając tak bardzo że skrapla się na chłodnych przedmiotach, zazwyczaj jednak jedynie powodując wilgotnienie materiałów za sprawą ich higroskopijności.
W zasadzie dopóki w mieszkaniu nie zapanują tropikalne warunki pełnego nasycenia parą wodną, równowaga między cieczą a parą nie jest zachowana i woda pozostawiona w szklance powoli paruje.
Inaczej będzie gdy w takim wilgotnym mieszkaniu postawimy roztwór zawierający dużo soli.
Sól niejako "rozcieńcza" wodę.
Gdy rozpatrzymy to sobie mikroskopowo, parowanie następuje gdy w granicę faz uderzy cząsteczka o wystarczającej energii. Jeśli teraz rozprowadzimy w wodzie sól, jej cząsteczki zajmą miejsce niektórych cząsteczek wody. Zatem, znów mikroskopowo patrząc, w granicą faz od dołu uderza mniejsza ilość cząsteczek, przez co roztwór jest mniej lotny (ma niższą prężność par).
Skoro tak, to do osiągnięcia stanu równowagi wystarczy zdecydowanie mniejsze nasycenie par nad roztworem. Jeśli do zamkniętego naczynia wstawimy szklankę z wodą i szklankę z roztworem soli, woda będzie parować aż osiągnie stan równowagi z czystą wodą - co będzie jednak stanem nadmiernie wilgotnym dla roztworu soli. Roztwór soli zacznie więc pochłaniać wodę a my obserwujemy, że w jednej szklance poziom opada a w drugiej rośnie.
Gdy w naszym wilgotnym mieszkaniu granulki chlorku wapnia w pochłaniaczu rozpłyną się, powstający roztwór nadal będzie pochłaniał wilgoć, coraz słabiej wraz z rozcieńczaniem. Tak powstały roztwór jest nieszkodliwy, choć może działać drażniąco. Można go odparować do sucha odzyskując środek wiążacy, po schłodzeniu gęstego roztworu wydzielają się kryształy hydratu. Roztworu bądź kryształów można użyć do odladzania przy silnych mrozach.
Inne osuszacze, mające postać saszetek i woreczków, zawierają różnego typu chłonne materiały ceramiczne i naturalne glinki, na przykład bentonit. Wchłaniają mniej wilgoci ale nie rozpływają się, dlatego można używać ich na przyklad w samochodzie.
Bardzo pospolitych środkiem chłonnym jest koloidalna krzemionka. W postaci mlecznych granulek w woreczkach jest wrzucana do butów lub umieszczana w opakowaniach leków - na przykład wewnątrz koreczków tubek z wapnem musującym.
Jest to wytrącony z roztworów krzemianów kwas krzemowy, silnie skondensowany, tak że w większości składa się w usieciowanego tlenku krzemu, na powierzchni mając wolne grupy hydroksylowe, które podobnie jak te w celulozie i w cukrze, łączą się chętnie z cząsteczkami wody. Jest to materiał wyjątkowo porowaty ze szczelinami wewnątrz ziarna, przez co faktyczna powierzchnia ziarna krzemionki jest ogromna.
Czasem dostępny jest typ zmieniający barwę zależnie od nasycenia, zwykle za sprawą dodatku chlorku kobaltu - suchy żel jest wtedy błękitny a gdy jest nasycony i przestaje pochłaniać wilgoć, staje się różowy
Z pochłaniaczy wilgoci korzystają także chemicy - niejednokrotnie ślady wilgoci przeszkadzają w reakcjach, a także utrudniają dokładne odważenie związku. Dlatego sypkie związki przechowuje się zwykle w szklanych naczyniach z grubego szkła - eksykatorach - zawierających w dolnej części sypkie osuszacze różnej mocy. Czasem jest to żel krzemionkowy, zwykle jednak używa się chlorku wapnia lub siarczan magnezu, często też nadchloran magnezu (ale ten ostrożnie bo zanieczyszczony związkami organicznymi może się zapalić) a także tlenku fosforu. Ten ostatni jest silnym pochłaniaczem wilgoci, wiąże ją przez reakcję chemiczną, tworząc kwas fosforowy.
W podobny sposób wiąże wodę tlenek wapnia, tworzący z nią stały wodorotlenek; zwykle suszy się nim niższe alkohole. Osuszacze te mogą być dodawane do płynnych cieczy organicznych aby usunąć z nich ślady wody, jeśli z nimi nie reagują. Skrajnym osuszaczem używanym do rozpuszczalników organicznych, jest metaliczny sód, reagujący z wodą z wydzieleniem wodoru - procedurę opisałem kiedyś w innym wpisie.
Szczególnym przypadkiem są sita molekularne - granulki masy ceramicznej zawierające niewielkie pory, w głąb których wcisnąć mogą się cząsteczki wody ale nie cząsteczki większych substancji. Dlatego dosyć selektywnie odciągają wodę z substancji, pozwalając osiągnąć bardzo dobre rezultaty.
W jaki sposób? W sposób fizyko-chemiczny...
Skłonność substancji do wchłaniania wody obecnej w powietrzu nazywamy higroskopijnością. Aby proces taki mógł zachodzić, między wodą a materiałem wchłaniającym powinny zachodzić odpowiednio silne oddziaływania. Bardzo hydrofobowy polietylen w zasadzie nie wchłania wilgoci, zaś hydrofilowa celuloza czyni to chętnie. Sam proces chłonięcia wody odbywa się na dwa sposoby - przez osadzanie wody na powierzchni, czyli adsorpcję, albo poprzez wchłanianie do wewnątrz struktury materiału.
Głównym oddziaływaniem mającym wpływ na zdolność osuszająca materiału, są wiązania wodorowe, rozpięte między atomem posiadającego wolne pary elektronowe niemetalu w jednej cząsteczce a wodorem w drugiej. Są to dosyć luźne połączenia, raczej przyciąganie elektrostatyczne niż prawdziwe wiązania, jednak występują często i licznie, wpływając na kształt dużych cząsteczek i właściwości fizyczne substancji. Przykładem może być woda w której każda cząsteczka może tworzyć takie wiązania z trzema innymi. Co prawda ruchy termiczne już w temperaturze pokojowej na tyle silnie miotają cząstkami, że wiązania co chwila rozrywają się i tworzą na nowo, ale sumą ich efemerycznego istnienia jest istotne zwiększenie temperatury wrzenia i krzepnięcia - bez nich tlenek wodoru byłby gazem o temperaturze skraplania poniżej -50 stopni.
Jeśli stały materiał zawiera na swej powierzchni grupy z silnie elektroujemnym niemetalem o wolnych parach elektronowych, to cząsteczka wody z powietrza może zostać z nim związana. Takimi materiałami będzie na przykład celuloza lub cukier, mające w strukturze wiele grup hydroksylowych. Między tlenem takiej grupy a wodorem cząsteczki wody powstaje wiązanie. Możliwe jest też wiązanie między wodorem grupy hydroksylowej a tlenem cząsteczki wody. W podobny sposób wodę chłoną białka, gdzie mamy pod dostatkiem atomów elektroujemnych (azot, tlen).
W przypadku naturalnych włókien, ilość pochłoniętej wilgoci wpływa na ich długość - włókno nawodnione rozciąga się a wysuszone kurczy. Praktycznie wykorzystano tą własność w "domkach pogodowych" gdzie włos lub nić bawełniana owinięty wokół osi, rozciągając się lub skracając przy różnej wilgotności powietrza powoduje, że raz z domku wysuwa się figurka kobiety a raz mężczyzny z parasolem.
Nieco inny jest mechanizm wchłaniania wody przez sole nieorganiczne i materiały ceramiczne. Sól taka składa się z anionów reszty kwasowej i kationów metalu. Każdy jon wytwarza wokół siebie niewielkie pole elektryczne, do którego przyciągane są cząsteczki wody o właściwościach dipola. Zależnie od wielkości i tego na ile jest osłonięty przez inne atomy, jon przyciągnie w ten sposób od jednej do sześciu cząsteczek wody. W taki sposób zwykle rozpoczyna się rozpuszczanie soli w wodzie, tu jednak powstaje jedynie jednocząsteczkowa warstwa na samej powierzchni
Ten powierzchniowy sposób nie ma zwykle wpływu na strukturę materiału, chyba że cząsteczki wody utworzą z jonami dużo trwalszą strukturę - hydrat.
W hydracie cząsteczki wody stają się części sieci krystalicznej. Kationy metali chętnie bowiem tworzą z wodą akwakompleksy, a więc związki z przeniesieniem elektronów tlenu na puste powłoki metalu. Powstający wówczas jon kompleksowy może być bardzo trwały. Aniony z kolei mogą wiązać wodę bądź elektrostatycznie, bądź przez wiązania wodorowe jeśli są resztami kwasów tlenowych.
Hydratacja soli często zmienia jej właściwości - bezwodny siarczan miedzi jest sypkim, białym proszkiem; po nawodnieniu staje się intensywnie niebieski za sprawą powstającego jonu kompleksowego Cu[(H2O)4]2+ , piątą cząsteczkę wody wiąże reszta siarczanowa poprzez wiązanie wodorowe, stąd pełny wzór hydratu CuSO4 X 5 H2O.
Wyjątkowo dużo wody może związać krystalicznie siarczan sodu, nazywany solą glauberską. Uwodnione kryształy zwierają 10 cząsteczek wody na jeden ekwiwalent związku, co stanowi więcej niż 50% masy. Sześć cząsteczek wiąże w mało trwałym kompleksie kation sodowy, dwie wiąże reszta siarczanowa zaś dwie kolejne zawierają się w pustych przestrzeniach sieci. Podobny związek w formie przezroczystych kryształów daje węglan sodu. Bezwodny chlorek kobaltu jest intensywnie niebieski (zabarwia się nim emalię), uwodniony staje się różowy.
Małe i silnie naładowane jony na powierzchni kryształu nie tylko przyciągają kilka cząsteczek wody, ale też często ich oddziaływanie jest nadal wystarczające aby do tej warstewki dołączać kolejne, przez co materiał pokrywa się warstwą wody w której może zachodzić rozpuszczanie. Takim jonem jest jon wodorotlenkowy, w efekcie rozpuszczalne wodorotlenki jak sodu czy potasu, pozostawione na powietrzu rozpływają się w gęsty roztwór.
Wreszcie w przypadku materiałów porowatych pewną rolę pełni też kondensacja kapilarna
Osuszacze
Jak wobec powyższego działają komercyjne osuszacze powietrza?
Część urządzeń opiera się na wykraplaniu wilgoci na elemencie chłodzącym, są to urządzenia potrzebujące prądu, ja jednak zajmę się tymi bezprądowymi, opartymi na higroskopii.
Typ jaki najczęściej spotykam to prosty pojemnik z podziurkowanym wieczkiem, do którego wsypuje się granulki, te po pewnym czasie rozpływają się zaś ilość roztworu zwiększa się do pewnego poziomu. Takie osuszacze bazują na pochłanianiu wody przez sole nieorganiczne, najczęściej przez suchy chlorek wapnia.
Związek ten chłonie wodę zamieniając się w hydrat, wiążąc w formie krystalicznej do sześciu cząsteczek wody na jeden równoważnik związku. Hydrat ten jest jednak nadal higroskopijny, chłonąc wodę na powierzchni ziaren tak silnie, że zaczyna rozpływać się "we własnym sosie" tworząc roztwór.
Gdy grudki się rozpłyną, w pojemniku tworzy się syropowata ciecz, zaś w pochłanianiu wilgoci przeważać zaczyna inne niż wyżej opisane zjawisko fizyczne - mianowicie równowaga między parą nasyconą a roztworem. Gdy umieścimy w pojemniku lotną ciecz, zacznie ona parować aż do momentu gdy gazowa część zbiornika osiągnie stan nasycenia. W takim stanie para pozostaje w równowadze z cieczą, co oznacza, że tyle samo cieczy paruje co pozostaje wchłonięte przez roztwór. Jeśli nasz pojemnik nie będzie szczelny, para będzie uciekała i nie osiągnie nasycenia, zaś lotna ciecz powolutku wyschnie.
Zamknięte mieszkanie może być potraktowane jak taki pojemnik, w którym znajdują się źródła pary wodnej. Jej stężenie w powietrzu zmienia się, czasem wzrastając tak bardzo że skrapla się na chłodnych przedmiotach, zazwyczaj jednak jedynie powodując wilgotnienie materiałów za sprawą ich higroskopijności.
W zasadzie dopóki w mieszkaniu nie zapanują tropikalne warunki pełnego nasycenia parą wodną, równowaga między cieczą a parą nie jest zachowana i woda pozostawiona w szklance powoli paruje.
Inaczej będzie gdy w takim wilgotnym mieszkaniu postawimy roztwór zawierający dużo soli.
Sól niejako "rozcieńcza" wodę.
Gdy rozpatrzymy to sobie mikroskopowo, parowanie następuje gdy w granicę faz uderzy cząsteczka o wystarczającej energii. Jeśli teraz rozprowadzimy w wodzie sól, jej cząsteczki zajmą miejsce niektórych cząsteczek wody. Zatem, znów mikroskopowo patrząc, w granicą faz od dołu uderza mniejsza ilość cząsteczek, przez co roztwór jest mniej lotny (ma niższą prężność par).
Skoro tak, to do osiągnięcia stanu równowagi wystarczy zdecydowanie mniejsze nasycenie par nad roztworem. Jeśli do zamkniętego naczynia wstawimy szklankę z wodą i szklankę z roztworem soli, woda będzie parować aż osiągnie stan równowagi z czystą wodą - co będzie jednak stanem nadmiernie wilgotnym dla roztworu soli. Roztwór soli zacznie więc pochłaniać wodę a my obserwujemy, że w jednej szklance poziom opada a w drugiej rośnie.
Gdy w naszym wilgotnym mieszkaniu granulki chlorku wapnia w pochłaniaczu rozpłyną się, powstający roztwór nadal będzie pochłaniał wilgoć, coraz słabiej wraz z rozcieńczaniem. Tak powstały roztwór jest nieszkodliwy, choć może działać drażniąco. Można go odparować do sucha odzyskując środek wiążacy, po schłodzeniu gęstego roztworu wydzielają się kryształy hydratu. Roztworu bądź kryształów można użyć do odladzania przy silnych mrozach.
Inne osuszacze, mające postać saszetek i woreczków, zawierają różnego typu chłonne materiały ceramiczne i naturalne glinki, na przykład bentonit. Wchłaniają mniej wilgoci ale nie rozpływają się, dlatego można używać ich na przyklad w samochodzie.
Bardzo pospolitych środkiem chłonnym jest koloidalna krzemionka. W postaci mlecznych granulek w woreczkach jest wrzucana do butów lub umieszczana w opakowaniach leków - na przykład wewnątrz koreczków tubek z wapnem musującym.
Jest to wytrącony z roztworów krzemianów kwas krzemowy, silnie skondensowany, tak że w większości składa się w usieciowanego tlenku krzemu, na powierzchni mając wolne grupy hydroksylowe, które podobnie jak te w celulozie i w cukrze, łączą się chętnie z cząsteczkami wody. Jest to materiał wyjątkowo porowaty ze szczelinami wewnątrz ziarna, przez co faktyczna powierzchnia ziarna krzemionki jest ogromna.
Czasem dostępny jest typ zmieniający barwę zależnie od nasycenia, zwykle za sprawą dodatku chlorku kobaltu - suchy żel jest wtedy błękitny a gdy jest nasycony i przestaje pochłaniać wilgoć, staje się różowy
Z pochłaniaczy wilgoci korzystają także chemicy - niejednokrotnie ślady wilgoci przeszkadzają w reakcjach, a także utrudniają dokładne odważenie związku. Dlatego sypkie związki przechowuje się zwykle w szklanych naczyniach z grubego szkła - eksykatorach - zawierających w dolnej części sypkie osuszacze różnej mocy. Czasem jest to żel krzemionkowy, zwykle jednak używa się chlorku wapnia lub siarczan magnezu, często też nadchloran magnezu (ale ten ostrożnie bo zanieczyszczony związkami organicznymi może się zapalić) a także tlenku fosforu. Ten ostatni jest silnym pochłaniaczem wilgoci, wiąże ją przez reakcję chemiczną, tworząc kwas fosforowy.
W podobny sposób wiąże wodę tlenek wapnia, tworzący z nią stały wodorotlenek; zwykle suszy się nim niższe alkohole. Osuszacze te mogą być dodawane do płynnych cieczy organicznych aby usunąć z nich ślady wody, jeśli z nimi nie reagują. Skrajnym osuszaczem używanym do rozpuszczalników organicznych, jest metaliczny sód, reagujący z wodą z wydzieleniem wodoru - procedurę opisałem kiedyś w innym wpisie.
Szczególnym przypadkiem są sita molekularne - granulki masy ceramicznej zawierające niewielkie pory, w głąb których wcisnąć mogą się cząsteczki wody ale nie cząsteczki większych substancji. Dlatego dosyć selektywnie odciągają wodę z substancji, pozwalając osiągnąć bardzo dobre rezultaty.
piątek, 10 stycznia 2014
Ostatnio w laboratorium (36.)
Dawno nie wrzucałem migawek z pracowni.
Gdy skończę kolumnę chromatograficzną, to jest oddzielę pożądany składnik od mieszaniny, muszę ją opróżnić. Wypełnienie, nasączone rozpuszczalnikiem, jest półpłynne, wystarczy więc obrócić kolumnę, podstawić pojemniczek i lekko popukać, aby wypełnienie wypłynęło.
Jest to jednakowoż błotko tiksotropowe - płynie gdy jest wstrząsane ale zastyga gdy już skapnie. Dlatego kolejne porcje spływające do naczynka tworzą rosnący stalagmit, czemu jako chemik-esteta z ciekawością się przyglądam.
Niedawno podczas takiego opróżniania kolumny, kapiące z dwóch miejsc błotko utworzyło taką oto trójwymiarową rzeźbę z czymś w rodzaju łuku:
Czyżby łuk triumfalny sukcesów syntetycznych?
Gdy skończę kolumnę chromatograficzną, to jest oddzielę pożądany składnik od mieszaniny, muszę ją opróżnić. Wypełnienie, nasączone rozpuszczalnikiem, jest półpłynne, wystarczy więc obrócić kolumnę, podstawić pojemniczek i lekko popukać, aby wypełnienie wypłynęło.
Jest to jednakowoż błotko tiksotropowe - płynie gdy jest wstrząsane ale zastyga gdy już skapnie. Dlatego kolejne porcje spływające do naczynka tworzą rosnący stalagmit, czemu jako chemik-esteta z ciekawością się przyglądam.
Niedawno podczas takiego opróżniania kolumny, kapiące z dwóch miejsc błotko utworzyło taką oto trójwymiarową rzeźbę z czymś w rodzaju łuku:
Czyżby łuk triumfalny sukcesów syntetycznych?
Subskrybuj:
Komentarze (Atom)
















-sulfate.jpg)



