Od czasu do czasu dostaję pytania od czytelników bloga. Część pojawia się w komentarzach, i tam staram się na nie odpowiadać co można zobaczyć pod popularnymi postami. Część osób woli jednak drogę bardziej bezpośrednią, używając maila kontaktowego, jaki można znaleźć w opisie profilu, i odpowiedzi na te pytania nie są już powszechnie dostępne. Ponieważ zaś część pytań się powtarza, a niektóre są przecież dość ciekawe, uznałem że warto zebrać je w jednym miejscu, abym nie musiał się powtarzać
Aluminium w glinkach kosmetycznych
O tą rzecz pytano mnie już kilka razy, dlatego warto chyba odpowiedzieć publicznie.
Glina to formalnie rzecz biorąc, skała osadowa. Bardzo miękka a w stanie wilgotnym dająca się formować w rękach, ale skała. Aby osad mógł być zaliczony do glin, musi zawierać odpowiednio dużą ilość minerałów ilastych, przemieszanych z drobnym pyłem kwarcowym i skaleniowym. Tlenki żelaza i manganu nadają glinom kolor od żółtawego, przez rdzawoczerwony, brunatny, szary do ziemisto-zielonego. Glinki z małą ilością metali mogą być też białe.
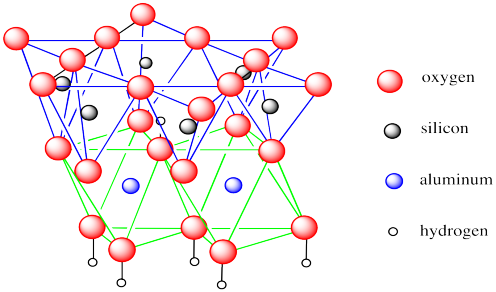
Minerały ilaste, uwalniane ze skał podczas wietrzenia, wypłukiwane w formie najdrobniejszego mułu czy wywiewane przez wiatr jako kurz, stanowią grupę krzemianów warstwowych, składających się z warstw połączonych tetraedrów tlenku krzemu SiO4 i tlenku glinu AlO4. Tlenek glinu jest izomorficzny z tlenkiem krzemu i może go naśladować, włączając się w krzemianową strukturę bez zmian. Poszczególne warstwy glinokrzemianowe są połączone wiązaniami wodorowymi, częściowo jonowymi, i potrafią wchłaniać między siebie inne substancje organiczne i nieorganiczne. Duży stopień uwodnienia powoduje, że warstwy mogą się względem siebie przesuwać, przez co glina staje się plastyczna. Właśnie zawartość tego pierwiastka w glinie stała się podstawą do zastąpienia w polskiej nomenklaturze łacińskiego aluminium nazwą glin.
Struktura warstwy kaolinu:
Wśród krzemianów warstwowych, najczęściej spotykamy się z talkiem, kaolinem będącym głównym składnikiem porcelany i montmorylonitem będącym głównym składnikiem bentonitu. Gliny zawierają mieszankę różnych glinokrzemianów ale niektóre posiadają przewagę jednego, konkretnego, stąd wyróżnia się białą glinkę kaolinową, glinkę pałygorskitową i inne.
A jak jest z tym aluminium?
Aby glin mógł być uwalniany z gliny, powinien być rozpuszczalny w wodzie. A gliny nie są. Nie dość, że zupełnie nierozpuszczalny w wodzie jest tlenek glinu, to w glinokrzemianach dodatkowo stabilizuje go włączenie w sieć krzemianową
Kwestia ta była zresztą szczegółowo badana, zwłaszcza z uwagi na używanie ceramiki jako naczyń kuchennych, oraz używanie glinokrzemianów jako dodatków do żywności. Wydaje się, że w warunkach odczynu obojętnego uwalnianie glinu nie zachodzi. Dopiero warunki kwaśne są w stanie uwolnić część jonów. W pewnym badaniu stwierdzono dla kwasowości pH 3 (sok pomarańczowy) minerały uwalniały dość niskie poziomy aluminium, ale tylko z bardzo cienkiej (3,5 mikrometra) warstwy powierzchniowej, co sugeruje, że w przypadku naczyń ceramicznych po pewnym czasie powstanie wypłukana warstewka powstrzymująca dalsze uwalnianie. Najsłabsze wymywanie stwierdzono dla kaolinu i montmorylonitu[1]. Uwolnienie ilości mających jakieś znaczenie toksykologiczne, zachodzi dopiero pod wpływem mocniejszych kwasów.
Glinki kosmetyczne nie mają tak kwaśnego odczynu, więc uwalniania aluminium nie ma co się obawiać.W dodatku czyste glinki, przepłukane dla wymycia zanieczyszczeń, jak to zwykle jest z glinkami kosmetycznymi, mają raczej skłonność do pochłaniania rozpuszczalnych jonów glinu niż do uwalniania.
W obszernym raporcie na temat bezpieczeństwa glinokrzemianów i tlenków glinu używanych w kosmetyce, nie stwierdzono negatywnych skutków dla minerałów ilastych. [2]
Podobne pytanie dotyczyło spożywania glinek na odtruwanie - tutaj także nie ma niebezpieczeństwa, kwasy żołądkowe są bowiem dosyć rozcieńczone. Jedynym istotnym wpływem jaki stwierdzono, jest zmniejszone wchłanianie żelaza u osób zażywających glinę, bowiem absorbowała żelazo z treści żołądkowej.
Aluminium w szczepionkach
Ze względu na popularny post o ałunie jestem chyba brany za eksperta od aluminium, skoro dotyczy tego koleje pytanie zadawane mi dwa razy.
Jak wiadomo, w niektórych szczepionkach dziecięcych pojawiają się związki aluminium. Podobno zawartość w jednej nie przekracza norm bezpieczeństwa. A co jakby zsumować zawartość we wszystkich - czy wtedy mogłoby zajść jakieś niebezpieczeństwo?
Wodorotlenek glinu pojawia się w szczepionkach jako nośnik białek lub polisacharydów mających wywołać reakcję organizmu. Normy z reguły uważają za najwyższą dopuszczalną dawkę glinu 60 mg/ kg. masy ciała dziennie. Z badań na zwierzętach wynika też, że najniższe dawki mające negatywny wpływ na płody i rozwijające się młode (u szczurów) to 45 mg/kg masy ciała dziennie.
Spośród szczepionek w kalendarzu szczepień, glin zawierają:
- EUVAX B 0,25 mg w jednej dawce lub ENGERIX B też 0,25 mg w jednej dawce (stosowane wymiennie)
- DTP 0,7 mg na dawkę
-IPV 0,5 mg na dawkę
Jak łatwo zauważyć, całkowita zawartość w jednej dawce jest kilkadziesiąt razy mniejsza od najniższych dawek toksycznych. Nawet gdyby wstrzyknąć wszystkie wymienione w ciągu jednego dnia, to nie doszłoby do przekroczenia choćby dziesiątej części toksycznej dawki.
Toksyczność ałunu
Czytelnik pytał o bezpieczeństwo ałunu dla dzieci. Chodziło mu o sytuację gdyby dziecko znalazło kawałek ałunu z pękniętego sztyftu i polizało lub połknęło.
Ałun potasowy i amonowy mają działanie drażniące na błony śluzowe, dlatego pierwszą reakcją w razie połknięcia będą zapewne wymioty. Po polizaniu dziecko pewnie straci ochotę na kolejny liz, ałun ma bowiem bardzo cierpki, nieprzyjemny smak i działanie ściągające. W razie połknięcia najlepiej dać dziecku dużo wody do wypicia i skontaktować się z lekarzem. W razie polizania też dać wody, ale lekarz pewnie nie będzie potrzebny.
Toksyczność ostra związku jest niska - dawka śmiertelna to 6 g/kg masy ciała
Co takiego rozpuszcza DMSO?
Pewien dociekliwy czytelnik zainteresowany medycznymi zastosowaniami DMSO dopytywał mnie o kwestie tego co się w tym rozpuszcza, a co nie i czy ma on zastosowania medyczne.
Dimetylosulfotlenek, czyli w skrócie DMSO to cenny rozpuszczalnik, używany w medycynie i chemii organicznej. Wykazuje dużą skłonność do wnikania w tkanki organizmu, na tyle, że trzeba uważać przy pracy z nim bo po wchłonięciu metabolizuje do związków o zapachu czosnku. Ponieważ rozluźnia strukturę lipidową skóry, może ułatwiać wchłonięcie przezskórnie różnych substancji, w tym wielu leków, dlatego czyni się próby z wykorzystaniem do terapii bez konieczności zastrzyków. Sam w sobie ma zresztą działanie przeciwzapalne.
Bywa rozpuszczalnikiem środków na grzybicę stóp, które zwykle dość słabo przenikają przez zrogowaciały naskórek na podeszwach, może być też składnikiem maści przeciwbólowych do działania miejscowego, może rozmiękczać skórę przy twardzinie i przerastających bliznach. Robiono na ten temat badania [3]
Drugie pytanie dotyczyło możliwości rozpuszczania chondroityny przez DMSO i smarowania tym stawów jako alternatywy dla suplementacji doustnej.
Chondroityna to mukopolisacharyd będący składnikiem chrząstek stawowych i w formie siarczanu stanowiący wraz z glukozaminą jeden z czynników zapewniających lepszy poślizg. W związku z tym powstał pomysł, że jeśli zbyt mała ilość mazi stawowej i mała elastyczność chrząstek stawu powodują bóle, to zażywanie chondroityny i dostarczanie jej do organizmu, powinno leczyć bądź powstrzymywać rozwój schorzeń stawów poprzez dostarczenie organizmowi składnika do wytworzenia większej ilości mazi. Na tym też opiera się potężna gałąź przemysłu suplemenciarskiego.
Niestety w niedawno opublikowanej potężnej metaanalizie wielu badań wykazano, że w porównaniu z placebo zażywanie chondroityny lub glukozaminy lub obu tych środków razem, nie zmniejsza bólów ani innych objawów[4]
Wygląda na to, że samo dostarczenie organizmowi składników potrzebnych do wytworzenia czegośtam w którymś organie, wcale nie musi go pobudzać aby tą substancję jednak wytworzyć, zwłaszcza że niedostateczne wydzielanie tej substancji wcale nie musi być wynikiem niedoboru podstawowego składnika, może być skutkiem innych czynników, w tym genetycznych. Dlatego jeśli przyjrzycie się emitowanym obecnie reklamom takich pigułek, zauważycie że wcale nie stwierdzają one wprost, iż zażycie tego składnika powstrzyma chorobę. Zamiast tego zawierają ogólniki, typu "glukozamina jest składnikiem chrząstki stawowej" i "maź stawowa ma decydujące znaczenie w zapewnieniu elastyczności stawu" i na koniec, że ich pigułka zawiera podwójną czy potrójną dawkę, zaś konstrukcję logiczną "skoro to jest składnikiem chrząstki a chrząstka jest potrzebna w stawach, to pomoże mi na stawy" widz musi sam sobie przeprowadzać, w czym udanie pomaga mu sugestia pokazywanego w reklamie pana którego bolą stawy, który bierze ich tabletki a potem wygląda na mniej cierpiącego.
Ale wróćmy do pytania - czy chondroityna rozpuszcza się w DMSO? Cóż - wedle obszernego podsumowania rozpuszczalności różnych substancji w tym rozpuszczalniku, chondroityna jest nie rozpuszczalna. Słabo rozpuszcza się chlorowodorek glukozaminy, natomiast bardzo dobrze przeciwbólowy Ibuprofen.[5]
Tak że raczej nie tędy droga.
Gdzie zbadać wodę?
Miałem też pytania o to gdzie można samemu zbadać wodę ze studni, źródła czy ujęcia.
Z tego co się orientuję, takie badania oferują jednostki Sanepidu, zbadają one zawartość metali ciężkich, czystość bakteriologiczną i własności fizyczne, jak zamulenie, obecność kwasów humusowych, zażelazienie itp. Oczywiście są to badania płatne.
Próbkę wody może pobrać wysłany pracownik, ale można ją też pobrać samemu. Warszawska stacja podaje na swojej stronie specyfikację sposobu pobierania próbek, aby nadawały się do badania.[6]
Dezodorant z podbiałem
Świadoma konsumentka zadała mi pytanie w sprawie używanego dezodorantu, który zawierał w swoim składzie podbiał pospolity. Chcąc dowiedzieć się czegoś o tym składniku, dowiedziała się że roślina zawiera uszkadzające wątrobę alkaloidy. I stąd powstało pytanie, czy taki alkaloid może wchłaniać się przez skórę?
Podbiał to cenne zioło lecznicze, lecz dopiero w ostatnich latach zorientowano się, że może zawierać alkaloidy pirolizydynowe, o działaniu hepatotoksycznym, które w wyniku zażywania dłuższym niż dwa miesiące mogą powodować toksyczną niewydolność wątroby. Ich zawartość w surowcach zbieranych w Europie jest jednak bardzo niska - w polskim badaniu stwierdzono poziomy rzędu 0,0013%[7]
W jednym badaniu na szczurach stwierdzono minimalne wchłanianie przezskórne alkaloidów żywokostu, w ilości 20 razy mniejszej niż przy podaniu doustnym. Stwierdzono też, że przy chłonięciu przeskórnym, nie dochodzi do zamiany nietoksycznego N-tlenku w toksyczną formę zredukowaną, co zwykle następowało w jelitach po spożyciu.[8] Zatem wydaje się, że kosmetyków z roślin zawierających te alkaloidy można używać bezpiecznie.
Czy to cyjanek?
Dwa lata temu czytelnik przesłał mi zdjęcie białego proszku, z pytaniem czy to cyjanek potasu. Cóż mogłem odpowiedzieć... Spektroskopu w oczach nie mam. Odpisałem, że może to być cyjanek albo soda, albo sól morska, albo cokolwiek innego bo bardzo wiele soli tak wygląda. Nie wiem o co chodziło.
----------
[1] http://www.clays.org/journal/archive/volume%2026/26-6-434.pdf
[2] http://www.ncbi.nlm.nih.gov/pubmed/12851164
[3] http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3460663/
[4] http://www.bmj.com/content/341/bmj.c4675
[5] http://www.gaylordchemical.com/uploads/images/pdfs/literature/102B_english.pdf
[6] http://www.wsse.waw.pl/PageContent.aspx?SubMenuID=100
[7] https://depot.ceon.pl/bitstream/handle/123456789/1121/hp%2058%204%202012%2062.pdf?sequence=1&isAllowed=y
[8] http://www.ncbi.nlm.nih.gov/pubmed/7128756?dopt=Abstract
informacje
Pokazywanie postów oznaczonych etykietą glin. Pokaż wszystkie posty
Pokazywanie postów oznaczonych etykietą glin. Pokaż wszystkie posty
poniedziałek, 15 czerwca 2015
niedziela, 30 czerwca 2013
Do więzienia za eksperyment chemiczny? - nie jest jeszcze tak źle
Na sam koniec czerwca proponuję taką historyjkę z drugiej strony globu, która jest i straszna i śmieszna.
Po licznych i bardzo tragicznych atakach w amerykańskich szkołach, prawo bardzo obostrzyło kwestę przynoszenia do szkoły różnych rzeczy. W większości szkół i uczelni nie można nosić przy sobie noży, ani tym bardziej broni palnej. Tego typu zakazy są zresztą krytykowane przez lobbystów ze stowarzyszeń strzeleckich, uważających naiwnie że przynajmniej studenci powinni mieć ze sobą broń na terenie kampusu i na zajęciach, aby bronić się przed podobnymi napaściami. Połączenie strachu przed strzelaniną, zamiłowania do broni i polityki "zero tolerancji" doprowadza z czasem do takich absurdów, jak zawieszenie dwójki uczniów, którzy przynieśli na zajęcia kolorowe, plastikowe pistolety-zabawki bo nauczyciel poprosił o przyniesienie ulubionych zabawek[1]
- bądź takich sytuacji jak niedawna panika, jaką wywołał w szkolnym autobusie pewien 6-latek, po pokazaniu kolegom miniaturowego, plastikowego karabinu maszynowego, z zestawu klocków Lego[2]
Ofiarą tego zamieszania stała się też niedawno 16-letnia Kiera Wilmot, która za namową znajomego, przeprowadziła na placu przed szkołą Bartow High School pewien eksperyment. Do plastikowej butelki wrzuciła kilka kawałków folii aluminiowej, i dodała rozcieńczony środek do czyszczenia toalet, po czym lekko przykręciła korek. Środki tego typu są zwykle zawierają silne kwasy, gdy więc zostaną zmieszane z takimi reaktywnymi metalami, jak cynk czy glin, będą wydzielały gazowy wodór. Tak też stało się w tym przypadku. Mieszanka rozgrzała się, a butelka rozdęła się, zaś korek wystrzelił z głośnym hukiem. Poszło nawet trochę pary wodnej, wyglądającej jak dym.
Nie wiedzący co się stało uczniowie wpadli w panikę, a policja została poinformowana o wybuchu bomby na terenie szkoły. Nasza nieszczęsna eksperymentatorka została wktótce aresztowana pod zarzutem wniesienia na teren szkoły broni, i detonacji urządzeń pirotechnicznych. W myśl obowiązujących przepisów została wyrzucona ze szkoły.[3]
Gdyby dzisiejsze przepisy obowiązywały sto temu, William Thompson nie mógłby przeprowadzać w trakcie wykładów swego ulubionego doświadczenia z wahadłem balistycznym, podczas którego strzelał ze sztucera do worka z piaskiem. Wedle anegdoty zdarzyło się, że nie trafił, a kula przeszła przez drzwi prowadzące do sąsiedniej sali wykładowej. Gdy przestraszony wbiegł tam, okazało się że wbiła się w ścianę nad głową przerażonego wykładowcy, zas studenci krzyknęli "Proszę spróbować jeszcze raz - może pan trafi!".
W obronie nastolatki stanęli uczniowie i nauczyciele. Krążący po internecie list poparcia podpisało 150 tysięcy osób. Media wyśmiewały nadgorliwość policji, mylącej butelkę detergentów z bombą. Wreszcie wziął ją pod obronę Homer Hickam - inżynier NASA, znany autor książek na temat kosmosu. Młody Homer, będąc jeszcze młodszy od niej, zbudował niewielką rakietę na paliwo karmelkowe i wystrzelił ją z łąki niedaleko domu. Od rakiety zajęła się sucha trawa, toteż został zaaresztowany za wandalizm. Jego nauczyciel fizyki obronił go, tłumacząc że był to skutek eksperymentu naukowego, dzięki czemu chłopiec nie stracił zapału do nauki.
Przy tak mocnej obronie, policji nie pozostawało nic innego, jak ogłosić że doszło do pomyłki i wycofać zarzuty. Wilmot została też przywrócona do szkoły, a także zaproszona na letni obóz naukowy w Kosmicznej Akademii, w ramach rekompensaty za niemiłe zdarzenia.[4]
W zasadzie więc wszystko skończyło się dobrze a morałem jest, że głupota nie może powstrzymać naukowej ciekawości.
Żeby wam jednak nie było za wesoło, opowiem jak mogłaby się skończyć ta historia, gdyby zdarzenia potoczyły się nieco inaczej. Gdyby butelka rozgrzała się już porządnie i ciśnienie wewnątrz odpowiednio wzrosło, butelka mogłaby rozstać rozerwana, opryskując dziewczynę gorącą, żrącą mieszanką. Wówczas w mediach zapewne pojawiłyby się przestrogi przed podobnymi eksperymentami, często niebezpiecznymi, i robionymi przez nastolatki bez świadomości zagrożeń.
Nawet w kontrolowanych warunkach w szkole, doświadczenia mogą być niebezpieczne. W Legnicy, podczas pokazów w ramach festiwalu nauki kilka osób zostało rannych w wybuchu chemikaliów[5]. Więc może nie przesadzajmy z pochwałą amatorskich eksperymentatorów.
-------
[1] http://www.nydailynews.com/news/national/students-suspended-nerf-gun-article-1.1363552
[2] http://www.nydailynews.com/news/national/lego-gun-panic-school-bus-article-1.1357236
[3] http://www.alternet.org/civil-liberties/16-year-old-girl-arrested-and-charged-felony-science-project-mistake
[4] http://www.good.is/posts/people-are-awesome-teen-arrested-for-science-experiment-now-heading-to-space-camp
[5] http://natablicy.pl/legnica-wybuch-podczas-eksperymentu-na-festiwalu-nauki-chemik-stracil-palec,artykul.html?material_id=4c9b23497233c7d478000000#zamknij
Po licznych i bardzo tragicznych atakach w amerykańskich szkołach, prawo bardzo obostrzyło kwestę przynoszenia do szkoły różnych rzeczy. W większości szkół i uczelni nie można nosić przy sobie noży, ani tym bardziej broni palnej. Tego typu zakazy są zresztą krytykowane przez lobbystów ze stowarzyszeń strzeleckich, uważających naiwnie że przynajmniej studenci powinni mieć ze sobą broń na terenie kampusu i na zajęciach, aby bronić się przed podobnymi napaściami. Połączenie strachu przed strzelaniną, zamiłowania do broni i polityki "zero tolerancji" doprowadza z czasem do takich absurdów, jak zawieszenie dwójki uczniów, którzy przynieśli na zajęcia kolorowe, plastikowe pistolety-zabawki bo nauczyciel poprosił o przyniesienie ulubionych zabawek[1]
- bądź takich sytuacji jak niedawna panika, jaką wywołał w szkolnym autobusie pewien 6-latek, po pokazaniu kolegom miniaturowego, plastikowego karabinu maszynowego, z zestawu klocków Lego[2]
Ofiarą tego zamieszania stała się też niedawno 16-letnia Kiera Wilmot, która za namową znajomego, przeprowadziła na placu przed szkołą Bartow High School pewien eksperyment. Do plastikowej butelki wrzuciła kilka kawałków folii aluminiowej, i dodała rozcieńczony środek do czyszczenia toalet, po czym lekko przykręciła korek. Środki tego typu są zwykle zawierają silne kwasy, gdy więc zostaną zmieszane z takimi reaktywnymi metalami, jak cynk czy glin, będą wydzielały gazowy wodór. Tak też stało się w tym przypadku. Mieszanka rozgrzała się, a butelka rozdęła się, zaś korek wystrzelił z głośnym hukiem. Poszło nawet trochę pary wodnej, wyglądającej jak dym.
Nie wiedzący co się stało uczniowie wpadli w panikę, a policja została poinformowana o wybuchu bomby na terenie szkoły. Nasza nieszczęsna eksperymentatorka została wktótce aresztowana pod zarzutem wniesienia na teren szkoły broni, i detonacji urządzeń pirotechnicznych. W myśl obowiązujących przepisów została wyrzucona ze szkoły.[3]
Gdyby dzisiejsze przepisy obowiązywały sto temu, William Thompson nie mógłby przeprowadzać w trakcie wykładów swego ulubionego doświadczenia z wahadłem balistycznym, podczas którego strzelał ze sztucera do worka z piaskiem. Wedle anegdoty zdarzyło się, że nie trafił, a kula przeszła przez drzwi prowadzące do sąsiedniej sali wykładowej. Gdy przestraszony wbiegł tam, okazało się że wbiła się w ścianę nad głową przerażonego wykładowcy, zas studenci krzyknęli "Proszę spróbować jeszcze raz - może pan trafi!".
W obronie nastolatki stanęli uczniowie i nauczyciele. Krążący po internecie list poparcia podpisało 150 tysięcy osób. Media wyśmiewały nadgorliwość policji, mylącej butelkę detergentów z bombą. Wreszcie wziął ją pod obronę Homer Hickam - inżynier NASA, znany autor książek na temat kosmosu. Młody Homer, będąc jeszcze młodszy od niej, zbudował niewielką rakietę na paliwo karmelkowe i wystrzelił ją z łąki niedaleko domu. Od rakiety zajęła się sucha trawa, toteż został zaaresztowany za wandalizm. Jego nauczyciel fizyki obronił go, tłumacząc że był to skutek eksperymentu naukowego, dzięki czemu chłopiec nie stracił zapału do nauki.
Przy tak mocnej obronie, policji nie pozostawało nic innego, jak ogłosić że doszło do pomyłki i wycofać zarzuty. Wilmot została też przywrócona do szkoły, a także zaproszona na letni obóz naukowy w Kosmicznej Akademii, w ramach rekompensaty za niemiłe zdarzenia.[4]
W zasadzie więc wszystko skończyło się dobrze a morałem jest, że głupota nie może powstrzymać naukowej ciekawości.
Żeby wam jednak nie było za wesoło, opowiem jak mogłaby się skończyć ta historia, gdyby zdarzenia potoczyły się nieco inaczej. Gdyby butelka rozgrzała się już porządnie i ciśnienie wewnątrz odpowiednio wzrosło, butelka mogłaby rozstać rozerwana, opryskując dziewczynę gorącą, żrącą mieszanką. Wówczas w mediach zapewne pojawiłyby się przestrogi przed podobnymi eksperymentami, często niebezpiecznymi, i robionymi przez nastolatki bez świadomości zagrożeń.
Nawet w kontrolowanych warunkach w szkole, doświadczenia mogą być niebezpieczne. W Legnicy, podczas pokazów w ramach festiwalu nauki kilka osób zostało rannych w wybuchu chemikaliów[5]. Więc może nie przesadzajmy z pochwałą amatorskich eksperymentatorów.
-------
[1] http://www.nydailynews.com/news/national/students-suspended-nerf-gun-article-1.1363552
[2] http://www.nydailynews.com/news/national/lego-gun-panic-school-bus-article-1.1357236
[3] http://www.alternet.org/civil-liberties/16-year-old-girl-arrested-and-charged-felony-science-project-mistake
[4] http://www.good.is/posts/people-are-awesome-teen-arrested-for-science-experiment-now-heading-to-space-camp
[5] http://natablicy.pl/legnica-wybuch-podczas-eksperymentu-na-festiwalu-nauki-chemik-stracil-palec,artykul.html?material_id=4c9b23497233c7d478000000#zamknij
niedziela, 15 lipca 2012
Ałun
Na trop dzisiejszego tematu wpadłem podczas zbierania informacji do wpisu o herbacie. Związki glinu są bowiem często stosowane w antyperspirantach, o czym wówczas nie napisałem, bo nijak się to miało do popularnych napojów. Wiele osób ma wątpliwości co do tego na ile takie środki są obojętne dla zdrowia i szukają innych rozwiązań. W sumie powstał cały przemysł kosmetyków, suplementów i innych środków mających zabić zapach ciała i usunąć pot - jest swoistym znakiem naszych czasów że wszelkie zewnętrzne przejawy czynności fizjologicznych ciała są dziś zwalczane z równym zapałem, co oznaki świadczące o istnieniu płci w społecznościach purytańskich, toteż nasze ciało nie może okazać że trawi, metabolizuje i od czasu do czasu musi wydalać, a burczenie w brzuchu, potliwość czy ślinienie są uważane za ogromnie wstydliwe przypadłości które należy szybko usunąć.
Ale wracając do tematu - wielu z tych poszukujących bardziej naturalnych sposobów na zabicie naturalnych woni cielesnych natyka się w końcu na dziwne, lśniące sztyfty, wykonane z krystalicznej masy, mające być naturalnymi minerałami zastępującymi dezodoranty. Czasem ktoś określa je nazwą ałunu. Krążą na ich temat różne opinie, ja zaś starałem się je jakoś podsumować - oczywiście po chemicznemu.
A zatem - czym jest krystaliczny ałun stosowany w takich sztyftach? Czy na prawdę działa? I czy na pewno jest taki naturalny...
Ałuny to ciekawa grupa soli podwójnych - a więc takich które zawierają jeden tylko rodzaj anionu kwasowego ale dwa rodzaje mogących się z nimi połączyć kationów. W zasadzie więc jest to mieszanina dwóch soli, jednak ałuny wyróżniają się tu szczególną cechą - po zmieszaniu nie da się oddzielić (klasycznymi metodami) jednej soli od drugiej, jakby tworzyły jeden związek. Wszystkie ałuny są siarczanami - a więc zawierają aniony siarczanowe VI dwu-ujemne - zaś kationy są różne, jeden (A) jednowartościowy, drugi (B) trójwartościowy. Obie sole składowe tworzą kryształy tego samego typu i mają podobną rozpuszczalność, dlatego gdy odparowujemy roztwór ałunu otrzymujemy kryształ mieszany w którego węzłach na przemian pojawia się kation A i kation B; ogólny wzór takich związków wygląda zatem:
Ałuny łatwo krystalizują tworząc przezroczyste kryształy, czasem zabarwione jeśli zawierają odpowiedni kation - ałun żelazowo-potasowy jest pomarańczowy a chromowo-potasowy fioletowy niczym ametyst. Dlatego jeśli szukacie dobrego materiału do zrobienia sobie kryształków, to oprócz polecanego przeze mnie kwasku cytrynowego możecie użyć ałunu. Ponieważ wszystkie ałuny krystalizują tak samo wykazując idealny izomorfizm, różne ich odmiany mogą krystalizować na sobie - Sękowski w jednej z książek proponował krystalizację w której rosnący zarodek był co kilka godzin przekładany z jednego roztworu do drugiego, i zależnie od użytych soli, po przecięciu kryształka i wyszlifowaniu przełomu pokazywał się wzór warstewek zielono-fioletowych, lub fioletowo-bezbarwnych. Jeszcze tego nie próbowałem ale kiedyś będę musiał.
Ałuny były znane już w starożytności, ich nazwa pochodzi od greckiego słowa "alum" oznaczającego cierpki smak. Były używane w farbiarstwie, ułatwiały bowiem związanie barwnika z tkaniną, a także w garbarstwie do wyprawiania skór. Znamy też zapisy mówiące o użyciu ałunu do impregnacji drewna, na przykład palisad lub dachów twierdz, dzięki któremu stawały się trudnopalne.
Najstarsze wzmianki sugerujące iż znano wówczas tą sól - choć nie została wymieniona z nazwy - pochodzą z Egiptu aż z 2 tysiąclecia p.n.e., w babilońskich tabliczkach glinowych jest wymieniana ok. XVIII-XVI wieku p.n.e. Szerszy opis podaje Piliniusz w Historii naturalnej, wymieniając kilka rodzajów ałunów. Głównym źródłem pozostawał Egipt, gdzie wydobywano złoża z wyschniętych okresowych jezior, w pewnym stopniu pozyskiwano go z ałunitu i skorupiastych wystąpień naskalnych
Znajdowała szerokie zastosowanie w średniowiecznej europie, będąc często składnikiem leków i kosmetyków. Arabowie wprowadzili go do alchemii. Duże złoża odkryto w Azji, głównie na pustyniach, inne odkryto w Hiszpanii. Przez pewien czas Anglia była pozbawiona tego surowca z powodu embarga nałożonego po aferze z Henrykiem XVIII, produkowano go wówczas z łupków i ludzkiego moczu. [1]
Jakoś tak się jednak stało że dopiero na początku XIX wieku zaczęto się domyślać, że ałuny są solami zawierającymi nie znany pierwiastek metaliczny, nazwany od nich właśnie Aluminium. Polska nazwa "glin" pochodzi od gliny w której występuje bardzo często.
Jeśli chodzi o zastosowanie jako dezodorant to prawdopodobnie po raz pierwszy użyto go w tym celu w Starożytności - znajdujemy luźne wzmianki o kamieniach na brzydki zapach i zapewne chodziło o tą sól. Działanie mają tutaj przede wszystkim sole glinu to zaś z dwóch powodów - z jednej strony działają bakteriobójczo, a więc zabijają bakterie, które rozkładając składniki potu nadają mu charakterystyczny zapach, z drugiej zaś mają działanie ściągające, zatem zmniejszają pory skóry a tym samym potliwość. Stosowany często w kosmetykach hydroksychlorek glinu hydrolizuje po rozpuszczeniu, zatykając gruczoły potowe i uniemożliwiając pocenie; podobne działanie ma hydroksochlorek glinowo-cyrkonowy. Oba te związki a dokładnie powstające z nich osady wodorotlenków zostawiają na ubraniu białe plamy. Niekiedy stosuje się sole organiczne, jak kompleks z glicyną.
Działanie dezodoryzujące ałunów wynika z obecności w nich glinu i opiera się głównie na zabijaniu wspomnianych bakterii, natomiast wpływ na potliwość jest nie wielki. Sam mam taki sztyft ale nie używam go często, zrobiłem jednak kilka eksperymentów, na przykład smarując nim jedną pachę i porównując zapach w ciągu dnia. Zauważalne było osłabienie zapadu ale nie było całkowite. Zresztą nie należę do osobników o szczególnie śmierdzącym pocie, więc dla mnie różnica była niewielka. Różnicy w potliwości nie zauważyłem. Co do czasu działania - przy normalnej pogodzie starcza na cały dzień, w upały zmywa się po kilku godzinach.
Sądząc z opinii użytkowników o ile większość jest zachwycona, to jednak niektórym nie pomaga, ci o dużej potliwości narzekają że przestaje działać po paru godzinach, bo zwyczajnie się zmywa. Niektórzy donoszą też o podrażnieniach, nawet bardzo dokuczliwych - pamiętajmy że pewien procent ludzkości jest uczulony na glin w każdej postaci.W szczególnych przypadkach oprócz podrażnień stosowanie ałunu może prowadzić do zapalenia skóry - notowano takie sytuacje[2] Warto też pamiętać że podrażnia tkanki, więc lepiej nie dotykać nim ust i uważać aby nie dostał się do oka. Ałun ścina białko i koaguluje krew - dawniej w czasach brzytew normą było posiadanie "kamyków do golenia" czy pałeczek ałunowych, którymi tamowano skaleczenia. Miałem okazję to sprawdzić - działa ale okropnie piecze.
Biodostępność glinu przez skórę pach oceniono na 0,012% - dla porównania biodostępność z wodą pitną to 0,3% [3]
[Dopisek 2015: komentujący zwrócił moją uwagę na jeszcze jedno miejsce gdzie jest użyty ałun - chodzi o ayurwedyjski proszek do zębów Vicco Vajradanti który ma w składzie ałun, co tłumaczy dlaczego powstrzymuje krwawienia dziąseł. W takim użyciu, ałun rozpuszczony w ślinie styka się z błonami śluzowymi i ma dużo większą szansę być wchłoniętym do organizmu niż w przypadku naniesienia na skórę. W zasadzie to tak jakby połknąć. Sprawdzałem pod tym kątem inne proszki i pasty ale często, zwłaszcza te indyjskie, nie mają pełnego składu. Ałun zawiera jeszcze chyba proszek na krwawiące dziąsła Gum Tone]
Bez aluminium
Aluminium i glin to to samo. Używane w sztyftach związki to ałun glinowo-potasowy lub glinowo-amonowy. Zatem kryształ na pot zawiera aluminium i to całkiem sporo. Mimo to wciąż natykam się na opisy, najczęściej na stronach promujących "naturalne" i "organiczne" kosmetyki ze stwierdzeniem, że akurat ten go nie zawiera. Czasem jednak ktoś pójdzie po rozum do głowy i zajrzy na skład, gdzie zobaczy łacińską nazwę alum ammonium, nabierając w tej sprawie podejrzeń. Gdy zaczyna szukać czegoś na ten temat, być może znajdzie stronę firmy NajMar, polskiego producenta, a tam w dziale FAQ taki uroczy fragment:
Na dobrą sprawę producent Deo Kryształu nigdzie o tym nie pisze a jednak jakoś ciągle natykam się na teksty w których takie absurdalne stwierdzenie się pojawia, co pewnie jest skutkiem niewiedzy. Zapewne przyczynia się do tego omawiany już schemat myślowy "chemiczne-sztuczne-szkodliwe / naturalne-zdrowe". Jeśli aluminium jest szkodliwe, to jest chemiczne i pojawia się w sztucznych kosmetykach, więc jeśli jakiś kosmetyk jest naturalny, to tego sztucznego aluminium nie zawiera.
Czasem jednak ktoś poczyta dokładniej i dowie się, że ten metal w ałunie amonowym także jest zawarty. I czy teraz należy odrzucić cały produkt? Przecież jest zachwalany jako naturalny, więc to musi być różnica. W efekcie pojawiają się czasem objaśnienia - ałun naturalny ma naturalną strukturę krystaliczną, więc nie jest wchłaniany; albo że to są naturalne cząsteczki które są duże, i nie wnikają w skórę. Tak tłumaczy to Alepia, jeden z producentów. Niestety, ałun naturalny to siarczan amonowo-glinowy a ałun syntetyczny to siarczan amonowo-glinowy, czyli dokładnie to samo. Jak niby struktura krystaliczna ma wpływać na wnikanie w skórę nie wiem, a zważywszy że ta "unikalna struktura" musi się najpierw podczas aplikacji rozpuścić w wodzie i ulec rozpadowi na jony, raczej wpływu to nie ma żadnego.
Różnica owszem jest, ale nikt na to nie wpadł - skóra z reguły jest tłusta i nieprzepuszczalna dla jonowych soli nieorganicznych. Jeśli posmarujemy się solanką nie wchłoniemy chloru, ale gdy użyjemy w tym celu chloroformu szybko zacznie się nam kręcić w głowie. Polarne rozpuszcza się w polarnym a niepolarne, w niepolarnym - proste.
Mimo to natknąłem się na badanie wskazujące, że sole glinu - konkretnie chlorek - mogą być wchłaniane przez skórę. Co prawda badanie dotyczyło ogolonej myszy a efekty stały się wyraźne po czterech miesiącach, ale zawsze jest to wskazówka że jakieś wchłanianie nieorganicznego glinu zachodzi i tak[4]
Naturalny
Naturalność sztyftu jest jego główną zaletą. W każdym razie sądząc z opinii, wiele osób kupiło go właśnie dlatego. Ałuny jak łatwo się domyśleć z powyższych rozważań, występują w przyrodzie. Ałun glinowo-potasowy jest najpospolitszy, nieco rzadszy jest ałun glinowo-sodowy. Natomiast ałun glinowo-amonowy to bardzo rzadki minerał.
Jony amonowe powstają w przyrodzie wskutek gnicia materii organicznej jednak ich żywot jest raczej krótki, bo albo są utleniane albo w zasadowym środowisku zamieniają się w lotny amoniak, dlatego nie zbyt dużo jest minerałów które go zawierają, pojawiają się głównie w okolicy otworów hydrotermalnych oraz w pobliżu szczelin którymi ulatują gazy z podziemnych pożarów węgla. Zatem ałun amonowy, występujący w formie Tschermigitu, nie może występować w dużych złożach. Stanowiło to dla mnie pierwszy zgrzyt.
Jeśli sztyfty robi się z minerału który jest rzadki, a sądząc z ilości ofert, produkuje się je na skalę masową, to chyba powinny być bardzo drogie?
Anglo i hiszpańskojęzyczne strony piszą zwykle, że ałun w tych sztyftach pochodzi z Tajlandii i jest wydobywany "z wygasłego wulkanu", zacząłem zatem szukać informacji na temat złóż Tschermigitu (Czermigit) w tamtym kraju i nie znalazłem, dopiero wzmianka o skale z której przerobu uzyskuje się ałun[5] rozjaśniła sytuację. W Tajlandii w skałach wulkanicznych znajdują się całkiem spore złoża Ałunitu - skały będącej hydroksysiarczanem glinowo-potasowym będącej efektem wietrzenia trachitu. Z niego właśnie otrzymuje się ałun - skałę należy rozkruszyć, pogotować z kwasem siarkowym i wykrystalizować gotowy związek - związkiem tym będzie oczywiście ałun glinowo-potasowy.
A amoniak? Jak widać w tym minerale nie występuje, dlatego aby otrzymać sól amonową należy dodać do roztworu siarczan amonu. Tan akurat jest łatwy do zdobycia - jest ubocznym produktem przy produkcji kaprolaktamu i powstaje go tak dużo, że zakłady szukają pomysłów gdzie go tylko zbyć. A więc łączymy przesącz z ałunitu rozgotowanego w kwasie z odpadowym siarczanem amonu, zagęszczamy i otrzymujemy kryształy zbijające się w jednolitą masę z której można wycinać bloki, pałeczki i sztfty.
Jak zatem widać wszystko wskazuje na to, że dostępny na rynku ałun amonowy jest o tyle tylko naturalny, że jeden z jego składników kiedyś widział jakąś skałę. Powstaje w związku z tym pytanie, czy aby reklamowanie go jako naturalnego minerału nie jest aby wprowadzaniem konsumentów w błąd?
Rzecz zresztą wyłapała konkurencja - producenci sztyftów z ałunem potasowym zaczynają pisać w reklamach, że w odróżnieniu od syntetycznej soli amonowej ich produkt jest naturalniejszy - co niekoniecznie musi być prawdą.
Ogółem zatem - sztyfty ałunowe działają jeśli chodzi o zapobieganie powstawaniu przykrych zapachów, są pozbawione dodatków i dlatego dla wielu osób mogą być idealnym rozwiązaniem, zawsze jednak byłem za ty, aby wybierać z głową i wiedzą. Jeśli ktoś wybrał ałun bo jest naturalny i bo nie zawiera aluminium, to się przejechał. Kupujący powinien wiedzieć wszystko o tym co mu wciskają i powinien sobie rozważyć, czy chce się zdecydować na dany produkt.
Tymczasem producenci robią wszystko co się da aby stworzyć ludziom w głowach fałszywy obraz, całkiem pomijając kwestię składu. I choć produkt działa, nie są to działania uczciwe. Nie informowanie o składzie i sugerowanie różnymi sztuczkami że produkt nie zawiera aluminium to chwyt nie zbyt chwalebny, natomiast oszukiwanie tak jak producent "Crystal Body Deodorant" w polskich etykietkach, zasługuje już na zgłoszenie do urzędu ochrony konsumenta. Coś podobnego pojawia się na ałunach serii N& B.
ps. 11.03.13
Ponieważ od tej publikacji dostałem kilka e-maili od ludzi, czujących się oszukanymi, bo po reklamach sądzili że ałuny są całkiem innymi preparatami, postanowiłem działać - wysłałem do UOKiK list z zauważonymi nieprawidłowościami. Co oni z tym zrobią to się zobaczy - najpierw muszą rozpatrzyć czy sprawa leży w ich kompetencjach i zrobić kontrole w sklepach. Jakby coś do mnie przysłali, to poinformuję.
ps. 2014
Ponieważ reakcji brak, wysyłam zapytanie do Rossmanna czy wiedzą że źle oznakowali sprzedawany kosmetyk. Zobaczymy co odpowie.
kwiecień 2014
Odpisali że przekażą uwagi producentowi odpowiedzialnemu za rozprowadzanie. Teraz poczekam - jeśli za kilka miesięcy nowe partie dalej będą zawierały błędną informację, to zainteresuję tym jakąś gazetę.
Listopad 2014
Mały sukces - nowe partie sztyftów ałunowych mają zmienioną etykietkę. Zamiast twierdzeń iż nie zawierają aluminium, jest tylko "nie zawiera aluminium chlorohydrate" - czyli z jednej strony usunęli wprowadzający w błąd napis ale z drugiej strony zdecydowali się nie tłumaczyć na polski nazwy związku. Teraz tylko pozostaje sprawić, aby opis zmienił się w internetowych sklepach, gdzie stara wersja nadal funkcjonuje i wprowadza w błąd.
-----
 [1] http://www.wovepaper.co.uk/alumessay1.html - obszerna historia ałunu
[1] http://www.wovepaper.co.uk/alumessay1.html - obszerna historia ałunu
[2] Gallego H, Lewis EJ, & Crutchfield CE 3rd (1999). Crystal deodorant dermatitis: irritant dermatitis to alum-containing deodorant. Cutis; cutaneous medicine for the practitioner, 64 (1), 65-6 PMID: 10431678
[3] Yokel RA, & McNamara PJ (2001). Aluminium toxicokinetics: an updated minireview. Pharmacology & toxicology, 88 (4), 159-67 PMID: 11322172
[4] Anane R, Bonini M, Grafeille JM, & Creppy EE (1995). Bioaccumulation of water soluble aluminium chloride in the hippocampus after transdermal uptake in mice. Archives of toxicology, 69 (8), 568-71 PMID: 8534202
[5] http://www.alliumherbal.com/es/articulos/43-cosmetica-belleza-natural/410-piedra-de-alumbre.html
Ale wracając do tematu - wielu z tych poszukujących bardziej naturalnych sposobów na zabicie naturalnych woni cielesnych natyka się w końcu na dziwne, lśniące sztyfty, wykonane z krystalicznej masy, mające być naturalnymi minerałami zastępującymi dezodoranty. Czasem ktoś określa je nazwą ałunu. Krążą na ich temat różne opinie, ja zaś starałem się je jakoś podsumować - oczywiście po chemicznemu.
A zatem - czym jest krystaliczny ałun stosowany w takich sztyftach? Czy na prawdę działa? I czy na pewno jest taki naturalny...
Ałuny to ciekawa grupa soli podwójnych - a więc takich które zawierają jeden tylko rodzaj anionu kwasowego ale dwa rodzaje mogących się z nimi połączyć kationów. W zasadzie więc jest to mieszanina dwóch soli, jednak ałuny wyróżniają się tu szczególną cechą - po zmieszaniu nie da się oddzielić (klasycznymi metodami) jednej soli od drugiej, jakby tworzyły jeden związek. Wszystkie ałuny są siarczanami - a więc zawierają aniony siarczanowe VI dwu-ujemne - zaś kationy są różne, jeden (A) jednowartościowy, drugi (B) trójwartościowy. Obie sole składowe tworzą kryształy tego samego typu i mają podobną rozpuszczalność, dlatego gdy odparowujemy roztwór ałunu otrzymujemy kryształ mieszany w którego węzłach na przemian pojawia się kation A i kation B; ogólny wzór takich związków wygląda zatem:
AB(III) (SO4)2 * 12 H2O
Na każdy mol soli podwójnej przypada średnio 12 moli wody, zależy to jednak od związku, w niektórych stosunek wynosi 1:6 a w innych nawet 1:24. .
Kationem jednowartościowym może być metal alkaliczny, na przykład potas lub sód, ale także kation amonowy a nawet organiczne kationy trimetyloamioniowe czy hydrazynowe. Kationem trójwartościowym jest najczęściej glin, możliwy jest też gal, chrom, tytan czy żelazo. Bardzo podobne związki tworzą seleniany, nazywane selene-alum co można by przetransponować na Polski jako "selałun". Istnieje zatem bardzo duża liczba kombinacji. Niekiedy błędnie do ałunów zalicza się sól Mohra.Ałuny łatwo krystalizują tworząc przezroczyste kryształy, czasem zabarwione jeśli zawierają odpowiedni kation - ałun żelazowo-potasowy jest pomarańczowy a chromowo-potasowy fioletowy niczym ametyst. Dlatego jeśli szukacie dobrego materiału do zrobienia sobie kryształków, to oprócz polecanego przeze mnie kwasku cytrynowego możecie użyć ałunu. Ponieważ wszystkie ałuny krystalizują tak samo wykazując idealny izomorfizm, różne ich odmiany mogą krystalizować na sobie - Sękowski w jednej z książek proponował krystalizację w której rosnący zarodek był co kilka godzin przekładany z jednego roztworu do drugiego, i zależnie od użytych soli, po przecięciu kryształka i wyszlifowaniu przełomu pokazywał się wzór warstewek zielono-fioletowych, lub fioletowo-bezbarwnych. Jeszcze tego nie próbowałem ale kiedyś będę musiał.
Ałuny były znane już w starożytności, ich nazwa pochodzi od greckiego słowa "alum" oznaczającego cierpki smak. Były używane w farbiarstwie, ułatwiały bowiem związanie barwnika z tkaniną, a także w garbarstwie do wyprawiania skór. Znamy też zapisy mówiące o użyciu ałunu do impregnacji drewna, na przykład palisad lub dachów twierdz, dzięki któremu stawały się trudnopalne.
Najstarsze wzmianki sugerujące iż znano wówczas tą sól - choć nie została wymieniona z nazwy - pochodzą z Egiptu aż z 2 tysiąclecia p.n.e., w babilońskich tabliczkach glinowych jest wymieniana ok. XVIII-XVI wieku p.n.e. Szerszy opis podaje Piliniusz w Historii naturalnej, wymieniając kilka rodzajów ałunów. Głównym źródłem pozostawał Egipt, gdzie wydobywano złoża z wyschniętych okresowych jezior, w pewnym stopniu pozyskiwano go z ałunitu i skorupiastych wystąpień naskalnych
Znajdowała szerokie zastosowanie w średniowiecznej europie, będąc często składnikiem leków i kosmetyków. Arabowie wprowadzili go do alchemii. Duże złoża odkryto w Azji, głównie na pustyniach, inne odkryto w Hiszpanii. Przez pewien czas Anglia była pozbawiona tego surowca z powodu embarga nałożonego po aferze z Henrykiem XVIII, produkowano go wówczas z łupków i ludzkiego moczu. [1]
Jakoś tak się jednak stało że dopiero na początku XIX wieku zaczęto się domyślać, że ałuny są solami zawierającymi nie znany pierwiastek metaliczny, nazwany od nich właśnie Aluminium. Polska nazwa "glin" pochodzi od gliny w której występuje bardzo często.
Jeśli chodzi o zastosowanie jako dezodorant to prawdopodobnie po raz pierwszy użyto go w tym celu w Starożytności - znajdujemy luźne wzmianki o kamieniach na brzydki zapach i zapewne chodziło o tą sól. Działanie mają tutaj przede wszystkim sole glinu to zaś z dwóch powodów - z jednej strony działają bakteriobójczo, a więc zabijają bakterie, które rozkładając składniki potu nadają mu charakterystyczny zapach, z drugiej zaś mają działanie ściągające, zatem zmniejszają pory skóry a tym samym potliwość. Stosowany często w kosmetykach hydroksychlorek glinu hydrolizuje po rozpuszczeniu, zatykając gruczoły potowe i uniemożliwiając pocenie; podobne działanie ma hydroksochlorek glinowo-cyrkonowy. Oba te związki a dokładnie powstające z nich osady wodorotlenków zostawiają na ubraniu białe plamy. Niekiedy stosuje się sole organiczne, jak kompleks z glicyną.
Działanie dezodoryzujące ałunów wynika z obecności w nich glinu i opiera się głównie na zabijaniu wspomnianych bakterii, natomiast wpływ na potliwość jest nie wielki. Sam mam taki sztyft ale nie używam go często, zrobiłem jednak kilka eksperymentów, na przykład smarując nim jedną pachę i porównując zapach w ciągu dnia. Zauważalne było osłabienie zapadu ale nie było całkowite. Zresztą nie należę do osobników o szczególnie śmierdzącym pocie, więc dla mnie różnica była niewielka. Różnicy w potliwości nie zauważyłem. Co do czasu działania - przy normalnej pogodzie starcza na cały dzień, w upały zmywa się po kilku godzinach.
Sądząc z opinii użytkowników o ile większość jest zachwycona, to jednak niektórym nie pomaga, ci o dużej potliwości narzekają że przestaje działać po paru godzinach, bo zwyczajnie się zmywa. Niektórzy donoszą też o podrażnieniach, nawet bardzo dokuczliwych - pamiętajmy że pewien procent ludzkości jest uczulony na glin w każdej postaci.W szczególnych przypadkach oprócz podrażnień stosowanie ałunu może prowadzić do zapalenia skóry - notowano takie sytuacje[2] Warto też pamiętać że podrażnia tkanki, więc lepiej nie dotykać nim ust i uważać aby nie dostał się do oka. Ałun ścina białko i koaguluje krew - dawniej w czasach brzytew normą było posiadanie "kamyków do golenia" czy pałeczek ałunowych, którymi tamowano skaleczenia. Miałem okazję to sprawdzić - działa ale okropnie piecze.
Biodostępność glinu przez skórę pach oceniono na 0,012% - dla porównania biodostępność z wodą pitną to 0,3% [3]
[Dopisek 2015: komentujący zwrócił moją uwagę na jeszcze jedno miejsce gdzie jest użyty ałun - chodzi o ayurwedyjski proszek do zębów Vicco Vajradanti który ma w składzie ałun, co tłumaczy dlaczego powstrzymuje krwawienia dziąseł. W takim użyciu, ałun rozpuszczony w ślinie styka się z błonami śluzowymi i ma dużo większą szansę być wchłoniętym do organizmu niż w przypadku naniesienia na skórę. W zasadzie to tak jakby połknąć. Sprawdzałem pod tym kątem inne proszki i pasty ale często, zwłaszcza te indyjskie, nie mają pełnego składu. Ałun zawiera jeszcze chyba proszek na krwawiące dziąsła Gum Tone]
Bez aluminium
Aluminium i glin to to samo. Używane w sztyftach związki to ałun glinowo-potasowy lub glinowo-amonowy. Zatem kryształ na pot zawiera aluminium i to całkiem sporo. Mimo to wciąż natykam się na opisy, najczęściej na stronach promujących "naturalne" i "organiczne" kosmetyki ze stwierdzeniem, że akurat ten go nie zawiera. Czasem jednak ktoś pójdzie po rozum do głowy i zajrzy na skład, gdzie zobaczy łacińską nazwę alum ammonium, nabierając w tej sprawie podejrzeń. Gdy zaczyna szukać czegoś na ten temat, być może znajdzie stronę firmy NajMar, polskiego producenta, a tam w dziale FAQ taki uroczy fragment:
W składzie jest: ammonium alum. Czy to oznacza aluminium?Fragment jest uroczy bo dokładnie odpowiada na pytanie. Czy Alum w nazwie to aluminium? - nie to angielska nazwa ałunu. Natomiast o tym że kosmetyk aluminium jednak zawiera producent nie zająknął się w ani fragmencie, a ten kawałek może zmylić wielu poszukujących sugerując, że nie zwiera. Jeszcze dalej idzie producent "Crystal Body Deodorant" który w polskojęzycznych nalepkach zapewnia, że jego produkt nie zawiera soli Al, co jest już oczywistym fałszerstwem.
- Nie. Nazwy składników należy podawać w języku angielskim. Przetłumaczenie nazwy polskiej jedynego składnika: amonowy ałun, znacza po angielsku: ammonium alum.
Na dobrą sprawę producent Deo Kryształu nigdzie o tym nie pisze a jednak jakoś ciągle natykam się na teksty w których takie absurdalne stwierdzenie się pojawia, co pewnie jest skutkiem niewiedzy. Zapewne przyczynia się do tego omawiany już schemat myślowy "chemiczne-sztuczne-szkodliwe / naturalne-zdrowe". Jeśli aluminium jest szkodliwe, to jest chemiczne i pojawia się w sztucznych kosmetykach, więc jeśli jakiś kosmetyk jest naturalny, to tego sztucznego aluminium nie zawiera.
Czasem jednak ktoś poczyta dokładniej i dowie się, że ten metal w ałunie amonowym także jest zawarty. I czy teraz należy odrzucić cały produkt? Przecież jest zachwalany jako naturalny, więc to musi być różnica. W efekcie pojawiają się czasem objaśnienia - ałun naturalny ma naturalną strukturę krystaliczną, więc nie jest wchłaniany; albo że to są naturalne cząsteczki które są duże, i nie wnikają w skórę. Tak tłumaczy to Alepia, jeden z producentów. Niestety, ałun naturalny to siarczan amonowo-glinowy a ałun syntetyczny to siarczan amonowo-glinowy, czyli dokładnie to samo. Jak niby struktura krystaliczna ma wpływać na wnikanie w skórę nie wiem, a zważywszy że ta "unikalna struktura" musi się najpierw podczas aplikacji rozpuścić w wodzie i ulec rozpadowi na jony, raczej wpływu to nie ma żadnego.
Różnica owszem jest, ale nikt na to nie wpadł - skóra z reguły jest tłusta i nieprzepuszczalna dla jonowych soli nieorganicznych. Jeśli posmarujemy się solanką nie wchłoniemy chloru, ale gdy użyjemy w tym celu chloroformu szybko zacznie się nam kręcić w głowie. Polarne rozpuszcza się w polarnym a niepolarne, w niepolarnym - proste.
Mimo to natknąłem się na badanie wskazujące, że sole glinu - konkretnie chlorek - mogą być wchłaniane przez skórę. Co prawda badanie dotyczyło ogolonej myszy a efekty stały się wyraźne po czterech miesiącach, ale zawsze jest to wskazówka że jakieś wchłanianie nieorganicznego glinu zachodzi i tak[4]
Naturalny
Naturalność sztyftu jest jego główną zaletą. W każdym razie sądząc z opinii, wiele osób kupiło go właśnie dlatego. Ałuny jak łatwo się domyśleć z powyższych rozważań, występują w przyrodzie. Ałun glinowo-potasowy jest najpospolitszy, nieco rzadszy jest ałun glinowo-sodowy. Natomiast ałun glinowo-amonowy to bardzo rzadki minerał.
Jony amonowe powstają w przyrodzie wskutek gnicia materii organicznej jednak ich żywot jest raczej krótki, bo albo są utleniane albo w zasadowym środowisku zamieniają się w lotny amoniak, dlatego nie zbyt dużo jest minerałów które go zawierają, pojawiają się głównie w okolicy otworów hydrotermalnych oraz w pobliżu szczelin którymi ulatują gazy z podziemnych pożarów węgla. Zatem ałun amonowy, występujący w formie Tschermigitu, nie może występować w dużych złożach. Stanowiło to dla mnie pierwszy zgrzyt.
Jeśli sztyfty robi się z minerału który jest rzadki, a sądząc z ilości ofert, produkuje się je na skalę masową, to chyba powinny być bardzo drogie?
Anglo i hiszpańskojęzyczne strony piszą zwykle, że ałun w tych sztyftach pochodzi z Tajlandii i jest wydobywany "z wygasłego wulkanu", zacząłem zatem szukać informacji na temat złóż Tschermigitu (Czermigit) w tamtym kraju i nie znalazłem, dopiero wzmianka o skale z której przerobu uzyskuje się ałun[5] rozjaśniła sytuację. W Tajlandii w skałach wulkanicznych znajdują się całkiem spore złoża Ałunitu - skały będącej hydroksysiarczanem glinowo-potasowym będącej efektem wietrzenia trachitu. Z niego właśnie otrzymuje się ałun - skałę należy rozkruszyć, pogotować z kwasem siarkowym i wykrystalizować gotowy związek - związkiem tym będzie oczywiście ałun glinowo-potasowy.
A amoniak? Jak widać w tym minerale nie występuje, dlatego aby otrzymać sól amonową należy dodać do roztworu siarczan amonu. Tan akurat jest łatwy do zdobycia - jest ubocznym produktem przy produkcji kaprolaktamu i powstaje go tak dużo, że zakłady szukają pomysłów gdzie go tylko zbyć. A więc łączymy przesącz z ałunitu rozgotowanego w kwasie z odpadowym siarczanem amonu, zagęszczamy i otrzymujemy kryształy zbijające się w jednolitą masę z której można wycinać bloki, pałeczki i sztfty.
Jak zatem widać wszystko wskazuje na to, że dostępny na rynku ałun amonowy jest o tyle tylko naturalny, że jeden z jego składników kiedyś widział jakąś skałę. Powstaje w związku z tym pytanie, czy aby reklamowanie go jako naturalnego minerału nie jest aby wprowadzaniem konsumentów w błąd?
Rzecz zresztą wyłapała konkurencja - producenci sztyftów z ałunem potasowym zaczynają pisać w reklamach, że w odróżnieniu od syntetycznej soli amonowej ich produkt jest naturalniejszy - co niekoniecznie musi być prawdą.
Ogółem zatem - sztyfty ałunowe działają jeśli chodzi o zapobieganie powstawaniu przykrych zapachów, są pozbawione dodatków i dlatego dla wielu osób mogą być idealnym rozwiązaniem, zawsze jednak byłem za ty, aby wybierać z głową i wiedzą. Jeśli ktoś wybrał ałun bo jest naturalny i bo nie zawiera aluminium, to się przejechał. Kupujący powinien wiedzieć wszystko o tym co mu wciskają i powinien sobie rozważyć, czy chce się zdecydować na dany produkt.
Tymczasem producenci robią wszystko co się da aby stworzyć ludziom w głowach fałszywy obraz, całkiem pomijając kwestię składu. I choć produkt działa, nie są to działania uczciwe. Nie informowanie o składzie i sugerowanie różnymi sztuczkami że produkt nie zawiera aluminium to chwyt nie zbyt chwalebny, natomiast oszukiwanie tak jak producent "Crystal Body Deodorant" w polskich etykietkach, zasługuje już na zgłoszenie do urzędu ochrony konsumenta. Coś podobnego pojawia się na ałunach serii N& B.
ps. 11.03.13
Ponieważ od tej publikacji dostałem kilka e-maili od ludzi, czujących się oszukanymi, bo po reklamach sądzili że ałuny są całkiem innymi preparatami, postanowiłem działać - wysłałem do UOKiK list z zauważonymi nieprawidłowościami. Co oni z tym zrobią to się zobaczy - najpierw muszą rozpatrzyć czy sprawa leży w ich kompetencjach i zrobić kontrole w sklepach. Jakby coś do mnie przysłali, to poinformuję.
ps. 2014
Ponieważ reakcji brak, wysyłam zapytanie do Rossmanna czy wiedzą że źle oznakowali sprzedawany kosmetyk. Zobaczymy co odpowie.
kwiecień 2014
Odpisali że przekażą uwagi producentowi odpowiedzialnemu za rozprowadzanie. Teraz poczekam - jeśli za kilka miesięcy nowe partie dalej będą zawierały błędną informację, to zainteresuję tym jakąś gazetę.
Listopad 2014
Mały sukces - nowe partie sztyftów ałunowych mają zmienioną etykietkę. Zamiast twierdzeń iż nie zawierają aluminium, jest tylko "nie zawiera aluminium chlorohydrate" - czyli z jednej strony usunęli wprowadzający w błąd napis ale z drugiej strony zdecydowali się nie tłumaczyć na polski nazwy związku. Teraz tylko pozostaje sprawić, aby opis zmienił się w internetowych sklepach, gdzie stara wersja nadal funkcjonuje i wprowadza w błąd.
-----
[2] Gallego H, Lewis EJ, & Crutchfield CE 3rd (1999). Crystal deodorant dermatitis: irritant dermatitis to alum-containing deodorant. Cutis; cutaneous medicine for the practitioner, 64 (1), 65-6 PMID: 10431678
[3] Yokel RA, & McNamara PJ (2001). Aluminium toxicokinetics: an updated minireview. Pharmacology & toxicology, 88 (4), 159-67 PMID: 11322172
[4] Anane R, Bonini M, Grafeille JM, & Creppy EE (1995). Bioaccumulation of water soluble aluminium chloride in the hippocampus after transdermal uptake in mice. Archives of toxicology, 69 (8), 568-71 PMID: 8534202
[5] http://www.alliumherbal.com/es/articulos/43-cosmetica-belleza-natural/410-piedra-de-alumbre.html
Subskrybuj:
Komentarze (Atom)