informacje
środa, 28 czerwca 2023
Chemiczne wieści (28.)
piątek, 24 grudnia 2021
Mulisty smak karpia, ziemisty barszczyk i zapach jak po deszczu
Gdy już zasiądniecie do wigilijnej kolacji, przełamiecie się opłatkiem i zabierzecie się za pałaszowanie dwunastu dań, to wówczas być może niektórych z was zastanowi jedna rzecz, o jakiej nie było mówione w szkole. Jeśli nawet dobrze obczyszczony karp smakuje trochę mułem z dna stawu, to czym właściwie smakuje?
Choć zapach jaki wydziela gleba, i jaki wydziela się z mulistych osadów, był znany od zarania dziejów, pierwsze badania na ten temat pojawiły się dopiero w XIX wieku, gdy to postanowiono sprawdzić co odpowiada za ten przyjemny zapach, jaki powstaje na początku deszczu, zwłaszcza po kilku dniach suchych. Po destylacji z parą wodną dużej ilości gleby odzyskano olejek eteryczny, składający się głównie z prostych terpenoidów. Wbrew oczekiwaniom nie pochodziły one z roślin, lecz były wytwarzane przez bakterie żyjące w glebie i wodzie.
Wszystkich produktów rozkładu roślin i metabolizmu bakterii jest bardzo wiele, ale w większości gleb i wód decydujące znaczenie mają dwa składniki występujące najczęściej - geosmina i 2-metyloizoborneol (MIB). Są to proste terpenoidy, które w czystej postaci są oleistymi cieczami, rozpuszczalnymi dobrze w tłuszczach a słabo w wodzie. Ludzki nos jest jednak mimo to bardzo silnie wyczulony na ich zapach, wyczuwając go nawet w stężeniu 400 części na milion.
Substancje te są jednymi z ubocznych metabolitów licznych gatunków bakterii. Geosminę wytwarzają głównie cyjanobakterie, będące organizmami fotosyntezującymi, występującymi głównie w wodach powierzchniowych i w wierzchniej warstwie wilgotnej gleby. Jej stężenie rośnie podczas zakwitów glonów i sinic. MIB wytwarzają także cyjanobakterie, ale ponadto też bakterie Streptomyces, znane jako glebowe patogeny roślin wywołujące choroby korzeni, na przykład gnicie bulw ziemniaków. Z warzyw, które mogą pochłaniać geosminę w trakcie wzrostu, często staje się wyczuwalna w korzeniach czerwonego buraka. W tym przypadku ziemisty zapach nie musi oznaczać porażenia przez bakterie.
Nie więc zaskakujące, że jesteśmy tak wyczuleni na ziemisty zapach - bakterie wytwarzające te związki mogą też tworzyć toksyny oraz być chorobotwórcze. Dlatego ewolucja przystosowała nas do wyczuwania, że jedzenie zostało skażone ziemią lub brudną wodą. Tego, że zechcemy zjadać rybę wylegującą się w mule, chyba nie przewidziała.
Związki te dość dobrze rozpuszczają się w tłuszczach, toteż tłuste ryby będą je akumulowały. Badano to już dla różnych gatunków. Jeśli woda w stawie zawierała geosminę lub MIB to w ciągu kilku dni ryba nabierała pewnego wyczuwalnego stężenia. Bakterie i glony nie musiały być przez rybę zjadane, wystarczył kontakt z wodą.
Jak sobie z nimi poradzić?
Najlepiej kupić ryby o dobrym smaku. Stężenie geosminy w rybie bardzo mocno zależy od wody w stawie, a jej jakość od gleby w jakiej staw był wykopany. Im bardziej torfiasta i zasobna w próchnicę gleba, tym więcej geosminy było w wodzie i w rybach. Częściowo można na to wpływać manipulując odczynem wody i warunkami natlenienia. Najważniejszym jednak sposobem usuwania niepożądanych zapachów, używanym na świecie też do małży i omułków, jest "płukanie" - umieszczenie żywej ryby w wodzie czystej. Rozkład geosminy i MIB w rybie następuje dość szybko, zwykle wystarczą dwa dni aby zapach stał się akceptowany. Im bardziej tłusta ryba tym wolniej to następuje.
A jeśli mamy już gotowa, ubitą rybę i podczas oprawiania wyszło, że wyjątkowo ten osobnik daje mułem trochę za mocno? Cóż, sprawdza się tu stara, dobra formuła - przyrządzić rybę w kwaśnej zalewie. Ma to podstawy naukowe. Zarówno geosmina jak i MIB ulegają w kwaśnych warunkach rozkładowi. Produkty rozkładu są bezwonne lub mają zapach kamforowo-żywiczny, ale dużo słabiej wyczuwalne. W publikacji badającej wpływ różnych kwasów na substancje w wodzie stwierdzono, że kwas cytrynowy rozkłada je łatwiej i w mniejszych stężeniach niż ocet. Wydaje się, że wynika to stąd, że jego roztwory są po prostu bardziej kwaśne. Bardzo łatwo rozkładał się metyloizoborneol, już od niewielkich dodatków kwasu. Geosmina była na rozkład bardziej oporna. [1]
Mogłoby to tłumaczyć czemu sposoby zmniejszania woni ryby czasem działają dobrze a czasem nie za bardzo. Ilości tych substancji w rybie mogą być różne, zależnie od warunków w stawie. Jeśli w karpiu dominuje MIB, to już niewiele soku z cytryny wystarczy aby zapach się zmniejszył. Jeśli dominuje geosmina, to kwasu potrzeba więcej. Ponadto im bardziej tłusta jest ryba, tym trudniej zachodzi rozkład, bo tkanka jest wolniej przenikana prze rozpuszczony w wodzie kwas. Stąd w jednym roku tak samo przyrządzony karp będzie smakował inaczej niż udało się w poprzednim roku.
------
[1] https://www.researchgate.net/publication/275954147_Reduction_of_off-flavour_compounds_geosmin_and_2-methylisoborneol_using_different_organic_acids
https://journals.asm.org/doi/10.1128/AEM.02250-06
poniedziałek, 30 listopada 2020
Obrzydliwa chemia (1.)
Czyli wszystko to co was kiedyś zaciekawiło na lekcjach chemii, ale wstydziliście się zapytać.
Skąd smród wymiocin?
Zapach wymiocin w dużej mierze wiąże się ze składem jedzenia - posiłki z reguły zawierają mniejsze lub większe ilości tłuszczy, te zaś stanowią połączenie kwasów tłuszczowych z gliceryną. Kwasy tłuszczowe, gdy mają długą cząsteczkę, mają postać woskowatych ciał o niewyczuwalnym zapachu, czego przykładem stearyna, to jest kwas stearynowy zawierający 17-węglowy łańcuch. Inaczej jest gdy kwasy są krótkie - stają się wówczas łatwo krzepnącymi cieczami o charakterystycznym zapachu. Najkrótsze, to jest mrówkowy, octowy i propionowy mają zapach kwaśny, ale począwszy od masłowego (4 węgle), ich wonie stają się coraz bardziej nieprzyjemne.
Kwas masłowy, jak sugeruje nazwa, jest tym który powoduje niemiły zapach zjełczałego masła, dłuższe od niego kwasy kapronowy, kaprylowy i kaprynowy, zostały nazwane od kozy i odpowiadają za zapach kozła i koziego mleka.
Skąd wolne kwasy tłuszczowe w zawartości żołądka?
Już podczas przeżuwania pokarmu, miesza się on ze śliną zwierającą lipazy, trawiące tłuszcze. Pewne znaczenie ma też lipaza żołądkowa. W wyniku ich działania część kwasów tłuszczowych zostaje uwolniona do treści żołądka. Gdy zaś w wyniku skurczu żołądka jego treść zostanie uwolniona do otoczenia, woń tych kwasów staje się zauważalna. Pewne znaczenie mogą tu mieć też wolne aminokwasy i aminy.
Zapach wymiocin wywołuje obrzydzenie u innych ludzi, do tego stopnia iż może wywołać wymioty. Podobny efekt wywołuje widok wymiotującej osoby a czasem nawet sam odgłos. W szczególnych przypadkach może to doprowadzić do wymiotów większą ilość zdrowych osób, a nawet przerodzić się w masowa histerię. Uważa się, że jest to zjawisko adaptacyjne - reakcja wymiotna na widok innej wymiotującej osoby miała w dawnych małych społecznościach ułatwić pozbycie się zatrutego jedzenia i uniknięcie choroby.
Mdłości pojawiają się także podczas ciąży. Niekiedy pojawia się wręcz niezdrowa nadwrażliwość na niektóre bodźce i do wymiotów skłonić mogą zapachy i skojarzenia normalnie neutralne, utrudniając ważne przecież w tym okresie odżywianie. W niedawnym badaniu z Malezji stwierdzono, że w takim przypadku najskuteczniejszym prowokatorem mdłości są ryby i smak gorzki, produkty o konsystencji ciastowatej, smażone, z konkretnych dań gotowany ryż. Najlepiej badane znosiły jedzenie chrupkie, słodkie i surowe, na przykład jabłko lub arbuza. [n]
Kwas masłowy bywa używany w bombach zapachowych oprócz merkaptanów.
Na koniec kwestia z którą się często spotykam - jak usunąć zapach wymiocin? Kwasy tłuszczowe słabo rozpuszczają się w wodzie, ale dobrze gdy są w formie jonowej. Ponieważ są słabymi kwasami, aby je w taką formę przeprowadzić należy użyć zasady. Wydaje się więc, że do czyszczenia zanieczyszczonych powierzchni powinno się używać alkalicznych środków czyszczących lub na przykład sody.
Czym śmierdzi gówno?
Przemiany metaboliczne zasadniczo mają za zadanie rozłożyć na czynniki prostsze to co można wykorzystać i wbudować, oraz usunąć to co niepotrzebne. Czasem jednak drogi przemian biochemicznych prowadzą w nieoczekiwaną stronę. Na przykład pewien niezbędny aminokwas tryptofan jest w części utleniany i przerabiany 3-metyloindol, nazywany też skatolem i wydalany z kałem. Związek ten w dużych ilościach ma swój charakterystyczny, nieprzyjemny zapach, jednak w małych stężeniach woń staje się słodkawa. W niewielkich ilościach występuje w olejkach eterycznych z kwiatu pomarańczy i jaśminu chińskiego, i bywa używany w perfumach jako wzmacniacz zapachu.
Odpowiada też za niemiły zapach mięsa niekastrowanych wieprzy i dzików. Ponieważ tryptofan najobficiej występuje w białku mleka i wieprzowinie, zaś najrzadziej w produktach zbożowych, łatwo się domyśleć, że zapach kału w dużej mierze zależy od diety.
Pewien wpływ ma też jeszcze bardziej skrócona pochodna tryptofanu - indol. Udział w przerobie aminokwasu do tego produktu mają enterobakterie zasiedlające wnętrze naszych jelit. Związek ten w dużych stężeniach ma woń nieprzyjemną, choć słabiej wyczuwalną niż w przypadku skatolu. W małych natomiast stężeniach nabiera miłego fiołkowego zapachu i jest istotnym składnikiem (ok. 2%) zapachu jaśminu, stąd też indol jest używany do produkcji sztucznych aromatów jaśminowych. Oczywiście nie izoluje się go do tych celów z odchodów, ale syntezuje za pomocą którejś z kilkunastu popularnych metod.
Do tych wyrazistych związków dokładają się merkaptany będące wynikiem przerobu aminokwasów zawierających siarkę.
Kolor kupy, sików i siniaków
W tym przypadku wszystko zaczyna się od krwi. Krwinki czerwone zawierające niezbędny do zaopatrywania organizmu w tlen barwnik hemoglobinę, mają pewien skończony czas życia, i po jego przekroczeniu lub po uszkodzeniu, są wyłapywane przez śledzionę zajmującą się ich bezpieczną utylizacją.
Hemoglobina składa się z białka globiny i aktywnej cząsteczki hemu, mogącej kompleksować tlen. Składa się z dość dużego pierścienia w kształcie z grubsza kwadratowym, z czterema azotami pośrodku, trzymającymi w kleszczach atom żelaza.
Pierwszym etapem rozpadu jest oderwanie żelaza i białka i rozerwanie pierścienia w jednym miejscu. Tak powstaje u-kształtna zielona biliwerdyna. Ta szybko jest redukowana i po odgięciu cząsteczki zamienia się w żółtą bilirubinę. Ponieważ wolna bilirubina jest słabo rozpuszczalna w wodzie a stosunkowo dobrze w tłuszczach i wobec nadmiaru, nazywanego żółtaczką, ma skłonność do gromadzenia się w skórze i mózgu, gdzie jest toksyczna, toteż organizm stara się tak ją przerobić, aby móc ją łatwo wydalić. Odbywa się to w wątrobie.
Wątroba sprzęga bilirubinę z kwasem glukuronowym, dzięki czemu całość staje się rozpuszczalna w wodzie, i dodaje tak powstałe połączenie do żółci, skąd też bierze się jej barwa. Żółć trafia do jelita a pochodna bilirubiny jest przerabiana przez bakterie jelitowe. Część, pod postacią urobilinogenu jest wchłaniana i wydalana z moczem, nadając mu żółtą barwę, a reszta jest utleniana i zamienia się w ciemnobrązową sterkobilinę, która zabarwia sami wiecie co.
Podczas żółtaczki związanej z niewydolnością wątroby proces usuwania bilirubiny z ustroju jest zaburzony. Gromadzi się ona w tkance łącznej i zabarwia skórą oraz białka oczu. Bardzo niewiele jest wydalane do jelit z żółcią, stąd kał nabiera szarego koloru.
Bardzo podobne przemiany mają miejsce w podskórnych wylewach krwi. Najpierw czerwona krew jest odtlenowana i staje się sino-niebieska, potem tworzy się biliwerdyna i stąd zielone przebarwienia. Dalszy rozpad do bilirubiny następuje gdy już siniaki się wchłaniają, dając nam okazję naocznie prześledzić opisane wyżej przemiany.
Kolor moczu może być zaburzony pod wpływem różnych czynników. W stosunkowo częstej betaninurii nieprzetrawiony wskutek niskiej aktywności soku żołądkowego czerwony barwnik buraka, zabarwia go na czerwono, wywołując efekt podobny do krwawienia. Na czerwono zabarwia się wówczas także kał. W podobny sposób mocz zabarwiają też inne silne barwniki - pamiętam że w sklepach ze śmiesznymi rzeczami można było kupić specjalne cukierki, które zabarwiały mocz poczęstowanych na różne kolory, jednym z takich barwników jest błękitny indygokarmin, na tyle chętnie wydalany tą drogą że czasem używa się go do badań czynności nerek. Efekt taki dawać mogą niektóre leki.
Na niebiesko przebarwiać może błękit metylenowy spotykany w niektórych lekach. Połączenie niewielkich ilości niebieskich barwników z żółtym kolorem własnym zwykle daje zieleń. Oprócz tego na zielono może zabarwić nasz mocz amitryptylina, propofol oraz szparagi.
Na pomarańczowo może zabarwiać duża ilość ryboflawiny, także lek przeciwgruźliczy izoniazyd i fenazopirydyna używana w infekcjach dróg moczowych. W pewnym stopniu też dieta obfitująca w marchewkę.
Istnieją też dwa szczególne stany chorobowe, które mogą wywoływać wrażenie zmiany koloru moczu. W "zespole niebieskich pieluszek" genetyczna mutacja powoduje zaburzenie wchłaniania tryptofanu, który gromadząc się w jelitach jest przerabiany na pochodne indolowe. Jedną z nich jest izatyna, która wchłonięta wydala się wraz z moczem, a po kontakcie z powietrzem utlenia się i dimeryzuje tworząc niebieski barwnik indygo. Ponieważ choroba ujawnia się już w okresie niemowlęcym, oznaką wystąpienia jest zazwyczaj niebieskie zabarwienie pieluszek.
Z kolei "zespół purpurowych worków na mocz" występuje u osób z założonymi cewnikami, w których na powierzchni cewnika pojawiają się bakterie. Będący produktem przerobu indolu siarczan indoksylu wydalany wraz z moczem, jest przerabiany i utleniany przez bakterie, z wytworzeniem niebieskiego indygo i czerwonej indirubiny. Sam w sobie nie wywołuje dolegliwości ale jest oznaką dużego ryzyka zakażenia dróg moczowych.
---------
[n] https://www.nature.com/articles/s41598-020-61114-y
piątek, 28 sierpnia 2020
Jak sprawdzić kurkumę?
Kurkuma to często używana przyprawa azjatycka, będąca składnikiem żółtego curry, ale też używana samodzielnie. Nadaje potrawom żółty kolor, lekko pikantny smak, może tylko zapach nie każdemu odpowiada. Wraz ze światową popularnością pojawiają się jednak problemy - bywa na różne sposoby fałszowana. Najpopularniejsza jak mi mówiono metoda, to chrzczenie mączką ryżową. Jeśli jest zmielona na drobny pył, to ziarenka skrobi zabarwią się od niej i ciężko je będzie wyłapać. Może tylko odcień stanie się jaśniejszy.
To jednak nie koniec. W zeszłym roku media doniosły o badaniach, z których wynikało, że mocno rozcieńczona innymi wypełniaczami kurkuma bywa podbarwiana różnymi innymi substancjami o podobnym kolorze.[1] Na przykład pigmentem chromianem ołowiu, który nie jest zbyt zdrowym zamiennikiem. Ponieważ sprawa zrobiła się głośna, pojawiły się propozycje testów na wykrycie fałszerstwa. Niektóre niestety są bałamutne i służą tylko nastraszeniu.
Jedną z porad jakie znajduję jest sprawdzenie zmiany barwy pod wpływem zasadowego środowiska. Chromian ołowiu w warunkach alkalicznych ulega przemianom do związków czerwono-brunatnych. Główny problem z tym testem jest taki, że substancja barwiąca przyprawy, kurkumina, także reaguje na zmiany odczynu. I w zasadowym robi się... czerwona.
 |
| Kurkuma potraktowana wodorotlenkiem sodu |
W istocie więc tak wykonany test jedynie nas nastraszy, bo każda próbka kurkumy zmieni kolor.
Zastanawiałem się zatem nad tym czy jest jakiś test na tyle prosty, że można go wykonać w domu nie posiadając specjalnych odczynników. I po kilku próbach stwierdziłem, że dobry rezultat daje ten najbardziej oczywisty - usunięcie żółtej kurkuminy w sposób, który nie rusza szkodliwego pigmentu. Kurkumina jest słabo rozpuszczalna w wodzie, natomiast dość dobrze w alkoholu i acetonie. Z kolei chromian ołowiu jest nierozpuszczalny zarówno w wodzie jak i tych rozpuszczalnikach.
Sposób przetestowałem na próbce kurkumy dobrej jakości - wziąłem kłącze kurkumy w kawałkach. Ciężko wprowadzić nierozpuszczalny pigment do wnętrza kawałka kłącza. W znanych przypadkach zafałszowania korzenie były pokrywane pigmentem z wierzchu. Często bowiem podczas suszenia i przechowywania kawałki korzenia z wierzchu ciemnieją i brązowieją, mogą więc dla nie znającego tego surowca wyglądać nieapetycznie, toteż zabarwienie powierzchni nadaje mu bardziej atrakcyjny wygląd. Użyte w teście kawałki kłącza były szarawe.
Rozdrobniłem je w moździerzu na drobny proszek:
Po czym w małej zlewce zalałem ciepłym alkoholem. Po dokładnym rozmieszaniu odstawiłem naczynie, aby próbka opadła na dno i odlałem żółto zabarwiony roztwór. Po czym znów zalałem osad ciepłym alkoholem. Po trzech razach ostatecznie odsączyłem osad na sączku papierowym, który umieściłem na lejku i przemywałem małymi porcjami ciepłego alkoholu do zaniku zabarwienia odcieku. Użyłem dosłownie odrobinę, około 0,2-0,4g proszku, po to aby nie zużyć zbyt dużej ilości rozpuszczalnika.
Na sam koniec otrzymałem pozbawioną kurkuminy pulpę o jasnym, kremowym kolorze. Ciemniejsze cząstki okazały się kawałkami kory korzenia, ale pod lupą było widać, że i one nie są zabarwione na żółto. Wniosek - przynajmniej pigmentu chromianu ołowiu badana kurkuma nie zawierała. Zrobiłem więc test na kurkumie w proszku z opakowania przyprawy i efekt wyszedł taki sam.
Inne polecane testy są bardziej subiektywne i nie dotyczą wykrywania ołowiu. Przykładowo próba z z zimną wodą da nam najwyżej informację, czy nie dodano do niej mąki lub barwników rozpuszczalnych.
Łyżeczkę przyprawy wymieszać z szklanką zimnej wody i odstawić na 20 minut. Przyprawa powinna opaść na dno. Kurkumina jest na zimno słabo rozpuszczalna, więc roztwór nad osadem powinien być słabo zabarwiony, w zasadzie to zabarwia go drobny pył. Mocny kolor roztworu, zwłaszcza bardziej pomarańczowy niż sama przyprawa, może sugerować użycie syntetycznego barwnika spożywczego. Z kolei długo się utrzymująca jasna zawiesina może wskazywać na domieszkę mąki - ale poza przypadkami skrajnie złej jakości ciężko obiektywnie ocenić, czy wygląd roztworu to już ten podejrzany kolor i mętność, czy tylko efekt mocnego zmielenia z dużą ilością bardzo drobnego pyłu, który dłużej się utrzymuje. Wykrycie któregoś z tych rodzajów fałszerstw nie oznacza, że przyprawa zawiera ołów; może wręcz zmniejszać takie ryzyko, bo jeśli już farbowano ją syntetycznym barwnikiem, to toksyczny pigment staje się niepotrzebny.
Doniesienia z Indii podają, że tym często używanym barwnikiem spożywczym, którym fałszują też szafran, jest żółć metanilowa, barwnik azowy. Oprócz lepszej rozpuszczalności w wodzie można go zidentyfikować na podstawie zmian koloru w bardzo kwaśnych warunkach. Jeśli ktoś ma dostęp do trochę mocniejszych kwasów, na przykład 10% kwasu solnego, może sprawdzić czy zabarwiony roztwór znad kurkumy zmienia kolor z żółtego na czerwony. Dla żółci metanilowej następuje to poniżej pH 2.
A jak wykryć, że próbka przyprawy w ogóle zawiera kurkuminę a nie jest tylko farbowaną czymś innym mąką? Nie sądzę aby komuś coś takiego się trafiło, ale można się pobawić z pewną charakterystyczną reakcją. Proponuję zrobić alkoholowy roztwór jak w pierwszej opisanej próbie. Do niezbyt stężonego dodać roztwór kwasu borowego, łatwego do nabycia w aptece, jest łagodnym środkiem ściągającym i odkażającym skórę. Kurkumina zawiera w cząsteczce dwie grupy ketonowe lub alkoholowe blisko siebie. Związki o takiej budowie łatwo tworzą z kwasem borowym związek kompleksowy spiro-boran. W przypadku kurkuminy powstały kompleks, rozocyjanina, ma różowo-czerwony kolor, trwały też w warunkach lekko kwaśnych. W praktyce wykorzystuje się to do oznaczania kwasu borowego w wodzie; reakcja jest bardzo czuła.
 |
| Barwy kurkuminy - pośrodku roztwór alkoholowy. Po lewej pomarańczowy kompleks z kwasem borowym, po prawej czerwone zabarwienie w środowisku alkalicznym. |
 |
| Rozocyjanina |
Oczywiście ostatecznie jeśli mamy do przyprawy dużo wątpliwości lub mamy interes w tym aby kupiona kurkuma była dobrej jakości, to najlepiej wysłać próbkę do laboratorium analizy żywności.
-----
[1] https://foodfakty.pl/falszowanie-kurkumy-chromianem-olowiu
wtorek, 14 stycznia 2020
Ostatnio w laboratorium (73.)
Po odpowiednio długiej ekstrakcji, gdy wszystko co mogło zostało już wymyte, ekstrakt odparowuje się a pozostały tłuszcz waży, i tak voila! - mamy zawartość tłuszczu w próbce.
Niedawno w laboratorium robiłem tak z wiórkami kokosowymi, które okazały się tego tłuszczu zawierać całkiem sporo, i przy tej okazji zauważyłem ładny efekt. Gdy ciepłą kolbę z tłuszczem zostawiono na noc, stygnący powoli tłuszcz zestalił się tworząc kryształy. W samej masie wyglądało to jak ziarnista faktura, zupełnie różna od gładkiego, smalcowatego wyglądu stałych tłuszczów jaki zwykle obserwujemy. Z kolei w cienkiej warstwie rozprowadzonej na ściankach, pierzaste kryształy przybrały formę podobną do szronu na zalodzonej szybie.
poniedziałek, 12 sierpnia 2019
Wody i ich minerały
Woda mineralna, wedle dziś uznawanej definicji, to woda wydobywana z ujęć podziemnych, która jest naturalnie czystsza od zwykłej wody pitnej, oraz ma określony, stabilny skład. Nie będzie więc wodą mineralną ta uzdatniana, która płynie w naszych kranach, choć niekiedy parametry obu wód są podobne. Dawniej, na potrzeby działalności zakładów wodoleczniczych stosowano definicję, uznającą za wodę mineralną tylko taką, która ma powyżej 1g/l składników rozpuszczonych. Zawężało to ilość wód mineralnych do około 30.
Dziś wodą mineralną może więc zostać w zasadzie każda woda głębinowa o niezmiennym składzie i czystości, stąd też namnożyło się ich nam na rynku na prawdę sporo (ponad 130), i trudno zdecydować jaką wybrać.
Czy wody mineralne mogą być potraktowane jako dobre suplementy składników mineralnych? Niespecjalnie. Mimo wszystko w popularnych wodach składników mineralnych nie jest zbyt wiele. Wprawdzie najbardziej nawapniona woda mineralna, zawiera w litrze 1/4 zalecanej dziennej dawki Ca, ale przy spożyciu doustnym wchłanialność soli wapnia wynosi do 30%. Biorąc pod uwagę znaczne rozcieńczenie, próba uzupełnienia dobowej dawki wodą mineralną może być trudna, oraz prowadzić może do zwiększonego wypłukania tychże minerałów z moczem. Wody mineralne są najwyżej jednym z dodatkowych źródeł, ale główne zapotrzebowanie powinna zaspokajać po prostu żywność dobrej jakości i odpowiednio zróżnicowana.
Na podstawie kilku różnych źródeł postanowiłem podsumować informacje o tym, jaka woda zawiera najwięcej różnych jonów.
Wapń
Pierwiastek dość rozpowszechniony i w praktycznie każdej wodzie mineralnej jest obecny. Najwięcej z tych, które znalazłem, jest go w trudnej do zdobycia litewskiej wodzie Vytatuas, bo ponad 500 mg/l. Jest to woda generalnie dość słona, zawierająca przede wszystkim chlorek sodu. Z wód krajowych, łatwiej dostępnych w sklepach, najwięcej wapnia jest w Muszynie Minerale (456 mg/l), Kryniczance (436 mg/l) i Galicjance (415 mg/l)
Sód
Najczęściej występuje jako chlorek i wodorowęglan, stąd najwięcej jest go w wodach bardzo słonych i alkalicznych. Najzasobniejsza jest woda uzdrowiskowa Magdalena, zawierająca 8g/l Na. Następne w kolejce są wody Zuber (6,1g/l), Szczawa II (5,1) Szczawa I (4,8) Franciszek (3,8); z łatwiej dostępnych Wysowianka (0,39 g/l) czy Słotwinka (0,29g/l)
Jeśli chodzi o wody niskosodowe, zwykle bardzo mało sodu mają wody źródlane, na przykład Górska Natura podaje na etykiecie tylko 1 mg/l co jest chyba najniższą jeszcze podawaną wartością, niewiele więcej podaje Dobrowianka (2 mg/l) i Primavera (2,4 mg/l)
Potas
Ma właściwości podobne do sodu i zwykle występuje wraz z nim w różnej proporcji, nie będzie więc zaskoczeniem, że najzasobniejsza w ten pierwiastek jest woda Zuber (288 mg/l). Następne w rankingu to Szczawa I (208 mg/l), Hanna (104), Franciszek (90), a z szerzej dostępnych, słodkich Wielka Pieniawa (64), Polanicka Zdrój (38).
Magnez
Ze względu na podobieństwo do wapnia i niekiedy występowanie z nim w skałach, zwykle towarzyszy mu w alkalicznych szczawach, jednak wodą zawierającą go najwięcej jest u nas Zuber, która po prostu zawiera najwięcej wszystkiego, przez co jest wodą uzdrowiskową trudną do przełknięcia. Zawiera 363 mg/l magnezu. Następna w kolejce to nie taka łatwa do znalezienia woda Muszyńskie Zdroje, zawierająca 292 mg/l, oraz pojawiająca się w sklepach
Słotwinka (244 mg/l). Z wód bardziej popularnych, obfitym źródłem jest Muszynianka (135 mg/l) i Galicjanka (90 mg/l).
Dla porównania wody rozprowadzane przez wodociągi są zwykle miękkie lub lekko twarde i nie zawierają zbyt wiele magnezu. Z kilku badań które przeglądałem, najbardziej w magnez obfitowała woda z ujęcia w Dąbrowie Górniczej, zawierająca 48 mg/l. [d]
Fluorki
Obecność w wodzie fluorków zwykle wiąże się ze złożami fluorytu i fluoroapatytu, ale może też wynikać z obecności niektórych turmalinów. Zwykle pojawiają się w ujęciach podgórskich, z uwagi na bliskie podchodzenie pod powierzchnię skał magmowych - i tutaj w badaniu z 2010 najwyższą zawartość fluorków miała Długopolanka (1,5 mg/l).
Fluorki mogą jednak pojawiać się na niżu w związku z obecnością w podłożu osadów polodowcowych z odseparowaną frakcją ciężkich minerałów, lub przenikaniem wód głębinowych. Chyba ta przyczyna spowodowała, że łatwo dostępną wodą mineralną o drugiej najwyższej zawartości fluorków, jest Augustowianka (1 mg/l - około 30% dziennej dawki). Jest to woda czerpana z dość dużej głębokości (450 m), lekko słonawa, zawierająca też chlorki sodu, wapnia i magnezu. Z innych łatwo dostępnych wód Polanica Zdrój zawiera o połowę mniej fluoru - 0,5 mg/l, podobnie Staropolanka i woda zdrojowa Henryk, kilkanaście wód zawiera 0,3-0,1 mg/l, a wiele innych w ogóle go nie wymienia.
Dla porównania są rejony, w których ze względu na minerały fluoru w glebie, zawartość fluorków w wodzie wodociągowej z ujęć lokalnych także osiąga spore wartości. W Toruniu dawniej czynne były ujęcia tzw. "studni kredowych" ujmujących wody z warstwy kredy, zawierające nawet 1,5 mg F w litrze; aktualnie toruńska kranówka zawiera 0,2-0,4 mg/l.[f] Wysokie poziomy fluoru związanego ze złożami osadów, notuje się w studniach na Żuławach. Wynika to zapewne z warstwy osadów z okresu Permu, w miejscu dawnej zatoki morskiej. Pomiędzy złożami soli i gipsu znaleziono skupiska fluorytu. W studniach głębinowych z okolic Malborka fluorków było nawet 3,5 mg/l.[g] Podwyższone poziomy notuje się też w Tczewie, Gdańsku, Sieradzu, i w okolicy Kalisza.
Siarczany
Obecność w wodzie siarczanów zwykle wiąże się ze złożami gipsu. Uzupełniają one nieorganiczną siarkę, ale ze względu na działanie osmotyczne, przy stężeniach przekraczających 1g/l zaczynają działać przeczyszczająco. Najwięcej zawiera ich litewska woda Vytatuas (989 mg/l), a z krajowych Solannova (472), czy MagneVita (192). Z szerzej dostępnych stosunkowo sporo zawiera ich Polanicka Zdrój (100 mg/l), Polaris (88 mg/l [p]) i Selenka (85 mg/l).
Lit
Pierwiastek ten ma właściwości podobne do innych metali alkalicznych, jak sód czy potas, toteż często im towarzyszy. Dlatego wodami mineralnymi o największej jego zawartości są zwykle wody silnie zmineralizowane, słone. Króluje tu wybitnie słona woda Zuber (18,5 mg/l), dalej Szczawa II (14,5), Szczawa I (11,6) i nieco bardziej znośna Franciszek (5,2). Z wód łatwo dostępnych, słodkich, stosunkowo dużo litu zawiera Piwniczanka (0,6 mg/l) i Galicjanka (0,2).
Nie ma zbyt wielu informacji o zawartości litu w wodach wodociągowych, z którymi można by porównać te wyniki. Zwykle się go nie bada.
Jod
Jod ma właściwości chemiczne podobne do chloru, więc często występuje w wodach słonych. Z tych, których skład sprawdzałem, najwięcej ma go woda Dziedzilla (4,4 mg/l) i Szczawa II (3,0 mg/l), nieco mniej Szczawa I i Hanna (2,5 mg/l), Franciszek (2,2 mg/l). Są to wody zdrojowe, czasami spotykane w sklepach w małych buteleczkach.
Selen
Selen jest pierwiastkiem rzadkim i potrzebnym organizmowi w śladowych ilościach. Chemicznie jest najbardziej podobny do siarki, stąd występuje w wodach siarczkowych i siarczanowych, często też żelazistych, wynikających z kontaktu ze złożami pirytu.
W analizie z 1999 roku stwierdzono, że najwięcej selenu zawierały wody Cristal (0,514 ug/l = 0,0005 mg/l), Krynica Zdrój niegazowana (0,5 ug/l), Nałęczowianka niegazowana (0,498) Muszynianka niegazowana (0,495), Multi Vita (0,460) i Kryniczanka (0,450). W wodach gazowanych zwykle było go mniej niż w niegazowanych, być może z powodu występowania części pierwiastka w lotnych formach. Podczas standardowych oznaczeń próbkę się odgazowuje, więc im więcej gazu miała woda, tym większe były różnice między wersją gazowaną i niegazowaną.[s]
Obecnością selenu chwali się woda z Wieńca Zdroju, o chwytliwej nazwie Selenka, choć trudno powiedzieć, czy jest w ten pierwiastek jakoś wyjątkowo zasobna. Podawana na etykiecie wartość <0,02 mg/l to tylko granica oznaczalności metody, pod nią mieszczą się wszystkie podane wcześniej wyniki zawartości, a także maksymalna dopuszczalna zawartość dla wód pitnych (0,01 mg/l). Miejsce w rankingu mogłyby ustalić dokładne wyniki analizy, ale tej nigdzie nie da się znaleźć.
Inne rzadkie
W teście popularnych wód na zlecenie UOKiK z 2012 roku[u] zbadano też niektóre rzadsze pierwiastki, w tym rad i radon.W żadnej z wód radioaktywność nie przekraczała norm, choć szczególnie duża była w Staropolance 2000 - całkowita dawka przy trwającym rok codziennym uzupełnianiu płynów tylko tą wodą wyniosłaby 0,175 mSv/r - przy czym producent zalecał dzienną dawkę wody 1l, co obniżało skumulowane narażenie do 0,088 mSv/r. Żadna z wód nie przekraczała też norm dla zawartości uranu ale największe stężenie wykazano dla Ustronianki (1,2 ug/l).
------
* http://www.wodamineralna.netmark.pl/ - ranking wód bazujący na informacjach z etykiet
* Łukasz J. Krzych i inni, CHARAKTERYSTYKA WÓD BUTELKOWANYCH DOSTĘPNYCH
W SPRZEDAŻY W WOJEWÓDZTWIE ŚLĄSKIM, ROCZN. PZH 2010, 61, Nr 1, 37 - 43
[d] D. Bodzek i inni, Zawartość wapnia i magnezu w wybranych wodach i osadach ściekowych Górnego Śląska, Ochrona Środowiska, 4(71) 1998
[f] http://www.wodociagi.torun.com.pl/index.php?lang=PL&m=faq
[g] Halina Łazarz i inni, Fluor w wodach podziemnych wschodniej części Żuław Wiślanych, Kwartalnik Geologiczny, I. 31, nr 1. 1987 r., Str. 69 - 82
[p] Anna Pasternakiewicz i inni, Badania zawartości wybranych anionów nieorganicznych
w wodach mineralnych i źródlanych – pod kątem bezpieczeństwa zdrowotnego wody, Probl Hig Epidemiol 2014, 95(3): 788-793
[s] Masłowska J., Ocena zawartości selenu w naturalnych wodach mineralnych dostępnych na rynku w Polsce, Żywność 3 (20) 1999
[u] https://www.bankier.pl/static/att/90000/2467072_Wybrwody.pdf
poniedziałek, 24 września 2018
Chemiczne wieści (19.)
Wykorzystanie żywych organizmów do wytwarzania energii jest jak na razie raczkującym działem technologii. Pewnym krokiem na przód jest doniesienie badaczy z Birmingham University o stworzeniu lekkiej minibaterii, której podstawowym materiałem jest zadrukowany papier. Na papierowe podłoże naniesiono warstwę przewodzącego polimeru z akceptorem elektronów, a na drugą stronę tusz zawierający cząstki metalu. Sam papier został ponadto pokryty przetrwalnikami wysuszonych bakterii elektrogennych.
Są to bakterie które potrafią tworzyć ładunki elektryczne generując niewielkie prądy. Nie tak dawno odkryto, że w kolonii tworzą między sobą połączenia przekazując sobie wzajemnie energię, oraz że mogą być pobudzane do wzrostu przez zewnętrzne napięcie.
W tym przypadku bakterie zostały użyte jako źródło prądu. Po nasyceniu papieru elektrolitem, którym może być na przykład ślina, woda pitna czy sok roślinny, bakterie zaczynają metabolizować i generować prąd. Drobne ładunki zebrane z zestawu wielu połączonych ogniw, na arkuszu złożonym w harmonijkę, wystarczyły aby po kilkunastu minutach od nawilżenia dało się tym prądem zapalić diodę czy zasilić kalkulator elektroniczny.
 |
| Credit: Seokheun Choi |
Badacze celują tym urządzeniem w przenośne urządzenia analityczne, na przykład do wykrywania substancji we krwi czy moczu, albo zanieczyszczeń w wodzie pitnej. Urządzenie nie potrzebowałoby zasilania, byłoby lekkie, a badany płyn byłby równocześnie elektrolitem.[1]
Nadmierne wzburzenie chmielonego piwa wyjaśnione
W najczęściej używanej technice warzenia piwa, głównym surowcem jest słód, otrzymywany z ziaren zbóż poddanych przeprocesowaniu, w którym namoczone ziarna rozciera się uwalniając enzymy rozkładające skrobię do prostych cukrów. Następnie mieszanina ta jest gotowana z chmielem, co zabija przeszkadzające bakterie i dzikie drożdżaki, oraz uwalnia z chmielu aromaty i goryczki. Następnie mieszanina jest poddawana fermentacji przy pomocy odpowiednio dobranych gatunków drożdży, a po zakończeniu fermentacji, gdy proste cukry zostaną rozłożone, piwo może zostać zabutelkowane.
W ostatnich latach coraz większą popularność zdobywa sobie technika chmielenia na zimno, polegająca na macerowaniu piwa z chmielem już po ustaniu fermentacji burzliwej. Dzięki temu piwo zyskuje wyraźniejszy i mocniejszy aromat chmielu, bez przesadnej ilości goryczki. Część bowiem substancji aromatycznych zwyczajnie odparowuje podczas warzenia, lub jest usuwana z bąbelkami.
Technika ta bywa jednak nieco kłopotliwa - piwowarzy częściej niż zwykle obserwowali w tak zrobionym piwie pojawienie się dodatkowej, nie kończącej się szybko fermentacji. Jeśli po pozornym spadku ilości cukrów i zaprzestaniu fermentacji piwo nachmielono i za szybko zabutelkowano, następująca w butelce dalsza fermentacja powodowała przy otwarciu gushing (fontanna piany pod ciśnieniem) a nawet pękanie butelek w trakcie leżakowania. Dodatkowym problemem mogła być za wysoka zawartość alkoholu.
Zwykle za przyczynę tego zjawiska uznawano natlenienie piwa powietrzem zawartym w chmielu, zanieczyszczenie dzikimi drożdżami czy obecność cukrów prostych w samym chmielu, co dostarczyło drożdżom dodatkowego pokarmu. Ostatnie badanie zespołu z Oregon State University dorzuca jeszcze jedną możliwość.
 |
| Credit: American Chemical Society |
Naukowcy poddali powtórnemu chmieleniu komercyjne piwa, a więc takie, w których co się miało przefermentować, to już przereagowało. Okazało się, że zawartość alkoholu i dwutlenku węgla ponownie się zwiększyła, zupełnie jakby w piwie pojawiły się dodatkowe cukry proste. Dokładne przeanalizowanie składu pozwoliło odnaleźć źródło.
Podczas produkcji słodu oraz dalszego warzenia, nie cała skrobia ulega rozkładowi do fermentowalnych cukrów prostych. Część łańcuchów skrobi ulega tylko podziałowi na dekstryny - fragmenty zawierające kilka - kilkanaście reszt glukozowych, które są rozpuszczalne w wodzie i nie da się ich oddzielić filtrowaniem. Drożdże nie za bardzo mogą się nimi pożywić, pozostają więc w piwie jako niefermentowalne węglowodany. Jak się jednak okazuje, sam chmiel zawiera enzymy mogące rozkładać dekstryny. W wyciągu z suszu oznaczono aktywność amyloglukozydazy, alfa i beta amylaz i dekstrynazy. Ich zawartość wystarcza aby rozłożyć dekstryny i dostarczyć dodatkowych porcji fermentowalnych cukrów prostych.
Podczas dalszych eksperymentów badacze sprawdzili, że stopień przereagowania można kontrolować temperaturą, czasem i ilością macerowanego chmielu, potencjalnie więc możliwe by było takie dobranie warunków procesu, aby przykre efekty uboczne pojawiały się rzadziej. [2]
Pasek do sprawdzania antybiotyków
Antybiotyki należą do najczęściej fałszowanych leków. Podróbki nie zawierające właściwego leku, lub z substancją właściwą rozmieszaną z czymś nieaktywnym, krążą po sklepach, pojawiają się na aukcjach internetowych oraz bywają sprzedawane do krajów trzeciego świata. Zespół badaczy z Carolina State University opracował prosty test kolorymetryczny, który może wykazać czy tabletka zawiera antybiotyk, oparty zasadą działania o testy ciążowe.
Fragment badanej tabletki rozpuszcza się w wodzie a roztwór nakłada na koniec papierowego paska. Gdy pasek nasiąknie, zawarty w nim związek, nitrocefina, może reagować z drugim składnikiem, enzymem betalaktamazą. Przy nieobecności antybiotyku, reakcja spowoduje powstanie produktu o czerwonym kolorze. Antybiotyk z grupy beta-laktamów (głównie penicyliny) będzie natomiast sam reagował z laktamazą, zmniejszając szybkość reakcji ze wskaźnikiem i powodując, że pasek pozostanie żółty.
Podczas ślepej próby z przemieszanymi próbkami z i bez antybiotyków test prawidłowo oznaczył zawartość penicylin w 29 z 32 próbek.[3]
 |
| Copyright © 2018 American Chemical Society |
---------
[1] Yang Gao Seokheun Choi, Merging Electric Bacteria with Paper, Adw. Mat. Tech. vol 3 issue 8
[2] Kaylyn R. Kirkpatrick and Thomas H. Shellhammer, Evidence of Dextrin Hydrolyzing Enzymes in Cascade Hops (Humulus lupulus), J. Agric. Food Chem., 2018, 66 (34), pp 9121–9126
[3] Katherine E. Boehle et al, Paper-Based Enzyme Competition Assay for Detecting Falsified β-Lactam Antibiotics, ACS Sens., 2018, 3 (7), pp 1299–1307
wtorek, 29 maja 2018
Krystalografia czekolady
Krystalografia to dziedzina na pograniczu chemii fizycznej i fizyki ciała stałego, zajmująca się badaniem właściwości kryształów i niektórych innych faz uporządkowanych, oraz ich teoretycznym opisem. Wedle definicji utworzonych w ramach tych badań, stan krystaliczny to forma materii charakteryzująca się wysokim uporządkowaniem struktury przestrzennej tworzonej przez pojedyncze cząsteczki lub jony. Cząstki tworzące kryształ są tak ułożone, iż tworzą pewien podstawowy schemat, mogący powtarzać się w trzech wymiarach praktycznie w nieskończoność - przynajmniej aż do zewnętrznej ściany ziarna krystalicznego.
Niech to będzie powiedzmy przestrzenny kwinkunks z ośmioma cząsteczkami w rogach domyślnego sześcianu i jedną w geometrycznym środku między nimi:
Wedle tego typu komórki krystalicznej, szeregujemy struktury kryształów w grupy oparte na konkretnej geometrii, czyli układy krystalograficzne, jest ich kilka: oparty na sześcianie układ regularny, układ heksagonalny oparty na heksagonie itp.
Dodatkowo w każdym typie możliwe jest że między narożami komórki pojawią się dodatkowe cząsteczki w centrum ścian lub w środku, stąd możliwość dodatkowych typów "centrowanych". Łącznie 7 układów wraz z centrowanymi kombinacjami daje 32 typy sieci krystalicznych, nazywane sieciami Bravais'go (czyt: 'brawego').
Wiele substancji może tworzyć kryształy różnego rodzaju, o różnej strukturze krystalicznej, zależnie od warunków krystalizacji. Jeden rodzaj sieci krystalicznej może przechodzić w drugi gdy zmienią się warunki. Znanym przykładem jest choćby siarka, która krystalizowana ze stopu tworzy igiełkowate kryształki o symetrii jednoskośnej, które w temperaturze poniżej 95 stopni powoli zamieniają się w kryształki o symetrii rombowej. Formy te różnią się też rozpuszczalnością w dwusiarczku węgla. Podobną sytuację widać w przypadku węgla, gdzie drastycznie różne właściwości mają dwie formy krystaliczne - czarny i miękki grafit oraz przezroczysty i twardy diament.
Istnienie różnych form krystalicznych tej samej substancji nazywane jest polimorfizmem.
 |
| Dwa zupełnie różnego kształtu i koloru kryształy tej samej substancji (kobalto-karboran) różniące się wzajemnym ułożeniem cząsteczek w komórce elementarnej. (publikacja) |
Odmiany krystaliczne tej samej substancji, poza geometrią i symetrią, różnią się też właściwościami fizycznymi. Mogą różnić się twardością, kolorem, przewodnością a także temperaturą topnienia.
Co to wszystko ma do czekolady?
Czekolada to mieszanina otrzymywana ze zmieszania kakao i tłuszczu kakaowego, także z mlekiem i cukrem; często zamiast kakao używa się miazgi kakaowej. Cząstki kakao i kropelki wodnistej części mleka tworzą zawiesinę w masie stałego masła kakaowego. Masło to w formie stałej składa się z drobnych ziaren krystalicznych, czego gołym okiem nie widać z powodu ich niewielkich rozmiarów. Kryształy masła z kolei mogą występować w kilku odmianach polimorficznych, różniącym się między innymi wytrzymałością mechaniczną i temperaturą topnienia.
Zatem znajomość własności kryształów tłuszczu kakaowego, pozwala na otrzymanie czekolady o właściwych parametrach.
Z kilku najważniejszych form krystalicznych tłuszczu w czekoladzie, trzy topią się w temperaturze poniżej 25 stopni, jedna (forma IV) w 27 stopniach, jedna (V) przy około 33 stopniach i jedna (VI) przy około 36-38 stopniach. Przy złym wykonaniu i schłodzeniu masy albo otrzymamy czekoladę, która pozostaje miękka w temperaturze pokojowej i łatwo topi się w dłoni, albo otrzymamy produkt twardy i z trudem rozpuszczający się nawet w ustach. W dodatku niskotopliwe formy chętnie tworzą duże kryształy, które rozpychają na boki cząstki kakao, powstaje wówczas czekolada o matowej, nierówno zabarwionej powierzchni.
Aby otrzymać czekoladę z przewagą formy krystalicznej właściwej, należy przeprocesować ją w odpowiedniej temperaturze. Proces ten nazywany jest temperowaniem.
Typowym sposobem temperowania jest najpierw stopienie masy czekoladowej w temperaturze, w której topią się wszystkie formy krystaliczne, czyli około 45 stopni. Następnie masa jest szybko schładzana do temperatury nieco poniżej topnienia średniotopliwej formy, około 26-27 stopni. W tej temperaturze w mieszanej szybko masie powstać mogą drobne kryształki trzech typów - formy IV o temperaturze topnienia 27 stopni, formy V i formy VI - które to drobne kryształki działają jak zarodki dla powstawania kolejnych kryształów w tych typach. Gdybyśmy teraz pozwolili masie powoli ostygać, zawierałaby mieszankę trzech form krystalicznych i miałaby wciąż niską temperaturę mięknięcia i topnienia.
Dlatego teraz masa jest precyzyjnie ogrzewana do temperatury około 30-31 stopni. Kryształki formy IV, topiące się w 27 stopniach, zanikną. Pozostaną więc już tylko kryształki form V i VI. Masa od tego momentu jest dość powoli ochładzana, na tyle, że gdy jej temperatura spadnie do około 25 stopni, większość masła kakaowego będzie już skrystalizowana i nie będą nam powstawały nowe kryształki form o niskich temperaturach topnienia. Tak otrzymanym ideałem jest masa topiąca się w temperaturze 34-35 stopni, czyli znana z reklam "czekolada rozpływająca się w ustach a nie w dłoni".
Dla otrzymania równomiernej masy o pożądanych właściwościach stosuje się precyzyjną kontrolę temperatury i szybkie mieszanie. Dokładne wartości temperatur zależą też od składu, dla czekolady ciemnej są wyższe, dla mlecznej niższe (ze względu na domieszkę tłuszczu mlecznego). Większy dodatek wody zwiększa miękkość czekolady.
Otrzymana w przewadze forma średniotopliwa V jest jednak w temperaturze pokojowej nie do końca stabilna termodynamicznie. Dłuższe przechowywanie powoduje, że część masła kakaowego ulega przemianie w formę VI. Odbywa się to najczęściej w warstwach powierzchniowych przy nieco podwyższonej temperaturze. Powstające kryształki nowej formy wyrastają z powierzchni czekolady, tworząc jaśniejszą warstwę, widoczną dobrze zwłaszcza na tabliczkach w pobliżu okresu ważności. Sam w sobie ten jasny osad nie jest oznaką zepsucia, ale może wskazywać na niezbyt dobre warunki przechowywania. Gdy tabliczka leżała w sklepie w warunkach tak ciepłych, że częściowo się nadtopiła, efekt ten wywołuje powstanie nieregularnych cętek, plam białych i żółtawych złożonych głównie z samego tłuszczu, które mogą nie smakować za dobrze.
---------
* Klaus Roth, Chocolate - The Noblest Polymorphism,
* https://en.wikipedia.org/wiki/Chocolate
środa, 14 lutego 2018
Słodziki cukropochodne
A ponieważ jest ich dość dużo, dobrze było poświęcić im osobny wpis.
Cukry to grupa związków organicznych, charakteryzująca się licznymi grupami hydroksylowymi (-OH) połączonymi z atomami węgla tworzącymi łańcuch nasycony, podobnie jak w alkoholach, oraz przynajmniej jedną grupą aldehydową (-CHO) lub ketonową (-C=O), za sprawą której możliwe jest dla nich utworzenie formy pierścieniowej jako hemiacetal. Są też nazywane węglowodanami, bo ich skład pierwiastkowy daje się sprowadzić do wzoru Cx(H2O)y, choć jest trochę wyjątków, jak cukry deoksy.
Na atomach węgla z dołączonymi grupami hydroksylowymi pojawia się szczególna geometria asymetrycznego ułożenia czterech podstawników, przy której możliwe stają się dwie konfiguracje - R i S, różniące się kolejnością przestrzenną dwóch podstawników.
Sytuacja taka dotyczy każdego atomu węgla z grupą hydroksylową, z wyjątkiem końcowego, który ma dwa takie same podstawniki, wodory. Ponieważ cukry zawierają wiele takich atomów, możliwych staje się wiele izomerów, różniących się tylko konfiguracją na poszczególnych węglach ale o takim samym składzie i budowie ogólnej. Dla cukrów sześciowęglowych cztery atomy węgla posiadają asymetrię, a ponieważ dla każdego możliwe są dwie konfiguracje, to istnieje 16 różnych cukrów sześciowęglowych. Jednym z nich jest glukoza.
Najpowszechniej używany do słodzenia cukier stołowy, czyli sacharoza, to związek złożony z dwóch cząsteczek cukrów, glukozy i fruktozy.
Ponieważ formalnie rzecz biorąc cukry są ketonami lub aldehydami, bo posiadają jedną taką grupę, można poddać je utlenieniu, do otrzymania kwasu karboksylowego, lub redukcji. W tym ostatnim przypadku zarówno grupa ketonowa jak i aldehydowa zamienią się w kolejny człon C-OH. Słodziki takie jak ksylitol czy sorbitol są zatem formalnie alkoholami!
Oczywiście nikt się nimi nie upije. Mają one smak słodki podobny do smaku wyjściowych cukrów, jednak zwykle nie są tak łatwo wchłaniane przez organizm, a co za tym idzie, nie mają tak samo dużej kaloryczności. Z tego też powodu zaczęły być używane jako niskokaloryczne słodziki polepszające smak żywności, zwłaszcza tej przeznaczonej dla cukrzyków, muszących dbać o poziom glukozy i insuliny. A ponieważ cukrów wyjściowych jest dużo, to i alkoholi cukrowych znamy i używamy dość wiele. Omówię te faktycznie stosowane w przemyśle spożywczym.
Omówienie alkoholi cukrowych najlepiej zacząć od tych najkrótszych, a więc po kolei:
Glicerol (E 442)
Lepiej znany jako gliceryna, składnik tłuszczów, bardziej kojarzony jako składnik kosmetyków. Łańcuch zawiera tylko trzy węgle. Jeszcze prostszy glikol etylenowy też bywa uznawany za alkohol cukrowy choć jego aldehyd nie jest cukrem, ale tego w żywności nie spotkamy.
Gliceryna to higroskopijna, gęsta, syropowata ciecz o lekko słodkawym smaku stanowiącym około 50-60% słodkości sacharozy. Raczej nie jest używana jako jedyny słodzik, bardziej służy za rozpuszczalnik wzmacniający smak innych środków słodzących, ponadto służy do zagęszczania i zapobiegania wysychaniu. Jest też składnikiem lukrów do ozdabiania ciastek, zapewnia bowiem półpłynną konsystencję bez krystalizacji w opakowaniu. Mieszając się z wodą nieco się ogrzewa, stąd może być mieszana ze słodzikami które ochładzają się przy rozpuszczaniu jeśli akurat nie jest to pożądane
Jako dodatek do żywności jest bezpieczna, organizm metabolizuje ją tylko częściowo, włączając do szlaku przetwarzania węglowodanów ale z minimalnym użyciem insuliny, stąd też jej bardzo niski indeks glikemiczny. Nie stanowi pożywki dla bakterii wywołujących próchnicę ani dla jelitowych, może jednak wykazywać efekt przeczyszczający, znany zresztą wszystkim używającym glicerynowych czopków. Bywa używana jako dodatkowy słodzik w żywności dla diabetyków oraz jako zamiennik alkoholu w preparatach farmaceutycznych i wyciągach ziołowych (gliceryty) jeśli akurat sam alkohol nie jest wskazany.
Erytrytol
Produkt redukcji erytrozy, czterowęglowego cukru prostego zawartego między innymi w ogonkach liści rabarbaru, od którego wziął nazwę (greckie "erythros" czyli "zaczerwieniony"). Wyjściowy cukier nie występuje w naturze zbyt często, dlatego substratem jest glukoza. Poddaje się ją fermentacji z użyciem kolonii grzybów z rodzaju Moniliella lub Aureobasidium, które zwykle odpowiadają za psucie się wysokosłodzonej żywności. Rozbijają one sześciowęglową cząsteczkę glukozy i w warunkach beztlenowych końcowym produktem jest gotowy erytrytol obok innych polioli.
Związek ten ma smak bardzo podobny co sacharozy i niewiele mniejszą słodkość, rzędu 70-80%. Wykazuje synergizm z innymi słodzikami, częściowo maskując gorzki posmak, stąd chętne użycie wraz ze stewią. Co jednak najbardziej interesujące, nie jest prawie w ogóle metabolizowany. Większość zażytej dawki wchłania się jeszcze w jelicie cienkim, po czym w formie niezmienionej zostaje wydalona z moczem. Około 10% dostaje się do jelita grubego, tam jednak bakterie nie za bardzo się nim interesują. Powoduje to, że w odróżnieniu od ksylitolu czy sorbitolu, które w większości przedostają się do okrężnicy i działają osmotycznie, erytrytol nie wywołuje rozwolnienia czy wzdęć.
Ostatecznie tylko niewielka ilość zostaje zmetabolizowana, bez wykorzystania insuliny, stąd przypisuje się mu indeks glikemiczny bliski zeru i kaloryczność ok. 0,2 Kcal.
[1]
Jego diastereoizomerem, różniącym się konfiguracją, jest treitol. Nie jest jednak używany jako słodzik.
Ksylitol
Pięciowęglowy poliol otrzymywany przez redukcję ksylozy, składnika zdrewniałych części roślin. W naturze w wolnej postaci występuje rzadko, głownie w soku niektórych owoców. Jego słodkość jest zbliżona do sacharozy, natomiast indeks glikemiczny wielokrotnie niższy. Wynika to stąd, że jest słabo wchłaniany, duża część pozostaje w treści jelit, część wchłoniętego jest wydalana z moczem. Pewna ilość ksylitolu może być trawiona przez bakterie jelitowe do krótkołańcuchowych kwasów tłuszczowych i w takiej formie wykorzystana; ponadto pewna ilość wchłoniętego związku może być zamieniana w glikogen w wątrobie, ale jest to proces powolny. Łącznie efekty te dają kaloryczność możliwą do wykorzystania przez organizm około 2,4 Kcal, o 40% mniejszą od cukru stołowego.
Przechodzenie dużej ilości ksylitolu do treści jelita grubego skutkuje działaniem osmotycznym, zauważalnym zwłaszcza u osób, których dieta nie zawierała dotychczas takiego składnika. Zanim organizm się przyzwyczai i zacznie inaczej reagować, odpowiednio duża jednorazowa dawka działa rozwalniająco. Ponadto pewien stopień trawienia przez bakterie jelitowe może u niektórych skutkować wzdęciami. Poza tymi drobnymi przypadłościami nie zaobserwowano szkodliwego działania nawet bardzo dużych dawek.
Ksylitol jest natomiast toksyczny dla psów i niektórych ptaków, ze względu na zbyt silne pobudzenie wydzielania insuliny. Dawanie zwierzętom diabetycznych smakołyków raczej nie jest dobrym pomysłem. Napisałem o nim osobny artykuł, tam więcej informacji (Link).
Sorbitol
Alkohol sześciowęglowy otrzymywany przez redukcję glukozy, w naturze występujący w niewielkich ilościach w soku jabłkowym i śliwkowym, po raz pierwszy wyizolowano go z owoców jarzębiny, skąd wzięła się nazwa. Jest chętnie używany w żywności dietetycznej czy gumach do żucia "bez cukru". Jest w małym stopniu wchłaniany i przechodzi do treści jelita grubego, gdzie w zbyt dużej ilości może działać przeczyszczająco. Prawdopodobnie obok samego tylko błonnika przyczynia się do przeczyszczającego działania suszonych śliwek, w których występuje obficie. Bywa używany w medycynie jako diuretyk do obniżania ciśnienia wewnątrz oka
Mannitol
Drugi alkohol sześciowęglowy, od sorbitolu różniący się konfiguracją na asymetrycznych atomach węgla, formalnie będący produktem redukcji mannozy. Zwykle otrzymywany przez uwodornianie fruktozy, ale także stosunkowo duża część zapotrzebowania jest uzupełniana ze źródeł naturalnych, obficie występuje w niektórych krasnorostach i owocach, oraz w soku jesionu mannowego od którego wziął nazwę. Słodkość podobna do cukru stołowego i niski indeks glikemiczny powodują, że także jest chętnie używany jako słodzik.
Stopiony tworzy masę podobną do szkła, która jest praktycznie niehigroskopijna, stąd użycie w cukierkach, gumach do żucia, w polewach pokrywających draże oraz jako składnik ozdób cukierniczych.
Mannitol ma ważne zastosowania medyczne. W formie zastrzyku dożylnego jest używany do szybkiego obniżania ciśnienia wewnątrz gałki ocznej, co wykorzystuje się w leczeniu jaskry, oraz obniża nadmierne ciśnienie wewnątrzczaszkowe. Dodatkowo może zmniejszać obrzęki regulując wydalanie wody. Dożylnie zwiększa też wydzielanie wody przez nerki, co wykorzystuje się przy leczeniu skąpomoczu i przy eliminacji toksyn.
Laktitol
Zredukowana forma laktozy, dwucukru występującego w mleku. Laktoza składa się z cząsteczki glukozy i cząsteczki galaktozy. Laktitol jest otrzymywany poprzez selektywne zredukowanie tylko składowej cząsteczki glukozy, w związku z czym formalnie jest połączeniem galaktozy z mannitolem. Słodycz stanowi około 40% słodkości białego cukru. Ponieważ związek jest dość stabilny w wysokich temperaturach oraz mikrobiologicznie, jest chętnie używanym dodatkiem do dietetycznych wypieków, ciasteczek, czekolady i kremów.
W większych ilościach może działać przeczyszczająco, bywa składnikiem leków przeciw zaparciom. Nie jest polecany osobom nie trawiącym galaktozy.
Maltitol
Produkt częściowej redukcji maltozy, dwucukru złożonego z dwóch cząsteczek glukozy, naturalnie obecnego w dekstrynach i słodzie. Redukcji ulega tylko jedna cząsteczka składowa, toteż formalnie jest to połączenie glukozy i sorbitolu. Produkuje się go w wyniku uwodornienia syropu kukurydzianego, produktu częściowej hydrolizy skrobi. Powstaje wówczas mieszanina maltitolu, sorbitolu i częściowo uwodornionych wielocukrów.
Właściwości fizyczne ma bardzo podobne do sacharozy - podobny smak, gęstość, temperaturę topnienia, skłonność do karmelizacji, dlatego może zastępować ją we wszystkich zastosowaniach spożywczych.
W bardzo dużych ilościach na raz, działa przeczyszczająco, choć ryzyko jest w tym przypadku małe.
Izomalt
Mieszanina częściowo zredukowanych dwucukrów. Wytwarzana w dwuetapowym procesie - najpierw sacharoza jest poddawana reakcji z enzymem otrzymywanym z pewnych bakterii, który zamienia ją w izomaltulozę. Jest to dwucukier w którym glukoza i fruktoza są połączone w inny sposób. W sacharozie jest to wiązanie łączące atom nr.1 jednej cząsteczki z atomem nr.2 drugiej. W izomaltulozie wiązanie przeskakuje w pozycję 1-6. Skutkuje to tym, że jest to cukier o właściwościach redukujących.
Uwodornienie izomaltulozy daje mieszaninę dwóch związków, w związku z tym, że w części przypadków uwodorniła się tylko składowa cząsteczka glukozy a w innym tylko fruktozy, powstaje więc glukozo-sorbitol czyli maltitol, oraz glukozo-mannitol.
Izomalt jest używany głównie do bezcukrowych cukierków, łatwo bowiem tworzy przezroczystą, niehigroskopijną masę i nie ma skłonności do zlepiania się z innymi cukierkami. Jest odporny na krystalizację, stąd użycie do ozdób cukierniczych i rzeźb z topionego cukru
Uwodorniony hydrolizat skrobiowy (HSH)
Mieszanina różnych związków, otrzymywana przez uwodornienie dekstryn wytwarzanych przez częściową hydrolizę skrobi. Może zawierać wyraźną przewagę jednego alkoholu cukrowego, na przykład sorbitolu czy mannitolu, jeśli jednak ponad 50% stanowią częściowo zredukowane wielocukry, używa się właśnie takiej nazwy. Słodkość zależy od stopnia uwodornienia, dochodzi do 50% słodkości białego cukru. Stanowi dodatkowy składnik obok innych słodzików, oraz środek zwiększający lepkość i gęstość
-------
[1] http://ncl.csircentral.net/920/1/th1868.pdf
niedziela, 14 stycznia 2018
Detoksy-Mistyfikacje
Natomiast wyolbrzymiane skutków oprócz obietnicy wyleczenia z ciężkich chorób, oraz równie ważnego schudnięcia w dwa tygodnie, odbywa się też przez zaprezentowanie detoksu w efektownej wizualnie formie. Najlepiej byłoby, gdyby uwalniane toksyny było dobrze widać. Jeszcze lepiej, gdyby wyglądało to obrzydliwie i przypominało brud. Jeśli zaś toksyny nie chcą tak ładnie wyglądać, trzeba im jakoś pomóc...
Plastry czyli brunatnienie octu
Plastry detoksyfikujące wciąż jeszcze są dosyć popularne. Nakleja się je na stopy na noc i rano są całe zbrązowiałe, pokryte kleistą substancją i niemile pachną. I oczywiście ta brązowa substancja to toksyny z organizmu.
Problem w tym, że podobny efekt daje zwilżenie plastra. W ich składzie znajdują się substancje chłonące wilgoć i wyciągi roślinne o brązowym kolorze. W ciągu nocy plaster chłonie wilgoć ze skóry, zwłaszcza pot, więc rano są wilgotne a zawartość saszetki zabawia plaster na brązowo.
Ale, ale - przecież jeśli stosuje się je regularnie, to po pewnym czasie przestają brązowieć. Z czego to wynika? Jednym ze składników takich plastrów jest ocet drzewny otrzymywany ponoć z pędów bambusa. Kwas octowy działając kilka godzin na skórę przez kilkanaście dni, powoduje obkurczenie gruczołów potowych i przejściowe zmniejszenie potliwości na tym fragmencie skóry.
Robiono już testy z ochotnikami i po przeanalizowaniu składu plastrów nie stwierdzono, aby po całonocnym użytkowaniu pojawiały się w nim jakieś metale ciężkie czy znane substancje toksyczne.[1]
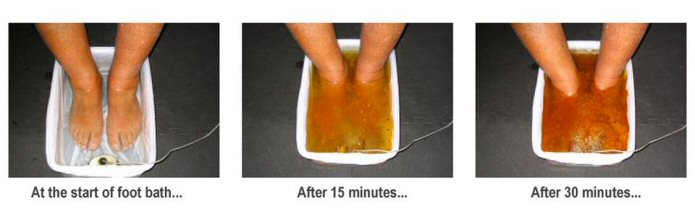
Wanna z błotkiem czyli elektroliza
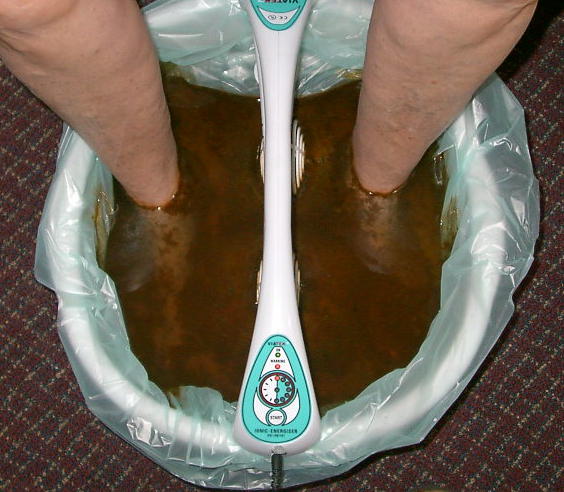
Pod pewnym względem podobna wydaje się popularna zwłaszcza kilka lat temu metoda z wanienkami, mającymi wywoływać wydalenie toksyn przez stopy. Zanurzało się stopy w korytku, trzymało w rękach elektrody, a po pewnym czasie od włączenia urządzenia, woda robiła się brązowa i śmierdziała. Prowadzący zabieg tłumaczył, że oto pole elektryczne spowodowało wydalenie toksyn do wody i to brązowe w misce to nasze toksyny.
Urządzenie składa się przede wszystkim z miski na wodę i płaskich elektrod, koniecznie stalowych bo inaczej nie zadziała, zasilane jest najczęściej zasilaczem podobnym do tych do telefonów komórkowych, stosując niskie napięcie 12 V i bezpiecznie niskie natężenie.
Dlaczego elektrody muszą być stalowe? Bo inaczej nie zrobi się nam błotko. Nie jest potrzebne nawet wkładanie stóp, zrobi się samo byle płynął prąd.
W urządzeniu takim zachodzi prosta elektroliza wody, zwykle lekko posolonej dla lepszego przewodnictwa, z prądem stałym podłączonym w taki sposób, że na elektrodach w wodzie pojawia się ładunek dodatni. Pod wpływem takiego ładunku zachodzi reakcja utlenienia żelaza z elektrody, w pewnym stopniu też wydzielenie tlenu. Jony żelaza i tlen tworzą tlenki i wodorotlenki, tworzące ostatecznie brązowy osad, zaciemniający wodę i udający toksyny. Efekty wizualne zabiegu nie mają żadnego związku z detoksem.
Biorąc pod uwagę, że stale nierdzewne zawierają domieszki niklu i chromu, które mogą uwalniać się podczas zabiegu do roztworu, namaczanie w nim stóp może się okazać bardzo szkodliwe dla skóry. Nie od dziś wiadomo, że nikiel jest silnym alergenem a chrom wywołuje podrażnienia.
Teoretycznie puszczenie napięcia od rąk do stóp mogłoby spowodować migrację jonów z organizmu do wody, za sprawą jonoforezy, czyli ruchu jonów pod wpływem prądu elektrycznego. Jednak aby, jak to piszą wykonujący ten zabieg szarlatani, usuwać w ten sposób kationy metali ciężkich należałoby... podłączyć prąd dokładnie odwrotnie! Kationy, czyli jony o ładunku dodatnim, migrują do elektrody o ładunku ujemnym, bo przeciwieństwa (elektryczne) się przyciągają.
Ale jak się już domyślacie, podłączenie prądu odwrotnie nie będzie utleniało elektrod i barwiło wody na brązowo. Warto by więc rozważyć, czy przypadkiem podczas zabiegu nie dochodzi do elektroforetycznego wchłaniania do organizmu wspomnianych niklu i chromu z rozpuszczonej elektrody. Co byłoby dla nas dużo bardziej szkodliwe.
W 2012 roku wykonano zresztą eksperymenty z użyciem dostępnych komercyjnie zestawów "Jonowej Kąpieli Stóp". Najpierw badacze przygotowali roztwór soli w destylowanej wodzie, w ilości podanej przez producenta urządzenia i zbadali zawartość w nim kilkunastu pierwiastków. Następnie wlali do urządzenia i włączyli zgodnie z przepisem na 20 minut, bo tyle trwa normalny zabieg, ale nikt nie wkładał tam stóp. Chodziło o sprawdzenie, na ile skład wody zmienia samo działanie urządzenia. Po minięciu odpowiedniego czasu, pobrali wodę z urządzenia i zbadali zmiany zawartości pierwiastków. Wyniki wyglądają bardzo niepokojąco:
- w wodzie pojawił się arsen, kobalt, mangan i kadm, toksyczne pierwiastki
- zawartość wanadu wzrosła o 5800% (z 1 do 59 ug/l)
- zawartość niklu wzrosła o 750 000% (z 2 do 15 179 ug/l)
- zawartość molibdenu wzrosła o 6100% (z 50 do 3155 ug/l)
- zawartość chromu wzrosła o 590 000% (z 4 do 23 634 ug/l)
- zawartość żelaza wzrosła o 375 000% (z 31 do 116 000 ug/l)
- łączny wzrost zawartości składników mineralnych przekroczył milion procentów.
Nic dziwnego, że woda zrobiła się brązowa. A to wszystko po włączeniu wanienki bez wkładania nóg. Zresztą, strach wkładać do czegoś takiego nogę. Skład odpowiada zawartości metali w stali nierdzewnej wysokochromowej.
Zrobiono też jednak testy z ochotnikami, którzy byli poddawani zabiegowi w wanience kilkakrotnie w ciągu czterech tygodni, zgodnie z zalecaną przez producenta kuracją. Także badano zmiany zawartości pierwiastków w wodzie przed i po zabiegu, w moczu ochotników przed i po zabiegu oraz we włosach ochotników przed serią wielu zabiegów i po czterech tygodniach. Ilość metali ciężkich w wanienkach podczas zabiegów wzrastała bardzo podobnie, do wody uwalniane były te same pierwiastki w podobnej ilości - może tylko chromu i niklu było jeszcze więcej, wzrosty ich stężeń dochodziły do miliona procent, co mogło wynikać ze zużywania się elektrod w urządzeniu. Sprawdzano zresztą całkowitą ilość uwalnianych pierwiastków, stwierdzając że stopniowo spadała w miarę kolejnych eksperymentów na tym samym urządzeniu, a ostatecznie przeprowadzono ich 30, wykazując jak szybko rozpuszczają się elektrody.
Podczas badania moczu ochotników stwierdzono u jednego z nich wzrost ilości metali ciężkich w miarę kolejnych zabiegów, zaś w badaniu składu mineralnego włosów także gwałtowny wzrost zawartości metali ciężkich u jednego ochotnika. W przypadku pozostałych ludzi, zmiany ilości pierwiastków były bardzo małe i miały różny kierunek. Nie dało się więc potwierdzić usunięcia metali ciężkich z organizmu w miarę powtarzanych zabiegów w wanience, bo w przypadku pozostałych badanych ilości pierwiastków się nie zmieniły, natomiast wzrost zawartości metali w moczu i włosach jednego pacjenta sugerowałby raczej wzrost zawartości w organizmie, a więc przytrucie.[2]
Ten sam widowiskowy efekt był też wykorzystywany przez przedstawicieli handlowych sprzedających filtry do wody - na pokazach, na które zapraszano głównie naiwne starsze osoby, pokazywano elektrolizę żelaznych elektrod w wodzie wodociągowej, po czym porównywano z elektrolizą w wodzie destylowanej, która przewodzi prąd bardzo słabo i nie daje takich skutków.
Kamienie prawie żółciowe
Jednym z najpopularniejszych domowych sposobów oczyszczania wątroby, jest wypijanie mieszanki oliwy z sokiem cytrynowym. Efekty ponoć mają być spektakularne, zwłaszcza wydalanie kamieni żółciowych w ilościach hurtowych, zupełnie bez bólu i z możliwością ominięcia operacji. Niestety wielu mających problemy z kamieniami żółciowymi przekonało się już, że mimo poprawnego wykonania takiego zabiegu i wydalenia żółtawych grudek, ilość złogów w ich woreczkach wcale nie spadła. Skoro tak, to skąd się one biorą?
 |
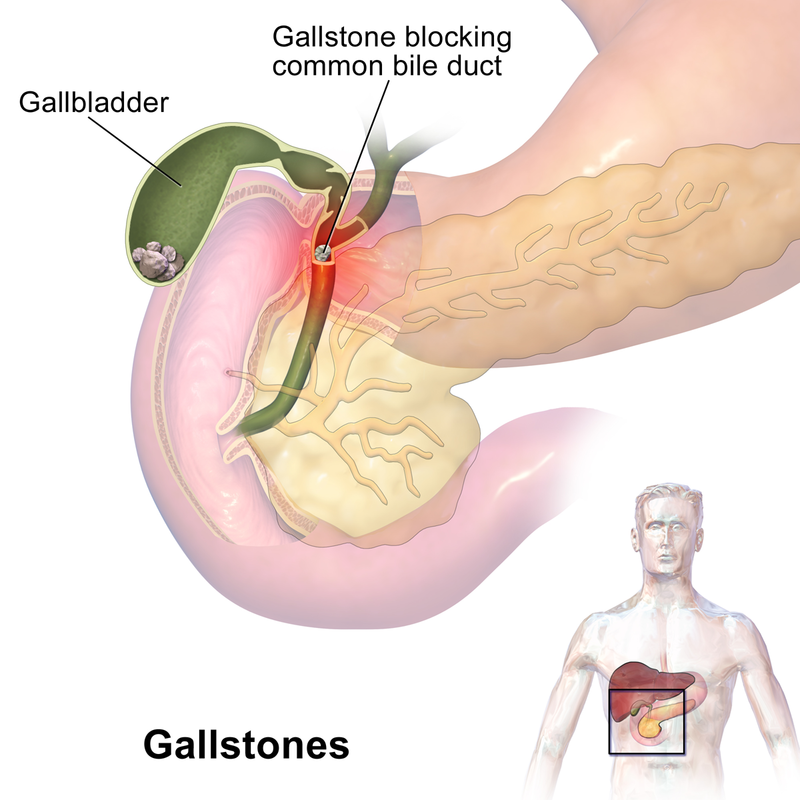
| Prawdziwe ludzkie kamienie żółciowe typu cholesterolowych |
Wątroba i trzustka produkują płyny obfitujące w enzymy trawienne, sole kwasów żółciowych, sole cholesterolu i związki mineralne. Powstała z ich zmieszania się w drogach żółciowych żółć, jest tymczasowo przechowywana w woreczku, oczywiście też żółciowym. Gdy receptory w jelicie w obszarze zakończenia przewodu żółciowego wyczują tłuszcz w treści jelita cienkiego, pobudzony pęcherzyk kurczy się, uwalniając żółć. Ma ona bardzo zasadowy odczyn więc neutralizuje kwas żołądkowy, oraz co ważniejsze, zawiera enzym lipazę który ma trawić tłuszcz. Lipaza rozbija cząsteczki tłuszczów, rozkładając je na kwasy tłuszczowe i glicerynę.
W dalszej kolejności kwasy tłuszczowe powinny zostać podczas trawienia wchłonięte, toteż w normalnej sytuacji kał nie zawiera zbyt dużo tłustych treści. Chyba, że zalejemy jelito dużą ilością tłuszczu i jeszcze popchniemy środkiem przeczyszczającym.
W najpopularniejszej wersji metody używa się jednorazowych dawek oliwy rzędu szklanki czy półtora, wypijanych duszkiem na pusty żołądek, i doprawianych sokiem cytrusowym, często dla lepszego oczyszczenia po pewnym czasie wypija się roztwór soli z Epsom, soli glauberskiej czy jakiegoś innego środka poprawiającego wypróżnianie. Po takiej dawce oleju w jelitach tworzy się dość dużo wolnych kwasów tłuszczowych, które nie mają czasu zostać dalej strawione i wchłonięte, zamiast tego zostają wydalone. W połączeniu z solami mineralnymi (zwłaszcza połkniętą solą z Epsom będącą siarczanem magnezu) kwasy te tworzą trudnorozpuszczalne mydła.
Tym, co zostaje ostatecznie wydalone, są grudki zawierające mydła, wolne kwasy tłuszczowe i składniki żółci, o kolorze od żółtego, przez żółtawozielony do wyraźnie zielonych (kolor zależy od składników oliwy, ilości żółci i treści jelit), uformowane przez ruchy robaczkowe w formę "kamyków".
Chorzy, którzy stosowali tą metodę wiele razy, donosili o liczbach rzędu setek a nawet tysięcy złogów, co przekracza pojemność woreczka żółciowego. Dlatego też szarlatani twierdzą, że dodatkowe ilości złogów schodzą z przewodów żółciowych czy nawet z wnętrza wątroby (wędrują przez miąższ organu?) i dlatego jest ich tak dużo. Jak łatwo się domyśleć, "kamyki" będą się pojawiały tak długo jak długo chory będzie pił oliwę a jego wątroba produkowała żółć. Chyba, że w trakcie "kuracji" woreczek się w końcu zatka a pacjent trafi do szpitala z ostrym zapaleniem.
W 2005 roku w czasopiśmie medycznym The Lancet opisano przypadek kobiety ze stwierdzonymi złogami w woreczku żółciowym, która chciała oczyścić się tą metodą. Prowadzący ją lekarze postanowili wykorzystać okazję i sprawdzić, czy to faktycznie działa. Pacjentka wypiła 600 ml oleju z oliwek i 300 ml soku z cytryny w kilku porcjach. Wydaliła wiele żółtozielonych "kamyczków", które wzięto do analizy. Złogi roztapiały się w gorącej wodzie, w ich składzie brakowało cholesterolu, bilirubiny i soli wapniowych kwasów żółciowych, a więc składników kamieni z woreczka żółciowego. Głównym składnikiem okazało się mydło kwasu oleinowego oraz długocząsteczkowe, trudnotopliwe kwasy tłuszczowe. Wnioskiem lekarzy było stwierdzenie, że wydalone złogi utworzyły się w wyniku trawienia oliwy w jelicie i nie pochodziły z dróg żółciowych.[3]
Wystarczy zresztą zastanowić się nad tym, w jaki sposób mogłoby wyglądać takie wydalanie - niektórzy opisują wydalenie tą metodą złogów o wielkości kilku centymetrów. Kanał żółciowy ma jednak ograniczoną szerokość, złóg większy niż kilka milimetrów po prostu go zatka. Masa tych rozmiarów, przesuwająca się wzdłuż żółciowodu, który jest przewodem dość dobrze unerwionym, musi skończyć się potwornym bólem, czyli atakiem kolki żółciowej. Jeśli więc ktoś nie czuł niczego szczególnego a wydalił centymetrową kulkę, to nie pochodzi ona z jego pęcherzyka.[4] Sól z Epsom nie poszerzy przewodu żółciowego aż tak bardzo (a tak twierdzą szarlatani), bo nie jest on zbyt elastyczny i się nie rozciągnie.
Ponieważ metoda przynosi efekty wyglądające spektakularnie, chętnie powołują się na nią różni dieto-uzdrawiacze. W Polsce najszerzej znana jest jako metoda Huldy Clark, od autorki książek na temat oczyszczania organizmu i leczenia raka, tytułującej się doktorem choć nie ukończyła nigdy medycyny. Inna nazwa to metoda dr Brouse, albo dr Kelley, albo dr. Moritza, bo wielu specjalistów od diety się pod nią podczepiało, z drobnymi modyfikacjami w rodzaju zastąpienia cytryny sokiem jabłkowym.
Pisał o niej też Tombak a za nim, z lekkimi modyfikacjami, Słonecki, tylko u nich miała to być metoda na kamienie kałowe, rzekomo gromadzące się w człowieku w kilogramowych ilościach. Obecnie bez cytowania źródła wspominają o niej liczne portale lifestylowe, jest to więc jedna z najbardziej popularnych medycznych bzdur w temacie oczyszczania organizmu.
Kapsułki oszustwa
W świetnej książce reporterskiej "Nic nie zdarza się przypadkiem" autor, włoski dziennikarz Tiziano Terzani, opisuje kilka lat walki z nowotworem, podczas której równolegle do leczenia klasycznego jeździł po świecie od uzdrawiacza do uzdrawiacza, w pewien sposób dając obraz kultur poprzez ich podejście do zdrowia i śmierci.
W jednym z rozdziałów opisuje jak to został zaproszony na egzotyczną wyspę na dwutygodniową sesję oczyszczającą, polegającą na głodówce, zażywaniu witamin i saunie. Prowadzący zachęcał obecnych aby codziennie oglądali na sitku, czy wydalają z organizmu złogi i toksyny, mające mieć postać żelowatych grudek różnych kolorów. Dowodem na to, że organizm się oczyścił, miało być ich zniknięcie z wydalin, jeśli do końca kuracji nie znikały, można było ją przedłużyć.
Po kilku dniach reporter zorientował się, że w skład suplementów witaminowych wchodził środek żelujący, a kolorowe kawałki to pozostałości osłonek kapsułek witamin. Gdy przestał je łykać, kolorowe grudki przestały się pojawiać.
Test burakowy
Nie jest to wprost metoda detoksyfikacji, a raczej wstęp do którejś z nich. Artykuły pseudodietetyków promują ten test jako metodę sprawdzenia stanu szczelności jelit. A jeśli jelita są nieszczelne, to organizm jest zatruty i trzeba go czyścić. Test polega bądź na zjedzeniu tartego buraka lub na wypiciu świeżego soku, jeśli po takiej potrawie mocz zabarwi się komuś na różowo lub czerwono, to znaczy, że ma nieszczelne jelita i kawałki treści jelit przedostają się mu do krwi. Bardzo obrazowy opis, trzeba przyznać.
W rzeczywistości zabarwienie moczu po burakach, czyli betaninuria, to stosunkowo częsty stan fizjologiczny, pojawiający się okresowo nawet u 10-15% ludzi. Wynika z wydalenia czerwonego barwnika buraka, betaniny, wraz z moczem po tym, jak został wchłonięty w jelitach. Nie następuje to u każdego i zawsze dlatego, bo zwykle betanina do jelita nie dociera. Barwnik ten jest dość wrażliwy na warunki, zwłaszcza kwasowość. Ulega rozpadowi do bezbarwnych produktów zarówno w środowisku zbyt kwaśnym (pH ok. 2 i mniejsze) jak i zbyt alkalicznym. W zasadzie zaczyna degradować już w warunkach obojętnych, zwłaszcza przy podgrzewaniu, stąd przy gotowaniu barszczu zawsze się go lekko zakwasza cytryną lub octem. Po drodze od ust do miejsca wchłonięcia, połknięty burak najpierw wpada do żołądka, który wytwarza kwas, po czym częściowo przetrawiona treść trafia do jelita cienkiego, gdzie zalewa ją dla odmiany bardzo zasadowa żółć. Ostatecznie więc w normalnych warunkach wchłania się niewielka ilość barwnika, niewystarczająca aby wpłynąć na kolor moczu.
Pojawienie się więc zabarwienia uryny oznacza, że po drodze warunki były dla buraka łagodniejsze niż zwykle - jeśli do żołądka trafiło dużo treści, jeszcze w dodatku popitej, barwnik nie był narażony na takie znów silne działanie kwasu. Jeśli ostatecznie posiłek nie był ciężkostrawny, to nie przebywał w żołądku zbyt długo. Z kolei na ilość wydzielonej żółci wpływ ma tłustość posiłku i jego pierwotna kwasowość. Gdy burak był mocniej zakwaszony sokiem z cytryny lub szczawiem, kwasy organiczne przeszkadzają żółci, działając jak bufor stabilizujący nieco kwaśniejsze warunki.
Nakładanie się tych dwóch efektów powoduje ostatecznie, że betanina nie zostaje zupełnie zdegradowana i wchłania się w dalszych odcinkach jelita dostatecznie, aby zabarwić mocz. W efekcie ta sama osoba może czasem doznawać zabarwienia a czasem nie, zależnie od kwasoty żołądka, obfitości posiłku, rodzaju posiłku i ilości buraka w porcji. Pewne badania sugerują częstsze pojawianie się betaninurii u osób z niedoborem żelaza, ale zjawisko jest zbyt mało specyficzne (jest za wiele sytuacji gdy efekt nie wynika z niedoboru żelaza tylko z rodzaju posiłku) aby służyło za test diagnostyczny.[5], [6]
----------
Źródła:
[1] https://www.livestrong.com/article/130395-detox-foot-patches-work/
[2] Deborah A. Kennedy et al. Objective Assessment of an Ionic Footbath (IonCleanse): Testing Its Ability to Remove Potentially Toxic Elements from the Body, Journal of Environmental and Public Health Volume 2012 (2012), Article ID 258968, 13 pages
[3] http://www.thelancet.com/journals/lancet/article/PIIS0140-6736(05)66373-8/fulltext
[4] https://sciencebasedmedicine.org/would-you-like-a-liver-flush-with-that-colon-cleanse/
[5] https://udel.edu/~mcdonald/mythbeeturia.html
[6] Eastwood, MA; Nyhlin, H (1995). "Beeturia and colonic oxalic acid". QJM. 88 (10): 711–7




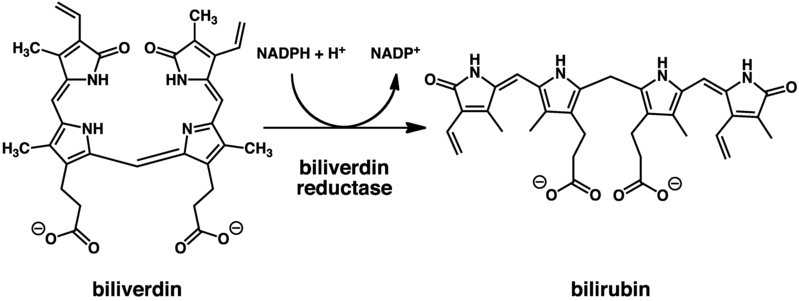
.jpg/800px-Black_eye_(3).jpg)