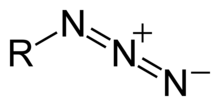Zdjęcia z archiwum - po zakończeniu ćwiczenia na preparatyce, podczas którego używaliśmy stopionego fenolu, zwróciłem uwagę na piękny pęk włóknistych kryształów powstały na dnie zlewki:
Wyglądały trochę jak lód. Sam fenol w formie proszku był nieco różowawy.
ps. Dopiero teraz zauważyłem, że to mój 200 wpis.
informacje
piątek, 26 czerwca 2015
poniedziałek, 15 czerwca 2015
Pytania czytelników
Od czasu do czasu dostaję pytania od czytelników bloga. Część pojawia się w komentarzach, i tam staram się na nie odpowiadać co można zobaczyć pod popularnymi postami. Część osób woli jednak drogę bardziej bezpośrednią, używając maila kontaktowego, jaki można znaleźć w opisie profilu, i odpowiedzi na te pytania nie są już powszechnie dostępne. Ponieważ zaś część pytań się powtarza, a niektóre są przecież dość ciekawe, uznałem że warto zebrać je w jednym miejscu, abym nie musiał się powtarzać
Aluminium w glinkach kosmetycznych
O tą rzecz pytano mnie już kilka razy, dlatego warto chyba odpowiedzieć publicznie.
Glina to formalnie rzecz biorąc, skała osadowa. Bardzo miękka a w stanie wilgotnym dająca się formować w rękach, ale skała. Aby osad mógł być zaliczony do glin, musi zawierać odpowiednio dużą ilość minerałów ilastych, przemieszanych z drobnym pyłem kwarcowym i skaleniowym. Tlenki żelaza i manganu nadają glinom kolor od żółtawego, przez rdzawoczerwony, brunatny, szary do ziemisto-zielonego. Glinki z małą ilością metali mogą być też białe.
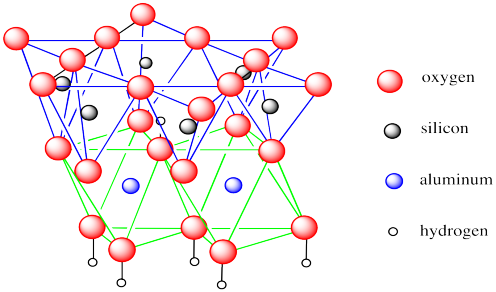
Minerały ilaste, uwalniane ze skał podczas wietrzenia, wypłukiwane w formie najdrobniejszego mułu czy wywiewane przez wiatr jako kurz, stanowią grupę krzemianów warstwowych, składających się z warstw połączonych tetraedrów tlenku krzemu SiO4 i tlenku glinu AlO4. Tlenek glinu jest izomorficzny z tlenkiem krzemu i może go naśladować, włączając się w krzemianową strukturę bez zmian. Poszczególne warstwy glinokrzemianowe są połączone wiązaniami wodorowymi, częściowo jonowymi, i potrafią wchłaniać między siebie inne substancje organiczne i nieorganiczne. Duży stopień uwodnienia powoduje, że warstwy mogą się względem siebie przesuwać, przez co glina staje się plastyczna. Właśnie zawartość tego pierwiastka w glinie stała się podstawą do zastąpienia w polskiej nomenklaturze łacińskiego aluminium nazwą glin.
Struktura warstwy kaolinu:
Wśród krzemianów warstwowych, najczęściej spotykamy się z talkiem, kaolinem będącym głównym składnikiem porcelany i montmorylonitem będącym głównym składnikiem bentonitu. Gliny zawierają mieszankę różnych glinokrzemianów ale niektóre posiadają przewagę jednego, konkretnego, stąd wyróżnia się białą glinkę kaolinową, glinkę pałygorskitową i inne.
A jak jest z tym aluminium?
Aby glin mógł być uwalniany z gliny, powinien być rozpuszczalny w wodzie. A gliny nie są. Nie dość, że zupełnie nierozpuszczalny w wodzie jest tlenek glinu, to w glinokrzemianach dodatkowo stabilizuje go włączenie w sieć krzemianową
Kwestia ta była zresztą szczegółowo badana, zwłaszcza z uwagi na używanie ceramiki jako naczyń kuchennych, oraz używanie glinokrzemianów jako dodatków do żywności. Wydaje się, że w warunkach odczynu obojętnego uwalnianie glinu nie zachodzi. Dopiero warunki kwaśne są w stanie uwolnić część jonów. W pewnym badaniu stwierdzono dla kwasowości pH 3 (sok pomarańczowy) minerały uwalniały dość niskie poziomy aluminium, ale tylko z bardzo cienkiej (3,5 mikrometra) warstwy powierzchniowej, co sugeruje, że w przypadku naczyń ceramicznych po pewnym czasie powstanie wypłukana warstewka powstrzymująca dalsze uwalnianie. Najsłabsze wymywanie stwierdzono dla kaolinu i montmorylonitu[1]. Uwolnienie ilości mających jakieś znaczenie toksykologiczne, zachodzi dopiero pod wpływem mocniejszych kwasów.
Glinki kosmetyczne nie mają tak kwaśnego odczynu, więc uwalniania aluminium nie ma co się obawiać.W dodatku czyste glinki, przepłukane dla wymycia zanieczyszczeń, jak to zwykle jest z glinkami kosmetycznymi, mają raczej skłonność do pochłaniania rozpuszczalnych jonów glinu niż do uwalniania.
W obszernym raporcie na temat bezpieczeństwa glinokrzemianów i tlenków glinu używanych w kosmetyce, nie stwierdzono negatywnych skutków dla minerałów ilastych. [2]
Podobne pytanie dotyczyło spożywania glinek na odtruwanie - tutaj także nie ma niebezpieczeństwa, kwasy żołądkowe są bowiem dosyć rozcieńczone. Jedynym istotnym wpływem jaki stwierdzono, jest zmniejszone wchłanianie żelaza u osób zażywających glinę, bowiem absorbowała żelazo z treści żołądkowej.
Aluminium w szczepionkach
Ze względu na popularny post o ałunie jestem chyba brany za eksperta od aluminium, skoro dotyczy tego koleje pytanie zadawane mi dwa razy.
Jak wiadomo, w niektórych szczepionkach dziecięcych pojawiają się związki aluminium. Podobno zawartość w jednej nie przekracza norm bezpieczeństwa. A co jakby zsumować zawartość we wszystkich - czy wtedy mogłoby zajść jakieś niebezpieczeństwo?
Wodorotlenek glinu pojawia się w szczepionkach jako nośnik białek lub polisacharydów mających wywołać reakcję organizmu. Normy z reguły uważają za najwyższą dopuszczalną dawkę glinu 60 mg/ kg. masy ciała dziennie. Z badań na zwierzętach wynika też, że najniższe dawki mające negatywny wpływ na płody i rozwijające się młode (u szczurów) to 45 mg/kg masy ciała dziennie.
Spośród szczepionek w kalendarzu szczepień, glin zawierają:
- EUVAX B 0,25 mg w jednej dawce lub ENGERIX B też 0,25 mg w jednej dawce (stosowane wymiennie)
- DTP 0,7 mg na dawkę
-IPV 0,5 mg na dawkę
Jak łatwo zauważyć, całkowita zawartość w jednej dawce jest kilkadziesiąt razy mniejsza od najniższych dawek toksycznych. Nawet gdyby wstrzyknąć wszystkie wymienione w ciągu jednego dnia, to nie doszłoby do przekroczenia choćby dziesiątej części toksycznej dawki.
Toksyczność ałunu
Czytelnik pytał o bezpieczeństwo ałunu dla dzieci. Chodziło mu o sytuację gdyby dziecko znalazło kawałek ałunu z pękniętego sztyftu i polizało lub połknęło.
Ałun potasowy i amonowy mają działanie drażniące na błony śluzowe, dlatego pierwszą reakcją w razie połknięcia będą zapewne wymioty. Po polizaniu dziecko pewnie straci ochotę na kolejny liz, ałun ma bowiem bardzo cierpki, nieprzyjemny smak i działanie ściągające. W razie połknięcia najlepiej dać dziecku dużo wody do wypicia i skontaktować się z lekarzem. W razie polizania też dać wody, ale lekarz pewnie nie będzie potrzebny.
Toksyczność ostra związku jest niska - dawka śmiertelna to 6 g/kg masy ciała
Co takiego rozpuszcza DMSO?
Pewien dociekliwy czytelnik zainteresowany medycznymi zastosowaniami DMSO dopytywał mnie o kwestie tego co się w tym rozpuszcza, a co nie i czy ma on zastosowania medyczne.
Dimetylosulfotlenek, czyli w skrócie DMSO to cenny rozpuszczalnik, używany w medycynie i chemii organicznej. Wykazuje dużą skłonność do wnikania w tkanki organizmu, na tyle, że trzeba uważać przy pracy z nim bo po wchłonięciu metabolizuje do związków o zapachu czosnku. Ponieważ rozluźnia strukturę lipidową skóry, może ułatwiać wchłonięcie przezskórnie różnych substancji, w tym wielu leków, dlatego czyni się próby z wykorzystaniem do terapii bez konieczności zastrzyków. Sam w sobie ma zresztą działanie przeciwzapalne.
Bywa rozpuszczalnikiem środków na grzybicę stóp, które zwykle dość słabo przenikają przez zrogowaciały naskórek na podeszwach, może być też składnikiem maści przeciwbólowych do działania miejscowego, może rozmiękczać skórę przy twardzinie i przerastających bliznach. Robiono na ten temat badania [3]
Drugie pytanie dotyczyło możliwości rozpuszczania chondroityny przez DMSO i smarowania tym stawów jako alternatywy dla suplementacji doustnej.
Chondroityna to mukopolisacharyd będący składnikiem chrząstek stawowych i w formie siarczanu stanowiący wraz z glukozaminą jeden z czynników zapewniających lepszy poślizg. W związku z tym powstał pomysł, że jeśli zbyt mała ilość mazi stawowej i mała elastyczność chrząstek stawu powodują bóle, to zażywanie chondroityny i dostarczanie jej do organizmu, powinno leczyć bądź powstrzymywać rozwój schorzeń stawów poprzez dostarczenie organizmowi składnika do wytworzenia większej ilości mazi. Na tym też opiera się potężna gałąź przemysłu suplemenciarskiego.
Niestety w niedawno opublikowanej potężnej metaanalizie wielu badań wykazano, że w porównaniu z placebo zażywanie chondroityny lub glukozaminy lub obu tych środków razem, nie zmniejsza bólów ani innych objawów[4]
Wygląda na to, że samo dostarczenie organizmowi składników potrzebnych do wytworzenia czegośtam w którymś organie, wcale nie musi go pobudzać aby tą substancję jednak wytworzyć, zwłaszcza że niedostateczne wydzielanie tej substancji wcale nie musi być wynikiem niedoboru podstawowego składnika, może być skutkiem innych czynników, w tym genetycznych. Dlatego jeśli przyjrzycie się emitowanym obecnie reklamom takich pigułek, zauważycie że wcale nie stwierdzają one wprost, iż zażycie tego składnika powstrzyma chorobę. Zamiast tego zawierają ogólniki, typu "glukozamina jest składnikiem chrząstki stawowej" i "maź stawowa ma decydujące znaczenie w zapewnieniu elastyczności stawu" i na koniec, że ich pigułka zawiera podwójną czy potrójną dawkę, zaś konstrukcję logiczną "skoro to jest składnikiem chrząstki a chrząstka jest potrzebna w stawach, to pomoże mi na stawy" widz musi sam sobie przeprowadzać, w czym udanie pomaga mu sugestia pokazywanego w reklamie pana którego bolą stawy, który bierze ich tabletki a potem wygląda na mniej cierpiącego.
Ale wróćmy do pytania - czy chondroityna rozpuszcza się w DMSO? Cóż - wedle obszernego podsumowania rozpuszczalności różnych substancji w tym rozpuszczalniku, chondroityna jest nie rozpuszczalna. Słabo rozpuszcza się chlorowodorek glukozaminy, natomiast bardzo dobrze przeciwbólowy Ibuprofen.[5]
Tak że raczej nie tędy droga.
Gdzie zbadać wodę?
Miałem też pytania o to gdzie można samemu zbadać wodę ze studni, źródła czy ujęcia.
Z tego co się orientuję, takie badania oferują jednostki Sanepidu, zbadają one zawartość metali ciężkich, czystość bakteriologiczną i własności fizyczne, jak zamulenie, obecność kwasów humusowych, zażelazienie itp. Oczywiście są to badania płatne.
Próbkę wody może pobrać wysłany pracownik, ale można ją też pobrać samemu. Warszawska stacja podaje na swojej stronie specyfikację sposobu pobierania próbek, aby nadawały się do badania.[6]
Dezodorant z podbiałem
Świadoma konsumentka zadała mi pytanie w sprawie używanego dezodorantu, który zawierał w swoim składzie podbiał pospolity. Chcąc dowiedzieć się czegoś o tym składniku, dowiedziała się że roślina zawiera uszkadzające wątrobę alkaloidy. I stąd powstało pytanie, czy taki alkaloid może wchłaniać się przez skórę?
Podbiał to cenne zioło lecznicze, lecz dopiero w ostatnich latach zorientowano się, że może zawierać alkaloidy pirolizydynowe, o działaniu hepatotoksycznym, które w wyniku zażywania dłuższym niż dwa miesiące mogą powodować toksyczną niewydolność wątroby. Ich zawartość w surowcach zbieranych w Europie jest jednak bardzo niska - w polskim badaniu stwierdzono poziomy rzędu 0,0013%[7]
W jednym badaniu na szczurach stwierdzono minimalne wchłanianie przezskórne alkaloidów żywokostu, w ilości 20 razy mniejszej niż przy podaniu doustnym. Stwierdzono też, że przy chłonięciu przeskórnym, nie dochodzi do zamiany nietoksycznego N-tlenku w toksyczną formę zredukowaną, co zwykle następowało w jelitach po spożyciu.[8] Zatem wydaje się, że kosmetyków z roślin zawierających te alkaloidy można używać bezpiecznie.
Czy to cyjanek?
Dwa lata temu czytelnik przesłał mi zdjęcie białego proszku, z pytaniem czy to cyjanek potasu. Cóż mogłem odpowiedzieć... Spektroskopu w oczach nie mam. Odpisałem, że może to być cyjanek albo soda, albo sól morska, albo cokolwiek innego bo bardzo wiele soli tak wygląda. Nie wiem o co chodziło.
----------
[1] http://www.clays.org/journal/archive/volume%2026/26-6-434.pdf
[2] http://www.ncbi.nlm.nih.gov/pubmed/12851164
[3] http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3460663/
[4] http://www.bmj.com/content/341/bmj.c4675
[5] http://www.gaylordchemical.com/uploads/images/pdfs/literature/102B_english.pdf
[6] http://www.wsse.waw.pl/PageContent.aspx?SubMenuID=100
[7] https://depot.ceon.pl/bitstream/handle/123456789/1121/hp%2058%204%202012%2062.pdf?sequence=1&isAllowed=y
[8] http://www.ncbi.nlm.nih.gov/pubmed/7128756?dopt=Abstract
Aluminium w glinkach kosmetycznych
O tą rzecz pytano mnie już kilka razy, dlatego warto chyba odpowiedzieć publicznie.
Glina to formalnie rzecz biorąc, skała osadowa. Bardzo miękka a w stanie wilgotnym dająca się formować w rękach, ale skała. Aby osad mógł być zaliczony do glin, musi zawierać odpowiednio dużą ilość minerałów ilastych, przemieszanych z drobnym pyłem kwarcowym i skaleniowym. Tlenki żelaza i manganu nadają glinom kolor od żółtawego, przez rdzawoczerwony, brunatny, szary do ziemisto-zielonego. Glinki z małą ilością metali mogą być też białe.
Minerały ilaste, uwalniane ze skał podczas wietrzenia, wypłukiwane w formie najdrobniejszego mułu czy wywiewane przez wiatr jako kurz, stanowią grupę krzemianów warstwowych, składających się z warstw połączonych tetraedrów tlenku krzemu SiO4 i tlenku glinu AlO4. Tlenek glinu jest izomorficzny z tlenkiem krzemu i może go naśladować, włączając się w krzemianową strukturę bez zmian. Poszczególne warstwy glinokrzemianowe są połączone wiązaniami wodorowymi, częściowo jonowymi, i potrafią wchłaniać między siebie inne substancje organiczne i nieorganiczne. Duży stopień uwodnienia powoduje, że warstwy mogą się względem siebie przesuwać, przez co glina staje się plastyczna. Właśnie zawartość tego pierwiastka w glinie stała się podstawą do zastąpienia w polskiej nomenklaturze łacińskiego aluminium nazwą glin.
Struktura warstwy kaolinu:
Wśród krzemianów warstwowych, najczęściej spotykamy się z talkiem, kaolinem będącym głównym składnikiem porcelany i montmorylonitem będącym głównym składnikiem bentonitu. Gliny zawierają mieszankę różnych glinokrzemianów ale niektóre posiadają przewagę jednego, konkretnego, stąd wyróżnia się białą glinkę kaolinową, glinkę pałygorskitową i inne.
A jak jest z tym aluminium?
Aby glin mógł być uwalniany z gliny, powinien być rozpuszczalny w wodzie. A gliny nie są. Nie dość, że zupełnie nierozpuszczalny w wodzie jest tlenek glinu, to w glinokrzemianach dodatkowo stabilizuje go włączenie w sieć krzemianową
Kwestia ta była zresztą szczegółowo badana, zwłaszcza z uwagi na używanie ceramiki jako naczyń kuchennych, oraz używanie glinokrzemianów jako dodatków do żywności. Wydaje się, że w warunkach odczynu obojętnego uwalnianie glinu nie zachodzi. Dopiero warunki kwaśne są w stanie uwolnić część jonów. W pewnym badaniu stwierdzono dla kwasowości pH 3 (sok pomarańczowy) minerały uwalniały dość niskie poziomy aluminium, ale tylko z bardzo cienkiej (3,5 mikrometra) warstwy powierzchniowej, co sugeruje, że w przypadku naczyń ceramicznych po pewnym czasie powstanie wypłukana warstewka powstrzymująca dalsze uwalnianie. Najsłabsze wymywanie stwierdzono dla kaolinu i montmorylonitu[1]. Uwolnienie ilości mających jakieś znaczenie toksykologiczne, zachodzi dopiero pod wpływem mocniejszych kwasów.
Glinki kosmetyczne nie mają tak kwaśnego odczynu, więc uwalniania aluminium nie ma co się obawiać.W dodatku czyste glinki, przepłukane dla wymycia zanieczyszczeń, jak to zwykle jest z glinkami kosmetycznymi, mają raczej skłonność do pochłaniania rozpuszczalnych jonów glinu niż do uwalniania.
W obszernym raporcie na temat bezpieczeństwa glinokrzemianów i tlenków glinu używanych w kosmetyce, nie stwierdzono negatywnych skutków dla minerałów ilastych. [2]
Podobne pytanie dotyczyło spożywania glinek na odtruwanie - tutaj także nie ma niebezpieczeństwa, kwasy żołądkowe są bowiem dosyć rozcieńczone. Jedynym istotnym wpływem jaki stwierdzono, jest zmniejszone wchłanianie żelaza u osób zażywających glinę, bowiem absorbowała żelazo z treści żołądkowej.
Aluminium w szczepionkach
Ze względu na popularny post o ałunie jestem chyba brany za eksperta od aluminium, skoro dotyczy tego koleje pytanie zadawane mi dwa razy.
Jak wiadomo, w niektórych szczepionkach dziecięcych pojawiają się związki aluminium. Podobno zawartość w jednej nie przekracza norm bezpieczeństwa. A co jakby zsumować zawartość we wszystkich - czy wtedy mogłoby zajść jakieś niebezpieczeństwo?
Wodorotlenek glinu pojawia się w szczepionkach jako nośnik białek lub polisacharydów mających wywołać reakcję organizmu. Normy z reguły uważają za najwyższą dopuszczalną dawkę glinu 60 mg/ kg. masy ciała dziennie. Z badań na zwierzętach wynika też, że najniższe dawki mające negatywny wpływ na płody i rozwijające się młode (u szczurów) to 45 mg/kg masy ciała dziennie.
Spośród szczepionek w kalendarzu szczepień, glin zawierają:
- EUVAX B 0,25 mg w jednej dawce lub ENGERIX B też 0,25 mg w jednej dawce (stosowane wymiennie)
- DTP 0,7 mg na dawkę
-IPV 0,5 mg na dawkę
Jak łatwo zauważyć, całkowita zawartość w jednej dawce jest kilkadziesiąt razy mniejsza od najniższych dawek toksycznych. Nawet gdyby wstrzyknąć wszystkie wymienione w ciągu jednego dnia, to nie doszłoby do przekroczenia choćby dziesiątej części toksycznej dawki.
Toksyczność ałunu
Czytelnik pytał o bezpieczeństwo ałunu dla dzieci. Chodziło mu o sytuację gdyby dziecko znalazło kawałek ałunu z pękniętego sztyftu i polizało lub połknęło.
Ałun potasowy i amonowy mają działanie drażniące na błony śluzowe, dlatego pierwszą reakcją w razie połknięcia będą zapewne wymioty. Po polizaniu dziecko pewnie straci ochotę na kolejny liz, ałun ma bowiem bardzo cierpki, nieprzyjemny smak i działanie ściągające. W razie połknięcia najlepiej dać dziecku dużo wody do wypicia i skontaktować się z lekarzem. W razie polizania też dać wody, ale lekarz pewnie nie będzie potrzebny.
Toksyczność ostra związku jest niska - dawka śmiertelna to 6 g/kg masy ciała
Co takiego rozpuszcza DMSO?
Pewien dociekliwy czytelnik zainteresowany medycznymi zastosowaniami DMSO dopytywał mnie o kwestie tego co się w tym rozpuszcza, a co nie i czy ma on zastosowania medyczne.
Dimetylosulfotlenek, czyli w skrócie DMSO to cenny rozpuszczalnik, używany w medycynie i chemii organicznej. Wykazuje dużą skłonność do wnikania w tkanki organizmu, na tyle, że trzeba uważać przy pracy z nim bo po wchłonięciu metabolizuje do związków o zapachu czosnku. Ponieważ rozluźnia strukturę lipidową skóry, może ułatwiać wchłonięcie przezskórnie różnych substancji, w tym wielu leków, dlatego czyni się próby z wykorzystaniem do terapii bez konieczności zastrzyków. Sam w sobie ma zresztą działanie przeciwzapalne.
Bywa rozpuszczalnikiem środków na grzybicę stóp, które zwykle dość słabo przenikają przez zrogowaciały naskórek na podeszwach, może być też składnikiem maści przeciwbólowych do działania miejscowego, może rozmiękczać skórę przy twardzinie i przerastających bliznach. Robiono na ten temat badania [3]
Drugie pytanie dotyczyło możliwości rozpuszczania chondroityny przez DMSO i smarowania tym stawów jako alternatywy dla suplementacji doustnej.
Chondroityna to mukopolisacharyd będący składnikiem chrząstek stawowych i w formie siarczanu stanowiący wraz z glukozaminą jeden z czynników zapewniających lepszy poślizg. W związku z tym powstał pomysł, że jeśli zbyt mała ilość mazi stawowej i mała elastyczność chrząstek stawu powodują bóle, to zażywanie chondroityny i dostarczanie jej do organizmu, powinno leczyć bądź powstrzymywać rozwój schorzeń stawów poprzez dostarczenie organizmowi składnika do wytworzenia większej ilości mazi. Na tym też opiera się potężna gałąź przemysłu suplemenciarskiego.
Niestety w niedawno opublikowanej potężnej metaanalizie wielu badań wykazano, że w porównaniu z placebo zażywanie chondroityny lub glukozaminy lub obu tych środków razem, nie zmniejsza bólów ani innych objawów[4]
Wygląda na to, że samo dostarczenie organizmowi składników potrzebnych do wytworzenia czegośtam w którymś organie, wcale nie musi go pobudzać aby tą substancję jednak wytworzyć, zwłaszcza że niedostateczne wydzielanie tej substancji wcale nie musi być wynikiem niedoboru podstawowego składnika, może być skutkiem innych czynników, w tym genetycznych. Dlatego jeśli przyjrzycie się emitowanym obecnie reklamom takich pigułek, zauważycie że wcale nie stwierdzają one wprost, iż zażycie tego składnika powstrzyma chorobę. Zamiast tego zawierają ogólniki, typu "glukozamina jest składnikiem chrząstki stawowej" i "maź stawowa ma decydujące znaczenie w zapewnieniu elastyczności stawu" i na koniec, że ich pigułka zawiera podwójną czy potrójną dawkę, zaś konstrukcję logiczną "skoro to jest składnikiem chrząstki a chrząstka jest potrzebna w stawach, to pomoże mi na stawy" widz musi sam sobie przeprowadzać, w czym udanie pomaga mu sugestia pokazywanego w reklamie pana którego bolą stawy, który bierze ich tabletki a potem wygląda na mniej cierpiącego.
Ale wróćmy do pytania - czy chondroityna rozpuszcza się w DMSO? Cóż - wedle obszernego podsumowania rozpuszczalności różnych substancji w tym rozpuszczalniku, chondroityna jest nie rozpuszczalna. Słabo rozpuszcza się chlorowodorek glukozaminy, natomiast bardzo dobrze przeciwbólowy Ibuprofen.[5]
Tak że raczej nie tędy droga.
Gdzie zbadać wodę?
Miałem też pytania o to gdzie można samemu zbadać wodę ze studni, źródła czy ujęcia.
Z tego co się orientuję, takie badania oferują jednostki Sanepidu, zbadają one zawartość metali ciężkich, czystość bakteriologiczną i własności fizyczne, jak zamulenie, obecność kwasów humusowych, zażelazienie itp. Oczywiście są to badania płatne.
Próbkę wody może pobrać wysłany pracownik, ale można ją też pobrać samemu. Warszawska stacja podaje na swojej stronie specyfikację sposobu pobierania próbek, aby nadawały się do badania.[6]
Dezodorant z podbiałem
Świadoma konsumentka zadała mi pytanie w sprawie używanego dezodorantu, który zawierał w swoim składzie podbiał pospolity. Chcąc dowiedzieć się czegoś o tym składniku, dowiedziała się że roślina zawiera uszkadzające wątrobę alkaloidy. I stąd powstało pytanie, czy taki alkaloid może wchłaniać się przez skórę?
Podbiał to cenne zioło lecznicze, lecz dopiero w ostatnich latach zorientowano się, że może zawierać alkaloidy pirolizydynowe, o działaniu hepatotoksycznym, które w wyniku zażywania dłuższym niż dwa miesiące mogą powodować toksyczną niewydolność wątroby. Ich zawartość w surowcach zbieranych w Europie jest jednak bardzo niska - w polskim badaniu stwierdzono poziomy rzędu 0,0013%[7]
W jednym badaniu na szczurach stwierdzono minimalne wchłanianie przezskórne alkaloidów żywokostu, w ilości 20 razy mniejszej niż przy podaniu doustnym. Stwierdzono też, że przy chłonięciu przeskórnym, nie dochodzi do zamiany nietoksycznego N-tlenku w toksyczną formę zredukowaną, co zwykle następowało w jelitach po spożyciu.[8] Zatem wydaje się, że kosmetyków z roślin zawierających te alkaloidy można używać bezpiecznie.
Czy to cyjanek?
Dwa lata temu czytelnik przesłał mi zdjęcie białego proszku, z pytaniem czy to cyjanek potasu. Cóż mogłem odpowiedzieć... Spektroskopu w oczach nie mam. Odpisałem, że może to być cyjanek albo soda, albo sól morska, albo cokolwiek innego bo bardzo wiele soli tak wygląda. Nie wiem o co chodziło.
----------
[1] http://www.clays.org/journal/archive/volume%2026/26-6-434.pdf
[2] http://www.ncbi.nlm.nih.gov/pubmed/12851164
[3] http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3460663/
[4] http://www.bmj.com/content/341/bmj.c4675
[5] http://www.gaylordchemical.com/uploads/images/pdfs/literature/102B_english.pdf
[6] http://www.wsse.waw.pl/PageContent.aspx?SubMenuID=100
[7] https://depot.ceon.pl/bitstream/handle/123456789/1121/hp%2058%204%202012%2062.pdf?sequence=1&isAllowed=y
[8] http://www.ncbi.nlm.nih.gov/pubmed/7128756?dopt=Abstract
czwartek, 11 czerwca 2015
6 substancji z którymi wolałbym nie pracować
Inspiracją do wpisu był ten, niedawno opublikowany film popularnonaukowy z serii "Uwaga! Naukowy bełkot":
Jest to cenna seria, w ciekawy sposób przedstawiająca informacje z różnych dziedzin, jednak z tym odcinkiem mam pewien kłopot - autor chyba nie zupełnie rozsądnie zebrał 6 groźnych substancji pod mylącym tytułem a opowiadając o nich zastosował nadmierne uproszczenia. Co postaram się pokrótce objaśnić zanim podam swoją listę
Z czym można pracować i co nie jest naj
Jedną z maksym przypisywanych Einsteinowi jest ta o przekazywaniu informacji, mówiąca że należy upraszczać jak można, ale nie bardziej. Bo jeśli coś uprościmy za bardzo, możemy wprowadzić inną osobę w błąd.
Ten problem dotyczy Polonu-210 opisanego przez autora jako "najbardziej promieniotwórcza substancja znana Ludzkości". Jak tłumaczy w komentarzach, wybrał tą substancję, bo jest dostępna w stosunkowo dużych ilościach, silnie radioaktywna i ma na tyle długi czas półrozpadu, że człowiek zdąży się nią zatruć. Ale o tym w filmie nie wspomina. Widz dostaje tylko prosty przekaz "Polon-210 jest najbardziej promieniotwórczy w ogóle", co nie jest prawdą.
Zgodnie z definicją aktywności promieniotwórczej, jest to szybkość z jaką następują rozpady promieniotwórcze. Największą aktywność mają te z najkrótszymi czasami półrozpadu i małymi masami, z czego wynika że najbardziej promieniotwórczą substancją jest Wodór-7 o czasie półtrwania 2,3×10−23 s i masie 8 unitów.
Tak że akurat Polon-210 byłby raczej "najbardziej promieniotwórczą substancją z jaką można się zetknąć" w tym znaczeniu, że jest stosunkowo dostępny i niektórzy muszą z nim pracować - choć można spekulować czy przypadkiem bardziej szkodliwy nie jest ameryk-243, spotykany w czujnikach dymu, który jest wytwarzany w większych ilościach a oprócz mało przenikliwego promieniowania alfa, produkuje też wysokoenergetyczne promienie gamma.
Podobny problem dotyczy "najbardziej palnej substancji" czyli trifluorku chloru, bo przecież fluorek ten sam w sobie nie jest specjalnie palny - jest natomiast silnym środkiem zapalającym, powodującym zapłon innych substancji z którymi się zetknie, a przy tym przeżerający substancje niepalne.
Myślę, że wśród najbardziej palnych substancji na pewno znajduje się silan, czyli krzemowy analog metanu. Duże powinowactwo krzemu do tlenu i ujemna jonizacja wodoru powodują, że w mieszance z tlenem ulega samozapłonowi w temperaturach około -100 °C, przy czym różne prace podają różne dane, w jednej opisano zapłon mieszanki z powietrzem w temperaturze -162 °C[1] Natomiast silniejszym od trifluorku chloru środkiem utleniającym i zapalającym inne substancje jest zapewne difluorek ditlenu, potrafiący zapalić stały metan w temperaturze 90 K.[2]
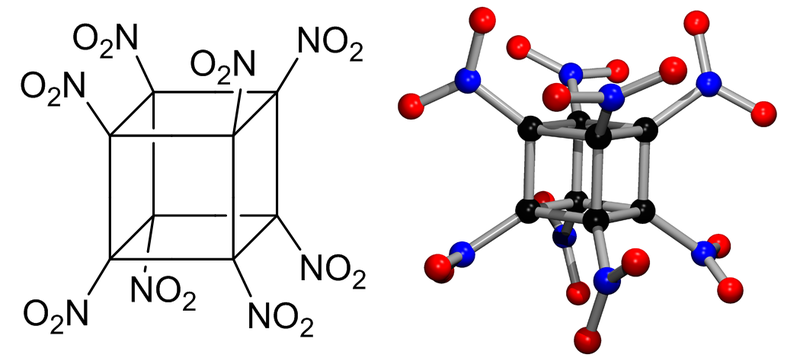
Inny problem dotyczy pozostałych substancji - tematem filmu są substancje "z którymi wolelibyście nie pracować" bo są niebezpieczne, trudne do obsługi, groźne jeśli się z nimi zetknąć. Tylko że w tym kontekście materiał wybuchowy oktanitrokuban pomimo swej niesamowitej siły wybuchowej zupełnie do zestawienia nie pasuje, jest bowiem stosunkowo bezpieczny - nie wybucha pod wpływem wstrząsów, nie powinien eksplodować nawet po uderzeniu młotkiem, dopiero wybuch spłonki inicjującej wywołuje eksplozję. Osobiście wolałbym pracować z nim, niż z na przykład chloranem potasu (jest ciekawszy).
Dlatego do zestawienia pasuje właściwie tylko batrachotoksyna, dwucyjan i ten bardzo azotowy materiał wybuchowy, eksplodujący spontanicznie.
Trochę zdziwiło mnie zatem, że autor filmu zapomniał o kilku innych substancjach, które warto tu pokrótce opisać.
Z czym ja wolałbym jako chemik nie pracować:
1. Diselenek węgla
Analog dwusiarczku węgla, przydatny w niektórych syntezach. A przy tym związek niesamowicie wprost śmierdzący. Po tym jak w 1936 roku otrzymano go po raz pierwszy, konieczna była ewakuacja najbliższej miejscowości, leżącej po zawietrznej stronie laboratorium. Jest lotny, łatwo przenika przez gumę i wchłania się do organizmu, łatwo przenika przez błony komórkowe i jest neurotoksyczny. Chemik pracujący z tym związkiem przez dłuższy czas otoczony byłby banieczką nieznośnego zapachu i bez wątpienia znalazłby wolne miejsce w tramwaju.
Podobne efekty mogą dawać też inne związki selenoorganiczne, jak selenol, analog etanolu, czy selenofenol.
Nie chcę zostać na kilka tygodni człowiekiem-skunksem, więc pracy z tym związkiem będę unikał.
2. Dimetylortęć
Jedna z najsilniejszych znanych trucizn. Dawka śmiertelna dla człowieka właściwie nie jest znana, estymuje się ją na podstawie kilku wypadków śmiertelnych. Znanym przypadkiem było zatrucie badaczki Karen Wetterhahn, której na rękawiczki rozprysnęło się ok. 0,05 ml substancji. Przeniknęła przez rękawiczki i w krótkim czasie wchłonęła się przez skórę w ilości wystarczającej do zabicia. Z batrachotoksyną czy jeszcze silniejszą ciguarotoksyną można w miarę bezpieczne pracować, z dimetylortęcią nie jest już tak dobrze.
Tak że jeśli na prawdę nie będzie mi to do czegoś potrzebne, wolę z tą substancją nie pracować.
3. Benzo-a-piren
Jeden z najważniejszych wielopierścieniowych węglowodorów aromatycznych (WWA) będących rakotwórczymi składnikami dymu. Metabolity benzo-a-pirenu łączą się z DNA wywołując mutacje. Spożyty wywołuje raka żołądka i jelit, obecność w powietrzu sprzyja nowotworom płu, a zanieczyszczenie skóry może wywołać raka skóry. W niektórych badaniach już jednokrotna iniekcja podskórna ekstraktu zwierającego WWA wywoływała nowotwory u badanych zwierzat.
Tak że pracy nad tym związkiem czystym, lub w ekstraktach wolałbym też unikać.
4. Gaz musztardowy
Środek bojowy będący silnym środkiem alkilującym. Wywołuje silne oparzenia skóry które ujawniają się nawet dobę po kontakcie z substancją, wchłonięty drogą inhalacyjną daje objawy zatrucia z dużym opóźnieniem, od 4 do 6 godzin dla małych dawek (dla dużych natychmiastowo). Jest potwierdzonym środkiem rakotwórczym.
Tak więc pragnącym zachować zdrowie i ładną twarz też radzę unikać styczności z tą substancją
5. Azydek sodu
Sól kwasu azotowodorowego, zawierająca trzy połączone atomy azotu. Azydki nieorganiczne zwykle są stosowane w syntezie azydków organicznych, oraz 1,2,3 triazyn, ewentualnie tetrazolu. Niestety azydki są związkami nietrwałymi i bardzo silnie trującymi, porównywalnie z cyjankami. Chętnie hydrolizują do azotowodoru, gazu bardziej toksycznego niż tlenek węgla, który w śladowych, niewyczuwalnych stężeniach jest w stanie wywołać zatrucie. Ekspozycja wywołuje mdłości, bóle głowy, uszkodzenie włókien nerwowych, zaburzenia oddychania zaś działaniem długofalowym po zatruciu jest uszkodzenie wątroby i jąder. Zatrucia tym związkiem wśród chemików są notowane dość często.
Przy ogrzewaniu potrafią eksplodować. Z jonami metali ciężkich tworzą wrażliwe na wstrząsy i nacisk azydki, używane czasem jeszcze w spłonkach.
Tak więc z tymi związkami bez konieczności też dobrze by było nie pracować
6. Siarczan niklu
Ten związek jest akurat stosunkowo często spotykany w laboratoriach chemii nieorganicznej. Jego głównym niebezpieczeństwem jest łatwość wywoływania alergii - powtarzalny kontakt ze związkiem skutkuje rozwinięciem się alergii na nikiel i kilkunastu procent ludzi. A zaistnienie takiej alergii może potem poważnie utrudniać życie, w związku z występowaniem niklu w wielu stopach metali używanych w elektronice czy medycynie.
------
[1] http://cdn.intechopen.com/pdfs-wm/24448.pdf
[2] http://pubs.acs.org/doi/abs/10.1021/ja00893a004
Z czym można pracować i co nie jest naj
Jedną z maksym przypisywanych Einsteinowi jest ta o przekazywaniu informacji, mówiąca że należy upraszczać jak można, ale nie bardziej. Bo jeśli coś uprościmy za bardzo, możemy wprowadzić inną osobę w błąd.
Ten problem dotyczy Polonu-210 opisanego przez autora jako "najbardziej promieniotwórcza substancja znana Ludzkości". Jak tłumaczy w komentarzach, wybrał tą substancję, bo jest dostępna w stosunkowo dużych ilościach, silnie radioaktywna i ma na tyle długi czas półrozpadu, że człowiek zdąży się nią zatruć. Ale o tym w filmie nie wspomina. Widz dostaje tylko prosty przekaz "Polon-210 jest najbardziej promieniotwórczy w ogóle", co nie jest prawdą.
Zgodnie z definicją aktywności promieniotwórczej, jest to szybkość z jaką następują rozpady promieniotwórcze. Największą aktywność mają te z najkrótszymi czasami półrozpadu i małymi masami, z czego wynika że najbardziej promieniotwórczą substancją jest Wodór-7 o czasie półtrwania 2,3×10−23 s i masie 8 unitów.
Tak że akurat Polon-210 byłby raczej "najbardziej promieniotwórczą substancją z jaką można się zetknąć" w tym znaczeniu, że jest stosunkowo dostępny i niektórzy muszą z nim pracować - choć można spekulować czy przypadkiem bardziej szkodliwy nie jest ameryk-243, spotykany w czujnikach dymu, który jest wytwarzany w większych ilościach a oprócz mało przenikliwego promieniowania alfa, produkuje też wysokoenergetyczne promienie gamma.
Podobny problem dotyczy "najbardziej palnej substancji" czyli trifluorku chloru, bo przecież fluorek ten sam w sobie nie jest specjalnie palny - jest natomiast silnym środkiem zapalającym, powodującym zapłon innych substancji z którymi się zetknie, a przy tym przeżerający substancje niepalne.
Myślę, że wśród najbardziej palnych substancji na pewno znajduje się silan, czyli krzemowy analog metanu. Duże powinowactwo krzemu do tlenu i ujemna jonizacja wodoru powodują, że w mieszance z tlenem ulega samozapłonowi w temperaturach około -100 °C, przy czym różne prace podają różne dane, w jednej opisano zapłon mieszanki z powietrzem w temperaturze -162 °C[1] Natomiast silniejszym od trifluorku chloru środkiem utleniającym i zapalającym inne substancje jest zapewne difluorek ditlenu, potrafiący zapalić stały metan w temperaturze 90 K.[2]
Inny problem dotyczy pozostałych substancji - tematem filmu są substancje "z którymi wolelibyście nie pracować" bo są niebezpieczne, trudne do obsługi, groźne jeśli się z nimi zetknąć. Tylko że w tym kontekście materiał wybuchowy oktanitrokuban pomimo swej niesamowitej siły wybuchowej zupełnie do zestawienia nie pasuje, jest bowiem stosunkowo bezpieczny - nie wybucha pod wpływem wstrząsów, nie powinien eksplodować nawet po uderzeniu młotkiem, dopiero wybuch spłonki inicjującej wywołuje eksplozję. Osobiście wolałbym pracować z nim, niż z na przykład chloranem potasu (jest ciekawszy).
Dlatego do zestawienia pasuje właściwie tylko batrachotoksyna, dwucyjan i ten bardzo azotowy materiał wybuchowy, eksplodujący spontanicznie.
Trochę zdziwiło mnie zatem, że autor filmu zapomniał o kilku innych substancjach, które warto tu pokrótce opisać.
Z czym ja wolałbym jako chemik nie pracować:
1. Diselenek węgla
Analog dwusiarczku węgla, przydatny w niektórych syntezach. A przy tym związek niesamowicie wprost śmierdzący. Po tym jak w 1936 roku otrzymano go po raz pierwszy, konieczna była ewakuacja najbliższej miejscowości, leżącej po zawietrznej stronie laboratorium. Jest lotny, łatwo przenika przez gumę i wchłania się do organizmu, łatwo przenika przez błony komórkowe i jest neurotoksyczny. Chemik pracujący z tym związkiem przez dłuższy czas otoczony byłby banieczką nieznośnego zapachu i bez wątpienia znalazłby wolne miejsce w tramwaju.
Podobne efekty mogą dawać też inne związki selenoorganiczne, jak selenol, analog etanolu, czy selenofenol.
Nie chcę zostać na kilka tygodni człowiekiem-skunksem, więc pracy z tym związkiem będę unikał.
2. Dimetylortęć
Jedna z najsilniejszych znanych trucizn. Dawka śmiertelna dla człowieka właściwie nie jest znana, estymuje się ją na podstawie kilku wypadków śmiertelnych. Znanym przypadkiem było zatrucie badaczki Karen Wetterhahn, której na rękawiczki rozprysnęło się ok. 0,05 ml substancji. Przeniknęła przez rękawiczki i w krótkim czasie wchłonęła się przez skórę w ilości wystarczającej do zabicia. Z batrachotoksyną czy jeszcze silniejszą ciguarotoksyną można w miarę bezpieczne pracować, z dimetylortęcią nie jest już tak dobrze.
Tak że jeśli na prawdę nie będzie mi to do czegoś potrzebne, wolę z tą substancją nie pracować.
3. Benzo-a-piren
Jeden z najważniejszych wielopierścieniowych węglowodorów aromatycznych (WWA) będących rakotwórczymi składnikami dymu. Metabolity benzo-a-pirenu łączą się z DNA wywołując mutacje. Spożyty wywołuje raka żołądka i jelit, obecność w powietrzu sprzyja nowotworom płu, a zanieczyszczenie skóry może wywołać raka skóry. W niektórych badaniach już jednokrotna iniekcja podskórna ekstraktu zwierającego WWA wywoływała nowotwory u badanych zwierzat.
Tak że pracy nad tym związkiem czystym, lub w ekstraktach wolałbym też unikać.
4. Gaz musztardowy
Środek bojowy będący silnym środkiem alkilującym. Wywołuje silne oparzenia skóry które ujawniają się nawet dobę po kontakcie z substancją, wchłonięty drogą inhalacyjną daje objawy zatrucia z dużym opóźnieniem, od 4 do 6 godzin dla małych dawek (dla dużych natychmiastowo). Jest potwierdzonym środkiem rakotwórczym.
Tak więc pragnącym zachować zdrowie i ładną twarz też radzę unikać styczności z tą substancją
5. Azydek sodu
Sól kwasu azotowodorowego, zawierająca trzy połączone atomy azotu. Azydki nieorganiczne zwykle są stosowane w syntezie azydków organicznych, oraz 1,2,3 triazyn, ewentualnie tetrazolu. Niestety azydki są związkami nietrwałymi i bardzo silnie trującymi, porównywalnie z cyjankami. Chętnie hydrolizują do azotowodoru, gazu bardziej toksycznego niż tlenek węgla, który w śladowych, niewyczuwalnych stężeniach jest w stanie wywołać zatrucie. Ekspozycja wywołuje mdłości, bóle głowy, uszkodzenie włókien nerwowych, zaburzenia oddychania zaś działaniem długofalowym po zatruciu jest uszkodzenie wątroby i jąder. Zatrucia tym związkiem wśród chemików są notowane dość często.
Przy ogrzewaniu potrafią eksplodować. Z jonami metali ciężkich tworzą wrażliwe na wstrząsy i nacisk azydki, używane czasem jeszcze w spłonkach.
Tak więc z tymi związkami bez konieczności też dobrze by było nie pracować
6. Siarczan niklu
Ten związek jest akurat stosunkowo często spotykany w laboratoriach chemii nieorganicznej. Jego głównym niebezpieczeństwem jest łatwość wywoływania alergii - powtarzalny kontakt ze związkiem skutkuje rozwinięciem się alergii na nikiel i kilkunastu procent ludzi. A zaistnienie takiej alergii może potem poważnie utrudniać życie, w związku z występowaniem niklu w wielu stopach metali używanych w elektronice czy medycynie.
------
[1] http://cdn.intechopen.com/pdfs-wm/24448.pdf
[2] http://pubs.acs.org/doi/abs/10.1021/ja00893a004
Subskrybuj:
Posty (Atom)