Na ten ciekawy przypadek natrafiłem przeglądając artykuły o twórczości Salvadora Dalego, jednego z moich ulubionych malarzy. Najszerzej znane jego dzieła, jak "Płonąca żyrafa" czy "Trwałość pamięci" pochodzą z początkowych lat kariery. Miał tę karierę jednak bardzo długą i w ostatnich dwóch dekadach zaczął tworzyć kolażowe zestawienia obiektów z różnych obiektów, czerpiąc inspirację z komercyjnych produktów, zdjęć, filmów. A także z wynalazków i osiągnięć nauki. Dali interesował się odkryciami naukowymi, korespondował z naukowcami i prenumerował czasopisma. Tematy związane z odkryciami i wynalazkami pojawiały się w obrazach z lat 70 i później, aż do końca jego życia, w tym też tematyka związana z odkryciami biologii i chemii [1]. Wśród tematów jakie szczególnie często go zastanawiały była fizyka jądrowa, nowoczesna matematyka i odkrycia biologii. Żywo zareagował na doniesienia o odkryciu struktury DNA, której regularna, helikalna symetria wyglądała fascynująco, mistycznie. Już w 1957 umieścił schemat podwójnej helisy na obrazie "Krajobraz motyli". Malarz miał zresztą okazję poznać Watsona, jednego z badaczy proponujących model DNA, więc temat nie był mu obcy. [2]
Artykuły omawiające naukowe inspiracje artysty często jednym tchem wymieniają ten obraz wraz z późnym dziełem "Structure of DNA", będącym parą obrazów stereoskopowych, które według wielu opisów mają przedstawiać zgodnie z tytułem strukturę DNA. Poszukałem tych obrazów i dobrze się im przyjrzałem. Cóż, można wybaczyć krytykom sztuki, że wzięli tytuł za dobrą monetę, ale mnie jako chemikowi trudno nie zauważyć, że struktura na obrazach w niczym nie przypomina DNA.

Para obrazów z 1975 roku zatytułowana "Structure of DNA" była stworzona z myślą o oglądaniu stereoskopowym. Należy spojrzeć na oba na raz tak, że jedno oko patrzy na jeden a drugie na drugi i oba nakładają się na siebie w przestrzeni. Można to osiągnąć patrząc przez odpowiednie okulary zakrzywiające obraz, oglądając zdjęcia w stereoskopie lub fotoplastikonie, ale zdecydowanie najczęściej ogląda się takie obrazy robiąc lekkiego zeza, tak aby półprzezroczysty obraz z jednej strony nałożył się na drugi, tworząc sumę, która jest odbierana jak obiekt 3D.
Tak więc przy odpowiednim spojrzeniu zaczniemy dostrzegać namalowane obiekty przestrzennie i zobaczymy, że najbliżej znajduje się czarna cząsteczka na dole, która jest skierowana ku nam trójdzielną grupą. W kolejnej warstwie są dwie, równoległe fioletowe (po lewej) lub żółte (po prawej), a nad nimi jedna biała/żółta. Jeden z atomów czarnej cząsteczki zostaje częściowo przesłonięty atomem jednej z fioletowej/żółtej, z kolei jeden z atomów górnej cząsteczki częściowo przesłania pierścień cząsteczki pod nim. Wszystko to tworzy ciekawą kompozycję przestrzenną. Tylko, że to nie ma za bardzo związku z DNA.
Przekonanie, że te obrazy przedstawiają DNA zgodnie z ich tytułem jest chyba dość powszechne - pojawia się w krótkim liście zamieszczonym w publicystycznej części czasopisma The Nature z 2003 roku. [3] Jan Domaradzki w artykule z 2015 roku omawia przykłady biologicznych inspiracji Dalego i wymienia tam te obrazy, opisując je jako przedstawiające różnokolorową podwójną helisę.[4] No ciekawe gdzie on tam widzi helisy?
Na co właściwie patrzymy na obrazach? Są to modele cząsteczek związku chemicznego, a konkretnie są to cztery oddzielne cząsteczki, nie tworzące żadnej helisy, przedstawione na tle szkieletu sześcianu. Atomy mają zdeformowany kształt mniej lub bardziej wydłużonego jajka. Oznacza to, że jest to model wykorzystujący elipsoidy termiczne.
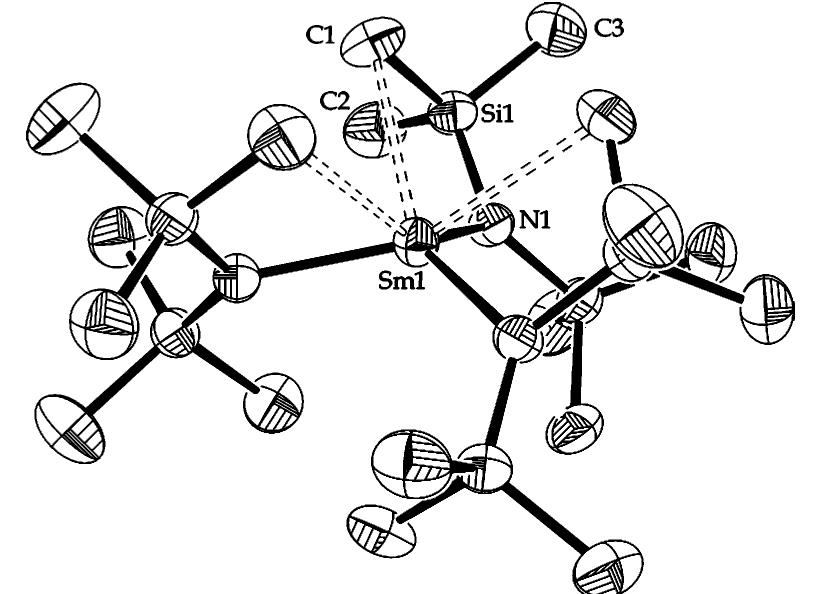 |
Cząsteczka kompleksu samaru z pracy:
Inorganic Chemistry 2003 42 (21), 6682-6690
|
Atomy w strukturze cząsteczki w krysztale ulegają drganiom termicznym, wpływa to na rozmycie przestrzenne sygnałów rejestrowanych metodami krystalografii. Można z tego rozmycia wydobyć informacje o tym jak bardzo atom drga w trzech prostopadłych kierunkach przestrzeni. Graficznym przedstawieniem tego zakresu drgań jest obła bryła będąca elipsoidą obrotową, a więc bryłą której przekrój jest eliptyczny wzdłuż, w poprzek i na płask. Kształt ten jest w różnych stylach rysowania podkreślany prostopadłymi liniami, lub wcięciem. Im mocniej drga atom w strukturze cząsteczki, tym bardziej wydłużona jest jego elipsoida. Atom wykonujący wiele złożonych drgań w trzech kierunkach przestrzeni jest w takim ujęciu większy od atomu bardziej statycznego.
Przedstawione cząsteczki nie przypominają żadnej ze składowych cząsteczki DNA, nie mogą stanowić jakiegoś bliskiego fragmentu tej struktury i jestem bardzo zdziwiony, że przez tyle lat nikt nie zwrócił na to uwagi. Czym mogą być te cząsteczki? Nie są narysowane całkiem poprawnie, co wyjaśnię później, ale ogólne pierwsze wrażenie jest takie, że to mogło być wzorowane na rysunkach struktury krystalicznej para-ksylenu.
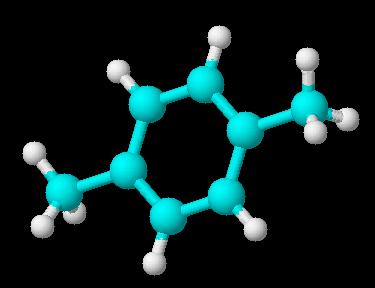
Pierścień w cząsteczkach ma sześciokątny kształt i jest płaski, co pasuje do aromatycznego pierścienia w p-ksylenie, jeśli w rysunku pominięto wodory przy pierścieniu. Pochodne cykloheksanu byłyby bardziej wygięte. Natomiast wygląd dwóch grup odstających od pierścienia pasuje do grup metylowych z pokazanymi pozycjami trzech wodorów. Dużo większe i wydłużone poprzecznie do dłuższej osi cząsteczki elipsoidy termiczne protonów to częsta cecha tych właśnie grup. To, że Dali mógł się wzorować na rysunkach tej właśnie struktury nie jest niemożliwe, bo w jego czasach już taką ją opisano. Tylko może być ciężko to dowieść.
Pierwsza publikacja na temat struktury krystalicznej p-ksylenu pochodzi jeszcze z 1960 roku (Indian J. Phys.(1960), 34, 263-271 ), ale w 1986 ukazała się nowa analiza, wykazująca między innymi, że dane podane w tamtej starej publikacji są niepoprawne. Biorąc jednak pod uwagę czas wykonania obrazów, musiały opierać się na rysunkach struktury z tej starszej publikacji. [5]
W nowszych publikacjach można znaleźć rysunki takiej struktury i sposób w jaki cząsteczki układają się w przestrzeni (na jodełkę) rzeczywiście bardzo przypomina strukturę Dalego. Jest to typowy układ dla prostych pochodnych benzenu wynikający z efektów magnetycznych pierścienia aromatycznego.
 |
| Crystal Growth & Design 2022, 22, 6 |
Z tym rozwiązaniem jest jednak ten problem, że Dali najwyraźniej przenosił rysunki struktury na obraz niedokładnie i ostateczny wynik zawiera dużo błędów. Najważniejsza kwestia jest taka, że pomimo sześciokątnego kształtu pierścieni, te na obrazach składają się z ośmiu a nie sześciu atomów. Jednak pierścienie cząsteczek organicznych złożone z ośmiu atomów nie mogą być płaskie - cyklooktan układa się w przestrzeni w kształt łódeczki, jego annulen cyklooktatetraen jest antyaromatyczny i także wygina się przestrzennie.
Można by to zwalić na licencję artystyczną, ale mi to wygląda na błąd przerysowania lub na celowe zepsucie cząsteczki dla gęstszego układu. Niektóre inne zmiany mają uzasadnienie i są zamierzone - brak atomów wodoru przy pierścieniach zmniejsza nakładanie cząsteczek i poprawia rozróżnianie atomów. Dolna grupa metylowa górnej cząsteczki ma zaznaczony tylko jeden wodór, ten bliżej nas (biały owal na niebieskiej wersji), pozostałe zasłaniałyby cząsteczkę z tyłu. Jednak wycinanie nadmiarowych atomów nie do końca się powiodło, i tak na niebieskiej wersji grupa metylowa fioletowej cząsteczki po lewej ma towarzyszące jej cztery atomy zamiast trzech. Nadmiarowa elipsoida jest bliżej nas niż cząsteczka. Widać to dobrze porównując cząsteczkę lewą z prawą lub sprawdzając wygląd na wersji brązowej, gdzie tego dodatkowego atomu nie ma. Skąd się tam wziął? Z grupy metylowej górnej cząsteczki.
Na prawej, brązowej wersji obrazu widać dobrze, że grupa ta ma tam zaznaczony tylko jeden wodór, bliżej obserwatora. Na niebieskiej wersji zapewne też tak miało być, ale podczas uzupełniania wstępnego szkicu położenia cząsteczek doszło do błędu, i elipsoida atomu wodoru, który w drugiej wersji pominięto aby nie zasłaniał, w tej wersji została przypisana lewej cząsteczce i pokolorowana na fioletowo. Widać tą tożsamość gdy nałoży się na to miejsce będącą w tym samym położeniu grupę metylową czarnej cząsteczki poniżej.
Czemu więc po skrupulatnym oddaniu na płótnie struktury krystalicznej jakiegoś prostego związku organicznego, Dali zatytułował obrazy "Struktura DNA"? Możliwe, że takie było jego początkowe założenie, że namaluje naukową strukturę tego związku, ale okazała się zbyt skomplikowana więc wziął coś innego. A może uznał, że taki tytuł będzie brzmiał lepiej niż "Struktura kryształu niepoprawnie narysowanego para-ksylenu"?
Można gdybać.
-------
[1] https://www.elespanol.com/ciencia/20180331/dali-genio-pintura-dejo-boquiabierto-severo-ochoa/295221428_0.html
[2] https://xn--archivoespaoldearte-53b.revistas.csic.es/index.php/aea/article/view/968/1001
[3] https://www.researchgate.net/publication/10690668_Dali_and_the_double_helix
[4] https://www.researchgate.net/publication/290142479_DNA_jako_kod_kulturowy
[5] https://journals.iucr.org/paper?S0108768186097847