W jednym z komiksów pod tytułem "Szalony Chemik" z 1944 roku. Donald zastaje siostrzeńców przy pracy nad doświadczeniami chemicznymi w ramach szkolnego projektu. Oczywiście musi się wmieszać, i pokazać co umie - po dodaniu do kolby przypadkowego reagenta prowokuje wybuch, po którym kolba spada mu na głowę.
Gdy z potężnym guzem na głowie przytomnieje, zaczyna zachowywać się jak chemik - guz bowiem, jak stwierdził potem doktor Qwik, wywołał u niego chorobliwą nadczynność mózgu. Produkuje wysoce łatwopalny Kaczynamit, po czym napełnia nim rakietę, i leci nią na księżyc. Po drodze guz znika, Donald przestaje pamiętać co robił i z przerażeniem obserwuje Księżyc, który następnie rakieta okrąża i powraca z taką dokładnością, że rozbija się w jego własnym ogródku.
Ta w sumie banalna historia nie zdobyłaby większego rozgłosu, gdyby nie naukowcy, którzy czasem lubią się odmóżdżać komiksami. Jeden z nich zauważył, że niedługo po przemianie, Donald wypowiada pewien przepis:
"Jeśli połączymy CH2 i NH4, i podgrzejemy atomy w mgle osmotycznej, otrzymamy pstry azot"**No cóż. Całość brzmi oczywiście całkiem absurdalnie, ale w końcu trudno jest cały czas zmyślać, aby nie zdarzyło się mimowolnie wymyślić coś prawdziwego.
Chemia organiczna, zasadniczo, jest chemią związków węgla czterowartościowego - to jest mającego cztery wiązania. Mogą one być w rozmaity sposób upakowane - bądź każde osobno, z podczepioną inną grupą, bądź jako wiązania podwójne czy potrójne. Chemia węgla dwuwartościowego jest natomiast bardzo uboga - w zasadzie dotyczy wyłącznie tlenku węgla i jego kompleksów z metalami. Czym jest to powodowane? Struktura elektronowa z czterema elektronami zhybrydyzowanymi, a więc o wyrównanej energii, przy której atom może tworzyć cztery wiązania, jest w tym przypadku zdecydowanie korzystniejsza, od struktury z dwoma wiązaniami, w tym drugim bowiem wypadku dwa spośród czterech elektronów walencyjnych pozostają niewykorzystane, nie powstaje więc korzystny dla atomu oktet. Cząstka taka jest zatem nietrwała i bardzo aktywna.
Istnieć mogą dwa stany elektronowe - singletowy, gdzie dwa wolne elektrony tworzą parę, i trypletowy, gdzie każdy zajmuje osobny orbital a cała cząsteczka staje się podwójnym rodnikiem. Stan decyduje o trwałości i geometrii cząsteczki.
Początkowo istnienie karbenów, bo tak nazywają się cząsteczki z dwuwartościowym węglem, było przewidywane teoretycznie, były bowiem dobrym sposobem na wyjaśnienie mechanizmów pewnych reakcji, jednak z powodu nietrwałości bardzo długo brakowało potwierdzenia doświadczalnego. Dopiero w 1954 roku Wiliam Doering potwierdził istnienie dichlorokarbenu CCl2, jednak dopiero w 1960 roku odkryto w zamrożonych gazach najprostszy karben węglowodorowy - metylen, o wzorze CH2...
Rysownik komiksu Carl Barks miał talent do wymyślania prawdopodobnych rozwiązań. Na tyle prawdopodobnych, że raz już sprawiły kłopot pewnemu wynalazcy. Duński wynalazca Karl Kroyer wynalazł metodę bardzo szybkiego podnoszenia z dna zatopionych statków - do ładowni należało wtłoczyć przy pomocy wody pod ciśnieniem, lekkie, puste wewnątrz plastikowe kulki. Każda kulka miała niewielką wyporność, lecz tysiące kulek wypierają sobą na tyle dużo wody że statek może zostać uniesiony. Metoda była kilka razy stosowana, na przykład w latach 60. w Kuwejcie, gdzie zatopiony w dokach statek Al Kuwait, przewożący owce był w ciepłych wodach zagrożeniem epidemicznym. Do jego podniesienia użyto 27 milionów styropianowych kulek, ekspandowanych parą wodną na nabrzeżu do rozmiarów piłek pingpongowych, które wprawdzie na sucho ważyły 60 ton, ale po wepchnięciu pod wodę zdołały unieść ważący 2 tysiące ton statek[1]
Kroyer opatentował metodę w Stanach i Wielkiej Brytanii, ale gdy próbował w Holandii urząd odmówił rejestracji, powołując się na przepis mówiący, ze w ciągu 15 lat przed złożeniem wniosku nie powinny być dostępne opisy podobnych rozwiązań. Jaki był to opis? Dokładnie nie wiadomo - dokumenty już się nie zachowały, poza ogólną notką, ale miłośnicy Kaczora powiązali to z komiksem z 1949 roku, w którym Donald podnosi z dna morza zatopiony jacht, wtłaczając do ładowni setki piłeczek pingpongowych.[2]
Zatem jak by nie patrzeć, karben metylenowy pojawił się w komiksie 16 lat przed faktycznym odkryciem. Naukowcy docenili fantazję rysownika, wykazując się przy tym subtelnym poczuciem humoru.
W 1963 roku wydano obszerną pracę Spin States of Carbenes, gdzie jej autorzy Gaspar i Hammond wspominają pod koniec o pewnej zasugerowanej kilkanaście lat wcześniej reakcji z wykorzystaniem kabenów, która dotychczas nie została zweryfikowana, choć należała do najciekawszych propozycji literaturowych. Przy tym akapicie widniał poważnie wyglądający przypis 91, odsyłający do pracy niejakiego D. Ducka opublikowanej w komiksie z 1944 roku[3]
Żart został później powtórzony w kilku pracach teoretycznych a nawet w pierwszym wydaniu sławnego podręcznika Morrisona i Boyda!
Ciekawe jaką cytowalność ma dziś pan D. Duck?
Karbeny, już po odkryciu, okazały się cząstkami niezwykle przydatnymi - wprawdzie z powodu niezwykłej reaktywności nie dało się ich wyodrębnić, ale wytwarzane in situ w mieszaninie reakcyjnej, stały się doskonałymi substratami do pewnych specyficznych reakcji.
Najprostszymi sposobami wytwarzania karbenów, jest fotoliza lub termoliza związków diazowych, z ugrupowaniem =N=N, odszczepianym w formie gazowego azotu, lub ketenów z ugrupowaniem C=C=O odszczepiającym tlenek węgla.
W roztworach proste keteny tworzą się podczas działania silnych zasad na cząsteczki zawierające dwa halogeny przy jednym węglu - przykładem generowanie metylenu z chlorku metylenu CH2Cl2, w stężonym roztworze wodorotlenku sodu.
Najczęstszą reakcją jakiej ulegają karbeny, jest addycja do wiązań podwójnych, z wytworzeniem trójkątnego pierścienia, przy czym sposób przebiegu reakcji jest zależny od rodzaju karbenu - w singletowym para elektronów oddziałuje równocześnie z obydwoma atomami, przez co zachowana zostaje pierwotna konfiguracja innych podstawników. Karbeny trypletowe reagują elektron po elektronie, dając cząsteczce czas na różne tam obroty i wygięcia, przez co konfiguracja może ulegać zmianie:
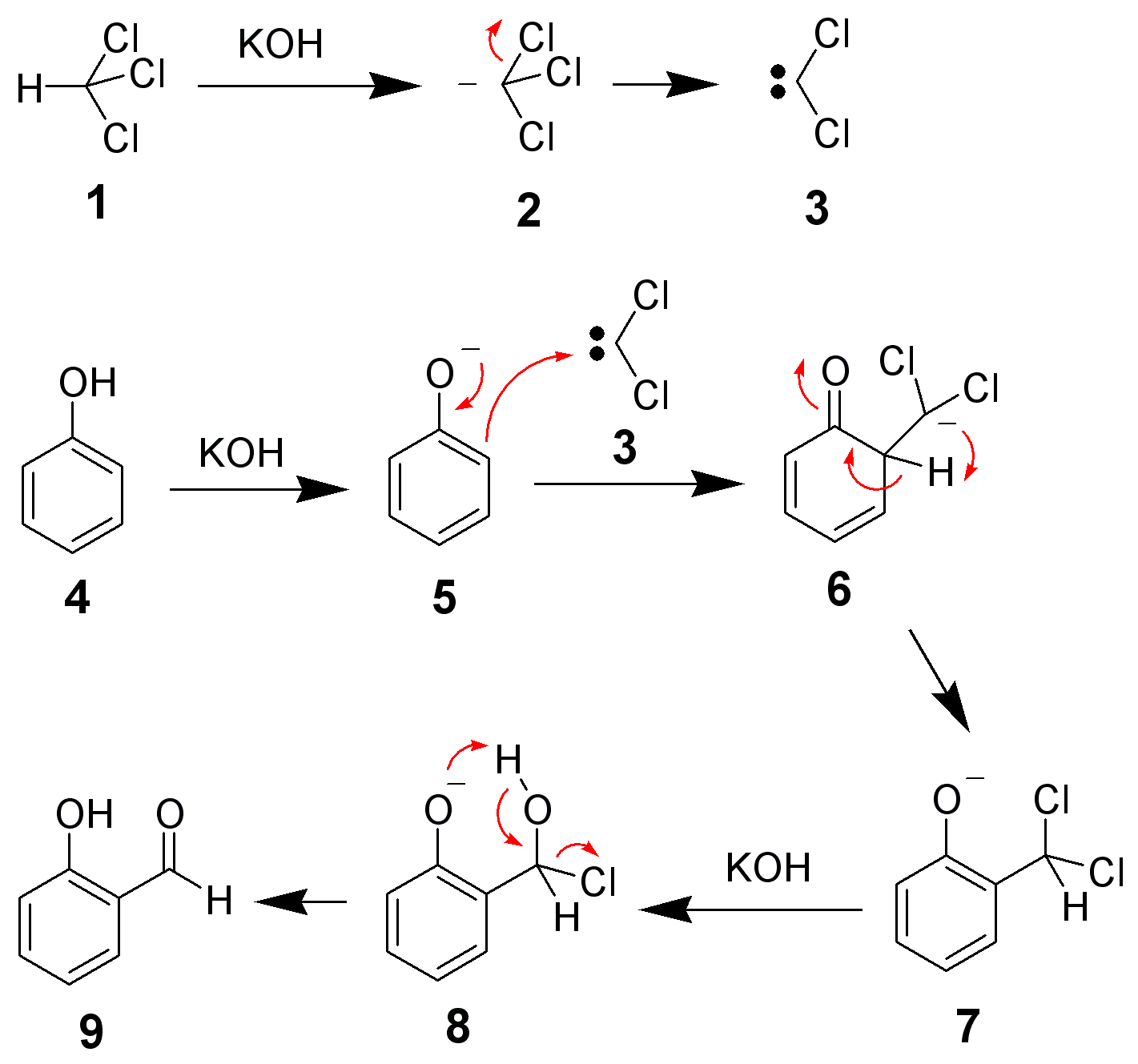
Do najważniejszych reakcji z użyciem karbenów należy synteza Reimera-Tiemanna , gdzie przyłączany do pierścienia aromatycznego dichlorokarben, hydrolizuje potem do grupy aldehydowej. Dawniej w ten sposób syntezowano wanilinę z gwajakolu, znanego jako lek wykrztuśny. Tutaj przykład syntezy kwasu salicylowego z fenolu:
Obecnie znamy też grupę karbenów na tyle dobrze stabilizowanych rozległymi podstawnikami, że nie tylko daje się je wydzielić z roztworu, ale też niektóre można wykrystalizować i przechowywać na powietrzu przez dłuższy czas. Innym ciekawym zastosowaniem są barwniki karbenowe - cząsteczki barwników do farbowania tkanin często słabo wiążą się z włóknem, co wymusza dodawanie do ich cząsteczek specjalnych ugrupowań, łączących się z substancją włókna. W niektórych przypadkach możliwe jest otrzymanie z barwnika pochodnej karbenowej, która będąc związkiem bardzo aktywnym, łączy się z włóknem bardzo trwałymi wiązaniami. Niektóre procesy polimeryzacji przebiegają z wytwarzaniem tych molekuł.
Wróćmy jednak do komiksu - co się stanie jeśli połączymy CH2 i NH4?
Karbeny chętnie przyłączają proton, natomiast jon amonowy chętnie go oddaje, można zatem spodziewać się powstania karbokationów metylowych CH3+, bardzo nietrwałych, i amoniaku. W dalszej kolejności można spodziewać się powstawania metanu lub metyloaminy. Czy przy okazji powstaje pstry azot, jak dotychczas chyba nie sprawdzano.
No proszę. Kto by pomyślał do czego może prowadzić czytanie komiksów.
Pozostaje mieć nadzieję że również dowciplina z komiksów o Tytusie, Romku i Atomku zostanie kiedyś odkryta - a szczegółowa struktura cząsteczki została w komiksie podana.
---------
* W komiksie tym Mickey siedział sam w pokoju, gdy rozległ się dzwonek u drzwi, donośne Ding! Dong! Podszedł, otworzył, ale za nimi nikogo nie było. Potem znów usłyszał dzwonek i znów za drzwiami nikogo nie było. Myśląc, że to jakiś żartowniś stanął z ręką na klamce i po pierwszym Ding! otworzył drzwi. Sprawcą zamieszania okazał się zwieszający na nici pająk, z jednych odnóżach trzymający dzwonki a w innych pałeczkę, który zapewne po każdym dzwonieniu szybko podciągał się do góry.
** Tłumaczenie "speckled nitrogen" jako "pstry azot" wydaje mi się lepsze niż "azot w ciapki" jak to zrobił polski tłumacz. Nie ubajkowiajmy nadmiernie.
[1] http://www.starch.dk/isi/kroyer/schrooge.asp
[2] http://www.iusmentis.com/patents/priorart/donaldduck/
[3] http://www.seriesam.com/barks/detc_ccus_wdc0044-x1.html
- Kaczor Donald: Szalony Chemik - skan jpg wersji polskiej.
- http://goodcomics.comicbookresources.com/2007/01/25/comic-book-urban-legends-revealed-87/















