Natomiast wyolbrzymiane skutków oprócz obietnicy wyleczenia z ciężkich chorób, oraz równie ważnego schudnięcia w dwa tygodnie, odbywa się też przez zaprezentowanie detoksu w efektownej wizualnie formie. Najlepiej byłoby, gdyby uwalniane toksyny było dobrze widać. Jeszcze lepiej, gdyby wyglądało to obrzydliwie i przypominało brud. Jeśli zaś toksyny nie chcą tak ładnie wyglądać, trzeba im jakoś pomóc...
Plastry czyli brunatnienie octu
Plastry detoksyfikujące wciąż jeszcze są dosyć popularne. Nakleja się je na stopy na noc i rano są całe zbrązowiałe, pokryte kleistą substancją i niemile pachną. I oczywiście ta brązowa substancja to toksyny z organizmu.
Problem w tym, że podobny efekt daje zwilżenie plastra. W ich składzie znajdują się substancje chłonące wilgoć i wyciągi roślinne o brązowym kolorze. W ciągu nocy plaster chłonie wilgoć ze skóry, zwłaszcza pot, więc rano są wilgotne a zawartość saszetki zabawia plaster na brązowo.
Ale, ale - przecież jeśli stosuje się je regularnie, to po pewnym czasie przestają brązowieć. Z czego to wynika? Jednym ze składników takich plastrów jest ocet drzewny otrzymywany ponoć z pędów bambusa. Kwas octowy działając kilka godzin na skórę przez kilkanaście dni, powoduje obkurczenie gruczołów potowych i przejściowe zmniejszenie potliwości na tym fragmencie skóry.
Robiono już testy z ochotnikami i po przeanalizowaniu składu plastrów nie stwierdzono, aby po całonocnym użytkowaniu pojawiały się w nim jakieś metale ciężkie czy znane substancje toksyczne.[1]
Wanna z błotkiem czyli elektroliza
Pod pewnym względem podobna wydaje się popularna zwłaszcza kilka lat temu metoda z wanienkami, mającymi wywoływać wydalenie toksyn przez stopy. Zanurzało się stopy w korytku, trzymało w rękach elektrody, a po pewnym czasie od włączenia urządzenia, woda robiła się brązowa i śmierdziała. Prowadzący zabieg tłumaczył, że oto pole elektryczne spowodowało wydalenie toksyn do wody i to brązowe w misce to nasze toksyny.
Urządzenie składa się przede wszystkim z miski na wodę i płaskich elektrod, koniecznie stalowych bo inaczej nie zadziała, zasilane jest najczęściej zasilaczem podobnym do tych do telefonów komórkowych, stosując niskie napięcie 12 V i bezpiecznie niskie natężenie.
Dlaczego elektrody muszą być stalowe? Bo inaczej nie zrobi się nam błotko. Nie jest potrzebne nawet wkładanie stóp, zrobi się samo byle płynął prąd.
W urządzeniu takim zachodzi prosta elektroliza wody, zwykle lekko posolonej dla lepszego przewodnictwa, z prądem stałym podłączonym w taki sposób, że na elektrodach w wodzie pojawia się ładunek dodatni. Pod wpływem takiego ładunku zachodzi reakcja utlenienia żelaza z elektrody, w pewnym stopniu też wydzielenie tlenu. Jony żelaza i tlen tworzą tlenki i wodorotlenki, tworzące ostatecznie brązowy osad, zaciemniający wodę i udający toksyny. Efekty wizualne zabiegu nie mają żadnego związku z detoksem.
Biorąc pod uwagę, że stale nierdzewne zawierają domieszki niklu i chromu, które mogą uwalniać się podczas zabiegu do roztworu, namaczanie w nim stóp może się okazać bardzo szkodliwe dla skóry. Nie od dziś wiadomo, że nikiel jest silnym alergenem a chrom wywołuje podrażnienia.
Teoretycznie puszczenie napięcia od rąk do stóp mogłoby spowodować migrację jonów z organizmu do wody, za sprawą jonoforezy, czyli ruchu jonów pod wpływem prądu elektrycznego. Jednak aby, jak to piszą wykonujący ten zabieg szarlatani, usuwać w ten sposób kationy metali ciężkich należałoby... podłączyć prąd dokładnie odwrotnie! Kationy, czyli jony o ładunku dodatnim, migrują do elektrody o ładunku ujemnym, bo przeciwieństwa (elektryczne) się przyciągają.
Ale jak się już domyślacie, podłączenie prądu odwrotnie nie będzie utleniało elektrod i barwiło wody na brązowo. Warto by więc rozważyć, czy przypadkiem podczas zabiegu nie dochodzi do elektroforetycznego wchłaniania do organizmu wspomnianych niklu i chromu z rozpuszczonej elektrody. Co byłoby dla nas dużo bardziej szkodliwe.
W 2012 roku wykonano zresztą eksperymenty z użyciem dostępnych komercyjnie zestawów "Jonowej Kąpieli Stóp". Najpierw badacze przygotowali roztwór soli w destylowanej wodzie, w ilości podanej przez producenta urządzenia i zbadali zawartość w nim kilkunastu pierwiastków. Następnie wlali do urządzenia i włączyli zgodnie z przepisem na 20 minut, bo tyle trwa normalny zabieg, ale nikt nie wkładał tam stóp. Chodziło o sprawdzenie, na ile skład wody zmienia samo działanie urządzenia. Po minięciu odpowiedniego czasu, pobrali wodę z urządzenia i zbadali zmiany zawartości pierwiastków. Wyniki wyglądają bardzo niepokojąco:
- w wodzie pojawił się arsen, kobalt, mangan i kadm, toksyczne pierwiastki
- zawartość wanadu wzrosła o 5800% (z 1 do 59 ug/l)
- zawartość niklu wzrosła o 750 000% (z 2 do 15 179 ug/l)
- zawartość molibdenu wzrosła o 6100% (z 50 do 3155 ug/l)
- zawartość chromu wzrosła o 590 000% (z 4 do 23 634 ug/l)
- zawartość żelaza wzrosła o 375 000% (z 31 do 116 000 ug/l)
- łączny wzrost zawartości składników mineralnych przekroczył milion procentów.
Nic dziwnego, że woda zrobiła się brązowa. A to wszystko po włączeniu wanienki bez wkładania nóg. Zresztą, strach wkładać do czegoś takiego nogę. Skład odpowiada zawartości metali w stali nierdzewnej wysokochromowej.
Zrobiono też jednak testy z ochotnikami, którzy byli poddawani zabiegowi w wanience kilkakrotnie w ciągu czterech tygodni, zgodnie z zalecaną przez producenta kuracją. Także badano zmiany zawartości pierwiastków w wodzie przed i po zabiegu, w moczu ochotników przed i po zabiegu oraz we włosach ochotników przed serią wielu zabiegów i po czterech tygodniach. Ilość metali ciężkich w wanienkach podczas zabiegów wzrastała bardzo podobnie, do wody uwalniane były te same pierwiastki w podobnej ilości - może tylko chromu i niklu było jeszcze więcej, wzrosty ich stężeń dochodziły do miliona procent, co mogło wynikać ze zużywania się elektrod w urządzeniu. Sprawdzano zresztą całkowitą ilość uwalnianych pierwiastków, stwierdzając że stopniowo spadała w miarę kolejnych eksperymentów na tym samym urządzeniu, a ostatecznie przeprowadzono ich 30, wykazując jak szybko rozpuszczają się elektrody.
Podczas badania moczu ochotników stwierdzono u jednego z nich wzrost ilości metali ciężkich w miarę kolejnych zabiegów, zaś w badaniu składu mineralnego włosów także gwałtowny wzrost zawartości metali ciężkich u jednego ochotnika. W przypadku pozostałych ludzi, zmiany ilości pierwiastków były bardzo małe i miały różny kierunek. Nie dało się więc potwierdzić usunięcia metali ciężkich z organizmu w miarę powtarzanych zabiegów w wanience, bo w przypadku pozostałych badanych ilości pierwiastków się nie zmieniły, natomiast wzrost zawartości metali w moczu i włosach jednego pacjenta sugerowałby raczej wzrost zawartości w organizmie, a więc przytrucie.[2]
Ten sam widowiskowy efekt był też wykorzystywany przez przedstawicieli handlowych sprzedających filtry do wody - na pokazach, na które zapraszano głównie naiwne starsze osoby, pokazywano elektrolizę żelaznych elektrod w wodzie wodociągowej, po czym porównywano z elektrolizą w wodzie destylowanej, która przewodzi prąd bardzo słabo i nie daje takich skutków.
Kamienie prawie żółciowe
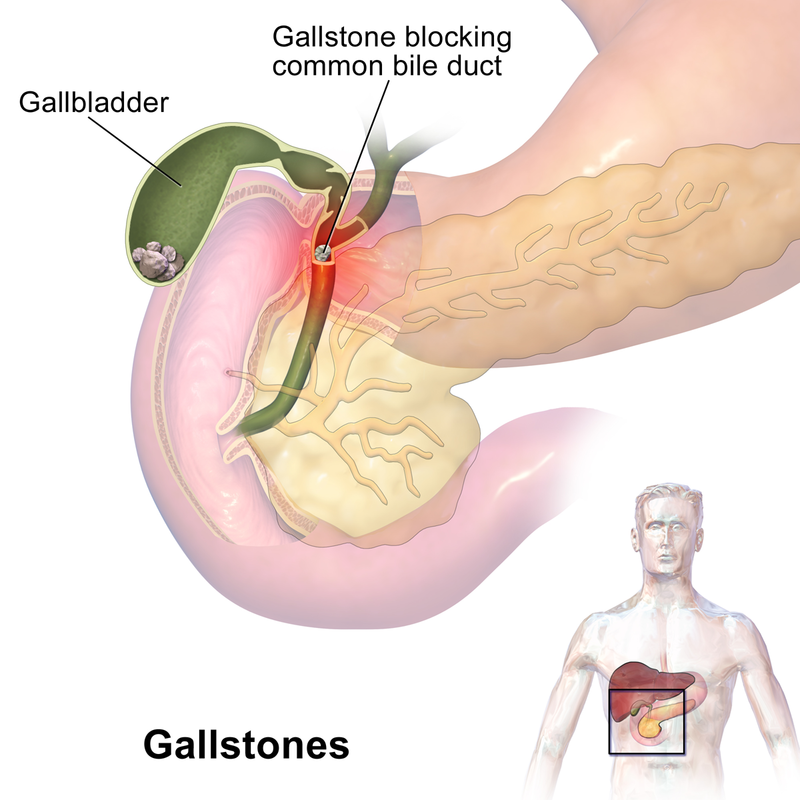
Jednym z najpopularniejszych domowych sposobów oczyszczania wątroby, jest wypijanie mieszanki oliwy z sokiem cytrynowym. Efekty ponoć mają być spektakularne, zwłaszcza wydalanie kamieni żółciowych w ilościach hurtowych, zupełnie bez bólu i z możliwością ominięcia operacji. Niestety wielu mających problemy z kamieniami żółciowymi przekonało się już, że mimo poprawnego wykonania takiego zabiegu i wydalenia żółtawych grudek, ilość złogów w ich woreczkach wcale nie spadła. Skoro tak, to skąd się one biorą?
 |
| Prawdziwe ludzkie kamienie żółciowe typu cholesterolowych |
Wątroba i trzustka produkują płyny obfitujące w enzymy trawienne, sole kwasów żółciowych, sole cholesterolu i związki mineralne. Powstała z ich zmieszania się w drogach żółciowych żółć, jest tymczasowo przechowywana w woreczku, oczywiście też żółciowym. Gdy receptory w jelicie w obszarze zakończenia przewodu żółciowego wyczują tłuszcz w treści jelita cienkiego, pobudzony pęcherzyk kurczy się, uwalniając żółć. Ma ona bardzo zasadowy odczyn więc neutralizuje kwas żołądkowy, oraz co ważniejsze, zawiera enzym lipazę który ma trawić tłuszcz. Lipaza rozbija cząsteczki tłuszczów, rozkładając je na kwasy tłuszczowe i glicerynę.
W dalszej kolejności kwasy tłuszczowe powinny zostać podczas trawienia wchłonięte, toteż w normalnej sytuacji kał nie zawiera zbyt dużo tłustych treści. Chyba, że zalejemy jelito dużą ilością tłuszczu i jeszcze popchniemy środkiem przeczyszczającym.
W najpopularniejszej wersji metody używa się jednorazowych dawek oliwy rzędu szklanki czy półtora, wypijanych duszkiem na pusty żołądek, i doprawianych sokiem cytrusowym, często dla lepszego oczyszczenia po pewnym czasie wypija się roztwór soli z Epsom, soli glauberskiej czy jakiegoś innego środka poprawiającego wypróżnianie. Po takiej dawce oleju w jelitach tworzy się dość dużo wolnych kwasów tłuszczowych, które nie mają czasu zostać dalej strawione i wchłonięte, zamiast tego zostają wydalone. W połączeniu z solami mineralnymi (zwłaszcza połkniętą solą z Epsom będącą siarczanem magnezu) kwasy te tworzą trudnorozpuszczalne mydła.
Tym, co zostaje ostatecznie wydalone, są grudki zawierające mydła, wolne kwasy tłuszczowe i składniki żółci, o kolorze od żółtego, przez żółtawozielony do wyraźnie zielonych (kolor zależy od składników oliwy, ilości żółci i treści jelit), uformowane przez ruchy robaczkowe w formę "kamyków".
Chorzy, którzy stosowali tą metodę wiele razy, donosili o liczbach rzędu setek a nawet tysięcy złogów, co przekracza pojemność woreczka żółciowego. Dlatego też szarlatani twierdzą, że dodatkowe ilości złogów schodzą z przewodów żółciowych czy nawet z wnętrza wątroby (wędrują przez miąższ organu?) i dlatego jest ich tak dużo. Jak łatwo się domyśleć, "kamyki" będą się pojawiały tak długo jak długo chory będzie pił oliwę a jego wątroba produkowała żółć. Chyba, że w trakcie "kuracji" woreczek się w końcu zatka a pacjent trafi do szpitala z ostrym zapaleniem.
W 2005 roku w czasopiśmie medycznym The Lancet opisano przypadek kobiety ze stwierdzonymi złogami w woreczku żółciowym, która chciała oczyścić się tą metodą. Prowadzący ją lekarze postanowili wykorzystać okazję i sprawdzić, czy to faktycznie działa. Pacjentka wypiła 600 ml oleju z oliwek i 300 ml soku z cytryny w kilku porcjach. Wydaliła wiele żółtozielonych "kamyczków", które wzięto do analizy. Złogi roztapiały się w gorącej wodzie, w ich składzie brakowało cholesterolu, bilirubiny i soli wapniowych kwasów żółciowych, a więc składników kamieni z woreczka żółciowego. Głównym składnikiem okazało się mydło kwasu oleinowego oraz długocząsteczkowe, trudnotopliwe kwasy tłuszczowe. Wnioskiem lekarzy było stwierdzenie, że wydalone złogi utworzyły się w wyniku trawienia oliwy w jelicie i nie pochodziły z dróg żółciowych.[3]
Wystarczy zresztą zastanowić się nad tym, w jaki sposób mogłoby wyglądać takie wydalanie - niektórzy opisują wydalenie tą metodą złogów o wielkości kilku centymetrów. Kanał żółciowy ma jednak ograniczoną szerokość, złóg większy niż kilka milimetrów po prostu go zatka. Masa tych rozmiarów, przesuwająca się wzdłuż żółciowodu, który jest przewodem dość dobrze unerwionym, musi skończyć się potwornym bólem, czyli atakiem kolki żółciowej. Jeśli więc ktoś nie czuł niczego szczególnego a wydalił centymetrową kulkę, to nie pochodzi ona z jego pęcherzyka.[4] Sól z Epsom nie poszerzy przewodu żółciowego aż tak bardzo (a tak twierdzą szarlatani), bo nie jest on zbyt elastyczny i się nie rozciągnie.
Ponieważ metoda przynosi efekty wyglądające spektakularnie, chętnie powołują się na nią różni dieto-uzdrawiacze. W Polsce najszerzej znana jest jako metoda Huldy Clark, od autorki książek na temat oczyszczania organizmu i leczenia raka, tytułującej się doktorem choć nie ukończyła nigdy medycyny. Inna nazwa to metoda dr Brouse, albo dr Kelley, albo dr. Moritza, bo wielu specjalistów od diety się pod nią podczepiało, z drobnymi modyfikacjami w rodzaju zastąpienia cytryny sokiem jabłkowym.
Pisał o niej też Tombak a za nim, z lekkimi modyfikacjami, Słonecki, tylko u nich miała to być metoda na kamienie kałowe, rzekomo gromadzące się w człowieku w kilogramowych ilościach. Obecnie bez cytowania źródła wspominają o niej liczne portale lifestylowe, jest to więc jedna z najbardziej popularnych medycznych bzdur w temacie oczyszczania organizmu.
Kapsułki oszustwa
W świetnej książce reporterskiej "Nic nie zdarza się przypadkiem" autor, włoski dziennikarz Tiziano Terzani, opisuje kilka lat walki z nowotworem, podczas której równolegle do leczenia klasycznego jeździł po świecie od uzdrawiacza do uzdrawiacza, w pewien sposób dając obraz kultur poprzez ich podejście do zdrowia i śmierci.
W jednym z rozdziałów opisuje jak to został zaproszony na egzotyczną wyspę na dwutygodniową sesję oczyszczającą, polegającą na głodówce, zażywaniu witamin i saunie. Prowadzący zachęcał obecnych aby codziennie oglądali na sitku, czy wydalają z organizmu złogi i toksyny, mające mieć postać żelowatych grudek różnych kolorów. Dowodem na to, że organizm się oczyścił, miało być ich zniknięcie z wydalin, jeśli do końca kuracji nie znikały, można było ją przedłużyć.
Po kilku dniach reporter zorientował się, że w skład suplementów witaminowych wchodził środek żelujący, a kolorowe kawałki to pozostałości osłonek kapsułek witamin. Gdy przestał je łykać, kolorowe grudki przestały się pojawiać.
Test burakowy
Nie jest to wprost metoda detoksyfikacji, a raczej wstęp do którejś z nich. Artykuły pseudodietetyków promują ten test jako metodę sprawdzenia stanu szczelności jelit. A jeśli jelita są nieszczelne, to organizm jest zatruty i trzeba go czyścić. Test polega bądź na zjedzeniu tartego buraka lub na wypiciu świeżego soku, jeśli po takiej potrawie mocz zabarwi się komuś na różowo lub czerwono, to znaczy, że ma nieszczelne jelita i kawałki treści jelit przedostają się mu do krwi. Bardzo obrazowy opis, trzeba przyznać.
W rzeczywistości zabarwienie moczu po burakach, czyli betaninuria, to stosunkowo częsty stan fizjologiczny, pojawiający się okresowo nawet u 10-15% ludzi. Wynika z wydalenia czerwonego barwnika buraka, betaniny, wraz z moczem po tym, jak został wchłonięty w jelitach. Nie następuje to u każdego i zawsze dlatego, bo zwykle betanina do jelita nie dociera. Barwnik ten jest dość wrażliwy na warunki, zwłaszcza kwasowość. Ulega rozpadowi do bezbarwnych produktów zarówno w środowisku zbyt kwaśnym (pH ok. 2 i mniejsze) jak i zbyt alkalicznym. W zasadzie zaczyna degradować już w warunkach obojętnych, zwłaszcza przy podgrzewaniu, stąd przy gotowaniu barszczu zawsze się go lekko zakwasza cytryną lub octem. Po drodze od ust do miejsca wchłonięcia, połknięty burak najpierw wpada do żołądka, który wytwarza kwas, po czym częściowo przetrawiona treść trafia do jelita cienkiego, gdzie zalewa ją dla odmiany bardzo zasadowa żółć. Ostatecznie więc w normalnych warunkach wchłania się niewielka ilość barwnika, niewystarczająca aby wpłynąć na kolor moczu.
Pojawienie się więc zabarwienia uryny oznacza, że po drodze warunki były dla buraka łagodniejsze niż zwykle - jeśli do żołądka trafiło dużo treści, jeszcze w dodatku popitej, barwnik nie był narażony na takie znów silne działanie kwasu. Jeśli ostatecznie posiłek nie był ciężkostrawny, to nie przebywał w żołądku zbyt długo. Z kolei na ilość wydzielonej żółci wpływ ma tłustość posiłku i jego pierwotna kwasowość. Gdy burak był mocniej zakwaszony sokiem z cytryny lub szczawiem, kwasy organiczne przeszkadzają żółci, działając jak bufor stabilizujący nieco kwaśniejsze warunki.
Nakładanie się tych dwóch efektów powoduje ostatecznie, że betanina nie zostaje zupełnie zdegradowana i wchłania się w dalszych odcinkach jelita dostatecznie, aby zabarwić mocz. W efekcie ta sama osoba może czasem doznawać zabarwienia a czasem nie, zależnie od kwasoty żołądka, obfitości posiłku, rodzaju posiłku i ilości buraka w porcji. Pewne badania sugerują częstsze pojawianie się betaninurii u osób z niedoborem żelaza, ale zjawisko jest zbyt mało specyficzne (jest za wiele sytuacji gdy efekt nie wynika z niedoboru żelaza tylko z rodzaju posiłku) aby służyło za test diagnostyczny.[5], [6]
----------
Źródła:
[1] https://www.livestrong.com/article/130395-detox-foot-patches-work/
[2] Deborah A. Kennedy et al. Objective Assessment of an Ionic Footbath (IonCleanse): Testing Its Ability to Remove Potentially Toxic Elements from the Body, Journal of Environmental and Public Health Volume 2012 (2012), Article ID 258968, 13 pages
[3] http://www.thelancet.com/journals/lancet/article/PIIS0140-6736(05)66373-8/fulltext
[4] https://sciencebasedmedicine.org/would-you-like-a-liver-flush-with-that-colon-cleanse/
[5] https://udel.edu/~mcdonald/mythbeeturia.html
[6] Eastwood, MA; Nyhlin, H (1995). "Beeturia and colonic oxalic acid". QJM. 88 (10): 711–7