Od czasu do czasu dostaję pytania od czytelników bloga. Część pojawia się w komentarzach, i tam staram się na nie odpowiadać co można zobaczyć pod popularnymi postami. Część osób woli jednak drogę bardziej bezpośrednią, używając maila kontaktowego, jaki można znaleźć w opisie profilu, i odpowiedzi na te pytania nie są już powszechnie dostępne. Ponieważ zaś część pytań się powtarza, a niektóre są przecież dość ciekawe, uznałem że warto zebrać je w jednym miejscu, abym nie musiał się powtarzać
Aluminium w glinkach kosmetycznych
O tą rzecz pytano mnie już kilka razy, dlatego warto chyba odpowiedzieć publicznie.
Glina to formalnie rzecz biorąc, skała osadowa. Bardzo miękka a w stanie wilgotnym dająca się formować w rękach, ale skała. Aby osad mógł być zaliczony do glin, musi zawierać odpowiednio dużą ilość minerałów ilastych, przemieszanych z drobnym pyłem kwarcowym i skaleniowym. Tlenki żelaza i manganu nadają glinom kolor od żółtawego, przez rdzawoczerwony, brunatny, szary do ziemisto-zielonego. Glinki z małą ilością metali mogą być też białe.
Minerały ilaste, uwalniane ze skał podczas wietrzenia, wypłukiwane w formie najdrobniejszego mułu czy wywiewane przez wiatr jako kurz, stanowią grupę krzemianów warstwowych, składających się z warstw połączonych tetraedrów tlenku krzemu SiO4 i tlenku glinu AlO4. Tlenek glinu jest izomorficzny z tlenkiem krzemu i może go naśladować, włączając się w krzemianową strukturę bez zmian. Poszczególne warstwy glinokrzemianowe są połączone wiązaniami wodorowymi, częściowo jonowymi, i potrafią wchłaniać między siebie inne substancje organiczne i nieorganiczne. Duży stopień uwodnienia powoduje, że warstwy mogą się względem siebie przesuwać, przez co glina staje się plastyczna. Właśnie zawartość tego pierwiastka w glinie stała się podstawą do zastąpienia w polskiej nomenklaturze łacińskiego aluminium nazwą glin.
Struktura warstwy kaolinu:
Wśród krzemianów warstwowych, najczęściej spotykamy się z talkiem, kaolinem będącym głównym składnikiem porcelany i montmorylonitem będącym głównym składnikiem bentonitu. Gliny zawierają mieszankę różnych glinokrzemianów ale niektóre posiadają przewagę jednego, konkretnego, stąd wyróżnia się białą glinkę kaolinową, glinkę pałygorskitową i inne.
A jak jest z tym aluminium?
Aby glin mógł być uwalniany z gliny, powinien być rozpuszczalny w wodzie. A gliny nie są. Nie dość, że zupełnie nierozpuszczalny w wodzie jest tlenek glinu, to w glinokrzemianach dodatkowo stabilizuje go włączenie w sieć krzemianową
Kwestia ta była zresztą szczegółowo badana, zwłaszcza z uwagi na używanie ceramiki jako naczyń kuchennych, oraz używanie glinokrzemianów jako dodatków do żywności. Wydaje się, że w warunkach odczynu obojętnego uwalnianie glinu nie zachodzi. Dopiero warunki kwaśne są w stanie uwolnić część jonów. W pewnym badaniu stwierdzono dla kwasowości pH 3 (sok pomarańczowy) minerały uwalniały dość niskie poziomy aluminium, ale tylko z bardzo cienkiej (3,5 mikrometra) warstwy powierzchniowej, co sugeruje, że w przypadku naczyń ceramicznych po pewnym czasie powstanie wypłukana warstewka powstrzymująca dalsze uwalnianie. Najsłabsze wymywanie stwierdzono dla kaolinu i montmorylonitu[1]. Uwolnienie ilości mających jakieś znaczenie toksykologiczne, zachodzi dopiero pod wpływem mocniejszych kwasów.
Glinki kosmetyczne nie mają tak kwaśnego odczynu, więc uwalniania aluminium nie ma co się obawiać.W dodatku czyste glinki, przepłukane dla wymycia zanieczyszczeń, jak to zwykle jest z glinkami kosmetycznymi, mają raczej skłonność do pochłaniania rozpuszczalnych jonów glinu niż do uwalniania.
W obszernym raporcie na temat bezpieczeństwa glinokrzemianów i tlenków glinu używanych w kosmetyce, nie stwierdzono negatywnych skutków dla minerałów ilastych. [2]
Podobne pytanie dotyczyło spożywania glinek na odtruwanie - tutaj także nie ma niebezpieczeństwa, kwasy żołądkowe są bowiem dosyć rozcieńczone. Jedynym istotnym wpływem jaki stwierdzono, jest zmniejszone wchłanianie żelaza u osób zażywających glinę, bowiem absorbowała żelazo z treści żołądkowej.
Aluminium w szczepionkach
Ze względu na popularny post o ałunie jestem chyba brany za eksperta od aluminium, skoro dotyczy tego koleje pytanie zadawane mi dwa razy.
Jak wiadomo, w niektórych szczepionkach dziecięcych pojawiają się związki aluminium. Podobno zawartość w jednej nie przekracza norm bezpieczeństwa. A co jakby zsumować zawartość we wszystkich - czy wtedy mogłoby zajść jakieś niebezpieczeństwo?
Wodorotlenek glinu pojawia się w szczepionkach jako nośnik białek lub polisacharydów mających wywołać reakcję organizmu. Normy z reguły uważają za najwyższą dopuszczalną dawkę glinu 60 mg/ kg. masy ciała dziennie. Z badań na zwierzętach wynika też, że najniższe dawki mające negatywny wpływ na płody i rozwijające się młode (u szczurów) to 45 mg/kg masy ciała dziennie.
Spośród szczepionek w kalendarzu szczepień, glin zawierają:
- EUVAX B 0,25 mg w jednej dawce lub ENGERIX B też 0,25 mg w jednej dawce (stosowane wymiennie)
- DTP 0,7 mg na dawkę
-IPV 0,5 mg na dawkę
Jak łatwo zauważyć, całkowita zawartość w jednej dawce jest kilkadziesiąt razy mniejsza od najniższych dawek toksycznych. Nawet gdyby wstrzyknąć wszystkie wymienione w ciągu jednego dnia, to nie doszłoby do przekroczenia choćby dziesiątej części toksycznej dawki.
Toksyczność ałunu
Czytelnik pytał o bezpieczeństwo ałunu dla dzieci. Chodziło mu o sytuację gdyby dziecko znalazło kawałek ałunu z pękniętego sztyftu i polizało lub połknęło.
Ałun potasowy i amonowy mają działanie drażniące na błony śluzowe, dlatego pierwszą reakcją w razie połknięcia będą zapewne wymioty. Po polizaniu dziecko pewnie straci ochotę na kolejny liz, ałun ma bowiem bardzo cierpki, nieprzyjemny smak i działanie ściągające. W razie połknięcia najlepiej dać dziecku dużo wody do wypicia i skontaktować się z lekarzem. W razie polizania też dać wody, ale lekarz pewnie nie będzie potrzebny.
Toksyczność ostra związku jest niska - dawka śmiertelna to 6 g/kg masy ciała
Co takiego rozpuszcza DMSO?
Pewien dociekliwy czytelnik zainteresowany medycznymi zastosowaniami DMSO dopytywał mnie o kwestie tego co się w tym rozpuszcza, a co nie i czy ma on zastosowania medyczne.
Dimetylosulfotlenek, czyli w skrócie DMSO to cenny rozpuszczalnik, używany w medycynie i chemii organicznej. Wykazuje dużą skłonność do wnikania w tkanki organizmu, na tyle, że trzeba uważać przy pracy z nim bo po wchłonięciu metabolizuje do związków o zapachu czosnku. Ponieważ rozluźnia strukturę lipidową skóry, może ułatwiać wchłonięcie przezskórnie różnych substancji, w tym wielu leków, dlatego czyni się próby z wykorzystaniem do terapii bez konieczności zastrzyków. Sam w sobie ma zresztą działanie przeciwzapalne.
Bywa rozpuszczalnikiem środków na grzybicę stóp, które zwykle dość słabo przenikają przez zrogowaciały naskórek na podeszwach, może być też składnikiem maści przeciwbólowych do działania miejscowego, może rozmiękczać skórę przy twardzinie i przerastających bliznach. Robiono na ten temat badania [3]
Drugie pytanie dotyczyło możliwości rozpuszczania chondroityny przez DMSO i smarowania tym stawów jako alternatywy dla suplementacji doustnej.
Chondroityna to mukopolisacharyd będący składnikiem chrząstek stawowych i w formie siarczanu stanowiący wraz z glukozaminą jeden z czynników zapewniających lepszy poślizg. W związku z tym powstał pomysł, że jeśli zbyt mała ilość mazi stawowej i mała elastyczność chrząstek stawu powodują bóle, to zażywanie chondroityny i dostarczanie jej do organizmu, powinno leczyć bądź powstrzymywać rozwój schorzeń stawów poprzez dostarczenie organizmowi składnika do wytworzenia większej ilości mazi. Na tym też opiera się potężna gałąź przemysłu suplemenciarskiego.
Niestety w niedawno opublikowanej potężnej metaanalizie wielu badań wykazano, że w porównaniu z placebo zażywanie chondroityny lub glukozaminy lub obu tych środków razem, nie zmniejsza bólów ani innych objawów[4]
Wygląda na to, że samo dostarczenie organizmowi składników potrzebnych do wytworzenia czegośtam w którymś organie, wcale nie musi go pobudzać aby tą substancję jednak wytworzyć, zwłaszcza że niedostateczne wydzielanie tej substancji wcale nie musi być wynikiem niedoboru podstawowego składnika, może być skutkiem innych czynników, w tym genetycznych. Dlatego jeśli przyjrzycie się emitowanym obecnie reklamom takich pigułek, zauważycie że wcale nie stwierdzają one wprost, iż zażycie tego składnika powstrzyma chorobę. Zamiast tego zawierają ogólniki, typu "glukozamina jest składnikiem chrząstki stawowej" i "maź stawowa ma decydujące znaczenie w zapewnieniu elastyczności stawu" i na koniec, że ich pigułka zawiera podwójną czy potrójną dawkę, zaś konstrukcję logiczną "skoro to jest składnikiem chrząstki a chrząstka jest potrzebna w stawach, to pomoże mi na stawy" widz musi sam sobie przeprowadzać, w czym udanie pomaga mu sugestia pokazywanego w reklamie pana którego bolą stawy, który bierze ich tabletki a potem wygląda na mniej cierpiącego.
Ale wróćmy do pytania - czy chondroityna rozpuszcza się w DMSO? Cóż - wedle obszernego podsumowania rozpuszczalności różnych substancji w tym rozpuszczalniku, chondroityna jest nie rozpuszczalna. Słabo rozpuszcza się chlorowodorek glukozaminy, natomiast bardzo dobrze przeciwbólowy Ibuprofen.[5]
Tak że raczej nie tędy droga.
Gdzie zbadać wodę?
Miałem też pytania o to gdzie można samemu zbadać wodę ze studni, źródła czy ujęcia.
Z tego co się orientuję, takie badania oferują jednostki Sanepidu, zbadają one zawartość metali ciężkich, czystość bakteriologiczną i własności fizyczne, jak zamulenie, obecność kwasów humusowych, zażelazienie itp. Oczywiście są to badania płatne.
Próbkę wody może pobrać wysłany pracownik, ale można ją też pobrać samemu. Warszawska stacja podaje na swojej stronie specyfikację sposobu pobierania próbek, aby nadawały się do badania.[6]
Dezodorant z podbiałem
Świadoma konsumentka zadała mi pytanie w sprawie używanego dezodorantu, który zawierał w swoim składzie podbiał pospolity. Chcąc dowiedzieć się czegoś o tym składniku, dowiedziała się że roślina zawiera uszkadzające wątrobę alkaloidy. I stąd powstało pytanie, czy taki alkaloid może wchłaniać się przez skórę?
Podbiał to cenne zioło lecznicze, lecz dopiero w ostatnich latach zorientowano się, że może zawierać alkaloidy pirolizydynowe, o działaniu hepatotoksycznym, które w wyniku zażywania dłuższym niż dwa miesiące mogą powodować toksyczną niewydolność wątroby. Ich zawartość w surowcach zbieranych w Europie jest jednak bardzo niska - w polskim badaniu stwierdzono poziomy rzędu 0,0013%[7]
W jednym badaniu na szczurach stwierdzono minimalne wchłanianie przezskórne alkaloidów żywokostu, w ilości 20 razy mniejszej niż przy podaniu doustnym. Stwierdzono też, że przy chłonięciu przeskórnym, nie dochodzi do zamiany nietoksycznego N-tlenku w toksyczną formę zredukowaną, co zwykle następowało w jelitach po spożyciu.[8] Zatem wydaje się, że kosmetyków z roślin zawierających te alkaloidy można używać bezpiecznie.
Czy to cyjanek?
Dwa lata temu czytelnik przesłał mi zdjęcie białego proszku, z pytaniem czy to cyjanek potasu. Cóż mogłem odpowiedzieć... Spektroskopu w oczach nie mam. Odpisałem, że może to być cyjanek albo soda, albo sól morska, albo cokolwiek innego bo bardzo wiele soli tak wygląda. Nie wiem o co chodziło.
----------
[1] http://www.clays.org/journal/archive/volume%2026/26-6-434.pdf
[2] http://www.ncbi.nlm.nih.gov/pubmed/12851164
[3] http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3460663/
[4] http://www.bmj.com/content/341/bmj.c4675
[5] http://www.gaylordchemical.com/uploads/images/pdfs/literature/102B_english.pdf
[6] http://www.wsse.waw.pl/PageContent.aspx?SubMenuID=100
[7] https://depot.ceon.pl/bitstream/handle/123456789/1121/hp%2058%204%202012%2062.pdf?sequence=1&isAllowed=y
[8] http://www.ncbi.nlm.nih.gov/pubmed/7128756?dopt=Abstract
informacje
poniedziałek, 15 czerwca 2015
czwartek, 11 czerwca 2015
6 substancji z którymi wolałbym nie pracować
Inspiracją do wpisu był ten, niedawno opublikowany film popularnonaukowy z serii "Uwaga! Naukowy bełkot":
Jest to cenna seria, w ciekawy sposób przedstawiająca informacje z różnych dziedzin, jednak z tym odcinkiem mam pewien kłopot - autor chyba nie zupełnie rozsądnie zebrał 6 groźnych substancji pod mylącym tytułem a opowiadając o nich zastosował nadmierne uproszczenia. Co postaram się pokrótce objaśnić zanim podam swoją listę
Z czym można pracować i co nie jest naj
Jedną z maksym przypisywanych Einsteinowi jest ta o przekazywaniu informacji, mówiąca że należy upraszczać jak można, ale nie bardziej. Bo jeśli coś uprościmy za bardzo, możemy wprowadzić inną osobę w błąd.
Ten problem dotyczy Polonu-210 opisanego przez autora jako "najbardziej promieniotwórcza substancja znana Ludzkości". Jak tłumaczy w komentarzach, wybrał tą substancję, bo jest dostępna w stosunkowo dużych ilościach, silnie radioaktywna i ma na tyle długi czas półrozpadu, że człowiek zdąży się nią zatruć. Ale o tym w filmie nie wspomina. Widz dostaje tylko prosty przekaz "Polon-210 jest najbardziej promieniotwórczy w ogóle", co nie jest prawdą.
Zgodnie z definicją aktywności promieniotwórczej, jest to szybkość z jaką następują rozpady promieniotwórcze. Największą aktywność mają te z najkrótszymi czasami półrozpadu i małymi masami, z czego wynika że najbardziej promieniotwórczą substancją jest Wodór-7 o czasie półtrwania 2,3×10−23 s i masie 8 unitów.
Tak że akurat Polon-210 byłby raczej "najbardziej promieniotwórczą substancją z jaką można się zetknąć" w tym znaczeniu, że jest stosunkowo dostępny i niektórzy muszą z nim pracować - choć można spekulować czy przypadkiem bardziej szkodliwy nie jest ameryk-243, spotykany w czujnikach dymu, który jest wytwarzany w większych ilościach a oprócz mało przenikliwego promieniowania alfa, produkuje też wysokoenergetyczne promienie gamma.
Podobny problem dotyczy "najbardziej palnej substancji" czyli trifluorku chloru, bo przecież fluorek ten sam w sobie nie jest specjalnie palny - jest natomiast silnym środkiem zapalającym, powodującym zapłon innych substancji z którymi się zetknie, a przy tym przeżerający substancje niepalne.
Myślę, że wśród najbardziej palnych substancji na pewno znajduje się silan, czyli krzemowy analog metanu. Duże powinowactwo krzemu do tlenu i ujemna jonizacja wodoru powodują, że w mieszance z tlenem ulega samozapłonowi w temperaturach około -100 °C, przy czym różne prace podają różne dane, w jednej opisano zapłon mieszanki z powietrzem w temperaturze -162 °C[1] Natomiast silniejszym od trifluorku chloru środkiem utleniającym i zapalającym inne substancje jest zapewne difluorek ditlenu, potrafiący zapalić stały metan w temperaturze 90 K.[2]
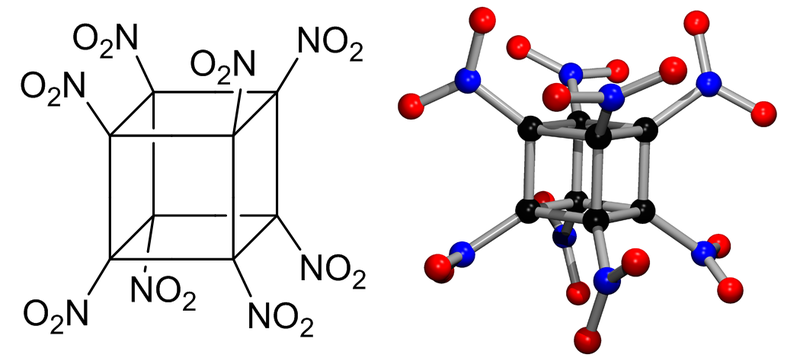
Inny problem dotyczy pozostałych substancji - tematem filmu są substancje "z którymi wolelibyście nie pracować" bo są niebezpieczne, trudne do obsługi, groźne jeśli się z nimi zetknąć. Tylko że w tym kontekście materiał wybuchowy oktanitrokuban pomimo swej niesamowitej siły wybuchowej zupełnie do zestawienia nie pasuje, jest bowiem stosunkowo bezpieczny - nie wybucha pod wpływem wstrząsów, nie powinien eksplodować nawet po uderzeniu młotkiem, dopiero wybuch spłonki inicjującej wywołuje eksplozję. Osobiście wolałbym pracować z nim, niż z na przykład chloranem potasu (jest ciekawszy).
Dlatego do zestawienia pasuje właściwie tylko batrachotoksyna, dwucyjan i ten bardzo azotowy materiał wybuchowy, eksplodujący spontanicznie.
Trochę zdziwiło mnie zatem, że autor filmu zapomniał o kilku innych substancjach, które warto tu pokrótce opisać.
Z czym ja wolałbym jako chemik nie pracować:
1. Diselenek węgla
Analog dwusiarczku węgla, przydatny w niektórych syntezach. A przy tym związek niesamowicie wprost śmierdzący. Po tym jak w 1936 roku otrzymano go po raz pierwszy, konieczna była ewakuacja najbliższej miejscowości, leżącej po zawietrznej stronie laboratorium. Jest lotny, łatwo przenika przez gumę i wchłania się do organizmu, łatwo przenika przez błony komórkowe i jest neurotoksyczny. Chemik pracujący z tym związkiem przez dłuższy czas otoczony byłby banieczką nieznośnego zapachu i bez wątpienia znalazłby wolne miejsce w tramwaju.
Podobne efekty mogą dawać też inne związki selenoorganiczne, jak selenol, analog etanolu, czy selenofenol.
Nie chcę zostać na kilka tygodni człowiekiem-skunksem, więc pracy z tym związkiem będę unikał.
2. Dimetylortęć
Jedna z najsilniejszych znanych trucizn. Dawka śmiertelna dla człowieka właściwie nie jest znana, estymuje się ją na podstawie kilku wypadków śmiertelnych. Znanym przypadkiem było zatrucie badaczki Karen Wetterhahn, której na rękawiczki rozprysnęło się ok. 0,05 ml substancji. Przeniknęła przez rękawiczki i w krótkim czasie wchłonęła się przez skórę w ilości wystarczającej do zabicia. Z batrachotoksyną czy jeszcze silniejszą ciguarotoksyną można w miarę bezpieczne pracować, z dimetylortęcią nie jest już tak dobrze.
Tak że jeśli na prawdę nie będzie mi to do czegoś potrzebne, wolę z tą substancją nie pracować.
3. Benzo-a-piren
Jeden z najważniejszych wielopierścieniowych węglowodorów aromatycznych (WWA) będących rakotwórczymi składnikami dymu. Metabolity benzo-a-pirenu łączą się z DNA wywołując mutacje. Spożyty wywołuje raka żołądka i jelit, obecność w powietrzu sprzyja nowotworom płu, a zanieczyszczenie skóry może wywołać raka skóry. W niektórych badaniach już jednokrotna iniekcja podskórna ekstraktu zwierającego WWA wywoływała nowotwory u badanych zwierzat.
Tak że pracy nad tym związkiem czystym, lub w ekstraktach wolałbym też unikać.
4. Gaz musztardowy
Środek bojowy będący silnym środkiem alkilującym. Wywołuje silne oparzenia skóry które ujawniają się nawet dobę po kontakcie z substancją, wchłonięty drogą inhalacyjną daje objawy zatrucia z dużym opóźnieniem, od 4 do 6 godzin dla małych dawek (dla dużych natychmiastowo). Jest potwierdzonym środkiem rakotwórczym.
Tak więc pragnącym zachować zdrowie i ładną twarz też radzę unikać styczności z tą substancją
5. Azydek sodu
Sól kwasu azotowodorowego, zawierająca trzy połączone atomy azotu. Azydki nieorganiczne zwykle są stosowane w syntezie azydków organicznych, oraz 1,2,3 triazyn, ewentualnie tetrazolu. Niestety azydki są związkami nietrwałymi i bardzo silnie trującymi, porównywalnie z cyjankami. Chętnie hydrolizują do azotowodoru, gazu bardziej toksycznego niż tlenek węgla, który w śladowych, niewyczuwalnych stężeniach jest w stanie wywołać zatrucie. Ekspozycja wywołuje mdłości, bóle głowy, uszkodzenie włókien nerwowych, zaburzenia oddychania zaś działaniem długofalowym po zatruciu jest uszkodzenie wątroby i jąder. Zatrucia tym związkiem wśród chemików są notowane dość często.
Przy ogrzewaniu potrafią eksplodować. Z jonami metali ciężkich tworzą wrażliwe na wstrząsy i nacisk azydki, używane czasem jeszcze w spłonkach.
Tak więc z tymi związkami bez konieczności też dobrze by było nie pracować
6. Siarczan niklu
Ten związek jest akurat stosunkowo często spotykany w laboratoriach chemii nieorganicznej. Jego głównym niebezpieczeństwem jest łatwość wywoływania alergii - powtarzalny kontakt ze związkiem skutkuje rozwinięciem się alergii na nikiel i kilkunastu procent ludzi. A zaistnienie takiej alergii może potem poważnie utrudniać życie, w związku z występowaniem niklu w wielu stopach metali używanych w elektronice czy medycynie.
------
[1] http://cdn.intechopen.com/pdfs-wm/24448.pdf
[2] http://pubs.acs.org/doi/abs/10.1021/ja00893a004
Z czym można pracować i co nie jest naj
Jedną z maksym przypisywanych Einsteinowi jest ta o przekazywaniu informacji, mówiąca że należy upraszczać jak można, ale nie bardziej. Bo jeśli coś uprościmy za bardzo, możemy wprowadzić inną osobę w błąd.
Ten problem dotyczy Polonu-210 opisanego przez autora jako "najbardziej promieniotwórcza substancja znana Ludzkości". Jak tłumaczy w komentarzach, wybrał tą substancję, bo jest dostępna w stosunkowo dużych ilościach, silnie radioaktywna i ma na tyle długi czas półrozpadu, że człowiek zdąży się nią zatruć. Ale o tym w filmie nie wspomina. Widz dostaje tylko prosty przekaz "Polon-210 jest najbardziej promieniotwórczy w ogóle", co nie jest prawdą.
Zgodnie z definicją aktywności promieniotwórczej, jest to szybkość z jaką następują rozpady promieniotwórcze. Największą aktywność mają te z najkrótszymi czasami półrozpadu i małymi masami, z czego wynika że najbardziej promieniotwórczą substancją jest Wodór-7 o czasie półtrwania 2,3×10−23 s i masie 8 unitów.
Tak że akurat Polon-210 byłby raczej "najbardziej promieniotwórczą substancją z jaką można się zetknąć" w tym znaczeniu, że jest stosunkowo dostępny i niektórzy muszą z nim pracować - choć można spekulować czy przypadkiem bardziej szkodliwy nie jest ameryk-243, spotykany w czujnikach dymu, który jest wytwarzany w większych ilościach a oprócz mało przenikliwego promieniowania alfa, produkuje też wysokoenergetyczne promienie gamma.
Podobny problem dotyczy "najbardziej palnej substancji" czyli trifluorku chloru, bo przecież fluorek ten sam w sobie nie jest specjalnie palny - jest natomiast silnym środkiem zapalającym, powodującym zapłon innych substancji z którymi się zetknie, a przy tym przeżerający substancje niepalne.
Myślę, że wśród najbardziej palnych substancji na pewno znajduje się silan, czyli krzemowy analog metanu. Duże powinowactwo krzemu do tlenu i ujemna jonizacja wodoru powodują, że w mieszance z tlenem ulega samozapłonowi w temperaturach około -100 °C, przy czym różne prace podają różne dane, w jednej opisano zapłon mieszanki z powietrzem w temperaturze -162 °C[1] Natomiast silniejszym od trifluorku chloru środkiem utleniającym i zapalającym inne substancje jest zapewne difluorek ditlenu, potrafiący zapalić stały metan w temperaturze 90 K.[2]
Inny problem dotyczy pozostałych substancji - tematem filmu są substancje "z którymi wolelibyście nie pracować" bo są niebezpieczne, trudne do obsługi, groźne jeśli się z nimi zetknąć. Tylko że w tym kontekście materiał wybuchowy oktanitrokuban pomimo swej niesamowitej siły wybuchowej zupełnie do zestawienia nie pasuje, jest bowiem stosunkowo bezpieczny - nie wybucha pod wpływem wstrząsów, nie powinien eksplodować nawet po uderzeniu młotkiem, dopiero wybuch spłonki inicjującej wywołuje eksplozję. Osobiście wolałbym pracować z nim, niż z na przykład chloranem potasu (jest ciekawszy).
Dlatego do zestawienia pasuje właściwie tylko batrachotoksyna, dwucyjan i ten bardzo azotowy materiał wybuchowy, eksplodujący spontanicznie.
Trochę zdziwiło mnie zatem, że autor filmu zapomniał o kilku innych substancjach, które warto tu pokrótce opisać.
Z czym ja wolałbym jako chemik nie pracować:
1. Diselenek węgla
Analog dwusiarczku węgla, przydatny w niektórych syntezach. A przy tym związek niesamowicie wprost śmierdzący. Po tym jak w 1936 roku otrzymano go po raz pierwszy, konieczna była ewakuacja najbliższej miejscowości, leżącej po zawietrznej stronie laboratorium. Jest lotny, łatwo przenika przez gumę i wchłania się do organizmu, łatwo przenika przez błony komórkowe i jest neurotoksyczny. Chemik pracujący z tym związkiem przez dłuższy czas otoczony byłby banieczką nieznośnego zapachu i bez wątpienia znalazłby wolne miejsce w tramwaju.
Podobne efekty mogą dawać też inne związki selenoorganiczne, jak selenol, analog etanolu, czy selenofenol.
Nie chcę zostać na kilka tygodni człowiekiem-skunksem, więc pracy z tym związkiem będę unikał.
2. Dimetylortęć
Jedna z najsilniejszych znanych trucizn. Dawka śmiertelna dla człowieka właściwie nie jest znana, estymuje się ją na podstawie kilku wypadków śmiertelnych. Znanym przypadkiem było zatrucie badaczki Karen Wetterhahn, której na rękawiczki rozprysnęło się ok. 0,05 ml substancji. Przeniknęła przez rękawiczki i w krótkim czasie wchłonęła się przez skórę w ilości wystarczającej do zabicia. Z batrachotoksyną czy jeszcze silniejszą ciguarotoksyną można w miarę bezpieczne pracować, z dimetylortęcią nie jest już tak dobrze.
Tak że jeśli na prawdę nie będzie mi to do czegoś potrzebne, wolę z tą substancją nie pracować.
3. Benzo-a-piren
Jeden z najważniejszych wielopierścieniowych węglowodorów aromatycznych (WWA) będących rakotwórczymi składnikami dymu. Metabolity benzo-a-pirenu łączą się z DNA wywołując mutacje. Spożyty wywołuje raka żołądka i jelit, obecność w powietrzu sprzyja nowotworom płu, a zanieczyszczenie skóry może wywołać raka skóry. W niektórych badaniach już jednokrotna iniekcja podskórna ekstraktu zwierającego WWA wywoływała nowotwory u badanych zwierzat.
Tak że pracy nad tym związkiem czystym, lub w ekstraktach wolałbym też unikać.
4. Gaz musztardowy
Środek bojowy będący silnym środkiem alkilującym. Wywołuje silne oparzenia skóry które ujawniają się nawet dobę po kontakcie z substancją, wchłonięty drogą inhalacyjną daje objawy zatrucia z dużym opóźnieniem, od 4 do 6 godzin dla małych dawek (dla dużych natychmiastowo). Jest potwierdzonym środkiem rakotwórczym.
Tak więc pragnącym zachować zdrowie i ładną twarz też radzę unikać styczności z tą substancją
5. Azydek sodu
Sól kwasu azotowodorowego, zawierająca trzy połączone atomy azotu. Azydki nieorganiczne zwykle są stosowane w syntezie azydków organicznych, oraz 1,2,3 triazyn, ewentualnie tetrazolu. Niestety azydki są związkami nietrwałymi i bardzo silnie trującymi, porównywalnie z cyjankami. Chętnie hydrolizują do azotowodoru, gazu bardziej toksycznego niż tlenek węgla, który w śladowych, niewyczuwalnych stężeniach jest w stanie wywołać zatrucie. Ekspozycja wywołuje mdłości, bóle głowy, uszkodzenie włókien nerwowych, zaburzenia oddychania zaś działaniem długofalowym po zatruciu jest uszkodzenie wątroby i jąder. Zatrucia tym związkiem wśród chemików są notowane dość często.
Przy ogrzewaniu potrafią eksplodować. Z jonami metali ciężkich tworzą wrażliwe na wstrząsy i nacisk azydki, używane czasem jeszcze w spłonkach.
Tak więc z tymi związkami bez konieczności też dobrze by było nie pracować
6. Siarczan niklu
Ten związek jest akurat stosunkowo często spotykany w laboratoriach chemii nieorganicznej. Jego głównym niebezpieczeństwem jest łatwość wywoływania alergii - powtarzalny kontakt ze związkiem skutkuje rozwinięciem się alergii na nikiel i kilkunastu procent ludzi. A zaistnienie takiej alergii może potem poważnie utrudniać życie, w związku z występowaniem niklu w wielu stopach metali używanych w elektronice czy medycynie.
------
[1] http://cdn.intechopen.com/pdfs-wm/24448.pdf
[2] http://pubs.acs.org/doi/abs/10.1021/ja00893a004
wtorek, 5 maja 2015
Czarne czy zielone?
Zaszedłem do sklepu aby przy okazji innych zakupów kupić też oliwki. Wybrałem słoiczek czarnych i oczywiście pierwsze co zrobiłem, to zajrzałem na masę netto i na skład. A tam oprócz soli i innych typowych składników zalewy, znalazłem też "stabilizator - glukonian żelazawy". Stabilizator czego? - zaciekawiłem się. A no stabilizator czarnej barwy.
Oliwka europejska to gatunek typowo śródziemnomorski. Jest wiecznie zielonym, niskim drzewem, często przybierającym formy krzewiaste. Za sprawą silnego systemu korzeniowego, dużej zdolności regeneracji i wolnego wzrostu może żyć długo, nawet ponad tysiąc lat. Owocem oliwki jest pestkowiec o tłustym miąższu otaczającym dużą pestkę. Większość światowych zbiorów jest przetwarzana na cenioną w kuchni oliwę, zdecydowanie mniejsza trafia na nasze stoły w formie zamarynowanej w soli lub occie.
I tutaj właśnie zaczyna się interesująca nas kwestia - owoc oliwki po zupełnym dojrzeniu ma kolor ciemnofioletowy, jednak większość oliwek zbiera się gdy są jeszcze zielone, niedojrzałe, głownie ze względu na lepszy smak. Skąd więc oliwka czarna?
Różne źródła różnie to podawały, ale wydaje się że są dwa typy - zebrane oliwki mogą być poddawane dalszej fermentacji, podczas której ciemnieją. Wydaje się jednak, że częściej poddawane są specjalnemu procesowi, polegającym na macerowaniu w alkalicznej zalewie z dodatkiem soli żelaza i przedmuchiwanej powietrzem. W alkalicznym środowisku związane polifenole w skórce oliwki ulegają uwolnieniu i mogą być utleniane przez powietrze do form ciemno zabarwionych. Sole żelaza dodatkowo tworzą z polifenolami ciemne kompleksy - opisałem to kiedyś w artykule o atramencie z dębowych galasów. W efekcie zielona oliwka staje się czarna.[1]
Identyczne procesy zachodzą podczas fermentacji, tutaj są jednak szybsze i dają równomierny kolor. Nawiasem mówiąc zielone oliwki są chronione przez dostępem powietrza aby same nie zaczęły ciemnieć - stąd zwykle zalewa zawiera kwas askorbinowy jako przeciwutleniacz.
Dodatek soli żelaza do zalewy utrwala kolor czarnych oliwek i zapobiega odbarwieniom. Ale czy wobec tego - zastanowią się niektórzy - czy przypadkiem aby taka czerniona oliwka nie jest szkodliwa? Wydaje się, że nie - sam owoc mógł wchłonąć nieco żelaza. Glukonian żelazawy jest natomiast solą nieszkodliwą - stanowi połączenie żelaza z pochodną glukozy, kwasem glukonowym. Połączenie to charakteryzuje się tym, że w takiej formie żelazo jest stosunkowo dobrze przyswajalne, stąd też używa się do w suplementach do leczenia anemii. Dopiero dość duże dawki mogą wywołać biegunki i podrażnienia, co związane jest z toksycznym działaniem samego żelaza.[2]
W anglojęzycznym internecie zauważyć można charakterystyczną pomyłkę - otóż wiele osób widząc nazwę "gluconate" sądzi, że jest to składnik zawierający gluten. A to nie prawda.
Wygląda na to, że sprzedawane w sklepach oliwki, nie są tak czarne jak to by się wydawało.
-------
[1] http://www.oliveoilsource.com/asktheexpert/are-olives-dyed-make-them-black
[2] http://en.wikipedia.org/wiki/Iron%28II%29_gluconate
Oliwka europejska to gatunek typowo śródziemnomorski. Jest wiecznie zielonym, niskim drzewem, często przybierającym formy krzewiaste. Za sprawą silnego systemu korzeniowego, dużej zdolności regeneracji i wolnego wzrostu może żyć długo, nawet ponad tysiąc lat. Owocem oliwki jest pestkowiec o tłustym miąższu otaczającym dużą pestkę. Większość światowych zbiorów jest przetwarzana na cenioną w kuchni oliwę, zdecydowanie mniejsza trafia na nasze stoły w formie zamarynowanej w soli lub occie.
I tutaj właśnie zaczyna się interesująca nas kwestia - owoc oliwki po zupełnym dojrzeniu ma kolor ciemnofioletowy, jednak większość oliwek zbiera się gdy są jeszcze zielone, niedojrzałe, głownie ze względu na lepszy smak. Skąd więc oliwka czarna?
Różne źródła różnie to podawały, ale wydaje się że są dwa typy - zebrane oliwki mogą być poddawane dalszej fermentacji, podczas której ciemnieją. Wydaje się jednak, że częściej poddawane są specjalnemu procesowi, polegającym na macerowaniu w alkalicznej zalewie z dodatkiem soli żelaza i przedmuchiwanej powietrzem. W alkalicznym środowisku związane polifenole w skórce oliwki ulegają uwolnieniu i mogą być utleniane przez powietrze do form ciemno zabarwionych. Sole żelaza dodatkowo tworzą z polifenolami ciemne kompleksy - opisałem to kiedyś w artykule o atramencie z dębowych galasów. W efekcie zielona oliwka staje się czarna.[1]
Identyczne procesy zachodzą podczas fermentacji, tutaj są jednak szybsze i dają równomierny kolor. Nawiasem mówiąc zielone oliwki są chronione przez dostępem powietrza aby same nie zaczęły ciemnieć - stąd zwykle zalewa zawiera kwas askorbinowy jako przeciwutleniacz.
Dodatek soli żelaza do zalewy utrwala kolor czarnych oliwek i zapobiega odbarwieniom. Ale czy wobec tego - zastanowią się niektórzy - czy przypadkiem aby taka czerniona oliwka nie jest szkodliwa? Wydaje się, że nie - sam owoc mógł wchłonąć nieco żelaza. Glukonian żelazawy jest natomiast solą nieszkodliwą - stanowi połączenie żelaza z pochodną glukozy, kwasem glukonowym. Połączenie to charakteryzuje się tym, że w takiej formie żelazo jest stosunkowo dobrze przyswajalne, stąd też używa się do w suplementach do leczenia anemii. Dopiero dość duże dawki mogą wywołać biegunki i podrażnienia, co związane jest z toksycznym działaniem samego żelaza.[2]
W anglojęzycznym internecie zauważyć można charakterystyczną pomyłkę - otóż wiele osób widząc nazwę "gluconate" sądzi, że jest to składnik zawierający gluten. A to nie prawda.
Wygląda na to, że sprzedawane w sklepach oliwki, nie są tak czarne jak to by się wydawało.
-------
[1] http://www.oliveoilsource.com/asktheexpert/are-olives-dyed-make-them-black
[2] http://en.wikipedia.org/wiki/Iron%28II%29_gluconate
sobota, 11 kwietnia 2015
Dlaczego sód wybucha w wodzie?
Czytelnik zwrócił jakiś czas temu moją uwagę na intrygujący artykuł ze styczniowego wydania The Nature*, sugerując że byłby to dobry temat na wpis. Po zapoznaniu się z tematem przyznałem mu rację. Bo to w sumie ciekawe, że tak znane i często wykonywane doświadczenie zawiera w sobie tak nietypowy i dopiero teraz poznany mechanizm.
Pierwiastki z grupy litowców to lekkie, miękkie metale o dużej aktywności, które reagują z powietrzem i wodą. W tym ostatnim przypadku reakcja jest silnie egzotermiczna doprowadzając często do zapalenia się powstającego wodoru zaś większe kawałki po prostu wybuchają, a dla najbardziej reaktywnych rubidu i cezu mamy do czynienia z detonacją wytwarzającą falę uderzeniową.
Tym jednak co zastanawiało badaczy, jest mechanizm wybuchu - eksplozja doprowadza często do rozdrobnienia reagującego kawałka, sądzono jednak że jej źródło jest zewnętrzne, a więc jest to wybuch wodoru na powierzchni, będący wynikiem gwałtownego przyspieszenia przebiegu reakcji. Jednak powierzchnia kontaktu metalu z wodą jest w tym przypadku raczej mała, zaś powstająca warstwa wodoru powinna raczej hamować proces niż przyspieszać - dla małych kawałków sodu powstający w reakcji gaz często jest w stanie unieść metal nad powierzchnię wody, działając niczym poduszka powietrzna.
Z dotychczasowych doświadczeń wynikało, że wybuch większych kawałków następuje gdy pod wpływem ciepła reakcji nastąpi częściowe stopienie, dlatego badacze z zespołu Pavela Jungwirtha z Czeskiej Akademii Nauk wybrali do badań stop sodu z potasem, będący eutektykiem ciekłym w temperaturze pokojowej. Wrzucenie kropli stopu do wody wywoływało natychmiastowy wybuch. Krople wkraplano do cylindra z wodą, filmując każdy wybuch bardzo szybką kamerą, przy czym upuszczano je z odpowiedniej wysokości, tak aby przerwać początkowo powstającą warstewkę gazu. Aby w obserwacjach nie przeszkadzało następujące później zapalenie się wodoru, cylinder napełniono gazem obojętnym.
Proces wybuchu kropli stopu okazał się bardzo szybki:
Rozpryskiwanie się bocznych strużek następuje już przy pierwszym kontakcie, zanim kropla zdąży zagłębić się w wodzie. Równocześnie podgląd od spodu ujawnił, że kropla rozpadła się na wiele drobnych igiełek ciekłego metalu. Kolejną ciekawą rzeczą jaką widać na zdjęciach jest fioletowy kolor rozprysku - sam sód jak i jego jony nie mają takiego koloru, dlatego najbardziej prawdopodobnym wyjaśnieniem było uznanie, że za kolor odpowiada krótko żyjące indywiduum - zsolwatowany elektron.
Solwatacja to proces otaczania jonu rozpuszczanego w roztworze przez cząsteczki rozpuszczalnika. Woda ma dość duży moment dipolowy i mimo obojętności elektrycznej jej cząsteczki są przyciągane przez pole elektryczne wokół jonu. Tak dzieje się przy rozpuszczaniu soli w wodzie, a wydzielanie się przy tym pewnej energii ma wpływ na łatwość rozpuszczania. Jon otoczony cząsteczkami rozpuszczalnika, to jon zsolwatowany:
W tym przypadku do wody został w dużych ilościach wprowadzony najmniejszy możliwy anion - wolny elektron. I na krótką chwilę, zanim nie doszło do reakcji redukcji wody, został on otoczony jej cząsteczkami. Ponieważ elektron może przyjmować w takiej postaci różne stany energetyczne, pochłania część światła widzialnego i nadaje wodzie fioletowy kolor. Znacznie trwalsze roztwory ze zsolwatowanym elektronem można otrzymać w ciekłym amoniaku i niektórych aminach, rozpuszczając w nich aktywne metale; roztwory takie mają kolor od niebieskiego co brunatnego a w dużych stężeniach elektronów zaczynają odbijać światło i wyglądają jak płynny metal.
Ale skończmy tą dygresję.
Było więc wiadomo że tuż po kontakcie sodu z wodą, zaczyna być on rozpryskiwany na wiele cienkich strużek metalu. Było też wiadome, że przy tym procesie do wody uwalniana jest tak duża ilość wolnych elektronów, że woda na krótko się zabarwia. Wiedząc o tym badacze mogli stwierdzić, że za owo rozpryśnięcie odpowiada znany już od dawna proces, znany dotychczas ze skali mikroskopijnej - eksplozja kulombowska.
Proces opisano teoretycznie już w XIX wieku ale w zasadzie dotyczył on dosyć małej skali. Jeśli weźmiemy skrawek dowolnej materii i usuniemy elektrony z atomów, powstanie nam skupisko położonych blisko siebie jonów dodatnich. W normalnym przypadku elektrony nie tylko zobojętniają ale też spajają ze sobą atomy. Po ich usunięciu elektrostatyczne odpychanie jednakowych ładunków przeważa nad przyciąganiem i całe skupisko rozpada się na wszystkie strony.
Makroskopowym modelem może być często pokazywane doświadczenie fizyczne, w którym po umieszczeniu garści spreparowanego ryżu w silnym polu elektrycznym, ziarenka zaczynają strzelać we wszystkie strony, odpychane od naelektryzowanego stosiku:
Efekt ten bywa wykorzystywany w laserowej abrazji pewnych materiałów - naświetlenie powierzchni odpowiednio silnym impulsem lasera nadaje jej punktowo tak duża energię, że uciekają z niej elektrony. Pozostałe naładowane jony rozpryskują się i powstaje nam zagłębienie o rozmiarach możliwych do regulowania.
W nieco większej skali eksplozja kulombowska jest używana w technice elektrospreju, używanej w spektroskopii mas - kropelka roztworu umieszczona w silnym polu elektrycznym rozpryskuje się na jeszcze drobniejsze. Zjawisko to ma jeszcze znaczenie w oddziaływaniu promieniowania na materię - uderzenie wysokoenergetycznej cząstki jonizuje część atomów, doprowadzając do ich przemieszczenia i powstania uszkodzenia w strukturze materiału.
W przypadku kropli ciekłego metalu alkalicznego, proces zachodzi w dużej skali.
Gdy tylko kropla zaczyna się stykać z wodą, zachodzi szybka reakcja chemiczna połączona z oddawaniem elektronów wodzie. Ładunek dodatni na powierzchni metalu rośnie na tyle gwałtownie, że początkowe czysto mechaniczne nieregularności kształtu, zaczynają się zachowywać jak indywidualne naładowane cząstki. Odpychane statycznie porcje, zamieniają się w igły płynnego metalu, które są wystrzeliwane w otaczającą wodę w dużym rozdrobnieniu. W efekcie następuje taka sytuacja, do jakiej by doszło gdybyśmy zmieszali z wodą sód w formie drobnego pyłu - gwałtowne zwiększenie powierzchni reagującej powoduje, że w stosunkowo małej objętości wody wydzielonych zostaje bardzo dużo ciepła i gazowego wodoru. Rozprężający się powstały gaz powoduje eksplozję, która rozrzuca gorące cząstki metalu i krople wody. Gdy reakcja jest prowadzona w powietrzu, rozpryśnięte krople w kontakcie z powietrzem zapalają się jasnymi iskrami a od nich zapala się wodór, wywołując drugą eksplozję.
Jest to dokładnie objaśnione na poniższym filmie:
Bonus
A tak wygląda reakcja kilku ton sodu, wrzuconego w beczkach wprost do morza:
W taki sposób unieszkodliwiano pozostałości po pociskach zapalających.
---------
* Mason, P. E. et al., Coulomb explosion during the early stages of the reaction of alkali metals with water, Nature Chem. (2015).
Pierwiastki z grupy litowców to lekkie, miękkie metale o dużej aktywności, które reagują z powietrzem i wodą. W tym ostatnim przypadku reakcja jest silnie egzotermiczna doprowadzając często do zapalenia się powstającego wodoru zaś większe kawałki po prostu wybuchają, a dla najbardziej reaktywnych rubidu i cezu mamy do czynienia z detonacją wytwarzającą falę uderzeniową.
Tym jednak co zastanawiało badaczy, jest mechanizm wybuchu - eksplozja doprowadza często do rozdrobnienia reagującego kawałka, sądzono jednak że jej źródło jest zewnętrzne, a więc jest to wybuch wodoru na powierzchni, będący wynikiem gwałtownego przyspieszenia przebiegu reakcji. Jednak powierzchnia kontaktu metalu z wodą jest w tym przypadku raczej mała, zaś powstająca warstwa wodoru powinna raczej hamować proces niż przyspieszać - dla małych kawałków sodu powstający w reakcji gaz często jest w stanie unieść metal nad powierzchnię wody, działając niczym poduszka powietrzna.
Z dotychczasowych doświadczeń wynikało, że wybuch większych kawałków następuje gdy pod wpływem ciepła reakcji nastąpi częściowe stopienie, dlatego badacze z zespołu Pavela Jungwirtha z Czeskiej Akademii Nauk wybrali do badań stop sodu z potasem, będący eutektykiem ciekłym w temperaturze pokojowej. Wrzucenie kropli stopu do wody wywoływało natychmiastowy wybuch. Krople wkraplano do cylindra z wodą, filmując każdy wybuch bardzo szybką kamerą, przy czym upuszczano je z odpowiedniej wysokości, tak aby przerwać początkowo powstającą warstewkę gazu. Aby w obserwacjach nie przeszkadzało następujące później zapalenie się wodoru, cylinder napełniono gazem obojętnym.
Proces wybuchu kropli stopu okazał się bardzo szybki:
Rozpryskiwanie się bocznych strużek następuje już przy pierwszym kontakcie, zanim kropla zdąży zagłębić się w wodzie. Równocześnie podgląd od spodu ujawnił, że kropla rozpadła się na wiele drobnych igiełek ciekłego metalu. Kolejną ciekawą rzeczą jaką widać na zdjęciach jest fioletowy kolor rozprysku - sam sód jak i jego jony nie mają takiego koloru, dlatego najbardziej prawdopodobnym wyjaśnieniem było uznanie, że za kolor odpowiada krótko żyjące indywiduum - zsolwatowany elektron.
Solwatacja to proces otaczania jonu rozpuszczanego w roztworze przez cząsteczki rozpuszczalnika. Woda ma dość duży moment dipolowy i mimo obojętności elektrycznej jej cząsteczki są przyciągane przez pole elektryczne wokół jonu. Tak dzieje się przy rozpuszczaniu soli w wodzie, a wydzielanie się przy tym pewnej energii ma wpływ na łatwość rozpuszczania. Jon otoczony cząsteczkami rozpuszczalnika, to jon zsolwatowany:
W tym przypadku do wody został w dużych ilościach wprowadzony najmniejszy możliwy anion - wolny elektron. I na krótką chwilę, zanim nie doszło do reakcji redukcji wody, został on otoczony jej cząsteczkami. Ponieważ elektron może przyjmować w takiej postaci różne stany energetyczne, pochłania część światła widzialnego i nadaje wodzie fioletowy kolor. Znacznie trwalsze roztwory ze zsolwatowanym elektronem można otrzymać w ciekłym amoniaku i niektórych aminach, rozpuszczając w nich aktywne metale; roztwory takie mają kolor od niebieskiego co brunatnego a w dużych stężeniach elektronów zaczynają odbijać światło i wyglądają jak płynny metal.
Ale skończmy tą dygresję.
Było więc wiadomo że tuż po kontakcie sodu z wodą, zaczyna być on rozpryskiwany na wiele cienkich strużek metalu. Było też wiadome, że przy tym procesie do wody uwalniana jest tak duża ilość wolnych elektronów, że woda na krótko się zabarwia. Wiedząc o tym badacze mogli stwierdzić, że za owo rozpryśnięcie odpowiada znany już od dawna proces, znany dotychczas ze skali mikroskopijnej - eksplozja kulombowska.
Proces opisano teoretycznie już w XIX wieku ale w zasadzie dotyczył on dosyć małej skali. Jeśli weźmiemy skrawek dowolnej materii i usuniemy elektrony z atomów, powstanie nam skupisko położonych blisko siebie jonów dodatnich. W normalnym przypadku elektrony nie tylko zobojętniają ale też spajają ze sobą atomy. Po ich usunięciu elektrostatyczne odpychanie jednakowych ładunków przeważa nad przyciąganiem i całe skupisko rozpada się na wszystkie strony.
Makroskopowym modelem może być często pokazywane doświadczenie fizyczne, w którym po umieszczeniu garści spreparowanego ryżu w silnym polu elektrycznym, ziarenka zaczynają strzelać we wszystkie strony, odpychane od naelektryzowanego stosiku:
Efekt ten bywa wykorzystywany w laserowej abrazji pewnych materiałów - naświetlenie powierzchni odpowiednio silnym impulsem lasera nadaje jej punktowo tak duża energię, że uciekają z niej elektrony. Pozostałe naładowane jony rozpryskują się i powstaje nam zagłębienie o rozmiarach możliwych do regulowania.
W nieco większej skali eksplozja kulombowska jest używana w technice elektrospreju, używanej w spektroskopii mas - kropelka roztworu umieszczona w silnym polu elektrycznym rozpryskuje się na jeszcze drobniejsze. Zjawisko to ma jeszcze znaczenie w oddziaływaniu promieniowania na materię - uderzenie wysokoenergetycznej cząstki jonizuje część atomów, doprowadzając do ich przemieszczenia i powstania uszkodzenia w strukturze materiału.
W przypadku kropli ciekłego metalu alkalicznego, proces zachodzi w dużej skali.
Gdy tylko kropla zaczyna się stykać z wodą, zachodzi szybka reakcja chemiczna połączona z oddawaniem elektronów wodzie. Ładunek dodatni na powierzchni metalu rośnie na tyle gwałtownie, że początkowe czysto mechaniczne nieregularności kształtu, zaczynają się zachowywać jak indywidualne naładowane cząstki. Odpychane statycznie porcje, zamieniają się w igły płynnego metalu, które są wystrzeliwane w otaczającą wodę w dużym rozdrobnieniu. W efekcie następuje taka sytuacja, do jakiej by doszło gdybyśmy zmieszali z wodą sód w formie drobnego pyłu - gwałtowne zwiększenie powierzchni reagującej powoduje, że w stosunkowo małej objętości wody wydzielonych zostaje bardzo dużo ciepła i gazowego wodoru. Rozprężający się powstały gaz powoduje eksplozję, która rozrzuca gorące cząstki metalu i krople wody. Gdy reakcja jest prowadzona w powietrzu, rozpryśnięte krople w kontakcie z powietrzem zapalają się jasnymi iskrami a od nich zapala się wodór, wywołując drugą eksplozję.
Jest to dokładnie objaśnione na poniższym filmie:
Bonus
A tak wygląda reakcja kilku ton sodu, wrzuconego w beczkach wprost do morza:
W taki sposób unieszkodliwiano pozostałości po pociskach zapalających.
---------
* Mason, P. E. et al., Coulomb explosion during the early stages of the reaction of alkali metals with water, Nature Chem. (2015).
piątek, 3 kwietnia 2015
To już 4 lata
No i stało się. Minęło 4 lata od założenia bloga.
Jak na razie statystyki przedstawiają się następująco:
- 194 opublikowane wpisy
- 742 opublikowane komentarze (ok. 10-15% to moje odpowiedzi)
- 498 103 wyświetlenia.
W ostatnim czasie średnia dzienna przeglądalność wynosiła ok. 400-500 wyświetleń dziennie. Myślę że jak na blog zajmujący się dziedziną ścisłą, jest to całkiem niezły wynik.
Spośród postów opublikowanych w ostatnim roku najpopularniejsze były następujące:
- Ile pierwiastków występuje w przyrodzie?
- Poison Story (6.)
- Chemia bardzo tłustego pączka czyli o niemożebnie długim składzie słów kilka
- Chemicy i ich zatrucia
- Poison Story (7.)
Oczywiście w planach mam następne interesujące wpisy, mimo zapewne zauważalnego w ostatnim czasie zmniejszenia częstości ich dodawania.
Zobaczymy jak to będzie dalej.
Jak na razie statystyki przedstawiają się następująco:
- 194 opublikowane wpisy
- 742 opublikowane komentarze (ok. 10-15% to moje odpowiedzi)
- 498 103 wyświetlenia.
W ostatnim czasie średnia dzienna przeglądalność wynosiła ok. 400-500 wyświetleń dziennie. Myślę że jak na blog zajmujący się dziedziną ścisłą, jest to całkiem niezły wynik.
Spośród postów opublikowanych w ostatnim roku najpopularniejsze były następujące:
- Ile pierwiastków występuje w przyrodzie?
- Poison Story (6.)
- Chemia bardzo tłustego pączka czyli o niemożebnie długim składzie słów kilka
- Chemicy i ich zatrucia
- Poison Story (7.)
Oczywiście w planach mam następne interesujące wpisy, mimo zapewne zauważalnego w ostatnim czasie zmniejszenia częstości ich dodawania.
Zobaczymy jak to będzie dalej.
niedziela, 15 marca 2015
Roztwory przekorne
Nie wiedzieć czemu w dydaktyce szkolnej temat buforów jakoś nie jest wiązany z regułą przekory, choć przecież ich działanie jest tej zasady najlepszym przykładem. Wydaje się, że ponieważ zwykle omawia się ją przed omówieniem praw gazowych i traktuje się ją wraz z prawem działania mas jako wstęp do tego działu, stąd działanie reguły uczniowie poznają na przykładzie przemian tlenku azotu II z formy jednocząsteczkowej w dimeryczną, lub syntezy amoniaku z pierwiastków. Potem jednak nie powraca się do niej w działach dotyczących innych typów i środowisk reakcji, w efekcie wiedza zamiast się kumulować i syntetyzować, ulega podziałowi na odosobnione bloki.
Tak zwana Reguła Przekory (ściślej zaś reguła le Chateliera-Browna), to dość arbitralne stwierdzenie, że pewne układy znajdujące się w stanie równowagi, reagują na bodźce zaburzające tą równowagę tak, jakby opierały się zmianie, dążąc do zmniejszenia skutków zmian. W tym sensie przekornie na dodatek wody reaguje układ soli na dnie naczynia z nasyconym jej roztworem - część soli się rozpuszcza i stężenie roztworu nie ulega zmianie. Zasada daje się zresztą uogólnić i na inne dziedziny, jako dotyczące również układów nie chemicznych, na przykład do przemian społecznych czy równowag ekonomicznych.
Równowaga w jakiej znajdują się układy podlegające tej regule, jest równowagą dynamiczną, co nie polega na tym, że nie zachodzą w nich żadne reakcje, lecz że reakcje przeciwstawne zachodzą z taką samą prędkością. Najlepszą ilustracją będzie tu układ naczyń połączonych, w których w prawdzie poziom wody pozostaje taki sam, lecz wskutek chaotycznych ruchów cząstek, co chwila małe porcje przedostają się z jednego naczynia do drugiego.
Jeśli podniesiemy jedno naczynie, woda będzie tak długo przepływała z niego do niższego, aż zrównoważy ją woda wpychana z powrotem. To chyba zrozumiałe. Chemicznym tego odpowiednikiem będzie na przykład równowaga między na przykład wodą, dwutlenkiem węgla i kwasem węglowym:
H2O + CO2 ⇌ H2CO3
dwutlenek węgla reaguje z wodą tworząc kwas węglowy, jednak równocześnie kwas węglowy rozkłada się na wodę i dwutlenek węgla. W normalnych warunkach równowaga jest silnie przesunięta w lewo, co oznacza że samego kwasu jest niewiele, a zresztą de facto występuje w postaci jonów jako że jego cząsteczka jest bardzo nietrwała. Jeśli zwiększymy ciśnienie gazu, tym samym zwiększając odczuwane przez roztwór stężenie (a więc ilość cząsteczek skorych do reakcji w jednostce czasu), równowaga przesunie się w prawo - część gazu się rozpuści a nadane ciśnienie opadnie. Jeśli zmniejszymy ciśnienie, bądź rozcieńczymy gaz nad roztworem na przykład azotem, część kwasu węglowego się rozpadnie i troszeczkę skompensuje spadek stężenia. Oto i przekorność.

Roztwór buforowy natomiast opiera się zmianom odczynu. Dodając kwas nie zakwasimy go do pewnych granic, dodając zasady również do pewnego stopnia go nie zalkalizujemy. Czysta przekora! Natomiast przyczyna takiego się ich zachowania jest paradoksalna - roztwory buforowe są mieszaninami kwasów z zasadami.
Żeby rzecz wyjaśnić, trzeba cofnąć się do tak podstawowej sprawy, jak definicja "kwasu" i "zasady" - a nie jest to rzecz oczywista. Pierwotnie kwasami nazywano substancje o kwaśnym smaku, zaś alkaliami nazywano produkty ługowania wodą popiołów i spalonych metali . Nieco później próbowano rzecz uściślić, przez stwierdzenie, że zasadami są substancje, które zobojętniają kwasy co jednak prowadziło do tautologii, bo dla odmiany "kwasy" definiowano jako substancje zobojętniające zasady.
Zasady, czy raczej alkalia otrzymywano z popiołów przez ługowanie wodą - skąd nazwa od arabskiego "al kali" - "popiół". Taki przesącz, nazywany potażem składał się głównie z węglanów potasu i sody z domieszką wodorotlenków. Dopiero po przereagowaniu z wapnem gaszonym (kaustyfikacji) otrzymywało się wodorotlenki, które po rozpuszczeniu w wodzie dawały "potaż żrący".
Aby nie wpaść w błędne koło w XVIII wieku ustalono ogólną definicję kwasów jako lotnych substancji zawierających niemetale, których roztwory w dużym stężeniu mają właściwości żrące i roztwarzają metale, natomiast zasadami były substancje nielotne, które reagując z kwasami usuwają ich właściwości żrące. Zasady uznano zatem za substancje będące podstawami, które zatrzymywały lotne kwasy i dawały obojętne sole i inne związki - to trochę jeszcze trącące alchemią twierdzenie przyczyniło się w pewnym stopniu do obecnego nazewnictwa. W języku angielskim, niemieckim, francuskim i w wielu innych, zasada to "baza", przy czym słowo to używane jest prawie zawsze również w niechemicznym kontekście jako "podstawa" lub "zasada działania".
Antoine Lavoisier, wybitny chemik tamtych czasów, uściślił definicję, dodając że kwasy zawierają centralny atom o wysokim stopniu utlenienia, otoczony przez atomy tlenu i powstają z tlenków niemetali, zaś z tlenków metali powstają zasady. Dla kwasów siarkowego czy fosforowego reguła się sprawdza bardzo ładnie, niestety wynika z niej, że wszystkie kwasu muszą być tlenowe. Autorytet francuskiego chemika był tak duży, że gdy Sheele odkrył chlor, dający z czystym wodorem substancję silnie kwasową, uznano że jest to tlenek nieznanego pierwiastka, nazwanego Murium. Skoro tlen miał być pierwiastkiem charakterystycznym dla kwasów, toteż gdy przyszło nadać mu nazwę naukową podkreślono ten fakt, i z połączenia łacińskich oxis - kwas - i gennao - tworzyć, utworzono nazwę oxygenium, co nasz Śniadecki, tworząc polskie nazewnictwo, próbował tłumaczyć jako Kwasoród. Na szczęście nazwa się nie przyjęła, bo już w 1810 roku Humphry Davy udowodnił , że kwas solny, a także siarkowodorowy i selenowodorowy, nie zawierają tlenu.
Dopiero w 1838 roku Justus von Liebig badając kwasy organiczne stwierdził, że dla kwasów charakterystyczna jest obecność wodoru, który łatwo ulega odszczepieniu i może być zastąpiony przez zawarty w zasadach atom metalu. Również w reakcji z aktywnymi metalami, jak żelazo czy cynk, wodór jest wypierany z kwasów. Ponieważ w podobny sposób w podwyższonej temperaturze aktywne metale reagują z wodą, o której było wiadome, że składa się z dwóch atomów wodoru i jednego atomu tlenu, po sprawdzeniu mas można było dojść do wniosku, o istnieniu "powodorowej pozostałości" - jonów OH. Z tą wiedzą w 1884 roku Svante Arrhenius sformułował teorię, że kwasami są substancje, które rozpuszczone w wodzie uwalniają jony wodorowe, zaś zasadami te, które uwalniają jony hydroksylowe. Zatem do zasad i kwasów zaliczały się zarówno kwasy i wodorotlenki, jak i tlenki metali i niemetali.
Kwasy:
HCl = H + + Cl -
SO2 + H2O = 2H + + SO3-
Zasady:
NaOH = Na+ + OH-
MgO + H2O = Mg(OH)2
SO2 + H2O = 2H + + SO3-
Zasady:
NaOH = Na+ + OH-
MgO + H2O = Mg(OH)2
Niestety nie dawało się w ten sposób wyjaśnić właściwości niektórych substancji. Głównie amoniaku, który po rozpuszczeniu nie oddawał lecz odbierał wodzie wodór, uwalniając jony hydroksylowe i wywołując odczyn alkaliczny. Można tu podać jeszcze przykład kwasu borowego, który rozpuszczając się w wodzie, odbiera od niej grupę OH, pozostawiając jony wodorowe i nadając roztworowi odczyn kwaśny. Jako uzupełnienie należy dodać, że de facto wolnych jonów wodorowych się nie obserwuje - byłyby swobodnymi protonami o dosyć krótkim czasie życia - łączą się jednak z następną cząsteczką wody w jony H3O+ .
Aby trochę uzupełnić te braki, w 1923 roku dwaj badacze Johannes Nicolaus Brønsted i Martin Lowry, całkiem zresztą niezależnie, sformułowali inną teorię. Kwasami miały być te substancje, które oddają protony, zaś zasadami te, które je przyjmują. No tak, amoniak przyjmuje wodór, i jego roztwór jest zasadowy - jest zasadą. Wodorotlenki wiążą protony kwasów. Kwasy oddają protony. Wszystko się w sumie zgadza. Ponieważ jednak nie wszystkie rzeczy pasowały, stworzono inne teorie, aby objaśnić zachowanie się substancji w rozpuszczalnikach innych niż woda, i w stopionych solach, ale nimi nie będę się zajmował.
I cóż z tego wszystkiego wynika? Jak powiedziałem, bufory są mieszaninami kwasów i zasad. Ale Brønsteda. W roztworze są zarówno substancje oddające jak i przyjmujące protony, a więc zarówno takie, które zobojętniają kwasy, jak i te, które zobojętniają zasady. Wyobraźmy sobie, że w zlewce mamy wstawione dwie mniejsze zleweczki, w jednej kwas, na przykład siarkowy, a w drugiej zasadę, na przykład wodorotlenek sodu, i powiedzmy że będziemy przyjmować sumaryczny odczyn zlewki jako różnicę odczynów w zleweczkach. Teraz do tej z zasadą dodajmy trochę kwasu - porcja zostanie zobojętniona, zaś nadmiar zasady sprawi ze pH roztworu nie zmieni się znacząco. Albo inaczej - dodajmy trochę zasady do zleweczki z kwasem - porcja się nam zobojętni a obecny nadmiar... itp.
No ale w końcu jednak to nasze "wypadkowe pH" trochę się zmieniło, w pierwszym przypadku ubyło nam trochę kwasu a drugim zasady. Więc teraz wyobraźmy sobie, że przy pomocy magicznego zaklęcia odwracamy reakcje tak aby poziomy powróciły do wyjściowych i wszystko jest w porządku. Tym naszym magicznym zaklęciem może być tu reguła przekory, zachodzi to jednak w tych specyficznych warunkach, gdy zasada zamienić się może w kwas, a kwas w zasadę.
\>

Jak już pisałem, wedle Broensteda kwas to substancja oddająca proton. Gdy proton zostaje oddany pozostaje nam reszta kwasowa, ta jednak może równie dobrze przyjąć proton i stać się znów wyjściową cząsteczką. Skoro może przyjąć proton to jest zasadą. To nawet całkiem logiczne - gdy zobojętnimy wodorotlenek sodu kwasem solnym, powstanie nam sól kuchenna czyli chlorek sodu, gdy do jej roztworu dodamy mocnego kwasu, na przykład siarkowego, równowaga reakcji zobojętnienia - dotychczas całkowicie przesunięta w prawo - ulegnie częściowemu odwróceniu i zacznie się nam wydzielać gazowy chlorowodór. Dawniej właśnie tak produkowano kwas solny, skąd też oczywiście bierze się nazwa.
Zatem kwas solny jest kwasem, a powstający zeń anion chlorkowy zasadą. Jednak roztwór kwasu solnego i chlorku sodu nie stanowi buforu - dodanie do tej mieszanki zasady zobojętni część kwasu, sól pozostanie natomiast niezmieniona. Dodawanie kwasu też nie wywoła reakcji, przynajmniej do momentu gdy silnie kwaśne warunki nie zaczną wypierać chlorowodoru. Inaczej jest w sytuacji gdy mamy do czynienia z kwasem słabo dysocjującym.
W roztworze kwasu octowego część cząsteczek przybiera formę obojętną, CH3COOH . Cząsteczka taka może oddać proton, jest więc kwasem. Część kwasu octowego w roztworze uległa dysocjacji, a więc uwolnieniu protonu. Powstająca reszta kwasowa, anion CH3COO− może przyjąć proton, zatem jest zasadą. Oczywiście w tych warunkach zachodzi między nimi równowaga, a proton co raz jest oddawany i przyjmowany. Co jednak zwraca uwagę - przyjęcie protonu przez jon octanowy usuwa go z roztworu. W przypadku kwasu solnego jony wodorowe pochodzące od kwasu były obecne w roztworze cały czas ze względu na jego dobrą dysocjację, tutaj łączą się w obojętną cząsteczkę kwasu i nie mają wpływu na pH roztworu
Dodatek niewielkiej ilości kwasu przesuwa równowagę - część anionów octanowych przyjmie nadmiarową ilość protonów. Znikną one więc z roztworu a odczyn obniży się mniej niżby to wynikało z dodanej ilości. Dodatek niewielkiej ilości zasady zobojętni małą ilość jonów hydroniowych, mniej ich zatem będzie się łączyło z jonami octanowymi i w wyniku niezrównoważenia nieco większa ilość kwasu zdysocjuje zakwaszając roztwór, przez co podwyższenie pH będzie mniejsze niżby to wynikała z dodanej ilości zasady.
To jak duże ilości kwasów lub zasad można dodać zależy od ilości obu form w roztworze. Dla samego kwasu octowego, anionów octanowych jest mało, łatwo więc przełamać taką przekorę. Aby mechanizm mógł więc pokazać się w pełnym świetle i przeciwstawiać się większym ilościom odczynników, tworzy się mieszaniny słabych elektrolitów i ich rozpuszczalnych soli, najlepiej w jednakowej ilości.
Kwas octowy zmieszany z odpowiednią ilością octanu sodu da zatem bufor octanowy, utrzymujący odczyn w zakresie pH 3-6 zależnie od stosunku kwasu do soli. Roztwór amoniaku z dodatkiem chlorku amonu to bufor amonowy z pH 8-11. Kwas borny rozpuszczony wraz z boranem sodu to bufor boranowy, o pH 7-9.
Każdy taki roztwór zawiera stosunkowo dużo form zdysocjowanych i niezdysocjowanych, dzięki czemu może buforować odczyn zaburzany dodatkami elektrolitów w ilościach podobnego rzędu. Bufory są używane tam, gdzie potrzebny jest stały, dobrze określony odczyn, nie zaburzany zanieczyszczeniami. Wiele pomiarów właściwości substancji wykonuje się w roztworach buforujących, które utrzymują znaną wartość pH w czasie całego pomiaru. Bufory po otrzymaniu mogą być też dłuższy czas przechowywane.

Działanie buforu można wyjaśnić w jeszcze jeden obrazowy sposób - jako naczynia połączone. Jeśli wlejemy roztwór do jednego ramiona częściowo napełnionej U-rurki, to zaburzymy równowagę. Układ zachowa się jednak przekornie - część roztworu przepłynie do drugiego ramienia do momentu odzyskania równowagi. Poziom w ramieniu do którego wlewaliśmy ciecz wzrośnie zatem o połowę mniej, niż by wynikało z dodanej ilości, bo część odpłynęła. Nie można jednak czynić tego w nieskończoność, bo w końcu w rurce miejsca zabraknie, a drugie ramię nie będzie mogło tego zrekompensować bo i jemu zabraknie wolnej objętości.
Tak też jest i z buforami - mogą powstrzymywać zmiany odczynu dla ilości kwasów lub zasad mniejszych lub porównywalnych ze stężeniem własnym. Jednak z dużymi ilościami sobie nie poradzą - po całkowitym zdysocjowaniu i zobojętnieniu słabego kwasu, bufor przestaje się opierać zasadom, po całkowitym sprotonowaniu anionu reszty kwasowej, roztwór przestaje się opierać dodatkom kwasu.
Ilość odczynnika potrzebna do przełamania buforu, określamy pojemnością buforu. Zależy ona od stopnia rozcieńczenia oraz stosunku ilości formy zdysocjowanej do niezdysocjowanej.
Ot i tyle.
Subskrybuj:
Posty (Atom)