Nawet podczas mycia próbówek można znaleźć chwilę na zabawę. Kończyły się roztwory odczynników, trzeba było umyć kolby i przygotować nowe. Jedna kolba po nadmanganianie potasu, druga po indygokarminie. Używam tego zestawu przy miareczkowaniu garbników, co zresztą szerzej omówię w innym wpisie. Dość że oba silnie zabarwione roztwory reagują do słabo żółtego produktu. Miałem więc podczas mycia trochę rozcieńczonych roztworów i mieszałem ze sobą, patrząc jak znikają kolory. A jakby udało się jeden na drugi nawarstwić?
Użyłem wąskiej probówki. Roztwór nadmanganianu okazał się lżejszy. Nakraplajac na ściankę doprowadziłem do dwuwarstwowego układu. Obie warstwy reagowały ze sobą, stąd bezbarwna granica faz. Szerokość granicy wynika z szybkości dyfuzji obu substancji - koloru nie widać w obszarze o za niskim stężeniu form barwnych. Z kolei różnice dyfuzji i stężeń molowych w warstwach wpływają na przesuwanie się granicy - w tym przypadku różowa faza wygrywała a granicą przesuwała się do dołu.
Byłoby to więc dobre doświadczenie edukacyjne.
informacje
Pokazywanie postów oznaczonych etykietą barwniki syntetyczne. Pokaż wszystkie posty
Pokazywanie postów oznaczonych etykietą barwniki syntetyczne. Pokaż wszystkie posty
sobota, 28 września 2019
sobota, 11 maja 2019
Kolory karminu
Indygokarmin to barwnik, będący pochodną indygo, znanego szerzej jako niebieski pigment, którym farbowane są dżinsy, a o którym kiedyś już pisałem (link). Dwie grupy sulfonowe, będące resztami kwasu siarkowego, powodują w jego przypadku, że związek ten w odróżnieniu od wolnego indygo jest dość dobrze rozpuszczalny w wodzie, oraz reaguje na zmiany kwasowości. Przy pH bardzo zasadowym, powyżej 13, zmienia kolor na żółty, przy obojętnym lub kwaśnym jest niebieski, zaś przy lekko zasadowym obie formy pojawiają się w ramach równowagi, dając wypadkowy kolor zielony.
Jest często stosowanym barwnikiem spożywczym, można go też spotkać w niebieskich kapsułkach leków.
Inną ciekawą właściwością związku jest wyraźna reakcja na redukcję lub utlenienie, co znajduje zastosowanie w tym ciekawym i efektownym eksperymencie.
Przepis jest w zasadzie dość prosty - należy wziąć około 3% roztwór glukozy i 3% roztwór wodorotlenku sodu, połączyć je w szklanej butelce na ciepło, w temperaturze około 40 stopni, dodając taką ilość indygokarmiu, aby widać było wyraźny kolor. Początkowo roztwór będzie zielony, potem pociemnieje i poprzez czerwonawy odcień stanie się żółty. W tym momencie nie trzeba go już ogrzewać, dalej będzie reagował na zimno. Co takiego będzie się działo?
Jeśli zaczniemy wytrząsać napełnioną do połowy butelkę, roztwór zmieni kolor. Najpierw z żółtego zrobi się czerwony, a po dokładniejszym wytrząsaniu zielony. Odstawiony powraca do żółtego koloru w ciągu około minuty, po czym znów może być wytrząsany ze zmianami koloru, odstawiony aż powróci do żółtego i tak kilkanaście razy.
Ze względu na zestaw kolorów eksperyment znany jest jako "chemiczne światła drogowe".
Nagrałem jeden taki cykl bez cięć, aby było widać szybkość przemian:
W tle kolbka z roztworem indygokarminu w wodzie destylowanej.
Na czym właściwie polegają te przemiany? Glukoza jest związkiem o właściwościach redukujących, co zawdzięcza obecności grupy aldehydowej na jednym z końców. Indygokarmin zaś jest na redukcję wrażliwy. W alkalicznych warunkach cząsteczki glukozy w formie pierścienia otwierają się, i stają się aktywnymi reduktorami. Barwnik zaczyna reagować, przyłączając elektrony i protony. Ponieważ cząsteczka posiada dwa miejsca mogące ulegać redukcji, w trakcie reakcji pojawia się związek pośredni, ze zredukowaną tylko jedną grupą, który ma w roztworze kolor czerwony. Całkowite przereagowanie daje związek żółty, tak zwany leuko-indygokarmin.
Glukoza jest natomiast utleniana, przede wszystkim do kwasu glukuronowego. Podczas wytrząsania następuje proces odwrotny - tlen z powietrza reaguje z leuko-barwnikiem w ten sam sposób przez związek pośredni. Mamy tutaj więc dość ciekawy przypadek dwuetapowego procesu, w którym ustala się pewna równowaga między formami. Pośrednia forma czerwona stanowi w fazie, w której roztwór jest czerwony, niemal jedyną postać barwnika. Całkowicie zredukowana forma żółta może pojawiać się dopiero od momentu zaniku w roztworze niezredukowanej formy zielonej, w przeciwnym razie ich cząsteczki będą wymieniać między sobą elektrony i protony do pośredniej formy czerwonej. Od tego momentu potrzebna jest dostatecznie duża ilość reduktora, bo przy za małym jego stężeniu, w formę żółtą nie zmieni się zauważalna ilość substancji.
Co ciekawe, bezpośrednia reakcja glukozy z tlenem z powietrza jest dość powolna. Indygokarmin przez to, że chętnie reaguje zarówno z jednym jak i drugim, jest katalizatorem procesu.
Przy podanych stężeniach cykle można powtarzać kilkanaście razy, aż do wyczerpania któregoś ze składników - przy małej ilości roztworu w dużej butelce pierwsza wyczerpie się glukoza i przy zbyt małym jej stężeniu, równowaga procesu zostanie zaburzona, a pozostawiony sam sobie roztwór osiągnie tylko czerwony etap pośredni. W tym momencie nawet mały dodatek zasadowego roztworu glukozy wystarczy aby dokończyć proces, toteż taki niedoredukowany roztwór mógłby ją wykrywać (lub inne reduktory).
Sprawdziłem to dodając do takiego roztworu sok jabłkowy, kilka mililitrów zawierających cukry redukujące i zapewne kwas askorbinowy wystarczało w zupełności.
W odwrotnej sytuacji, gdy dużo roztworu umieścimy w małej butelce, z małą ilością powietrza, to tlen pierwszy się skończy. Wówczas żółty roztwór podczas wytrząsania stanie się najwyżej czerwony. Zdarzyło mi się tak z jedną z prób. Kolba zostawiona na noc, następnego dnia nie reagowała na wytrząsanie. Sądziłem, że widocznie składniki się już zużyły i chciałem wylać. Zauważyłem jednak, że zassał się koreczek. Po otwarciu kolby przedmuchałem ją więc i wytrząsnąłem. Zielony kolor powrócił.
Szybkość zmian kolorów zależy od stężeń glukozy i barwnika, oraz od temperatury. Na kanale Royal Society podano formułę, która w temperaturze roztworu około 45 stopni po wytrząśnięciu powraca do żółtego koloru w 10 sekund. Żółty roztwór z końcowym, zredukowanym związkiem, stanowi dość czuły odczynnik wykrywający tlen, wodę utlenioną lub nadtlenki, co wykorzystuje się nawet w badaniach biologicznych.
Przy podanych stężeniach roztwór jest na tyle mało szkodliwy, że po rozcieńczeniu wodą można go wylać do zlewu.
Co ciekawe, indygokarmin może też ulegać przeciwnej reakcji i ze stanu podstawowego może zostać utleniony. Powstaje wówczas żółte dehydroindygo, które rozpada się na sulfonowaną izatynę. Wykorzystuje się tę reakcję przy manganometrycznym oznaczaniu garbników, zanik koloru wskaźnika wyznacza moment, gdy polifenole z roztworu zostały już utlenione.
-----
* Beyond The Blue Bottle - Royal Society of Chemistry, YT
Jest często stosowanym barwnikiem spożywczym, można go też spotkać w niebieskich kapsułkach leków.
Inną ciekawą właściwością związku jest wyraźna reakcja na redukcję lub utlenienie, co znajduje zastosowanie w tym ciekawym i efektownym eksperymencie.
Przepis jest w zasadzie dość prosty - należy wziąć około 3% roztwór glukozy i 3% roztwór wodorotlenku sodu, połączyć je w szklanej butelce na ciepło, w temperaturze około 40 stopni, dodając taką ilość indygokarmiu, aby widać było wyraźny kolor. Początkowo roztwór będzie zielony, potem pociemnieje i poprzez czerwonawy odcień stanie się żółty. W tym momencie nie trzeba go już ogrzewać, dalej będzie reagował na zimno. Co takiego będzie się działo?
Jeśli zaczniemy wytrząsać napełnioną do połowy butelkę, roztwór zmieni kolor. Najpierw z żółtego zrobi się czerwony, a po dokładniejszym wytrząsaniu zielony. Odstawiony powraca do żółtego koloru w ciągu około minuty, po czym znów może być wytrząsany ze zmianami koloru, odstawiony aż powróci do żółtego i tak kilkanaście razy.
Ze względu na zestaw kolorów eksperyment znany jest jako "chemiczne światła drogowe".
Nagrałem jeden taki cykl bez cięć, aby było widać szybkość przemian:
W tle kolbka z roztworem indygokarminu w wodzie destylowanej.
Na czym właściwie polegają te przemiany? Glukoza jest związkiem o właściwościach redukujących, co zawdzięcza obecności grupy aldehydowej na jednym z końców. Indygokarmin zaś jest na redukcję wrażliwy. W alkalicznych warunkach cząsteczki glukozy w formie pierścienia otwierają się, i stają się aktywnymi reduktorami. Barwnik zaczyna reagować, przyłączając elektrony i protony. Ponieważ cząsteczka posiada dwa miejsca mogące ulegać redukcji, w trakcie reakcji pojawia się związek pośredni, ze zredukowaną tylko jedną grupą, który ma w roztworze kolor czerwony. Całkowite przereagowanie daje związek żółty, tak zwany leuko-indygokarmin.
Glukoza jest natomiast utleniana, przede wszystkim do kwasu glukuronowego. Podczas wytrząsania następuje proces odwrotny - tlen z powietrza reaguje z leuko-barwnikiem w ten sam sposób przez związek pośredni. Mamy tutaj więc dość ciekawy przypadek dwuetapowego procesu, w którym ustala się pewna równowaga między formami. Pośrednia forma czerwona stanowi w fazie, w której roztwór jest czerwony, niemal jedyną postać barwnika. Całkowicie zredukowana forma żółta może pojawiać się dopiero od momentu zaniku w roztworze niezredukowanej formy zielonej, w przeciwnym razie ich cząsteczki będą wymieniać między sobą elektrony i protony do pośredniej formy czerwonej. Od tego momentu potrzebna jest dostatecznie duża ilość reduktora, bo przy za małym jego stężeniu, w formę żółtą nie zmieni się zauważalna ilość substancji.
Co ciekawe, bezpośrednia reakcja glukozy z tlenem z powietrza jest dość powolna. Indygokarmin przez to, że chętnie reaguje zarówno z jednym jak i drugim, jest katalizatorem procesu.
Przy podanych stężeniach cykle można powtarzać kilkanaście razy, aż do wyczerpania któregoś ze składników - przy małej ilości roztworu w dużej butelce pierwsza wyczerpie się glukoza i przy zbyt małym jej stężeniu, równowaga procesu zostanie zaburzona, a pozostawiony sam sobie roztwór osiągnie tylko czerwony etap pośredni. W tym momencie nawet mały dodatek zasadowego roztworu glukozy wystarczy aby dokończyć proces, toteż taki niedoredukowany roztwór mógłby ją wykrywać (lub inne reduktory).
Sprawdziłem to dodając do takiego roztworu sok jabłkowy, kilka mililitrów zawierających cukry redukujące i zapewne kwas askorbinowy wystarczało w zupełności.
W odwrotnej sytuacji, gdy dużo roztworu umieścimy w małej butelce, z małą ilością powietrza, to tlen pierwszy się skończy. Wówczas żółty roztwór podczas wytrząsania stanie się najwyżej czerwony. Zdarzyło mi się tak z jedną z prób. Kolba zostawiona na noc, następnego dnia nie reagowała na wytrząsanie. Sądziłem, że widocznie składniki się już zużyły i chciałem wylać. Zauważyłem jednak, że zassał się koreczek. Po otwarciu kolby przedmuchałem ją więc i wytrząsnąłem. Zielony kolor powrócił.
Szybkość zmian kolorów zależy od stężeń glukozy i barwnika, oraz od temperatury. Na kanale Royal Society podano formułę, która w temperaturze roztworu około 45 stopni po wytrząśnięciu powraca do żółtego koloru w 10 sekund. Żółty roztwór z końcowym, zredukowanym związkiem, stanowi dość czuły odczynnik wykrywający tlen, wodę utlenioną lub nadtlenki, co wykorzystuje się nawet w badaniach biologicznych.
Przy podanych stężeniach roztwór jest na tyle mało szkodliwy, że po rozcieńczeniu wodą można go wylać do zlewu.
Co ciekawe, indygokarmin może też ulegać przeciwnej reakcji i ze stanu podstawowego może zostać utleniony. Powstaje wówczas żółte dehydroindygo, które rozpada się na sulfonowaną izatynę. Wykorzystuje się tę reakcję przy manganometrycznym oznaczaniu garbników, zanik koloru wskaźnika wyznacza moment, gdy polifenole z roztworu zostały już utlenione.
-----
* Beyond The Blue Bottle - Royal Society of Chemistry, YT
piątek, 19 maja 2017
Anegdoty o chemikach i kolorach
Niebieski
Gdy pies nasika chemikowi na ścianę...
Pittakall to prawdopodobnie pierwszy syntetyczny barwnik organiczny*, jaki pojawił się w handlu, choć nie zdobył zbyt dużej popularności i dość szybko zarzucono jego produkcję. Jego przypadkowym odkrywcą był niemiecki chemik Karl Reichenbach. Na początku XIX wieku zarządzając małą fabryką chemiczną zajął się badaniem produktów suchej destylacji drewna, węgla i szczątków organicznych. To on wydzielił ze smoły różne wartościowe frakcje, w tym kreozot, parafinę czy fenol, a także pierwszy olej opałowy nazwany eupinonem.
Kreozot, będący frakcją smoły z drewna drzew liściastych, miał dość charakterystyczną, silną woń oraz dobre właściwości konserwujące, dlatego chemik zaczął stosować go do impregnowania drewna. Do dziś zresztą jest częstym składnikiem impregnatów, na przykład do podkładów kolejowych.
Postanowił wypróbować go także w zastosowaniu dużo bardziej przyziemnym - przeszkadzało mu, że psy sikają mu zewnętrzną ścianę domu, więc posmarował ją kreozotem aby zapach je odstraszał. Psom najwyraźniej było wszystko jedno, bardzo lubiły tam stawać i podnosić nogę, lejąc bezczelnie po wysmarowanej ścianie. Cóż, widocznie nie było to dobry środek na psy.
Przyglądając się ich działalności zauważył jednak ciekawą rzecz - w miejscu gdzie stały plamy moczu, na ziemi pojawiło się wyraźne, niebieskie zabarwienie. A ponieważ był człowiekiem bardzo praktycznym, zaczął czynić próby powtórzenia reakcji. Szybko wykrył, że mocz nie jest w jej potrzebny, stanowił jedynie alkaliczny reagent. Prowadząc destylację surowej smoły stwierdził, że frakcja o temperaturze wrzenia wyższej niż kreozot, po wprowadzeniu do wody wapiennej lub roztworu wodorotlenku baru, po pewnym czasie zamienia się w ciemnogranatowy proszek.
Wprowadził go na rynek jako pigment nadający się do farbowania po rozpuszczeniu w alkaliach. Najwyraźniej jednak nie miał zbyt dobrych właściwości i po pewnym czasie przestał być używany, pojawiając się jedynie od czasu do czasu w historycznych spisach barwników. Dopiero pod koniec XIX wieku ustalono, że jest to związek będący produktem kondensacji pirogallolu, o strukturze podobnej do barwników trifenylometylenowych. W formie anionowej przybierał intensywny kolor. Pigment Reichenbacha był laką, to jest nierozpuszczalną solą barową lub wapniową.
Pittakall jest dziś w zasadzie historyczną ciekawostką. Mam wrażenie, że od ponad stu lat nikt go nie otrzymywał, bo poza wzmiankami w pracach o historii barwników nie znalazłem o nim żadnej dalszej informacji ani tym bardziej zdjęcia próbki. Ponoć miał dość ciemny odcień niebieskiego.[1]
Ftalocyjanina
Kolejny niebieski barwnik także został odkryty niezamierzenie, podczas otrzymywania czegoś innego, i to dwa razy.
W 1927 roku szwajcarscy chemicy Henri Diesbach i Edmond von de Weid zajmowali się znalezieniem lepszej niż już znane metody otrzymywania ftalonitrylu, to jest pochodnej benzenu z dwiema grupami -CN. Znana była już w tym czasie reakcja Sandmeyera, polegająca na podstawieniu soli diazoniowych, gdzie grupa -NN była łatwo zamieniana na inne. Przy jej pomocy otrzymywano ftalonitryl z o-aminobenzonitrylu (a ten z rozkładu termicznego amidu kwasu antranilowego).
Badacze postanowili spróbować nieco innej metody, której substrat był bardziej stabilny i łatwiejszy w otrzymaniu. Była to reakcja Rosenmunda-von Brauna (nie mylić z reakcją Rosenmunda samego, czyli redukcją kwasów do aldehydów) polegająca na podstawieniu halogenku przy pierścieniu aromatycznym, przez anion cyjankowy z cyjanku miedzi.[2]
Jako substratu użyli 1,2-dibromobenzenu. Pomysł był w istocie dosyć prosty, reakcja powinna przebiegać w taki oto sposób:
Produktem powinna być bezbarwna lub nieco żółtawa krystaliczna substancja. Jakież więc było zdziwienie chemików, gdy po reakcji znaleźli w kolbie osad intensywnie niebieski.
Produkt był bardzo trwały, nierozpuszczalny w wodzie i dość trudno w innych rozpuszczalnikach. Po wyznaczeniu przez analizę elementarną składu C26H18N6Cu uznali, że prawdopodobnie mają do czynienia ze związkiem kompleksowym ftalonitrylu i pirydyny, zawierającym jeden atom miedzi i po dwie cząsteczki tych związków [3]. Ale mylili się.
Drugimi odkrywcami byli chemicy w fabryce Scottish Dyes (dziś ICI), którzy w 1928 roku analizowali metodę przemysłowego otrzymywania ftalimidu. Bezwodnik ftalowy był w tej syntezie poddawany reakcji z amoniakiem w stężonym roztworze wodnym, zaś jako reaktorów używano emaliowanych żeliwnych kotłów. Mechaniczne mieszadło powodowało, że emalia z czasem się zdzierała, zaś pilnujący procesu technolodzy zauważyli, że partie produktu z tych najbardziej wytartych kotłów były zanieczyszczone drobnym, niebieskawym osadem. Było zresztą zauważalne, że na niebieskawy kolor zabarwił się odsłonięty metal.
Po zebraniu większej ilości zanieczyszczenia, pracownicy fabryki zdali sobie sprawę z tego, że potencjalnie mógłby to być niezły pigment, miał bowiem niską rozpuszczalność i bardzo dużą siłę barwiącą. Kolejną więc syntezę przeprowadzono dodając do masy wiórki żelazne, był to jednak proces mało wydajny. Należało odpowiedzieć na pytanie, co właściwie zachodzi w reaktorze i jaki związek otrzymano.
Po wpływem silnych alkaliów związek tracił metal, powstała wolna forma nadal była niebieska ale o dużo słabszym odcieniu. Można było połączyć ją z innymi metalami, zwłaszcza ze szczególnie chętnie wiązaną miedzią, tworząc kompleksy bardzo trwałe i intensywnie zabarwione. Analizy pokazały, że związek ma charakter aromatyczny i być może zawiera układ skumulowanych pierścieni. Dopiero w 1933 roku Patrick Linstead zaproponował dla związku budowę makrocykliczną, podobną do porfiryny, z czterema fragmentami benzopirolu połączonymi przez mostkowe azoty, co potwierdziły potem badania rentgenowskie.
Firma ICI zaczęła produkować pigment w 1934 roku po udoskonaleniu metod pod nazwą Monastral Blue, lub błękit ftalocyjaninowy. Był wielkim osiągnięciem. Niebieskich pigmentów było w tym czasie niewiele, w zasadzie istniały tylko nieorganiczne oparte o sole miedzi i ultramarynę, oraz indygo i jego pochodne. Błękit ftalocyjaninowy miał tą zaletę, że będąc barwnikiem organicznym posiadał wysoką odporność na blaknięcie, miał dużą siłę barwiącą, był na tyle słabo rozpuszczalny że nie migrował do innych warstw malarskich, oraz był dosyć odporny na czynniki fizyczne i chemiczne. Związek ten rozkłada się dopiero w temperaturze 600 stopni.
Do dziś jest jednym z najczęściej wykorzystywanych barwników, zwłaszcza do farb do metalu, ale też atramentów czy tuszu do długopisów. Jest na przykład składnikiem standardowego tuszu niebieskiego do drukarek, a ze względu na znikomą toksyczność także pigmentów do tatuażu.
Niezamierzony niebieski pigment
To odkrycie także miało pewien element przypadkowości.
Zespół profesora Subramaniana, na uniwersytecie stanowym w Oregonie, zajmował się badaniami tlenkowych materiałów ceramicznych z solami ziem rzadkich, które mogłyby potencjalnie znaleźć zastosowanie w elektronice. Niektóre mogłyby okazać się magnesami stałymi, inne nadprzewodnikami niskotemperaturowymi, ferroelektrykami czy superopornikami. Studenci profesora biorący udział w pracach testowali więc różne mieszanki tlenków i chlorków metali, które po wymieszaniu w młynie kulowym na bardzo drobny proszek wypalano w odpowiedniej temperaturze.
Doktorant Andrew E. Smith spróbował pewnego razu nietypowej mieszanki tlenku itru, indu i manganu VI. Dwutlenek manganu jest intensywnie czarny, dlatego po zmieleniu uzyskał ciemnoszary proszek. Następnie wsadził go na chwilkę do pieca aby się wygrzał. Temperatura szybko osiągnęła prawie 1100 stopni, a tlenki przereagowały ze sobą, tworząc nowe połączenie. Akurat to konkretne nie miało szczególnie ciekawych własności elektrycznych czy magnetycznych, lecz jedna właściwość rzucała się w oczy od razu po wyjęciu z pieca - otrzymany proszek okazał się niesamowicie niebieski.[4]
Gdy profesor zobaczył próbkę od razu przyszło mu do głowy, że to może znaleźć zastosowanie. Właściwie jeszcze przed publikacją na temat związku zaczęto starania nad komercjalizacją.
Jak się okazało podczas wyprażania powstaje związek zawierający warstwy tlenku manganu o nietypowej koordynacji w formie bipiramidy trygonalnej. W każdej takiej jednostce atom manganu otoczony jest przez pięć atomów tlenu, w tym trzy w płaszczyźnie warstwy i po jednym nad i pod nią. W takim położeniu oddziaływanie ligandów powoduje rozszczepienie poziomów energetycznych orbitali d manganu w taki sposób, że związek pochłania światło czerwone i zielone dając w efekcie niebieski kolor.
Wcześniej znany był pigment oparty o manganian baru, ale miał małą stabilność, nowy pigment nazwany YInMn nie tylko jest odporny na utlenienie czy redukcję, ale też zachowuje kolor w bardzo wysokich temperaturach i nie blaknie pod wpływem wilgoci. Szybko okazało się, że dobrze nadaje się zarówno do farb olejowych jak i wodnych, a także jako pigment do barwienia mas plastycznych. W tych zastosowaniach ważną własnością jest też jego nietoksyczność. Inne pigmenty nieorganiczne podobnej trwałości zwykle zawierają sole rakotwórczego kobaltu lub sole miedzi.
Podczas dalszych badań stwierdzono, że choć związek silnie pochłania światło czerwone, to zarazem silnie odbija podczerwień, osiągając jeden z najwyższych współczynników odbicia dla materiałów niemetalicznych (srebro odbija niemal 100% podczerwieni). Dzięki temu powierzchnie pomalowane farbą z tym pigmentem bardzo mało się nagrzewają, co miałoby znaczenie w przypadku na przykład dachów w cieplejszych krajach
Obecnie pigment zaczyna powoli wchodzić na rynek, niedawno producent kredek świecowych i pasteli Crayola ogłosił wprowadzenie kredki z YInMn, trwa konkurs na wymyślenie nazwy [5].
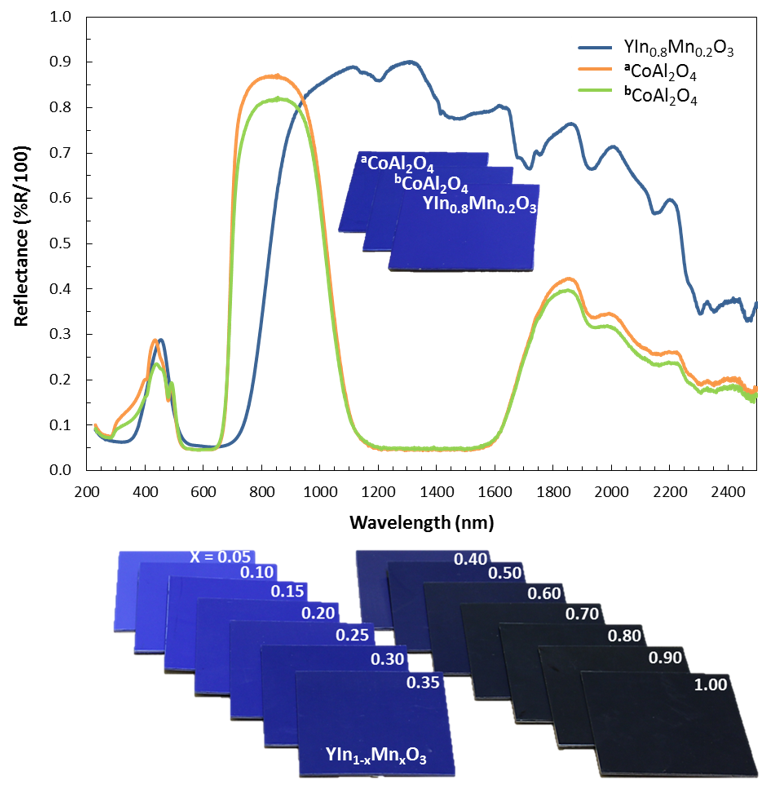
Jednak wbrew temu co piszą media, pigment nie posiada nowego, dopiero teraz odkrytego odcienia niebieskiego. W najbardziej optymalnym składzie YIn0.8Mn0.2O3 , związek ma kolor błękitu kobaltowego lub nieco cieplejszy, mimo zupełnie różnego przebiegu krzywej absorpcji:
Odcień może płynnie zmieniać się w zależności od stosunku itru do manganu. Dodatek innych metali, na przykład tytanu czy cynku może natomiast zmienić kolor na zielony lub fioletowy.[6]
W zespole prof. Subramaniana trwają prace nad uzyskaniem pigmentu czerwonego o odcieniu i intensywności nie stosowanych dziś z powodu toksyczności pigmentów rtęciowych jak cynober.
Może jeszcze kiedyś napiszę coś o projektowaniu barwników aby pokazać, jak takie rzeczy otrzymuje się planowo, bez czekania na szczęśliwy przypadek.
-------
* Aczkolwiek wcześniej niż Pittakall bo w XVIII wieku stworzono kwas pikrynowy, przez pewien czas używany do farbowania wełny, zastosowanie jako barwnik znalazł jednak dużo później. Półsyntetyczny był natomiast otrzymany w podobnym czasie indygokarmin, znany jako błękit saksoński, pozyskiwany przez traktowanie indygo dymiącym kwasem siarkowym.
[1] George B. Kauffman, Pittacal - The first synthetic dyestuff, Journal of Chemical Education (12) 1977 str. 753
[2] Sandmeyer-von Braun reaction
[3] De Diesbach, Henri; von Der Weid, Edmond (1927). "Quelques sels complexes des o-dinitriles avec le cuivre et la pyridine". Helvetica Chimica Acta. 10: 886.
[4] http://oregonstate.edu/ua/ncs/archives/2009/nov/accidental-discovery-produces-durable-new-blue-pigment-multiple-applications-0
[5] http://oregonstate.edu/ua/ncs/archives/2017/may/pigment-discovered-oregon-state-university-inspires-new-crayola-crayon-color
[6] http://chemistry.oregonstate.edu/content/story-yinmn-blue
Gdy pies nasika chemikowi na ścianę...
Pittakall to prawdopodobnie pierwszy syntetyczny barwnik organiczny*, jaki pojawił się w handlu, choć nie zdobył zbyt dużej popularności i dość szybko zarzucono jego produkcję. Jego przypadkowym odkrywcą był niemiecki chemik Karl Reichenbach. Na początku XIX wieku zarządzając małą fabryką chemiczną zajął się badaniem produktów suchej destylacji drewna, węgla i szczątków organicznych. To on wydzielił ze smoły różne wartościowe frakcje, w tym kreozot, parafinę czy fenol, a także pierwszy olej opałowy nazwany eupinonem.
Kreozot, będący frakcją smoły z drewna drzew liściastych, miał dość charakterystyczną, silną woń oraz dobre właściwości konserwujące, dlatego chemik zaczął stosować go do impregnowania drewna. Do dziś zresztą jest częstym składnikiem impregnatów, na przykład do podkładów kolejowych.
Postanowił wypróbować go także w zastosowaniu dużo bardziej przyziemnym - przeszkadzało mu, że psy sikają mu zewnętrzną ścianę domu, więc posmarował ją kreozotem aby zapach je odstraszał. Psom najwyraźniej było wszystko jedno, bardzo lubiły tam stawać i podnosić nogę, lejąc bezczelnie po wysmarowanej ścianie. Cóż, widocznie nie było to dobry środek na psy.
Przyglądając się ich działalności zauważył jednak ciekawą rzecz - w miejscu gdzie stały plamy moczu, na ziemi pojawiło się wyraźne, niebieskie zabarwienie. A ponieważ był człowiekiem bardzo praktycznym, zaczął czynić próby powtórzenia reakcji. Szybko wykrył, że mocz nie jest w jej potrzebny, stanowił jedynie alkaliczny reagent. Prowadząc destylację surowej smoły stwierdził, że frakcja o temperaturze wrzenia wyższej niż kreozot, po wprowadzeniu do wody wapiennej lub roztworu wodorotlenku baru, po pewnym czasie zamienia się w ciemnogranatowy proszek.
Wprowadził go na rynek jako pigment nadający się do farbowania po rozpuszczeniu w alkaliach. Najwyraźniej jednak nie miał zbyt dobrych właściwości i po pewnym czasie przestał być używany, pojawiając się jedynie od czasu do czasu w historycznych spisach barwników. Dopiero pod koniec XIX wieku ustalono, że jest to związek będący produktem kondensacji pirogallolu, o strukturze podobnej do barwników trifenylometylenowych. W formie anionowej przybierał intensywny kolor. Pigment Reichenbacha był laką, to jest nierozpuszczalną solą barową lub wapniową.
Pittakall jest dziś w zasadzie historyczną ciekawostką. Mam wrażenie, że od ponad stu lat nikt go nie otrzymywał, bo poza wzmiankami w pracach o historii barwników nie znalazłem o nim żadnej dalszej informacji ani tym bardziej zdjęcia próbki. Ponoć miał dość ciemny odcień niebieskiego.[1]
Ftalocyjanina
Kolejny niebieski barwnik także został odkryty niezamierzenie, podczas otrzymywania czegoś innego, i to dwa razy.
W 1927 roku szwajcarscy chemicy Henri Diesbach i Edmond von de Weid zajmowali się znalezieniem lepszej niż już znane metody otrzymywania ftalonitrylu, to jest pochodnej benzenu z dwiema grupami -CN. Znana była już w tym czasie reakcja Sandmeyera, polegająca na podstawieniu soli diazoniowych, gdzie grupa -NN była łatwo zamieniana na inne. Przy jej pomocy otrzymywano ftalonitryl z o-aminobenzonitrylu (a ten z rozkładu termicznego amidu kwasu antranilowego).
Badacze postanowili spróbować nieco innej metody, której substrat był bardziej stabilny i łatwiejszy w otrzymaniu. Była to reakcja Rosenmunda-von Brauna (nie mylić z reakcją Rosenmunda samego, czyli redukcją kwasów do aldehydów) polegająca na podstawieniu halogenku przy pierścieniu aromatycznym, przez anion cyjankowy z cyjanku miedzi.[2]
Jako substratu użyli 1,2-dibromobenzenu. Pomysł był w istocie dosyć prosty, reakcja powinna przebiegać w taki oto sposób:
Produktem powinna być bezbarwna lub nieco żółtawa krystaliczna substancja. Jakież więc było zdziwienie chemików, gdy po reakcji znaleźli w kolbie osad intensywnie niebieski.
Produkt był bardzo trwały, nierozpuszczalny w wodzie i dość trudno w innych rozpuszczalnikach. Po wyznaczeniu przez analizę elementarną składu C26H18N6Cu uznali, że prawdopodobnie mają do czynienia ze związkiem kompleksowym ftalonitrylu i pirydyny, zawierającym jeden atom miedzi i po dwie cząsteczki tych związków [3]. Ale mylili się.
Drugimi odkrywcami byli chemicy w fabryce Scottish Dyes (dziś ICI), którzy w 1928 roku analizowali metodę przemysłowego otrzymywania ftalimidu. Bezwodnik ftalowy był w tej syntezie poddawany reakcji z amoniakiem w stężonym roztworze wodnym, zaś jako reaktorów używano emaliowanych żeliwnych kotłów. Mechaniczne mieszadło powodowało, że emalia z czasem się zdzierała, zaś pilnujący procesu technolodzy zauważyli, że partie produktu z tych najbardziej wytartych kotłów były zanieczyszczone drobnym, niebieskawym osadem. Było zresztą zauważalne, że na niebieskawy kolor zabarwił się odsłonięty metal.
Po zebraniu większej ilości zanieczyszczenia, pracownicy fabryki zdali sobie sprawę z tego, że potencjalnie mógłby to być niezły pigment, miał bowiem niską rozpuszczalność i bardzo dużą siłę barwiącą. Kolejną więc syntezę przeprowadzono dodając do masy wiórki żelazne, był to jednak proces mało wydajny. Należało odpowiedzieć na pytanie, co właściwie zachodzi w reaktorze i jaki związek otrzymano.
Po wpływem silnych alkaliów związek tracił metal, powstała wolna forma nadal była niebieska ale o dużo słabszym odcieniu. Można było połączyć ją z innymi metalami, zwłaszcza ze szczególnie chętnie wiązaną miedzią, tworząc kompleksy bardzo trwałe i intensywnie zabarwione. Analizy pokazały, że związek ma charakter aromatyczny i być może zawiera układ skumulowanych pierścieni. Dopiero w 1933 roku Patrick Linstead zaproponował dla związku budowę makrocykliczną, podobną do porfiryny, z czterema fragmentami benzopirolu połączonymi przez mostkowe azoty, co potwierdziły potem badania rentgenowskie.
Firma ICI zaczęła produkować pigment w 1934 roku po udoskonaleniu metod pod nazwą Monastral Blue, lub błękit ftalocyjaninowy. Był wielkim osiągnięciem. Niebieskich pigmentów było w tym czasie niewiele, w zasadzie istniały tylko nieorganiczne oparte o sole miedzi i ultramarynę, oraz indygo i jego pochodne. Błękit ftalocyjaninowy miał tą zaletę, że będąc barwnikiem organicznym posiadał wysoką odporność na blaknięcie, miał dużą siłę barwiącą, był na tyle słabo rozpuszczalny że nie migrował do innych warstw malarskich, oraz był dosyć odporny na czynniki fizyczne i chemiczne. Związek ten rozkłada się dopiero w temperaturze 600 stopni.
Do dziś jest jednym z najczęściej wykorzystywanych barwników, zwłaszcza do farb do metalu, ale też atramentów czy tuszu do długopisów. Jest na przykład składnikiem standardowego tuszu niebieskiego do drukarek, a ze względu na znikomą toksyczność także pigmentów do tatuażu.
Niezamierzony niebieski pigment
To odkrycie także miało pewien element przypadkowości.
Zespół profesora Subramaniana, na uniwersytecie stanowym w Oregonie, zajmował się badaniami tlenkowych materiałów ceramicznych z solami ziem rzadkich, które mogłyby potencjalnie znaleźć zastosowanie w elektronice. Niektóre mogłyby okazać się magnesami stałymi, inne nadprzewodnikami niskotemperaturowymi, ferroelektrykami czy superopornikami. Studenci profesora biorący udział w pracach testowali więc różne mieszanki tlenków i chlorków metali, które po wymieszaniu w młynie kulowym na bardzo drobny proszek wypalano w odpowiedniej temperaturze.
Doktorant Andrew E. Smith spróbował pewnego razu nietypowej mieszanki tlenku itru, indu i manganu VI. Dwutlenek manganu jest intensywnie czarny, dlatego po zmieleniu uzyskał ciemnoszary proszek. Następnie wsadził go na chwilkę do pieca aby się wygrzał. Temperatura szybko osiągnęła prawie 1100 stopni, a tlenki przereagowały ze sobą, tworząc nowe połączenie. Akurat to konkretne nie miało szczególnie ciekawych własności elektrycznych czy magnetycznych, lecz jedna właściwość rzucała się w oczy od razu po wyjęciu z pieca - otrzymany proszek okazał się niesamowicie niebieski.[4]
Gdy profesor zobaczył próbkę od razu przyszło mu do głowy, że to może znaleźć zastosowanie. Właściwie jeszcze przed publikacją na temat związku zaczęto starania nad komercjalizacją.
Jak się okazało podczas wyprażania powstaje związek zawierający warstwy tlenku manganu o nietypowej koordynacji w formie bipiramidy trygonalnej. W każdej takiej jednostce atom manganu otoczony jest przez pięć atomów tlenu, w tym trzy w płaszczyźnie warstwy i po jednym nad i pod nią. W takim położeniu oddziaływanie ligandów powoduje rozszczepienie poziomów energetycznych orbitali d manganu w taki sposób, że związek pochłania światło czerwone i zielone dając w efekcie niebieski kolor.
Wcześniej znany był pigment oparty o manganian baru, ale miał małą stabilność, nowy pigment nazwany YInMn nie tylko jest odporny na utlenienie czy redukcję, ale też zachowuje kolor w bardzo wysokich temperaturach i nie blaknie pod wpływem wilgoci. Szybko okazało się, że dobrze nadaje się zarówno do farb olejowych jak i wodnych, a także jako pigment do barwienia mas plastycznych. W tych zastosowaniach ważną własnością jest też jego nietoksyczność. Inne pigmenty nieorganiczne podobnej trwałości zwykle zawierają sole rakotwórczego kobaltu lub sole miedzi.
Podczas dalszych badań stwierdzono, że choć związek silnie pochłania światło czerwone, to zarazem silnie odbija podczerwień, osiągając jeden z najwyższych współczynników odbicia dla materiałów niemetalicznych (srebro odbija niemal 100% podczerwieni). Dzięki temu powierzchnie pomalowane farbą z tym pigmentem bardzo mało się nagrzewają, co miałoby znaczenie w przypadku na przykład dachów w cieplejszych krajach
Obecnie pigment zaczyna powoli wchodzić na rynek, niedawno producent kredek świecowych i pasteli Crayola ogłosił wprowadzenie kredki z YInMn, trwa konkurs na wymyślenie nazwy [5].
Jednak wbrew temu co piszą media, pigment nie posiada nowego, dopiero teraz odkrytego odcienia niebieskiego. W najbardziej optymalnym składzie YIn0.8Mn0.2O3 , związek ma kolor błękitu kobaltowego lub nieco cieplejszy, mimo zupełnie różnego przebiegu krzywej absorpcji:
Odcień może płynnie zmieniać się w zależności od stosunku itru do manganu. Dodatek innych metali, na przykład tytanu czy cynku może natomiast zmienić kolor na zielony lub fioletowy.[6]
W zespole prof. Subramaniana trwają prace nad uzyskaniem pigmentu czerwonego o odcieniu i intensywności nie stosowanych dziś z powodu toksyczności pigmentów rtęciowych jak cynober.
Może jeszcze kiedyś napiszę coś o projektowaniu barwników aby pokazać, jak takie rzeczy otrzymuje się planowo, bez czekania na szczęśliwy przypadek.
-------
* Aczkolwiek wcześniej niż Pittakall bo w XVIII wieku stworzono kwas pikrynowy, przez pewien czas używany do farbowania wełny, zastosowanie jako barwnik znalazł jednak dużo później. Półsyntetyczny był natomiast otrzymany w podobnym czasie indygokarmin, znany jako błękit saksoński, pozyskiwany przez traktowanie indygo dymiącym kwasem siarkowym.
[1] George B. Kauffman, Pittacal - The first synthetic dyestuff, Journal of Chemical Education (12) 1977 str. 753
[2] Sandmeyer-von Braun reaction
[3] De Diesbach, Henri; von Der Weid, Edmond (1927). "Quelques sels complexes des o-dinitriles avec le cuivre et la pyridine". Helvetica Chimica Acta. 10: 886.
[4] http://oregonstate.edu/ua/ncs/archives/2009/nov/accidental-discovery-produces-durable-new-blue-pigment-multiple-applications-0
[5] http://oregonstate.edu/ua/ncs/archives/2017/may/pigment-discovered-oregon-state-university-inspires-new-crayola-crayon-color
[6] http://chemistry.oregonstate.edu/content/story-yinmn-blue
piątek, 22 kwietnia 2016
Reakcja nie całkiem charakterystyczna
Czyli dłuższa anegdota o odkryciu pewnego związku.
Wraz z rozwojem przemysłu w XIX wiecznej Europie, w tym maszyn parowych i pieców hutniczych, duże znaczenie jako paliwo zaczął odgrywać węgiel kamienny. Dla pewnych zastosowań korzystniejszym niż surowe paliwem był koks, otrzymany przez ogrzewanie węgla bez dostępu powietrza tak, że ulatywała zeń woda i lotnie związki. Koks, o wyższej wartości opałowej, zużywano głównie do wytopu stali; gazy palne zużywano do oświetlania ulic w latarniach i jako gaz do kuchenek; wykraplana woda pogazowa zawierająca amoniak była zużywana do produkcji nawozów sztucznych.
Jedynym produktem ubocznym jaki nie dawał się wprost zastosować była smoła pogazowa, często po prostu wylewana albo po oddzieleniu najbardziej lotnych składników używana do impregnacji drewna. Szybko zainteresowali się nią chemicy świadomi, że jest mieszanką wielu interesujących substancji. Stwierdzili oni na przykład, że przez destylację surowej smoły można otrzymać frakcje o rozmaitych właściwościach. Z jednych odzyskiwano naftalen, z innych dawało się wyprodukować fenol, zaś najlżejsza i niskowrząca frakcja dawała się zastosować jako rozpuszczalnik i olej oświetleniowy. Frakcja ta stanowiła też zresztą uciążliwe zanieczyszczenie gazu koksowniczego używanego do oświetlenia, zauważalne zwłaszcza gdy doprowadzany gaz był jeszcze ciepły. Wykraplała się na chłodnych kloszach latarń i przemieszana z sadzą zbierała na dnie.
Tam też na lepkie zanieczyszczenie zwrócił uwagę w 1825 roku Michael Faraday, który będąc bardzo praktycznym człowiekiem podjął się jej destylacji, chcąc otrzymać palny olej. Przydatnym produktem okazała się jedna z frakcji, o temperaturze wrzenia 80°C. Była to rzadka, lekko żółtawa ciecz spalająca się bardzo kopcącym płomieniem i będąca dobrym rozpuszczalnikiem. W następnych dekadach nauczono się wyodrębniać ją na duża skalę ze smoły pogazowej, a ze względu na obfite występowanie w benzolu, cieczy absorbowanej z gazu koksowniczego na stałych pochłaniaczach, nazwano ją benzenem.
Benzen odegrał dużą rolę w rozwoju chemii organicznej. To od niego pewną grupę niereaktywnych związków, często posiadających charakterystyczny zapach, nazwano związkami aromatycznymi. W tym wczesnym okresie duży problem sprawiało chemikom określenie jego struktury cząsteczkowej. Całkiem niedawno przyjęło się uważać, że pierwiastki składają się z atomów, a związki ze złożeń tych atomów w drobne całostki, nazwane cząsteczkami, o określonej budowie i układzie połączonych atomów. Jedyną informację o przypuszczalnym składzie cząsteczki stanowiły stosunki ilościowe pierwiastków składowych. Wiedząc w jakich ilościach łączą się ze sobą atomy, należało domyśleć się jaką prawdopodobnie tworzyły ze sobą strukturę.
Chemikiem który włożył w tą dziedzinę najwięcej, był opisywany już tutaj August Friedrich Kekule. On to po raz pierwszy na podstawie swych badań ustalił, że węgiel w związkach organicznych łączy się z maksymalnie czterema innymi atomami. W późniejszym okresie zastanawiając się jak połączyć ze sobą budulcowe atomy, doszedł do wniosku, że atomy węgla w bardziej skomplikowanych związkach muszą łączyć się tworząc łańcuchy. Wedle opowiadanej przezeń po latach anegdoty, myśl tą podsunął mu sen w którym dostrzegł tańczące atomy, które w pewnym momencie zaczęły się bawić w lokomotywę.
Pomysł ten nie dawał się jednak zastosować do niektórych związków, czego przykładem był benzen, złożony z węgla i wodoru w stosunku 1:1, i zawierający najwyraźniej sześć węgli. Rozwiązanie podsunął mu kolejny sen, w którym tańczące atomy utworzyły węża, a ten w pewnym momencie uchwycił swój ogon i w takiej formie wirował mu przed oczami. No tak - załóżmy że atomy są połączone w pierścień i mają wolną możliwość przyłączenia jeszcze tylko po jednym, a skład będzie się zgadzał.
Po upływie kolejnych lat chemicy coraz śmielej poczynali sobie z tworzeniem nowych pochodnych tego związku, aż w roku 1879 słynny chemik Bayer, założyciel zakładu produkującego między innymi Aspirynę, zauważył bardzo specyficzną reakcję - gdy wytrząsnął benzen ze stężonym kwasem siarkowym i dodał izatyny, żółtopomarańczowej substancji otrzymywanej z indygo, powstawało wyraźne niebieskie zabarwienie, zauważalne nawet przy niewielkich ilościach substancji. Wyglądało zatem na to, że odkryto prostą i szybką reakcję charakterystyczną, pozwalającą wykrywać benzen.
Odkrycie szybko zostało uznane i niektórzy postępowi profesorowie chemii zaczęli uczyć o tej reakcji na uniwersytetach. Jednym z nich był profesor Wiliam Weith wykładający chemię na uniwersytecie w Zurychu. Miał on specjalny lektorat poświęcony związkom aromatycznym, podczas którego pokazywał najbardziej charakterystyczne reakcje. Niestety na początku 1882 roku zmarł, toteż zajęciami podczas wiosennego semestru zajął się jego bliski przyjaciel Viktor Meyer.
Gdy przygotowywał się do zajęć polecił swojemu asystentowi aby przygotował mu próbkę benzenu. Tylko miał być czysty, tak aby pokaz poszedł bez problemów.
W dniu wykładu asystent dostarczył odpowiednią ilość związku. Meyer omówił historię i strukturę benzenu, po czym przeszedł do omawiania reakcji. Można wyobrazić sobie jak mówi studentom, że gdy teraz wytrząsie benzen ze stężonym kwasem i doda izatyny, to zobaczymy piękny niebieski kolor. Następnie tak jak mówił wytrząsa w próbówce benzen i stężony kwas, dodaje izatynę i... nic się nie dzieje. Powtarza reakcję, bo może coś akurat źle zrobił, ale nic nie pomaga. No cóż, tak się czasem zdarza, powtórzymy na następnych zajęciach.
Po skończonym wykładzie zwrócił się zatem do asystenta z delikatnym zapytaniem, co on u licha mu na te zajęcia przygotował. Bo jeśli nie szyny i nie izatyna, to benzen był zły. Asystent, znany później Traugott Sandmeyer bronił się że ależ skąd, przygotował benzen czysty, jak profesor chciał, wszystko wedle przepisu z dekarboksylacji kwasu benzoesowego bo tylko wtedy dawało się otrzymać zupełnie czysty. To już było zastanawiające. Jeszcze tego samego dnia Meyer wziął komercyjnie dostępny benzen otrzymywany z powęglowego benzolu, wytrząsnął z kwasem, dodał izatyny i otrzymał zgodnie z opisem Bayera piękny niebieski barwnik, znany jako indofenina.
Nie wiedząc co z tym faktem począć, wziął większą ilość komercyjnego benzenu, wytrząsnął z kwasem, oddzieloną warstwę kwasową zobojętnił stwierdzając, że wydzieliła mu się rzadka, lekko żółtawa ciecz o charakterystycznym zapachu, która wydawała się identyczna z benzenem. Meyer sądził zatem, że benzen występuje w dwóch formach, jednej mało aktywnej i drugiej "zaktywizowanej" i wchodzącej w reakcję barwną. Powtórzenie reakcji z otrzymaną cieczą pozwoliło mu na wytworzenie większej ilości niebieskiego barwnika, który wysłał do zbadania Bayerowi. Ten orzekł, że faktycznie jest to indofenina, ale zarazem w analizie elementarnej wyszło mu, że związek zawiera siarkę, której nie było w izatynie. Dalsze testy "aktywizowanego benzenu" pokazały, że musi być to substancja różna od benzenu. W odróżnieniu od niego nie krystalizowała w lodzie, i wrzała w temperaturze 84 stopni, w porównaniu z 80 stopni dla benzenu zupełnie czystego. Wreszcie analiza chemiczna wykazała, że jest to związek zawierający jeden atom siarki, cztery atomy węgla i cztery wodoru.
I tak Meyer odkrył Tiofen.
Odkrycie tiofenu zelektryzowało ówczesnych chemików. Okazało się że przez kilka dekad nie zauważyli, że benzen ze smoły węglowej jest mieszanką dwóch związków, przy czym ten drugi, tiofen, stanowił w niektórych partiach do 10%
Tiofen należy do grupy pięciokątnych związków aromatycznych, w których aromatyczność nadaje im zdelokalizowany układ sześciu elektronów - dwóch pochodzących z wiązań podwójnych na części węglowej i jednej wolnej pary pożyczonej z heteroatomu. Pełnowęglowy odpowiednik czyli cyklopentadien nie jest aromatyczny, a dodatkowo efekty antyaromatyczne tylko zmniejszają jego trwałość. Dążąc do utrwalenia chętnie odszczepia jeden wodór tworząc karboanion cyklopentadienylowy który już jest aromatyczny.
Podstawienie jednego węgla w tym układzie heteroatomem posiadającym wolną parę elektronową tworzy aromatyczną cząsteczkę obojętną. Gdy tym atomem jest tlen, otrzymujemy furan, gdy azot jest to pirol. Udało się także otrzymać analogiczne cząsteczki z niektórymi metalami i półmetalami, takie jak silol z krzemem, arsol z arsenem, stannol z cyną a nawet tytanol z tytanem. Zachowują one częściową aromatyczność, ale znacznie osłabioną.
Dziś możemy już odpowiedzieć na pytanie co takiego zachodziło w próbówce Meyera i co właściwie wykrywała reakcja. Tiofen w odróżnieniu od benzenu jest bardziej reaktywny. Tyle samo bo sześć elektronów stłoczonych jest jednak na mniejszym bo pięcioatomowym pierścieniu. Większe zagęszczenie ładunku (oraz karboanionowe struktury mezomeryczne) powoduje, że chętniej reaguje z czynnikami elektrofilowymi. Takim czynnikiem może być też proton uwalniany przez odpowiednio silny kwas.
Podczas wytrząsania benzolu ze stężonym kwasem, tiofen ulegał protonowaniu i w formie jonowej przechodził do warstwy kwasowej. Dalsza reakcja z izatyną jest dość skomplikowana i nie zupełnie rozgryziona, zaczyna się prawdopodobnie od sprotonowania izatyny i wytworzenia formy z ładunkiem dodatnim, która jako elektrofil atakuje cząsteczkę tiofenu. Powstające połączenie dimeryzuje i ulega przegrupowaniu tworząc niebieski barwnik:
Indofenina występuje w kilku izomerach różniących się konformacją trans/cis na wiązaniach podwójnych, w zasadzie więc powstaje mieszanina izomerów. Reakcja ma dziś jeszcze zastosowanie do oznaczania niektórych mało podstawionych pochodnych tiofenu.
Jakie zastosowania ma tiofen?
Jednym które samo się narzuca jest produkcja barwników. Chętnie jest też używany w syntezach nowych leków. Może zastępować pierścień benzenowy bez utraty właściwości leku, a dzięki łatwiejszemu podstawieniu łatwiej jest wytworzyć różnorodne pochodne.
Najciekawszym zastosowaniem jest jednak wytwarzanie politiofenu, polimeru mogącego przewodzić prąd elektryczny.
Spolimeryzowany tiofen po utlenieniu staje się przewodnikiem typu metalicznego. Utleniony tylko częściowo stanowi natomiast organiczny półprzewodnik. Możliwe jest więc wytworzenie na przykład przezroczystej folii przewodzącej prąd, co powinno znaleźć zastosowanie w ogniwach słonecznych. Szersze zastosowanie znalazła dobrze rozpuszczalna pochodna poli(etylenodioksytiofenu) (PEDOT-PSS), która dzięki przewodnictwu jest używana w powłokach antystatycznych, nie pozwalających na elektryzowanie się powierzchni.
Sam poli(etylenodioksytiofen) jest słabo rozpuszczalny w rozpuszczalnikach organicznych. Folie i przewody wytworzone z tego materiału są używane w elastycznych wyświetlaczach OLED.
------------
* H. D. Hartough, The Chemistry of Heterocyclic Compounds, Thiophene and Its Derivatives,
* https://en.wikipedia.org/wiki/Thiophene
* https://en.wikipedia.org/wiki/Polythiophene
Wraz z rozwojem przemysłu w XIX wiecznej Europie, w tym maszyn parowych i pieców hutniczych, duże znaczenie jako paliwo zaczął odgrywać węgiel kamienny. Dla pewnych zastosowań korzystniejszym niż surowe paliwem był koks, otrzymany przez ogrzewanie węgla bez dostępu powietrza tak, że ulatywała zeń woda i lotnie związki. Koks, o wyższej wartości opałowej, zużywano głównie do wytopu stali; gazy palne zużywano do oświetlania ulic w latarniach i jako gaz do kuchenek; wykraplana woda pogazowa zawierająca amoniak była zużywana do produkcji nawozów sztucznych.
Jedynym produktem ubocznym jaki nie dawał się wprost zastosować była smoła pogazowa, często po prostu wylewana albo po oddzieleniu najbardziej lotnych składników używana do impregnacji drewna. Szybko zainteresowali się nią chemicy świadomi, że jest mieszanką wielu interesujących substancji. Stwierdzili oni na przykład, że przez destylację surowej smoły można otrzymać frakcje o rozmaitych właściwościach. Z jednych odzyskiwano naftalen, z innych dawało się wyprodukować fenol, zaś najlżejsza i niskowrząca frakcja dawała się zastosować jako rozpuszczalnik i olej oświetleniowy. Frakcja ta stanowiła też zresztą uciążliwe zanieczyszczenie gazu koksowniczego używanego do oświetlenia, zauważalne zwłaszcza gdy doprowadzany gaz był jeszcze ciepły. Wykraplała się na chłodnych kloszach latarń i przemieszana z sadzą zbierała na dnie.
Tam też na lepkie zanieczyszczenie zwrócił uwagę w 1825 roku Michael Faraday, który będąc bardzo praktycznym człowiekiem podjął się jej destylacji, chcąc otrzymać palny olej. Przydatnym produktem okazała się jedna z frakcji, o temperaturze wrzenia 80°C. Była to rzadka, lekko żółtawa ciecz spalająca się bardzo kopcącym płomieniem i będąca dobrym rozpuszczalnikiem. W następnych dekadach nauczono się wyodrębniać ją na duża skalę ze smoły pogazowej, a ze względu na obfite występowanie w benzolu, cieczy absorbowanej z gazu koksowniczego na stałych pochłaniaczach, nazwano ją benzenem.
Benzen odegrał dużą rolę w rozwoju chemii organicznej. To od niego pewną grupę niereaktywnych związków, często posiadających charakterystyczny zapach, nazwano związkami aromatycznymi. W tym wczesnym okresie duży problem sprawiało chemikom określenie jego struktury cząsteczkowej. Całkiem niedawno przyjęło się uważać, że pierwiastki składają się z atomów, a związki ze złożeń tych atomów w drobne całostki, nazwane cząsteczkami, o określonej budowie i układzie połączonych atomów. Jedyną informację o przypuszczalnym składzie cząsteczki stanowiły stosunki ilościowe pierwiastków składowych. Wiedząc w jakich ilościach łączą się ze sobą atomy, należało domyśleć się jaką prawdopodobnie tworzyły ze sobą strukturę.
Chemikiem który włożył w tą dziedzinę najwięcej, był opisywany już tutaj August Friedrich Kekule. On to po raz pierwszy na podstawie swych badań ustalił, że węgiel w związkach organicznych łączy się z maksymalnie czterema innymi atomami. W późniejszym okresie zastanawiając się jak połączyć ze sobą budulcowe atomy, doszedł do wniosku, że atomy węgla w bardziej skomplikowanych związkach muszą łączyć się tworząc łańcuchy. Wedle opowiadanej przezeń po latach anegdoty, myśl tą podsunął mu sen w którym dostrzegł tańczące atomy, które w pewnym momencie zaczęły się bawić w lokomotywę.
Pomysł ten nie dawał się jednak zastosować do niektórych związków, czego przykładem był benzen, złożony z węgla i wodoru w stosunku 1:1, i zawierający najwyraźniej sześć węgli. Rozwiązanie podsunął mu kolejny sen, w którym tańczące atomy utworzyły węża, a ten w pewnym momencie uchwycił swój ogon i w takiej formie wirował mu przed oczami. No tak - załóżmy że atomy są połączone w pierścień i mają wolną możliwość przyłączenia jeszcze tylko po jednym, a skład będzie się zgadzał.
Po upływie kolejnych lat chemicy coraz śmielej poczynali sobie z tworzeniem nowych pochodnych tego związku, aż w roku 1879 słynny chemik Bayer, założyciel zakładu produkującego między innymi Aspirynę, zauważył bardzo specyficzną reakcję - gdy wytrząsnął benzen ze stężonym kwasem siarkowym i dodał izatyny, żółtopomarańczowej substancji otrzymywanej z indygo, powstawało wyraźne niebieskie zabarwienie, zauważalne nawet przy niewielkich ilościach substancji. Wyglądało zatem na to, że odkryto prostą i szybką reakcję charakterystyczną, pozwalającą wykrywać benzen.
Odkrycie szybko zostało uznane i niektórzy postępowi profesorowie chemii zaczęli uczyć o tej reakcji na uniwersytetach. Jednym z nich był profesor Wiliam Weith wykładający chemię na uniwersytecie w Zurychu. Miał on specjalny lektorat poświęcony związkom aromatycznym, podczas którego pokazywał najbardziej charakterystyczne reakcje. Niestety na początku 1882 roku zmarł, toteż zajęciami podczas wiosennego semestru zajął się jego bliski przyjaciel Viktor Meyer.
Gdy przygotowywał się do zajęć polecił swojemu asystentowi aby przygotował mu próbkę benzenu. Tylko miał być czysty, tak aby pokaz poszedł bez problemów.
W dniu wykładu asystent dostarczył odpowiednią ilość związku. Meyer omówił historię i strukturę benzenu, po czym przeszedł do omawiania reakcji. Można wyobrazić sobie jak mówi studentom, że gdy teraz wytrząsie benzen ze stężonym kwasem i doda izatyny, to zobaczymy piękny niebieski kolor. Następnie tak jak mówił wytrząsa w próbówce benzen i stężony kwas, dodaje izatynę i... nic się nie dzieje. Powtarza reakcję, bo może coś akurat źle zrobił, ale nic nie pomaga. No cóż, tak się czasem zdarza, powtórzymy na następnych zajęciach.
Po skończonym wykładzie zwrócił się zatem do asystenta z delikatnym zapytaniem, co on u licha mu na te zajęcia przygotował. Bo jeśli nie szyny i nie izatyna, to benzen był zły. Asystent, znany później Traugott Sandmeyer bronił się że ależ skąd, przygotował benzen czysty, jak profesor chciał, wszystko wedle przepisu z dekarboksylacji kwasu benzoesowego bo tylko wtedy dawało się otrzymać zupełnie czysty. To już było zastanawiające. Jeszcze tego samego dnia Meyer wziął komercyjnie dostępny benzen otrzymywany z powęglowego benzolu, wytrząsnął z kwasem, dodał izatyny i otrzymał zgodnie z opisem Bayera piękny niebieski barwnik, znany jako indofenina.
Nie wiedząc co z tym faktem począć, wziął większą ilość komercyjnego benzenu, wytrząsnął z kwasem, oddzieloną warstwę kwasową zobojętnił stwierdzając, że wydzieliła mu się rzadka, lekko żółtawa ciecz o charakterystycznym zapachu, która wydawała się identyczna z benzenem. Meyer sądził zatem, że benzen występuje w dwóch formach, jednej mało aktywnej i drugiej "zaktywizowanej" i wchodzącej w reakcję barwną. Powtórzenie reakcji z otrzymaną cieczą pozwoliło mu na wytworzenie większej ilości niebieskiego barwnika, który wysłał do zbadania Bayerowi. Ten orzekł, że faktycznie jest to indofenina, ale zarazem w analizie elementarnej wyszło mu, że związek zawiera siarkę, której nie było w izatynie. Dalsze testy "aktywizowanego benzenu" pokazały, że musi być to substancja różna od benzenu. W odróżnieniu od niego nie krystalizowała w lodzie, i wrzała w temperaturze 84 stopni, w porównaniu z 80 stopni dla benzenu zupełnie czystego. Wreszcie analiza chemiczna wykazała, że jest to związek zawierający jeden atom siarki, cztery atomy węgla i cztery wodoru.
I tak Meyer odkrył Tiofen.
Odkrycie tiofenu zelektryzowało ówczesnych chemików. Okazało się że przez kilka dekad nie zauważyli, że benzen ze smoły węglowej jest mieszanką dwóch związków, przy czym ten drugi, tiofen, stanowił w niektórych partiach do 10%
Tiofen należy do grupy pięciokątnych związków aromatycznych, w których aromatyczność nadaje im zdelokalizowany układ sześciu elektronów - dwóch pochodzących z wiązań podwójnych na części węglowej i jednej wolnej pary pożyczonej z heteroatomu. Pełnowęglowy odpowiednik czyli cyklopentadien nie jest aromatyczny, a dodatkowo efekty antyaromatyczne tylko zmniejszają jego trwałość. Dążąc do utrwalenia chętnie odszczepia jeden wodór tworząc karboanion cyklopentadienylowy który już jest aromatyczny.
Podstawienie jednego węgla w tym układzie heteroatomem posiadającym wolną parę elektronową tworzy aromatyczną cząsteczkę obojętną. Gdy tym atomem jest tlen, otrzymujemy furan, gdy azot jest to pirol. Udało się także otrzymać analogiczne cząsteczki z niektórymi metalami i półmetalami, takie jak silol z krzemem, arsol z arsenem, stannol z cyną a nawet tytanol z tytanem. Zachowują one częściową aromatyczność, ale znacznie osłabioną.
Dziś możemy już odpowiedzieć na pytanie co takiego zachodziło w próbówce Meyera i co właściwie wykrywała reakcja. Tiofen w odróżnieniu od benzenu jest bardziej reaktywny. Tyle samo bo sześć elektronów stłoczonych jest jednak na mniejszym bo pięcioatomowym pierścieniu. Większe zagęszczenie ładunku (oraz karboanionowe struktury mezomeryczne) powoduje, że chętniej reaguje z czynnikami elektrofilowymi. Takim czynnikiem może być też proton uwalniany przez odpowiednio silny kwas.
Podczas wytrząsania benzolu ze stężonym kwasem, tiofen ulegał protonowaniu i w formie jonowej przechodził do warstwy kwasowej. Dalsza reakcja z izatyną jest dość skomplikowana i nie zupełnie rozgryziona, zaczyna się prawdopodobnie od sprotonowania izatyny i wytworzenia formy z ładunkiem dodatnim, która jako elektrofil atakuje cząsteczkę tiofenu. Powstające połączenie dimeryzuje i ulega przegrupowaniu tworząc niebieski barwnik:
Indofenina występuje w kilku izomerach różniących się konformacją trans/cis na wiązaniach podwójnych, w zasadzie więc powstaje mieszanina izomerów. Reakcja ma dziś jeszcze zastosowanie do oznaczania niektórych mało podstawionych pochodnych tiofenu.
Jakie zastosowania ma tiofen?
Jednym które samo się narzuca jest produkcja barwników. Chętnie jest też używany w syntezach nowych leków. Może zastępować pierścień benzenowy bez utraty właściwości leku, a dzięki łatwiejszemu podstawieniu łatwiej jest wytworzyć różnorodne pochodne.
Najciekawszym zastosowaniem jest jednak wytwarzanie politiofenu, polimeru mogącego przewodzić prąd elektryczny.
Spolimeryzowany tiofen po utlenieniu staje się przewodnikiem typu metalicznego. Utleniony tylko częściowo stanowi natomiast organiczny półprzewodnik. Możliwe jest więc wytworzenie na przykład przezroczystej folii przewodzącej prąd, co powinno znaleźć zastosowanie w ogniwach słonecznych. Szersze zastosowanie znalazła dobrze rozpuszczalna pochodna poli(etylenodioksytiofenu) (PEDOT-PSS), która dzięki przewodnictwu jest używana w powłokach antystatycznych, nie pozwalających na elektryzowanie się powierzchni.
Sam poli(etylenodioksytiofen) jest słabo rozpuszczalny w rozpuszczalnikach organicznych. Folie i przewody wytworzone z tego materiału są używane w elastycznych wyświetlaczach OLED.
------------
* H. D. Hartough, The Chemistry of Heterocyclic Compounds, Thiophene and Its Derivatives,
* https://en.wikipedia.org/wiki/Thiophene
* https://en.wikipedia.org/wiki/Polythiophene
środa, 14 października 2015
Tajemnice czerni czyli bardzo długie nazwy
Będąc ostatnio w sklepie przeglądałem różne płyny i proszki do płukania tkanin, szukając czegoś do usuwania zafarbowania, bowiem po nieopatrznym wrzuceniu wraz z bielizną czarnych skarpet, okazało się, że wszystkie rzeczy zabarwiły się na kolor szaro-niebieski. Oczywiście zaglądałem na składy bo nie chodziło mi po prostu o wybielacz. Niestety składy środków czyszczących są zwykle nadmiernie ogólnikowe. Nawet mi, jako chemikowi, skład "10% anionowe środki powierzchniowo czynne, 10% kationowe środki czynne, 10% niejonowe środki czynne" nic właściwie nie mówi. Dlatego też w pewnym zdumieniem odczytałem skład środka mającego przywracać czarny kolor, gdzie nie tylko podano główne składniki, ale w dodatku podano ich pełne nazwy chemiczne. A były to nazwy tak długie i skomplikowane, że ledwie się zmieściły. Osobę nie zorientowaną takie nazwy mogą przerazić. Zaś chemika zaciekawić.
Nazwy te to:
* 4-amino-6-[5-(5-chloro-2,6-difluoropirymidyno-4-ylamino)-2-sulfonianofenyloazo]-5-hydroky-3-{4-[2-(sulfonianooksy)etylosulfonylo]fenyloazo} naftaleno-2,7-disulfonian litu-sodu-wodoru
* 7-(4,6-dichloro-1,3,5-triazyn-2-yloamino-4-hydroksy-3-{4-[2(sulfonianoksy)etylsulfonylo] fenyloazo} naftaleno-2-sulfonian disodu;
* kwas 5-naftaleno-disulfonowy,2-[2-8[[4-chloro-6[[4-[[2-(sulfooksy)etylo]sulfonylo]fenylo]amino-1,3,5-triazin-2-yl]amino]-1-hydroksy-3,6-disulfo-2-naftalenylo]diazenylo]-, sól sodowa(1:5)
Zaś aby je prawidłowo odczytać należy dowiedzieć się coś niecoś na temat tego jak właściwie tworzone są nazwy związków chemicznych.
Nazewnictwo związków organicznych podporządkowane jest zasadzie opisania związków tak, aby możliwe było dysponując samą nazwą rozrysować strukturę cząsteczki. Najczęściej używany sposób traktuje strukturę cząsteczki hierarhicznie, to jest wyróżnia pewien rdzeń do którego przyczepione są podstawniki, do tych mogą być dołączone inne poboczne podstawniki zależnie od stopnia rozgałęzienia. Nazwa wymienia więc kolejno podstawniki podczepione do rdzenia, najczęściej w kolejności alfabetycznej aby na końcu przejść do nazwy rdzenia i zakończyć końcówką specyficzną dla grupy funkcyjnej. Podstawnikom przypisywane są liczbowe określenia miejsca w którym są dołączone do rdzenia, liczone począwszy od grupy funkcyjnej rdzenia. Najbardziej optymalna zasada jest taka, aby zaczynać liczenie podstawników od takiego miejsca, aby przypisane im liczby były jak najmniejsze.
Nazwy podstawników są zwykle tworzone od nazw związków z jakich można by je otrzymać. Podstawnik -CH3, będący metanem bez jednego wodoru, to metyl, podstawnik -CH2-CH3 będący etanem bez jednego wodoru to etyl. Czasem nazwy podstawników pochodzą od innej niż zwykle używana nazwy związku wyjściowego, podstawnik będący benzenem bez jednego wodoru to nie benzenyl tylko fenyl. Pewne grupy mają swoje stałe nazwy, przykładowo złożona z pięciu węgli grupa którą można by nazwać dimetyloprolylową, jest nazywana tert-amylową, zaś grupa utworzona z etenu to grupa winylowa.
Zacznijmy więc od najprostszych przypadków:
Rdzeniem cząsteczki jest dwuwęglowy łańcuch etanu. Do niego podłączone są dwa podstawniki - chlorowy i hydroksylowy. Ten drugi można uznać za grupę funkcyjną zaś sam związek za pochodną alkoholu etylowego. Licząc od węgla przy którym jest grupa -OH, chlor jest połączony z drugim, stąd też nazwa 2-chloroetanol. Następny przykład:
Tutaj sytuację możemy potraktować dwojako - albo uznamy, że to nadal pochodna etanolu, tylko że z dodaną grupą metylową -CH3, albo uznamy że to pochodna propanolu. W tym pierwszym przypadku zaczniemy nazwę od podstawnika zaczynającego się na literę wcześniejszą w alfabecie, będzie to 2-chloro-2-metyloetanol. Zwykle jednak w takich sytuacjach preferuje się przedłużenie rdzenia czyli potraktowanie metylu jako dalszej części łańcucha. Związek będzie wtedy pochodną propanolu i nazywać się będzie 2-chloropropanol.
Oba sposoby opisu są w zasadzie równoważne bo z obu można wywnioskować poprawną strukturę, preferowany jest jednak ten drugi, bowiem skutkuje prostszą nazwą. Różnice w sposobie opisu powodują, że często związek na wiele synonimów nazwy.
Tutaj znów sytuację można różnie opisywać. Możemy na przykład uznać, że jest to pochodna etanu, z chlorem przy jednym węglu, dwoma metylami przy drugim i grupą fenylową przy tymże. Wtedy nazwa będzie brzmiała 1-chloro-2,2-dimetylo-2-fenyloetan. Możemy uznać jedną z grup metylowych za przedłużenie łańcucha, tak że będzie to pochodna propanu o nazwie 1-chloro-2-metylo-2-fenylopropan. Ale możemy też uznać, że dwie grupy metylowe i łączący je węgiel to główny rdzeń, wtedy związek będzie się nazywał 2-chlorometylo-2-fenylopropan. Ja preferowałbym tą drugą ale w internecie związek częściej występuje pod tą ostatnią.
Kolejny przypadek zawiera podstawniki połączone przez różne miejsca:
Tą cząsteczkę można opisać na dwa sposoby - albo jako pochodną chlorobenzenu albo jako pochodną kwasu benzoesowego. W tym pierwszym przypadku grupa złożona z kwasu benzoesowego będzie grupą 3-karboksyfenolową albowiem dla tego podstawnika grupą funkcyjną od której liczone są miejsca jest grupa karboksylowa. Podstawnik jest podłączony przez węgiel od którego grupa ta jest przy trzecim stąd nazwa całego podstawnika 3-karboksyfenylowy. Licząc w rdzeniu od chloru, grupa ta znajduje się na drugim miejscu, stąd aby nie pomieszać cyferek, trzeba dodać nawias w którym mieścić się będzie nazwa całej grupy, stąd zapis: 2-(3-karboksyfenlo)-chlorobenzen.
Możemy też potraktować cząsteczkę jak pochodną kwasu benzoesowego, wówczas nazwa będzie brzmiała kwas 3-(2-chlorofenylo)-benzoesowy. Ta druga wersja jest częściej używana.
A teraz podstawnik z podstawnikiem z podstawnikiem:
I trzy możliwości - albo to pochodna chlorobenzenu, albo fenolu albo kwasu benzoesowego. Dla pierwszej wersji nazwa brzmi: 2-{4-[2-(2-karboksylofenylo)fenoksylo]}-metylenochlorobenzen bo jest to chlorobenzen do którego w miejscu 2 podłączono przez mostek metylenowy -CH2- fenol, łączony przez pozycję 4 wobec grupy hydroksylowej i sam mający przy pozycji 2 grupę karboksyfenylową, połączoną przez węgiel w pozycji 2. I tu widać ten hierarchiczny opis.
Dla drugiej opcji będzie to 4-(2-chlorofenylometyleno)-2-(2-karboksyfenylo)-fenol. Dla trzeciej kwas 2-{2-[4-(2-chlorofenylometyleno)-fenoksy]}-benzoesowy. Ta druga wersja jest preferowana bo jest w niej mniej nawiasów.
Skoro już przeszliśmy ten krótki kurs nazewnictwa, zajmijmy się tymi długaśnymi nazwami z doczerniacza.
4-amino-6
Pierwszy związek jest bardzo długi:
Wiemy, że rdzeń ten zwiera już dwie grupy sulfonowe, a co z resztą? Resztą są cztery podstawniki, w tym dwa bardzo rozbudowane, pierwszy to fragment "4-amino" i jest to grupa aminowa -NH2 podłączona przy pozycji 4 a drugi zaczyna się od "6-[5-(5-chloro-" trzeci to "5-hydroksy" i jest grupą hydroksylową -OH podczepioną przy pozycji 5, czwarty zaczyna się od "3-{4-[2(sulfonianooksy". Nazwę można więc rozbić na części oznaczając je kolorami:
4-amino-6-[5-(5-chloro-2,6-difluoropirymidyno-4-ylamino)-2-sulfonianofenyloazo]-5-hydroksy-3-{4-[2-(sulfonianooksy)etylosulfonylo]fenyloazo} naftaleno-2,7-disulfonian litu-sodu-wodoru
To nadal jest zawiłe ale już widzimy jak to opanować. Teraz rozbierzmy na części podstawniki:
* 6-[5-(5-chloro-2,6-difluoropirymidyno-4-ylamino)-2-sulfonianofenyloazo] - tutaj mamy trzy wyraźne części. Grupa zaczyna się od pirymidyny zawierającej dwa podstawniki fluorowe w pozycjach 2 i 6 wobec azotu od którego zaczynamy liczyć i chlorowy w pozycji 5, i jest połączona przez węgiel 4 z mostkową aminą:
Poprzez tą aminę połączona jest z węglem 5 grupy 2-sulfonianofenyloazowej:
Która poprzez grupę azową połączona jest z rdzeniem naftalenowym w pozycji 6
Drugi podstawnik:
* 3-{4-[2-(sulfonianooksy)etylosulfonylo]fenyloazo} - zaczyna się od grupy sulfonianooksylowej, czyli reszty kwasu siarkowego połączonej przez tlen -OHSO3 z grupą etylową do drugiego węgla. Grupa ta przez pierwszy węgiel etylu jest połączona z sulfonylem poprzez który w pozycji 4 łączy się z grupą fenyloazową:
a przez ugrupowanie azowe z miejscem 3 rdzenia naftalenowego.
Po złożeniu tego do kupy otrzymujemy taki oto związek, tu w wersji soli sodowej:
Czym jest ten skomplikowany związek? Rozpuszczalną formą barwnika azowego. Grupy azowe -N=N- to silne chromofory a więc zapewniają cząsteczce kolor, podstawione wzmacniającymi efekt grupami aromatycznymi z wyciągającymi elektrony podstawnikami halogenowymi dają w efekcie silne zabarwienie. Ten konkretny związek znany jest też pod nazwą handlową Reactive Blue 225 i farbuje na kolor ciemnoniebieski
7-[4-(6-dichloro
Następny związek w składzie to także bardzo rozgałęziona sól sulfoniowa będąca pochodną naftalenu. Zaznaczmy poszczególne części:
7-(4,6-dichloro-1,3,5-triazyn-2-yloamino-4-hydroksy-3-{4-[2(sulfonianoksy)etylsulfonylo] fenyloazo} naftaleno-2-sulfonian disodu;
Rdzeniem jest naftalen, który w pozycji 4 ma dołączoną grupę hydroksylową a w pozycji 2 sulfonylową. Dwa pozostałe podstawniki są rozbudowane.
Pierwszy to pierścień 1,3,5-triazyny, związku aromatycznego w którym w sześciokątnym pierścieniu co drugi atom stanowi azot. Pierścień w dwóch miejscach podstawiony jest chlorem i poprzez węgiel w pozycji 2 połączony z aminą, a ta z naftalenem w pozycji 7. Drugi jest taki sam jak w poprzednim związku - grupa sulfoksylowa połączona przez tlen z etanem, ten z ugrupowaniem sulfonowym, to z benzenem a ten z grupą azową łączącą go z naftalenem.
Ostateczny wzór przedstawia się zatem następująco:
Związek ma też oznaczenie handlowe Orange HF SNK lub Reactive Orange FD 19969 FW, jest to zatem kolejny barwnik azowy, tym razem zapewne ciemno-pomarańczowy. Znajduje się na listach substancji niebezpiecznych w dziale substancji wywołujących podrażnienia skóry[2] [3]
kwas 5-naftaleno-disulfonowy
Ten związek będzie można już łatwiej rozszyfrować bo pewne jego elementy są podobne do poprzednich.
Zaznaczając poszczególne części, jest to: kwas 2-[2-[8-[[4-chloro-6[[4-[[2-(sulfooksy)etylo]sulfonylo]fenylo]amino-1,3,5-triazin-2-yl]amino]-1-hydroksy-3,6-disulfo-2-naftalenylo]diazenylo]-5-naftaleno-disulfonowy sól sodowa(1:5)
Cząsteczka wygląda zatem następująco:
Nazwa handlowa Reactive Red 195A [4]
I po co to wszystko?
Cóż. Czarne tkaniny szarzeją z powodu spierania lub ścierania ciemnych barwników. Dlatego omawiany doczerniacz po prostu farbuje tkaninę. Są to barwniki reaktywne, to jest wchodzące w reakcję z materiałem włókna i tworzące trwałe połączenia; reakcji ulegają włókna naturalne, dlatego preparat nie nadaje się do tkanin z włókiem całkowicie sztucznych.
Zauważmy, że żaden z wymienionych barwników nie jest czarny. Tak na prawdę nie ma czarnych barwników, czerń oznacza, że dany przedmiot pochłonął na tyle dużo światła, iż nie jesteśmy w stanie określić jego koloru, jednak rozcieńczając czarne tusze możemy się przekonać, że zwykle są one po prostu mieszanką bardzo ciemnych brązów i błękitów (zaś brąz to bardzo ciemny odcień pomarańczy). Czarne tulipany są w rzeczywistości fioletowe, tylko dość intensywnie. Czerń można osiągnąć zatem albo używając jakiegoś barwnika w tak dużym stężeniu, że będzie pochłaniał większość światła, albo mieszankę barwników, z których każdy pochłania jakąś część spektrum.
W tym przypadku zmieszanie barwników intensywnie niebieskiego, pomarańczowego i żółtego, daje czerń. Być może gdybyśmy włożyli do prania białą tkaninę, to okazałaby się ostatecznie raczej szara, ale dla tkanin czarnych które tylko nieco spłowiały i wytarły się wystarczy przyciemnienie jasnych miejsc aby wyglądały na zdecydowanie czarniejsze.
----------
* http://www.auchandirect.pl/sklep/artykuly/1171_1240_1630/99701801/Dla-Domu/Pralnia/Odplamiacze/Renowator-koloru-czarnego-Dylon-2-szt.-1-szt
[2] http://www.pis.gov.pl/userfiles/file/departament%20Higieny%20%C5%9Arodowiska%20JUPIK/chemia%20prawo/elincsk-wykaz%20substancji.pdf pozycja 404-600-07
[3] http://www.chemindustry.com/chemicals/41146.html
[4] http://ofmpub.epa.gov/sor_internet/registry/substreg/searchandretrieve/advancedsearch/externalSearch.do?p_type=CASNO&p_value=77365-64-1
Nazwy te to:
* 4-amino-6-[5-(5-chloro-2,6-difluoropirymidyno-4-ylamino)-2-sulfonianofenyloazo]-5-hydroky-3-{4-[2-(sulfonianooksy)etylosulfonylo]fenyloazo} naftaleno-2,7-disulfonian litu-sodu-wodoru
* 7-(4,6-dichloro-1,3,5-triazyn-2-yloamino-4-hydroksy-3-{4-[2(sulfonianoksy)etylsulfonylo] fenyloazo} naftaleno-2-sulfonian disodu;
* kwas 5-naftaleno-disulfonowy,2-[2-8[[4-chloro-6[[4-[[2-(sulfooksy)etylo]sulfonylo]fenylo]amino-1,3,5-triazin-2-yl]amino]-1-hydroksy-3,6-disulfo-2-naftalenylo]diazenylo]-, sól sodowa(1:5)
Zaś aby je prawidłowo odczytać należy dowiedzieć się coś niecoś na temat tego jak właściwie tworzone są nazwy związków chemicznych.
Nazewnictwo związków organicznych podporządkowane jest zasadzie opisania związków tak, aby możliwe było dysponując samą nazwą rozrysować strukturę cząsteczki. Najczęściej używany sposób traktuje strukturę cząsteczki hierarhicznie, to jest wyróżnia pewien rdzeń do którego przyczepione są podstawniki, do tych mogą być dołączone inne poboczne podstawniki zależnie od stopnia rozgałęzienia. Nazwa wymienia więc kolejno podstawniki podczepione do rdzenia, najczęściej w kolejności alfabetycznej aby na końcu przejść do nazwy rdzenia i zakończyć końcówką specyficzną dla grupy funkcyjnej. Podstawnikom przypisywane są liczbowe określenia miejsca w którym są dołączone do rdzenia, liczone począwszy od grupy funkcyjnej rdzenia. Najbardziej optymalna zasada jest taka, aby zaczynać liczenie podstawników od takiego miejsca, aby przypisane im liczby były jak najmniejsze.
Nazwy podstawników są zwykle tworzone od nazw związków z jakich można by je otrzymać. Podstawnik -CH3, będący metanem bez jednego wodoru, to metyl, podstawnik -CH2-CH3 będący etanem bez jednego wodoru to etyl. Czasem nazwy podstawników pochodzą od innej niż zwykle używana nazwy związku wyjściowego, podstawnik będący benzenem bez jednego wodoru to nie benzenyl tylko fenyl. Pewne grupy mają swoje stałe nazwy, przykładowo złożona z pięciu węgli grupa którą można by nazwać dimetyloprolylową, jest nazywana tert-amylową, zaś grupa utworzona z etenu to grupa winylowa.
Zacznijmy więc od najprostszych przypadków:
Rdzeniem cząsteczki jest dwuwęglowy łańcuch etanu. Do niego podłączone są dwa podstawniki - chlorowy i hydroksylowy. Ten drugi można uznać za grupę funkcyjną zaś sam związek za pochodną alkoholu etylowego. Licząc od węgla przy którym jest grupa -OH, chlor jest połączony z drugim, stąd też nazwa 2-chloroetanol. Następny przykład:
Tutaj sytuację możemy potraktować dwojako - albo uznamy, że to nadal pochodna etanolu, tylko że z dodaną grupą metylową -CH3, albo uznamy że to pochodna propanolu. W tym pierwszym przypadku zaczniemy nazwę od podstawnika zaczynającego się na literę wcześniejszą w alfabecie, będzie to 2-chloro-2-metyloetanol. Zwykle jednak w takich sytuacjach preferuje się przedłużenie rdzenia czyli potraktowanie metylu jako dalszej części łańcucha. Związek będzie wtedy pochodną propanolu i nazywać się będzie 2-chloropropanol.
Oba sposoby opisu są w zasadzie równoważne bo z obu można wywnioskować poprawną strukturę, preferowany jest jednak ten drugi, bowiem skutkuje prostszą nazwą. Różnice w sposobie opisu powodują, że często związek na wiele synonimów nazwy.
Tutaj znów sytuację można różnie opisywać. Możemy na przykład uznać, że jest to pochodna etanu, z chlorem przy jednym węglu, dwoma metylami przy drugim i grupą fenylową przy tymże. Wtedy nazwa będzie brzmiała 1-chloro-2,2-dimetylo-2-fenyloetan. Możemy uznać jedną z grup metylowych za przedłużenie łańcucha, tak że będzie to pochodna propanu o nazwie 1-chloro-2-metylo-2-fenylopropan. Ale możemy też uznać, że dwie grupy metylowe i łączący je węgiel to główny rdzeń, wtedy związek będzie się nazywał 2-chlorometylo-2-fenylopropan. Ja preferowałbym tą drugą ale w internecie związek częściej występuje pod tą ostatnią.
Kolejny przypadek zawiera podstawniki połączone przez różne miejsca:
Tą cząsteczkę można opisać na dwa sposoby - albo jako pochodną chlorobenzenu albo jako pochodną kwasu benzoesowego. W tym pierwszym przypadku grupa złożona z kwasu benzoesowego będzie grupą 3-karboksyfenolową albowiem dla tego podstawnika grupą funkcyjną od której liczone są miejsca jest grupa karboksylowa. Podstawnik jest podłączony przez węgiel od którego grupa ta jest przy trzecim stąd nazwa całego podstawnika 3-karboksyfenylowy. Licząc w rdzeniu od chloru, grupa ta znajduje się na drugim miejscu, stąd aby nie pomieszać cyferek, trzeba dodać nawias w którym mieścić się będzie nazwa całej grupy, stąd zapis: 2-(3-karboksyfenlo)-chlorobenzen.
Możemy też potraktować cząsteczkę jak pochodną kwasu benzoesowego, wówczas nazwa będzie brzmiała kwas 3-(2-chlorofenylo)-benzoesowy. Ta druga wersja jest częściej używana.
A teraz podstawnik z podstawnikiem z podstawnikiem:
I trzy możliwości - albo to pochodna chlorobenzenu, albo fenolu albo kwasu benzoesowego. Dla pierwszej wersji nazwa brzmi: 2-{4-[2-(2-karboksylofenylo)fenoksylo]}-metylenochlorobenzen bo jest to chlorobenzen do którego w miejscu 2 podłączono przez mostek metylenowy -CH2- fenol, łączony przez pozycję 4 wobec grupy hydroksylowej i sam mający przy pozycji 2 grupę karboksyfenylową, połączoną przez węgiel w pozycji 2. I tu widać ten hierarchiczny opis.
Dla drugiej opcji będzie to 4-(2-chlorofenylometyleno)-2-(2-karboksyfenylo)-fenol. Dla trzeciej kwas 2-{2-[4-(2-chlorofenylometyleno)-fenoksy]}-benzoesowy. Ta druga wersja jest preferowana bo jest w niej mniej nawiasów.
Skoro już przeszliśmy ten krótki kurs nazewnictwa, zajmijmy się tymi długaśnymi nazwami z doczerniacza.
4-amino-6
Pierwszy związek jest bardzo długi:
4-amino-6-[5-(5-chloro-2,6-difluoropirymidyno-4-ylamino)-2-sulfonianofenyloazo]-5-hydroksy-3-{4-[2-(sulfonianooksy)etylosulfonylo]fenyloazo} naftaleno-2,7-disulfonian litu-sodu-wodorujednak już z pobieżnego przejrzenia wychwycić można czym jest tutaj rdzeń do którego podczepiono podstawniki - to sama końcówka nazwy "naftaleno-2,7-disulfonian litu-sodu-wodoru". Mamy tu więc do czynienia z rozbudowaną solą sulfonową, zobojętnioną częściowo sodem a częściowo litem, z dwiema grupami sulfonowymi pochodzącymi od kwasu siarkowego w pozycjach 2 i 7. Naftalen to związek złożony z dwóch pierścieni aromatycznych połączonych bokiem i może mieć maksymalnie do ośmiu podstawników liczonych w tej kolejności:
Wiemy, że rdzeń ten zwiera już dwie grupy sulfonowe, a co z resztą? Resztą są cztery podstawniki, w tym dwa bardzo rozbudowane, pierwszy to fragment "4-amino" i jest to grupa aminowa -NH2 podłączona przy pozycji 4 a drugi zaczyna się od "6-[5-(5-chloro-" trzeci to "5-hydroksy" i jest grupą hydroksylową -OH podczepioną przy pozycji 5, czwarty zaczyna się od "3-{4-[2(sulfonianooksy". Nazwę można więc rozbić na części oznaczając je kolorami:
4-amino-6-[5-(5-chloro-2,6-difluoropirymidyno-4-ylamino)-2-sulfonianofenyloazo]-5-hydroksy-3-{4-[2-(sulfonianooksy)etylosulfonylo]fenyloazo} naftaleno-2,7-disulfonian litu-sodu-wodoru
To nadal jest zawiłe ale już widzimy jak to opanować. Teraz rozbierzmy na części podstawniki:
* 6-[5-(5-chloro-2,6-difluoropirymidyno-4-ylamino)-2-sulfonianofenyloazo] - tutaj mamy trzy wyraźne części. Grupa zaczyna się od pirymidyny zawierającej dwa podstawniki fluorowe w pozycjach 2 i 6 wobec azotu od którego zaczynamy liczyć i chlorowy w pozycji 5, i jest połączona przez węgiel 4 z mostkową aminą:
Poprzez tą aminę połączona jest z węglem 5 grupy 2-sulfonianofenyloazowej:
Która poprzez grupę azową połączona jest z rdzeniem naftalenowym w pozycji 6
Drugi podstawnik:
* 3-{4-[2-(sulfonianooksy)etylosulfonylo]fenyloazo} - zaczyna się od grupy sulfonianooksylowej, czyli reszty kwasu siarkowego połączonej przez tlen -OHSO3 z grupą etylową do drugiego węgla. Grupa ta przez pierwszy węgiel etylu jest połączona z sulfonylem poprzez który w pozycji 4 łączy się z grupą fenyloazową:
a przez ugrupowanie azowe z miejscem 3 rdzenia naftalenowego.
Po złożeniu tego do kupy otrzymujemy taki oto związek, tu w wersji soli sodowej:
Czym jest ten skomplikowany związek? Rozpuszczalną formą barwnika azowego. Grupy azowe -N=N- to silne chromofory a więc zapewniają cząsteczce kolor, podstawione wzmacniającymi efekt grupami aromatycznymi z wyciągającymi elektrony podstawnikami halogenowymi dają w efekcie silne zabarwienie. Ten konkretny związek znany jest też pod nazwą handlową Reactive Blue 225 i farbuje na kolor ciemnoniebieski
7-[4-(6-dichloro
Następny związek w składzie to także bardzo rozgałęziona sól sulfoniowa będąca pochodną naftalenu. Zaznaczmy poszczególne części:
7-(4,6-dichloro-1,3,5-triazyn-2-yloamino-4-hydroksy-3-{4-[2(sulfonianoksy)etylsulfonylo] fenyloazo} naftaleno-2-sulfonian disodu;
Rdzeniem jest naftalen, który w pozycji 4 ma dołączoną grupę hydroksylową a w pozycji 2 sulfonylową. Dwa pozostałe podstawniki są rozbudowane.
Pierwszy to pierścień 1,3,5-triazyny, związku aromatycznego w którym w sześciokątnym pierścieniu co drugi atom stanowi azot. Pierścień w dwóch miejscach podstawiony jest chlorem i poprzez węgiel w pozycji 2 połączony z aminą, a ta z naftalenem w pozycji 7. Drugi jest taki sam jak w poprzednim związku - grupa sulfoksylowa połączona przez tlen z etanem, ten z ugrupowaniem sulfonowym, to z benzenem a ten z grupą azową łączącą go z naftalenem.
Ostateczny wzór przedstawia się zatem następująco:
Związek ma też oznaczenie handlowe Orange HF SNK lub Reactive Orange FD 19969 FW, jest to zatem kolejny barwnik azowy, tym razem zapewne ciemno-pomarańczowy. Znajduje się na listach substancji niebezpiecznych w dziale substancji wywołujących podrażnienia skóry[2] [3]
kwas 5-naftaleno-disulfonowy
Ten związek będzie można już łatwiej rozszyfrować bo pewne jego elementy są podobne do poprzednich.
Zaznaczając poszczególne części, jest to: kwas 2-[2-[8-[[4-chloro-6[[4-[[2-(sulfooksy)etylo]sulfonylo]fenylo]amino-1,3,5-triazin-2-yl]amino]-1-hydroksy-3,6-disulfo-2-naftalenylo]diazenylo]-5-naftaleno-disulfonowy sól sodowa(1:5)
Cząsteczka wygląda zatem następująco:
Nazwa handlowa Reactive Red 195A [4]
I po co to wszystko?
Cóż. Czarne tkaniny szarzeją z powodu spierania lub ścierania ciemnych barwników. Dlatego omawiany doczerniacz po prostu farbuje tkaninę. Są to barwniki reaktywne, to jest wchodzące w reakcję z materiałem włókna i tworzące trwałe połączenia; reakcji ulegają włókna naturalne, dlatego preparat nie nadaje się do tkanin z włókiem całkowicie sztucznych.
Zauważmy, że żaden z wymienionych barwników nie jest czarny. Tak na prawdę nie ma czarnych barwników, czerń oznacza, że dany przedmiot pochłonął na tyle dużo światła, iż nie jesteśmy w stanie określić jego koloru, jednak rozcieńczając czarne tusze możemy się przekonać, że zwykle są one po prostu mieszanką bardzo ciemnych brązów i błękitów (zaś brąz to bardzo ciemny odcień pomarańczy). Czarne tulipany są w rzeczywistości fioletowe, tylko dość intensywnie. Czerń można osiągnąć zatem albo używając jakiegoś barwnika w tak dużym stężeniu, że będzie pochłaniał większość światła, albo mieszankę barwników, z których każdy pochłania jakąś część spektrum.
W tym przypadku zmieszanie barwników intensywnie niebieskiego, pomarańczowego i żółtego, daje czerń. Być może gdybyśmy włożyli do prania białą tkaninę, to okazałaby się ostatecznie raczej szara, ale dla tkanin czarnych które tylko nieco spłowiały i wytarły się wystarczy przyciemnienie jasnych miejsc aby wyglądały na zdecydowanie czarniejsze.
----------
* http://www.auchandirect.pl/sklep/artykuly/1171_1240_1630/99701801/Dla-Domu/Pralnia/Odplamiacze/Renowator-koloru-czarnego-Dylon-2-szt.-1-szt
[2] http://www.pis.gov.pl/userfiles/file/departament%20Higieny%20%C5%9Arodowiska%20JUPIK/chemia%20prawo/elincsk-wykaz%20substancji.pdf pozycja 404-600-07
[3] http://www.chemindustry.com/chemicals/41146.html
[4] http://ofmpub.epa.gov/sor_internet/registry/substreg/searchandretrieve/advancedsearch/externalSearch.do?p_type=CASNO&p_value=77365-64-1
środa, 16 lipca 2014
Barwienie bakterii metodą Grama
Dawno, dawno temu, kiedy jeszcze uczyłem się w technikum chemicznym, jednym z przedmiotów była bioanaliza, gdzie uczyliśmy się jak badać mocz, rozpoznawać pod mikroskopem różne limfocyty, albo badać zawartość cholesterolu w osoczu.
Jednym z ciekawszych ćwiczeń była hodowla bakterii z powietrza - sterylną płytkę z podłożem odkrywało się na określony czas w nieruchowym powietrzu pomieszczenia, zakrywało i wstawiało do inkubatora. Bakterie które znajdowały się w powietrzu osiadały na płytce i tworzyły kolonie - jedna bakteria tworzyła jedną kolonię. Zliczając ilość kolonii na powierzchni płytki i znając czas wystawienia płytki, można było policzyć stężenie bakterii w powietrzu - całkiem proste.
Jednak otrzymane bakterie dobrze jest też jakoś zidentyfikować. Oprócz opisanych już kiedyś metod hodowli na podłożu różnicującym, inną techniką jest barwienie metodą Grama. Badanie obejmuje kilka etapów, a wszystkie je sfotografowałem.
Zasadnicza różnica między typami bakterii jaką wykrywa się w tym badaniu, to grubość i przenikliwość ściany komórkowej - w jednym bakteriach jest cienka, w innych stosunkowo gruba. Ma to wpływ na ogólną fizjologię bakterii, zaś dla medycyny znaczenie ma różna wrażliwość na leki - zasadniczo bakterie o grubszej ścianie komórkowej są bardziej odporne, z powodu słabszego wchłaniania antybiotyku do wnętrza. Różna grubość ścian komórkowych wykrywana jest przez selektywne wybarwianie fioletem krystalicznym. W jaki sposób?
Na początek należy sobie wybrać jakąś kolonię z której będziemy robić rozmaz:
Ja akurat wybrałem sobie taką w której na kolonię żółtą naciekała biała, mając nadzieję że uda mi się złapać dwa różne typy. Masę kolonii pobierałem ezą, to jest pętelką z drutu z rączką. Tę jednak należało przedtem wyżarzyć, aby usunąć wszystkie inne bakterie:
Ponieważ kolonia miała postać stałej masy, najpierw nabrałem nieco soli fizjologicznej:
potem nieco kolonii:
i rozmazałem na płytce:
Rozmaz należało teraz wysuszyć i utrwalić, aby bakterie dobrze przylegały do podłoża. Dlatego po podsuszeniu w suszarce przeciągnęliśmy płytki nad płomykiem lampki spirytusowej, tak aby masa bakteryjna "przyschła" do płytki.
Wszystkie płytki należało teraz umieścić nad tacką, założyć rękawiczki i uważać na ubranie, bo można się było nieźle pobrudzić. Najpierw każda płytka została zalana roztworem fioletu krystalicznego:
Następnie czekaliśmy dwie minuty, po czym zlaliśmy barwnik do tacki:
Nie usuwając całej cieczy, zalewaliśmy płytki płynem Lugola - na powierzchni płynu powstawała błyszcząca warstewka, jak podejrzewam był to wydzielający się jod. Płyn dzięki temu błyszczał i opalizował, wyglądając jak odwłok złotego żuka:
Po około trzydziestu sekundach zlaliśmy ciecz i dokładnie przemyliśmy alkoholem:
A następnie wodą:
Na sam koniec zalaliśmy płytki roztworem fuksyny:
Pół minuty potem zlaliśmy ją do tacki, płytki przemyliśmy wodą i osuszyliśmy w suszarce. Tak zabarwione płytki nadawały się do badania mikroskopowego:
Co takiego następowało podczas wybarwiania? Gdy zalewaliśmy płytki roztworem fioletu krystalicznego, wnikał on do bakterii zabarwiając je wszystkie. Dodany potem roztwór jodu dodatkowo przyciemniał zabarwienie poprzez tworzenie kompleksów jodu z barwnikiem. Na tym etapie zabarwione były wszystkie.
Jednak gdy przemywaliśmy płytki alkoholem, zaznaczyła się różnica - łatwo wypłukiwał on barwnik z bakterii o cienkiej ściance, natomiast nie był w stanie odbarwić bakterii o ścianie grubej. W efekcie te pierwsze stawały się bezbarwne, zaś te drugie ciemnofioletowe. Gdy zalaliśmy płytki fuksyną, odbarwione bakterie o cienkiej ścianie zabarwiły się na różowo. Te o grubej także, ale mocniejszy kolor fioletu zagłuszał róż.
W efekcie bakterie o ściance cienkiej zabarwiły się na różowo a te o grubej na ciemno fioletowo. Rożróżnianie bakterii pod mikroskopem jest zatem bardzo łatwe - bakterie Gram+ są fioletowe a Gram- różowe.
Akurat mnie, jako chemika-estetę bardziej zainteresowały kryształy fuksyny, które wykrystalizowały na płytce. Tutaj pęk kryształów w otoczeniu bakterii gram-ujemnych (powiększenie ok. 400X):
A tutaj w otoczeniu gram-dodatnich (pow. ok. 600X):
I na koniec mieszanka dwóch różnych typów bakterii:
Jednym z ciekawszych ćwiczeń była hodowla bakterii z powietrza - sterylną płytkę z podłożem odkrywało się na określony czas w nieruchowym powietrzu pomieszczenia, zakrywało i wstawiało do inkubatora. Bakterie które znajdowały się w powietrzu osiadały na płytce i tworzyły kolonie - jedna bakteria tworzyła jedną kolonię. Zliczając ilość kolonii na powierzchni płytki i znając czas wystawienia płytki, można było policzyć stężenie bakterii w powietrzu - całkiem proste.
Jednak otrzymane bakterie dobrze jest też jakoś zidentyfikować. Oprócz opisanych już kiedyś metod hodowli na podłożu różnicującym, inną techniką jest barwienie metodą Grama. Badanie obejmuje kilka etapów, a wszystkie je sfotografowałem.
Zasadnicza różnica między typami bakterii jaką wykrywa się w tym badaniu, to grubość i przenikliwość ściany komórkowej - w jednym bakteriach jest cienka, w innych stosunkowo gruba. Ma to wpływ na ogólną fizjologię bakterii, zaś dla medycyny znaczenie ma różna wrażliwość na leki - zasadniczo bakterie o grubszej ścianie komórkowej są bardziej odporne, z powodu słabszego wchłaniania antybiotyku do wnętrza. Różna grubość ścian komórkowych wykrywana jest przez selektywne wybarwianie fioletem krystalicznym. W jaki sposób?
Na początek należy sobie wybrać jakąś kolonię z której będziemy robić rozmaz:
Ja akurat wybrałem sobie taką w której na kolonię żółtą naciekała biała, mając nadzieję że uda mi się złapać dwa różne typy. Masę kolonii pobierałem ezą, to jest pętelką z drutu z rączką. Tę jednak należało przedtem wyżarzyć, aby usunąć wszystkie inne bakterie:
Ponieważ kolonia miała postać stałej masy, najpierw nabrałem nieco soli fizjologicznej:
potem nieco kolonii:
i rozmazałem na płytce:
Rozmaz należało teraz wysuszyć i utrwalić, aby bakterie dobrze przylegały do podłoża. Dlatego po podsuszeniu w suszarce przeciągnęliśmy płytki nad płomykiem lampki spirytusowej, tak aby masa bakteryjna "przyschła" do płytki.
Wszystkie płytki należało teraz umieścić nad tacką, założyć rękawiczki i uważać na ubranie, bo można się było nieźle pobrudzić. Najpierw każda płytka została zalana roztworem fioletu krystalicznego:
Następnie czekaliśmy dwie minuty, po czym zlaliśmy barwnik do tacki:
Nie usuwając całej cieczy, zalewaliśmy płytki płynem Lugola - na powierzchni płynu powstawała błyszcząca warstewka, jak podejrzewam był to wydzielający się jod. Płyn dzięki temu błyszczał i opalizował, wyglądając jak odwłok złotego żuka:
Po około trzydziestu sekundach zlaliśmy ciecz i dokładnie przemyliśmy alkoholem:
A następnie wodą:
Na sam koniec zalaliśmy płytki roztworem fuksyny:
Pół minuty potem zlaliśmy ją do tacki, płytki przemyliśmy wodą i osuszyliśmy w suszarce. Tak zabarwione płytki nadawały się do badania mikroskopowego:
Co takiego następowało podczas wybarwiania? Gdy zalewaliśmy płytki roztworem fioletu krystalicznego, wnikał on do bakterii zabarwiając je wszystkie. Dodany potem roztwór jodu dodatkowo przyciemniał zabarwienie poprzez tworzenie kompleksów jodu z barwnikiem. Na tym etapie zabarwione były wszystkie.
Jednak gdy przemywaliśmy płytki alkoholem, zaznaczyła się różnica - łatwo wypłukiwał on barwnik z bakterii o cienkiej ściance, natomiast nie był w stanie odbarwić bakterii o ścianie grubej. W efekcie te pierwsze stawały się bezbarwne, zaś te drugie ciemnofioletowe. Gdy zalaliśmy płytki fuksyną, odbarwione bakterie o cienkiej ścianie zabarwiły się na różowo. Te o grubej także, ale mocniejszy kolor fioletu zagłuszał róż.
W efekcie bakterie o ściance cienkiej zabarwiły się na różowo a te o grubej na ciemno fioletowo. Rożróżnianie bakterii pod mikroskopem jest zatem bardzo łatwe - bakterie Gram+ są fioletowe a Gram- różowe.
Akurat mnie, jako chemika-estetę bardziej zainteresowały kryształy fuksyny, które wykrystalizowały na płytce. Tutaj pęk kryształów w otoczeniu bakterii gram-ujemnych (powiększenie ok. 400X):
A tutaj w otoczeniu gram-dodatnich (pow. ok. 600X):
I na koniec mieszanka dwóch różnych typów bakterii:
czwartek, 17 kwietnia 2014
Barwniki do jaj - chemicznie ujmując
Dwa lata temu opisałem w wielkanocnym wpisie jakie są naturalne metody barwienia pisanek i jakie związki za to odpowiadają. W tym roku zatem opiszę te sztuczne barwniki.
Wprawdzie różni producenci produkują tego typu barwniki, ale jak zauważyłem, praktycznie wszyscy używają tych samych, więc opis na podstawie składu barwników które mam w domu, powinien być reprezentatywny.
Czerwony
W moim zestawie za czerwień odpowiada E 124 czyli czerwień koszenilowa. To dość skomplikowany związek:
Dwie cząsteczki pochodnych naftalenu połączone grupą azową -N=N-. Grupa ta jest silnym chromoforem, a więc ugrupowaniem nadającym barwę, a jej kolor wzmacniają duże cząsteczki aromatyczne.
Wszystkie barwniki azowe mogą wywoływać uczulenia, u osób nadwrażliwych na salicylany zwiększają objawy a u astmatyków zwiększają wydzielanie histaminy. Z tego powodu ich użycie w żywności jest coraz bardziej ograniczane a normy zawartości systematycznie obniżane.
Różowy
W niektórych zestawach kolor różowy jest otrzymywany przez dodatek amarantu czyli E-123, kolejnego barwnika azowego. Ze względu na częste doniesienia o reakcjach nadwrażliwości jest coraz rzadziej używany w przemyśle spożywczym, podbarwia kawior, galaretki w proszku i napoje alkoholowe. Jest podejrzewany o rakotwórczość ale nie potwierdzono tego u ludzi.
Żółty
W moim zestawie znajdują się dwa żółte barwniki. Pierwszy to żółcień pomarańczowa czyli E 110 o kolorze bliższym pomarańczy, także będąca barwnikiem azowym:
Podobnie jak inne tego typu związki może wywoływać uczulenia i pokrzywki, u nadwrażliwych na salicylany daje reakcję. Jest podejrzewana o rakotwórczość ale nie wykazano tego u ludzi, mimo tego wiele krajów jej nie stosuje. Używa się jej do podbarwiania słodyczy i żywności która musi być podgrzewana, jednak coraz rzadkiej. Kiedyś była często stosowana do dożółcania margaryny.
Znalazłem informację, że stężone roztwory wodne przybierają w pewnych temperaturach formę ciekłego kryształu.
Drugi barwnik to tartrazyna, czyli E 102, mająca dość ciekawą budowę:
Jest to także barwnik azowy z grupami aromatycznymi, ale także pierścieniem diazolowym. Charakteryzuje się dużą siłą barwiącą. Pojawia się w szerokiej gamie produktów, zwłaszcza napojach i słodyczach, choć w ostatnich latach jest wycofywania. Używa się jej też w kosmetykach i jako barwnika do wełny.
Może wywoływać te same problemy zdrowotne jak i pozostałe barwniki azowe - pokrzywki, uczulenia, nadwrażliwość itp ale też migreny. Wydaje się, że u pewnych ludzi występuje specyficzna nadwrażliwość konkretnie na tą substancję, także u tych którzy nie wykazują objawów na inne barwniki azowe.
Z tego co czytałem, niektóre zestawy zawierają jeszcze żółć chinolinową czyli E 104, także barwnik azowy, inne też kurkuminę.
Niebieski
Niebieskim barwnikiem jest tu błękit brylantowy, czyli E 133, nie jest to tym razem barwnik azowy:
Jednak grupy sulfonowe przy pierścieniach aromatycznych powodują, że także może wywoływać nadwrażliwość. Uważany jednak za bezpieczny z powodu bardzo nikłego wchłaniania. Jest często stosowany w napojach i słodyczach.
Możliwy do stosowania jest też indygokarmin E 132, pochodna pigmentu indygo (tego od dżinsów), kiedyś o nim pisałem. Nie jest barwnikiem azowym, nie wywołuje uczuleń i należy do najmniej szkodliwych substancji barwiących, jest bowiem bardzo szybko wydalany - na tyle szybko, że może zabarwić mocz na niebiesko.
Nie wiem natomiast czy w zestawach używa się czerni brylantowej - barwnika o intensywnym, niebiesko-fioletowym kolorze
Zielony
Mój zestaw nie zawierał żadnego specyficznego barwnika zielonego. Zielony był zapewne otrzymany ze zmieszania błękitu brylantowego i tartrazyny. W zasadzie możliwe jest użycie w niektórych zestawach E140 czyli chlorofilu lub lepiej rozpuszczalnej E 141 czyli chlorofiliny miedziowej, barwników pochodzenia naturalnego które spotykałem w zestawach barwników spożywczych do deserów.
Jak zatem widzicie, barwniki do jaj to kawał chemii. Czy wobec tego są groźne? Raczej nie - nie wnikają do wnętrza jajka, lecz pozostają związane w skorupce - a tą zdejmujemy i wyrzucamy. Jeśli zaś ktoś ma obawy to powinien od teraz pamiętać, by niezużytych barwników do jaj nie używać do innych rzeczy - a już parę razy czytałem o barwieniu nimi domowych ciast i lukrów, które się przecież spożywa w całości.
Post scriptum:
Znalazłem wynik ciekawego badania - analitycy ze Zgierza przebadali w 2009 roku komercyjne zestawy do barwienia przy pomocy chromatografii cienkowarstwowej. Wykazali, że na 9 przebadanych zestawów, trzy nie zawierały deklarowanych barwników, bądź zawierały w śladowych ilościach, a głównymi składnikami barwiącymi były barwniki do wełny, niedopuszczone do barwienia żywości. Opis badań jest dosyć przystępny:
http://zgierz.impib.pl/images/pdf/181.pdf
Wprawdzie różni producenci produkują tego typu barwniki, ale jak zauważyłem, praktycznie wszyscy używają tych samych, więc opis na podstawie składu barwników które mam w domu, powinien być reprezentatywny.
Czerwony
W moim zestawie za czerwień odpowiada E 124 czyli czerwień koszenilowa. To dość skomplikowany związek:
Dwie cząsteczki pochodnych naftalenu połączone grupą azową -N=N-. Grupa ta jest silnym chromoforem, a więc ugrupowaniem nadającym barwę, a jej kolor wzmacniają duże cząsteczki aromatyczne.
Wszystkie barwniki azowe mogą wywoływać uczulenia, u osób nadwrażliwych na salicylany zwiększają objawy a u astmatyków zwiększają wydzielanie histaminy. Z tego powodu ich użycie w żywności jest coraz bardziej ograniczane a normy zawartości systematycznie obniżane.
Różowy
W niektórych zestawach kolor różowy jest otrzymywany przez dodatek amarantu czyli E-123, kolejnego barwnika azowego. Ze względu na częste doniesienia o reakcjach nadwrażliwości jest coraz rzadziej używany w przemyśle spożywczym, podbarwia kawior, galaretki w proszku i napoje alkoholowe. Jest podejrzewany o rakotwórczość ale nie potwierdzono tego u ludzi.
Żółty
W moim zestawie znajdują się dwa żółte barwniki. Pierwszy to żółcień pomarańczowa czyli E 110 o kolorze bliższym pomarańczy, także będąca barwnikiem azowym:
Podobnie jak inne tego typu związki może wywoływać uczulenia i pokrzywki, u nadwrażliwych na salicylany daje reakcję. Jest podejrzewana o rakotwórczość ale nie wykazano tego u ludzi, mimo tego wiele krajów jej nie stosuje. Używa się jej do podbarwiania słodyczy i żywności która musi być podgrzewana, jednak coraz rzadkiej. Kiedyś była często stosowana do dożółcania margaryny.
Znalazłem informację, że stężone roztwory wodne przybierają w pewnych temperaturach formę ciekłego kryształu.
Drugi barwnik to tartrazyna, czyli E 102, mająca dość ciekawą budowę:
Jest to także barwnik azowy z grupami aromatycznymi, ale także pierścieniem diazolowym. Charakteryzuje się dużą siłą barwiącą. Pojawia się w szerokiej gamie produktów, zwłaszcza napojach i słodyczach, choć w ostatnich latach jest wycofywania. Używa się jej też w kosmetykach i jako barwnika do wełny.
Może wywoływać te same problemy zdrowotne jak i pozostałe barwniki azowe - pokrzywki, uczulenia, nadwrażliwość itp ale też migreny. Wydaje się, że u pewnych ludzi występuje specyficzna nadwrażliwość konkretnie na tą substancję, także u tych którzy nie wykazują objawów na inne barwniki azowe.
Z tego co czytałem, niektóre zestawy zawierają jeszcze żółć chinolinową czyli E 104, także barwnik azowy, inne też kurkuminę.
Niebieski
Niebieskim barwnikiem jest tu błękit brylantowy, czyli E 133, nie jest to tym razem barwnik azowy:
Jednak grupy sulfonowe przy pierścieniach aromatycznych powodują, że także może wywoływać nadwrażliwość. Uważany jednak za bezpieczny z powodu bardzo nikłego wchłaniania. Jest często stosowany w napojach i słodyczach.
Możliwy do stosowania jest też indygokarmin E 132, pochodna pigmentu indygo (tego od dżinsów), kiedyś o nim pisałem. Nie jest barwnikiem azowym, nie wywołuje uczuleń i należy do najmniej szkodliwych substancji barwiących, jest bowiem bardzo szybko wydalany - na tyle szybko, że może zabarwić mocz na niebiesko.
Nie wiem natomiast czy w zestawach używa się czerni brylantowej - barwnika o intensywnym, niebiesko-fioletowym kolorze
Zielony
Mój zestaw nie zawierał żadnego specyficznego barwnika zielonego. Zielony był zapewne otrzymany ze zmieszania błękitu brylantowego i tartrazyny. W zasadzie możliwe jest użycie w niektórych zestawach E140 czyli chlorofilu lub lepiej rozpuszczalnej E 141 czyli chlorofiliny miedziowej, barwników pochodzenia naturalnego które spotykałem w zestawach barwników spożywczych do deserów.
Jak zatem widzicie, barwniki do jaj to kawał chemii. Czy wobec tego są groźne? Raczej nie - nie wnikają do wnętrza jajka, lecz pozostają związane w skorupce - a tą zdejmujemy i wyrzucamy. Jeśli zaś ktoś ma obawy to powinien od teraz pamiętać, by niezużytych barwników do jaj nie używać do innych rzeczy - a już parę razy czytałem o barwieniu nimi domowych ciast i lukrów, które się przecież spożywa w całości.
Post scriptum:
Znalazłem wynik ciekawego badania - analitycy ze Zgierza przebadali w 2009 roku komercyjne zestawy do barwienia przy pomocy chromatografii cienkowarstwowej. Wykazali, że na 9 przebadanych zestawów, trzy nie zawierały deklarowanych barwników, bądź zawierały w śladowych ilościach, a głównymi składnikami barwiącymi były barwniki do wełny, niedopuszczone do barwienia żywości. Opis badań jest dosyć przystępny:
http://zgierz.impib.pl/images/pdf/181.pdf
Subskrybuj:
Komentarze (Atom)